Айзек Азимов ЭНЕРГИЯ ЖИЗНИ От искры до фотосинтеза
Часть первая. ЭНЕРГИЯ
Глава 1. УСИЛИЯ, КОТОРЫЕ МЫ СОВЕРШАЕМ
Человек всегда чувствовал разницу между собой и всеми остальными объектами окружающего мира. Практически в любой культуре человек считает себя венцом творения. Возможно, не столь значимым, как боги, демоны, ангелы и прочие сверхъестественные существа, но уж точно более главным, чем все, что можно увидеть своими глазами и пощупать своими руками.
Однако пропасть между человеком и всем остальным неоднородна. Одни предметы отличаются от человека больше, другие — меньше. Многие существа, как и человек, являются «живыми» и тем самым находятся гораздо ближе к нам, чем те, кому не посчастливилось обладать этим свойством.
С нашей, безусловно предвзятой, точки зрения, разделение на живое и неживое — самое принципиальное и важное разделение предметов Вселенной, которое только можно вообразить. А отличить одно от другого с обычной точки зрения (чем проще, тем лучше!) не составляет никакого труда. Камень посреди поля — конечно, неживой. А ящерка, пробежавшая по камню, — конечно, живая.
Как же мы их так легко различили? Ну, камень лежит неподвижно, и что бы с ним ни происходило — он никак не отреагирует. А ящерица быстро двигается и реагирует на все происходящее: на солнце, на голод, на опасность; она прячется в тени, отправляется на поиски пищи, ныряет в укрытие.
В общем, ящерицы, а также всякие воробьи и сурки легко причисляются к классу живых существ, потому что, в отличие от камней, они двигаются и действуют самостоятельно. Но как нам в таком случае провести границу между камешком и устрицей, между песчинкой и крошечным семечком? Уверены ли мы, что первые — неживые, а вторые — живые?
Да, уверены. Устрица, какой бы неподвижной она ни казалась на первый взгляд, может открывать створки своей раковины, втягивать воду, отфильтровывать из нее частички пищи, выбрасывать отходы. А семечку, хотя оно-то уж полностью недвижимо, достаточно лишь предоставить подходящие условия — почву, воду, соответствующую температуру, — и оно тут же примется за дело. Во все стороны из него потянутся ростки и корешки, и вскоре на свет появится растение. По сравнению с песчинкой семечко проявляет настоящие чудеса активности.
Но для того чтобы не просто терпеливо переносить все изменения в окружающей среде, а реагировать на каждое из них соответствующим образом, требуются усилия. «Совершение усилий» — достаточно тонкий момент, и я еще вернусь к нему более подробно, но пока давайте воспримем его в самом простом, «бытовом» понимании.
Так, нет никаких сомнений, что бег, лазанье, поднятие тяжестей — все это требует усилий. Мы тратим силы, даже если просто лежим на диване, — ведь мы раздвигаем грудную клетку с каждым вдохом и прогоняем пять литров крови по кровеносным сосудам с каждым ударом сердца. Наши почки и печень, как и другие органы, постоянно участвуют в деятельности, которая хотя и не является осознанной, но тоже нуждается в затратах энергии.
Даже самые малоподвижные растения совершают действия, которые необходимо признать усилиями, — цветы распускаются, ростки тянутся к свету, а корни — к воде.
Ни один камень, ни один неживой предмет не совершает усилий в том смысле, которое мы вкладываем в это слово, говоря о живых существах, даже самых простейших. Так что житейский опыт в итоге подталкивает нас к тому, чтобы признать главным признаком различения живого и неживого именно способность совершать усилия. Соответственно потеря этой способности и есть то, что мы именуем смертью.
Тогда для того, чтобы понять природу самой жизни, а главное, механизм работы совершенно особенного живого существа — человеческого организма, мы должны разобраться в том, что же вкладывается в понятие «совершения усилий». Именно этому вопросу и посвящена книга, которую вы держите в руках.
Если уж мы приняли умение совершать усилия за основное свойство живых существ, то следует задаться вопросом о том, чем же с этой точки зрения человек отличается от всех остальных.
Первое, что приходит в голову, — это то, что человек, как самое разумное из всех живых существ, организует свои усилия наиболее обдуманным и предусмотрительным образом. Человек может посадить зерна и бережно ухаживать за ними в течение многих месяцев, хотя никакого видимого эффекта его усилия вначале приносить не будут. Однако в конечном итоге эти усилия снабдят его достаточным количеством еды, чтобы пережить зиму, тогда как другим животным придется мигрировать, погружаться в спячку или переходить на голодный паек.
Эти ценнейшие усилия люди описывают разными словами: «работа», «труд», «дело», «занятие»… Физики выбрали для описания усилий, прилагаемых для получения результата, самое общеупотребительное слово — «работа».
Это был не совсем удачный выбор, потому что в естественном языке слово «работа» с психологической точки зрения далеко не нейтрально. Игра в теннис требует гораздо больших затрат усилий, чем раскладывание картотечных карточек в алфавитном порядке, но тем не менее последнее мы называем «работой», а первое — «развлечением», «игрой», «физкультурой», чем угодно, только не «работой». Опять же, человек может долго тужиться, пытаясь поднять тяжелый предмет, так и не поднять его в результате и рассказывать потом, как он «уработался».
В общем, ученым пришлось придумывать термину «работа» строгое математическое определение, которое было бы независимым от субъективной точки зрения. В частности, по этому математическому определению, как бы ни пыжился и ни потел человек, пытаясь поднять тяжелый груз, — если груз не поднят, то никакой работы с ним и не совершено.
Тот факт, что смысл слова «работа» в бытовом и в строго научном значении различен, многих новичков основательно сбивает с толку. Кажется, лучше было бы, если бы ученые взяли для использования какое-нибудь другое слово или придумали новое. Но — так уж сложилось. Позже я объясню подробнее, какое именно определение работы выдвинули физики, но пока нам достаточно будет и интуитивного понимания того, что работа — это результат приложения усилия.
Ученые посчитали нужным отметить отдельно и способности того или иного предмета совершать работу. Для определения этой способности было использовано слово «энергия». Оно происходит от греческого «энергос», что означает «деятельный». По строению своему греческое слово состоит из «эн» — «в, внутри» и «эргон» — «работа», то есть «энергию», таким образом, можно рассматривать как нечто, «внутри чего содержится работа». У энергии тоже есть точное математическое определение, но пока что нам, опять же, хватит и интуитивного понимания этого термина.
Энергия — это нечто, необходимое живому существу для осуществления усилий; но не только. Неживой предмет усилия совершать не способен, но обладать энергией — может. Нависший на краю скалы камень не способен совершить усилие для того, чтобы рухнуть вниз, но если его подтолкнет человек (или, скажем, ветер), то он может разрушить стоящий у подножия скалы дом. Это уже работа, а раз камень совершил работу, значит, он обладал энергией.
Таким образом, можно сказать, что ящерица и камень из примера, которым я начал эту книгу, различаются тем, что ящерица может переводить энергию, которой обладает, в работу по собственному усмотрению, а камень, какой бы энергией он ни обладал, не может перевести ее в работу без посторонней помощи.
Но давайте вернемся теперь, обогатив свой словарь такими понятиями, как «работа» и «энергия», к различию между человеком и другими формами жизни. Теперь мы можем отметить, что человек способен тратить энергию и производить работу ради отдаленного результата в некоем будущем.
Но является ли это уникальным отличительным свойством человека? Ведь и бобры строят плотины, и белки запасают орехи, и пауки плетут свои сети не для немедленного получения результата.
С нашей точки зрения, это совершенно разные вещи. Ни в одном из этих случаев, ни в одном из прочих примеров сложной деятельности животных и речи не идет ни о чем подобном человеческой предусмотрительности. Разница между действиями человека и животных столь очевидна, что человек автоматически заслуживает выделения в отдельный класс.
Но, повторюсь, так дело обстоит лишь с нашей точки зрения. Не является ли эта «очевидность» лишь проявлением предвзятости мышления и самооценки? Если некий инопланетянин возьмется изучать живой мир на Земле, увидит ли он какую-нибудь существенную разницу между пауком, ткущим паутину, и человеком, забрасывающим в море невод?
Было бы любопытно (и очень лестно) найти такое различие между нами и всеми прочими существами, которое было бы физическим, конкретным и явно понятным даже самому отстраненному внеземному наблюдателю. Мы уже сделали первый шаг, попытавшись провести различие между собой и другими живыми существами по способу использования энергии. Попытаемся развить эту тему.
Для этого стоило бы вернуться, например, в те далекие времена, когда человек еще не так сильно отличался от животного, и попытаться найти тот момент, когда в процессе развития цивилизации безошибочно проявилось то самое принципиальное различие между человеком и остальными живыми существами. Тогда мы и увидим, что это за различие.
В процессе такого исследования нам придется еще глубже изучить значение «энергии» и «работы». А это, в свою очередь, даст нам лучшее понимание механизмов жизни, которую мы определили пока что лишь как «способность совершать усилия».
Давайте зададимся вопросом не о том, с какой целью человек тратит энергию (это было бы слишком сложно объяснить инопланетянину), а о том, каким образом он это делает.
Начнем с того, что человек может тратить энергию, совершая работу, лишь в некоторых ограниченных пределах. Если ему нужно один за другим перенести двадцать камней по двадцать пять килограммов каждый на другое место, метрах в ста отсюда, он сможет выполнить такую задачу. Человек при этом будет двигаться медленно и периодически отдыхать, чтобы организм успевал возобновить запас энергии в количестве равном потраченному. Так, правильно рассчитывая силы и не торопясь, человек способен перетащить практически любое количество таких камней на практически любое расстояние — естественно, в рамках разумного.
Но если все эти камни объединить в один полутонный валун, то ни один человек не сможет его сдвинуть. Организм человека не способен аккумулировать достаточное количество энергии и потратить ее настолько быстро, чтобы разом поднять камень весом в полтонны. Скорость расходования энергии ученые называют «силой». Таким образом, мы можем сказать, что у человека, хоть и имеется достаточно энергии, чтобы поднять груз в полтонны весом, если на то будет достаточно времени, тем не менее силы для единовременного совершения такого действия не хватает.
Все вышеописанное в равной мере относится и к человеку, и к другим животным, разницы между ними в этой ситуации никакой. Человек обладает большей силой, чем мелкие зверьки, типа кошки или мышки, и меньшей силой, чем, например, лошадь или слон. Любое животное, сколь велико бы оно ни было, обладает лишь ограниченной силой.
Всем живым существам пришлось разработать способы более эффективного использования имеющейся в их распоряжении энергии. Например, бесполезно было бы пытаться прокусить толстый слой мышц добычи двумя плоскими деснами. А вот если снабдить эти десны твердыми зубами с острыми концами, то вся энергия смыкающихся челюстей, сама по себе не увеличившись, будет теперь сосредоточена на этих остриях. В целом прилагаемое усилие остается таким же, но усилие на единицу площади возрастет многократно, и поэтому в точке контакта удается прорвать плоть жертвы. Таким образом, тигр, с его клыками и когтями, является страшным хищником, а крупная лошадь, располагающая большим, чем у тигра, запасом энергии, становится для него не более чем легкой добычей.
Живые существа выработали множество способов потрясающего увеличения эффективности использования своей энергии, обретая таким образом способность быстро бегать, плавать и даже летать. Но расход энергии живого существа всегда остается ограниченным.
Если организм того или иного животного не выработал способности эффективно использовать энергию для некоего определенного действия, на помощь ему может прийти использование внешних предметов («инструментов»). Среди животных (не считая человека) способность использовать инструменты не особенно распространена, но все равно примеров можно привести достаточно. Птицы способны разбивать скорлупу устриц камнями, а некоторые насекомые даже умеют заваливать туннели камушками. Однако человек и родственные ему вымершие виды человекоподобных существ настолько превзошли всех остальных животных в использовании посторонних предметов в своей деятельности, что все достижения других животных в этой области можно отмести и определить человека как «животное, использующее инструменты».
Важным этапом стал момент, когда первобытный человек перестал довольствоваться теми более-менее подходящими предметами, что попадались ему под руку (как это делают и животные), а принялся специально изготовлять камни с особенно острыми гранями и наконечниками.
Поскольку инструмент — это вещь, с помощью которой энергия, прилагаемая на входе, передается на выход в измененном (более полезном с практической точки зрения) виде, то инструмент можно назвать «машиной». Мы привыкли думать о машинах как о сложных и больших механизмах, но на протяжении многих тысяч лет человечество пользовалось крайне простыми машинами.
Одна из простейших машин — рычаг. Представим, что под полутонный валун подложили один конец перекладины, под которую, в свою очередь, подставили небольшой камень (рис. 1). Длинный конец перекладины торчит далеко наружу. Если вы начнете опускать длинный конец перекладины, то прилагаемое вами усилие будет переведено в подъем короткого конца. Примером рычага могут служить детские качели, где движение одного ребенка вниз является силой, поднимающей вверх второго, сидящего на противоположной стороне.
Рис. 1. Рычаг
Рычаг изменяет направление прилагаемого усилия, и этого в принципе достаточно, чтобы счесть его машиной, но этим действие рычага не ограничивается. Путь, который проделывает, поднимаясь, короткий конец перекладины, в несколько раз меньше, чем путь длинного ее конца, поэтому сила[1], с которой действует короткий конец, возрастает во столько же раз. Произведение прикладываемой силы на проходимое концом рычага (его называют «плечом») расстояние равно на обоих его концах. Это и есть «принцип рычага», открытый впервые Архимедом — греческим математиком, который жил в III веке до нашей эры, хотя, конечно, и за тысячи лет до того люди использовали этот принцип на практике, пусть и не понимая его сути.
Если длинное плечо рычага в десять раз длиннее короткого, то, опустив дальний конец перекладины на 1 метр, вы, таким образом, поднимете камень на 10 сантиметров, то есть расстояние, на которое переместятся концы перекладины, будет различаться во столько же раз, во сколько различается длина плеч рычага. С другой стороны, во столько же раз, только в обратном отношении, будет различаться и сила на обоих концах рычага. К длинному концу достаточно приложить лишь одну десятую часть той силы, которая необходима для того, чтобы поднять камень, лежащий на коротком конце. Иными словами, если опускать длинный конец перекладины на 1 метр с силой 50 килограммов, то коротким концом удастся сдвинуть камень весом в полтонны на 10 сантиметров. Так следует из принципа, сформулированного Архимедом, — ведь если 1 метр умножить на 50 килограммов, то будет столько же, сколько если и 0,1 метра умножить на 500 килограммов.
Общее количество энергии, потраченной на обоих концах рычага, одинаково, но, перемещая 50 килограммов на расстояние 1 метра, мы не выходим за пределы человеческих возможностей по скорости приложения энергии, в отличие от задачи по подъему 500 килограммов хоть на 1 сантиметр. В последнем случае организм человека просто не успевает выработать необходимое для совершения действия количество энергии. Таким образом, применение рычага делает выполнимой задачу, решение которой без него было бы невозможно. Архимед высказался об этом весьма красноречиво: «Дайте мне точку опоры, и я переверну весь мир!»
На заре своей истории человек изобрел и другие простые машины, служившие одной цели — привести количество энергии, которое необходимо одномоментно приложить для решения задачи, к уровню реальному для человека. Среди этих изобретений — колесо, подъемный блок, клин, наклонные плоскости и многое другое.
Среди этих устройств не было и не могло быть таких, которые увеличивали бы общее количество энергии, доступное для использования человеком. Однако с помощью только таких механизмов древние египтяне построили свои пирамиды, а китайцы — Великую Китайскую стену. Конечно, для этого требовался и изнурительный труд десятков тысяч человек на протяжении десятилетий.
Если бы нашему инопланетному наблюдателю пришло в голову проследить за работой в каменоломнях и пустынях Египта и сравнить процесс медленного, камень за камнем, созидания Великой пирамиды с процессом построения насекомыми термитника, наверное, большой разницы он не увидел бы. Более того, термитник по отношению к отдельному термиту крупнее, чем пирамида — по отношению к человеку, так что результат труда термитов, возможно, произвел бы на инопланетянина большее впечатление. Да, человеку приходится самому изготавливать свои нехитрые инструменты, а термиту все необходимое дано от рождения, однако, возможно, инопланетянин счел бы подобное проявление величия человеческого разума моментом интересным, но не принципиальным.
Несмотря на все инструменты, изобретенные за десятки тысяч лет своей ранней истории, человек все еще оставался таким же ограниченным энергетическими возможностями собственного организма, как и термит. До принципиального различия между этими двумя видами живых существ мы до сих пор так и не добрались.
Для того чтобы выполнить больше работы за меньшее время, чем то способен сделать человек со своими ручными инструментами, требуется возможность расходовать за единицу времени больше энергии, чем может вырабатывать человеческий организм. Один из способов решения этой задачи — использование прирученных животных.
Когда именно человек впервые приручил животное — тайна, покрытая мраком множества веков.
Возможно, одомашнивание животных получилось из стихийно сложившихся союзов, когда животные определенных видов тайком поселялись возле стоянок первобытного человека, рассчитывая на то, чтобы поживиться пищевыми отходами; их могли приручать просто для забавы, из тех побуждений, что и сейчас порой манят детей к черепахам, жукам, крысам и прочим не самым симпатичным созданиям.
В конце концов человеку пришло в голову, что выращивать этих животных можно прямо в неволе, в результате их количество естественным образом увеличится и животных можно будет использовать в различных практических целях: мясо — в пищу, шкуру — на одежду, зубы и кости — на украшения и инструменты.
Таким же образом и, наверное, примерно в ту же историческую эпоху были «одомашнены» и растения — так зародилось земледелие. Разрозненные группки людей, прежде всего — охотников и собирателей, зависимых от прихотей судьбы, теперь принялись сами выращивать себе пищу, стали пастухами и земледельцами. Теперь территория племени могла прокормить гораздо больше людей, в первую очередь благодаря земледелию, и результатом стал взрывной рост численности человеческого населения.
А одомашненные животные, помимо прочего, оказались неплохими помощниками в работе. Те из них, что были крупнее человека и могли, соответственно, расходовать энергию более высокими темпами, оказались чрезвычайно полезными; они довольствовались более грубой пищей, чем та, что требуется человеку, а при должном обращении (например, будучи кастрированными) оказывались и более послушными и управляемыми, чем рабы-люди.
Самым распространенным в доисторические времена рабочим скотом были ослы и быки. Эти животные обладали первое в два, а второе в семь раз большим запасом энергии для совершения работы, чем человек. У лошадей этот показатель еще выше, но из-за своей анатомии они задохнулись бы, накинь им ремень с грузом на шею, а хомут придумали только приблизительно около 1000 года нашей эры. Лишь после этого стало возможным использовать лошадей для перевозки грузов.
А пока лошадей нельзя было использовать в качестве тяглового скота — зато можно было ездить на них верхом. Организм лошади гораздо лучше человеческого приспособлен к быстрому бегу, так что даже с человеком на спине лошадь развивает гораздо большую скорость, чем когда-либо мог сам человек. Лишь последнюю пару веков человек смог наконец-то путешествовать по суше быстрее, чем верхом на лошади.
Применение животных несколько увеличило запас энергии, имевшейся в распоряжении человека, но на самом деле не очень сильно, даже если учитывать таких крупных животных, как верблюды и слоны. Частично это объясняется тем, что за животными необходимо ухаживать, кормить их и тому подобное. Этим заниматься должен был человек, и на это тоже уходила часть энергии, которую он мог бы потратить на собственные нужды.
В использовании животных наш инопланетный наблюдатель увидел бы, возможно, лишь несколько более широкомасштабное и искусное применение навыков, свойственных и животным.
К примеру, морские анемоны иногда путешествуют, прикрепившись к раковине краба. Анемоны, неспособные к самостоятельному перемещению, от этого выигрывают, поскольку движение увеличивает их шансы найти себе пищу. Краб тоже получает выгоду от такого союза, поскольку стрекающие щупальца анемона удерживают хищников от того, чтобы напасть на краба. Более того, краб иногда питается крошками со стола анемона, которые тот роняет вниз.
Увидит ли наш инопланетянин принципиальную разницу между этим симбиозом и отношениями человека и лошади, когда первый ездит на второй верхом, а взамен предоставляет ей корм и защиту?
Думаю, мы так и не подобрались к принципиальному отличию человека от прочих живых существ.
Существует еще один способ высвобождать энергию быстрее, чем это может делать человеческий организм. Для этого необходимо обратиться к неодушевленным предметам.
Кажется не совсем очевидным, что неодушевленные предметы могут обладать энергией, но подметить это не так уж и сложно, если захотеть. Бурный поток воды перемещает попадающие в него предметы; если бы то же самое делал человек, это явно была бы работа. Вода и ветер, если разбушуются, могут сотворить больше разрушений, чем целая армия людей.
Со временем человек научился использовать и эти неодушевленные источники энергии. Реки несут вниз по течению тяжелогруженые корабли, а по морю, там, где нет течения, те же корабли влечет сила ветра, толкающего судно в предусмотрительно подставленные паруса. Энергию воды и ветра можно использовать и для вращения мельничных колес, которые растирают зерно в муку.
Понятно, что первобытного человека ставил в тупик факт присутствия такого количества энергии в неодушевленной природе. Непосвященному кажется, что энергия — это то же самое, что и способность совершать усилия, свойственная, как известно, только живым существам. Поэтому в глазах первобытного человека явно неживая материя тоже становилась живой, обретала душу; он придумывал демонов и богов, которые являли себя в грозах и бурях. Ветер становился дыханием этих сверхъестественных живых существ, а вода бурлила по их воле.
Однако еще задолго до того, как человек начал предпринимать первые робкие попытки приручить ветер и воду, в его распоряжении уже давно находился еще один мощный источник дополнительной энергии. Речь идет об овладении огнем, которое произошло не менее ста тысяч лет назад. Впервые огнем овладели не люди современного типа — их тогда еще не было, — а представители близких биологических видов, давно вымершие человекообразные.
Огонь существовал всегда, и любое наделенное чувствами существо впадало в ужас, когда во время грозы молния попадала в дерево и начинался лесной пожар. Это была катастрофа, все живое спасалось бегством в панике, но, видимо, некоторые из первобытных людей находили какой-то странный интерес в том, чтобы поиграть потом с небольшими горящими участками — остатками большого лесного пожара. Они подбрасывали в огонь веточки и наблюдали за пожирающими пищу языками пламени. (И сейчас всем родителям знакома та завороженность, с которой дети могут играть с огнем.)
Если за такой игрой первобытного человека застала ночь, то он наверняка по достоинству оценил тепло и свет от такого соседства. К тому же он мог заметить, что другие животные, пугаясь огня, не подходили к костру и к сидящему рядом человеку, что обеспечивало дополнительную защиту.
В конце концов человек рискнул «приручить» огонь. Он развел костер у себя на стоянке или в пещере и стал поддерживать его, чтобы постоянно пользоваться всеми новообретенными преимуществами. А уже потом со временем выяснилось, что если пищу (в первую очередь мясо) подогреть как следует на огне, то его становится гораздо легче есть, да и вкус еды меняется в лучшую сторону.
Но это еще не было «овладением огня». Просто поддерживать огонь недостаточно. Как внимательно за ним ни наблюдай, все равно рано или поздно он может погаснуть. Конечно, можно поддерживать несколько костров и, если погаснет один, снова разжечь его с помощью углей от второго костра. В принципе можно использовать угли и от костра с другой стоянки или даже от костра другого племени. Но это — не решение проблемы, а скорее способ избежать ее.
Так что истинное овладение огнем — это возможность разжигать огонь там, где его прежде не было. Оказалось, что если хоть искру пламени уронить на кучку предварительно хорошо измельченного легковоспламенимого материала, то получится именно то, что нужно! Для того чтобы получить саму искру, оказалось достаточно просто ударить друг о друга двумя подходящими камнями, а еще оказалось возможным добиться того же самого долгим трением вращающейся палочки о желобок или внезапным сжатием большого количества воздуха.
Какова бы ни была в том или ином случае техника, обретение возможности разжигать огонь и стало событием, ознаменовавшим истинное овладение огнем.
Так огонь стал воплощением сконцентрированной энергии. Теперь в распоряжении человека оказалось во много раз больше энергии, чем может вырабатывать его собственный организм. По этой причине овладение огнем можно назвать, пожалуй, самым главным достижением человека. Теперь человек мог забыть о том, как ограничен энергетический запас его организма и организмов прирученных животных.
И вот на этом месте даже наш инопланетный наблюдатель признает наконец четкую принципиальную разницу между человеком и животными. Вполне научно-практическое достижение в области использования энергии безошибочно выделяет человека (и его предков) из ряда прочих живых существ на планете. Никакие другие животные не предпринимали даже попыток овладеть огнем или хоть как-то использовать его, а что касается человека — то сейчас на земле нет ни одного племени людей, пусть самого примитивного, которое не владело бы огнем.
Глава 2. ПЛОДЫ ОГНЯ
Овладение огнем — не просто удобный признак для выделения человека из общего ряда живых существ. Огромное количество энергии, оказавшееся в распоряжении человека после овладения огнем, произвело коренные изменения в самом образе жизни человека.
И человек всегда понимал, сколь многим он обязан огню. У древних греков был миф о титане Прометее, который спас род человеческий от мучительного прозябания тем, что принес людям в дар огонь, урвав его у Солнца. Солнце вообще многими обожествлялось как квинтэссенция огня. В XIV веке до нашей эры Древним Египтом правил фараон Аменхотеп IV, который пытался ввести культ единого бога — Солнца и даже сменил свое имя на Эхнатон («угодный Атону», от имени бога Солнца — Атон). Правда, солнцепоклонничество в Египте не прижилось и закончилось вместе с жизнью фараона. Сам огонь, в его земной форме, обожествляли древнеперсидские зороастрийцы. Этот культ и по сей день исповедуют индийские парсы.
Древние скандинавы персонифицировали огонь в его злокозненной ипостаси — богом огня у них был Локи, этакий скандинавский аналог Сатаны. Зато у древних греков и римлян Гефест (Вулкан) и Гестия (Веста) ассоциировались с благотворным огнем кузнечного горна и домашнего очага. Весталки бережно поддерживали священное пламя, не давая ему угаснуть, — возможно, этот ритуал являлся отголоском тех давних времен, когда угасание единственного источника огня становилось катастрофой для племени.
Однако, несмотря на всевозможное поклонение огню, вряд ли многие осознавали, что постижение феномена огня — это путь к постижению основ Вселенной, а в частности — постижению природы жизни.
Сейчас я буду излагать историю огня. Начну я с описания того воздействия, которое он оказал на образ жизни человечества, но конечная цель этой части моего повествования — осмыслить само существование живых существ, так сказать, в свете Огня.
Сам факт наличия источника света и тепла, независимого от Солнца, предоставил человеку возможность выйти за пределы тропиков, до сих пор ограничивающие ареал распространения его ближайших родственников — крупных обезьян, в холодные края, где ночи длинны и темны, а зимой выпадает снег. В частности, именно обладание огнем позволило человеку пережить ледниковый период.
Мало того, возможность готовить еду на огне изменила и рацион человека, включив в него виды пищи, которые раньше были для людей совершенно несъедобными. К тому же огонь обеспечивал и дополнительную безопасность, отпугивая крупных хищников.
Именно огонь, и только он, превратил человека в существо творческое, научил создавать и сделал владыкой мира. И со временем значение огня не уменьшилось, скорее наоборот. Даже если взять последние два века, когда с момента овладения огнем прошло больше ста тысяч лет, и то открытие новых видов топлива и новых способов воспламенения привело к радикальным изменениям в жизни человека. Первым известным человеку топливом, несомненно, была древесина. Однако в XVII веке наиболее важным видом топлива стал уголь, а в XX пальма первенства перешла к нефтепродуктам.
Практически все то время, что человек владел огнем, огромные возможности последнего оставались почти неиспользуемыми; человек довольствовался получением от огня тепла и света. Лишь перед самым началом исторической эпохи человек вдруг выяснил, что от огня можно получить вполне материальные плоды. Речь идет о металлах.
Само знание о том, что существуют металлы, значения имело не больше, чем знание о существовании огня. Не раз, должно быть, за всю историю существования человечества то один, то другой индивидуум натыкался на блестящие камушки, не похожие по своим свойствам на другие камни. Так, камень, если им с силой бить по другому камню, трескается и крошится, а этот блестящий материал сминался, но оставался целым. Форму такого самородка можно было изменять, его можно было расплющить или придать ему другой необходимый вид. Понятно, что из такого материала в первую очередь стали делать украшения. И действительно, золотые и медные украшения находят в египетских гробницах, датируемых доисторическими временами.
Принципиально важным оказался тот момент, когда было сделано открытие, что металлы можно получать и из тех материалов, которые сами по себе совершенно не кажутся похожими на металл. Именно открытие способа создавать металл там, где его раньше вроде бы не было, и произвело революцию, как за много тысяч лет до того — открытие способа разводить огонь, там, где только что не было никакого огня.
Наверняка впервые металл был получен случайно. Медь образует довольно непрочные соединения с другими веществами, например с кислородом или серой, в результате чего получается камнеподобное вещество голубоватого цвета. Если куски такого вещества нагреть на огне среди углей, углерод перетягивает непрочно закрепленные кислород и серу к себе и связывается с ними; получившееся соединение улетучивается вместе с дымом, а в очаге остается чистая медь.
Сам по себе уголь не способен превращать камни в металл. Для этого необходимо сочетание угля и жара, которого первобытный человек мог добиться только с помощью огня. Поэтому медь, да и другие металлы древними воспринимались как дары огня. Со временем, когда достаточное развитие получила металлургия, широкое применение получили сперва бронза (сплав меди с оловом), а затем и железо, как материалы для оружия и доспехов.
Представьте себе, что какие-нибудь кочующие пастухи случайно развели костер на камнях, содержащих медь (на медной руде). Угли костра сделали свое дело, и, когда огонь погас, остроглазый пастух вдруг заметил среди пепла слитки меди. В конце концов, то, что произошло (возможно, много раз) по случайности, не могли не повторить нарочно, и всем стало ясно, что огонь можно использовать для того, чтобы выплавлять из камня металл. К 3500 году до нашей эры выплавка меди из руды стала уже вполне развитой отраслью на Ближнем Востоке.
Руды металлов встречаются не очень часто, но все же гораздо чаще, чем месторождения чистых металлов, так что только к 3500 году до нашей эры человечество впервые получило металлы в более-менее серьезном объеме. Теперь медь можно было использовать не только для украшений, которые стали доступны и простым людям, но и как материал для домашней утвари. Энергия огня обеспечила и другие достижения, возможно, менее значительные по сравнению с развитием металлургии, но все же достаточно важные, чтобы помнить о них. Так, с умением обжигать глину человек получил керамику, фарфор и строительный кирпич, а путем усиленного нагревания песка вместе с содой и известняком — стекло.
Средневековье принято считать эпохой упадка и деградации после великих дней расцвета греко-римской цивилизации. Однако именно в средневековой Европе был достигнут ошеломительный успех в области разработки источников энергии, отличных от обычного дровяного костра.
Так, греки Византийской империи (один из осколков былой Римской империи, существовавший в Средневековье) в VII веке нашей эры разработали некую горючую смесь, тайна состава которой была в дальнейшем утеряна. Смесь горела, будучи разлитой по воде, и водой это пламя погасить было невозможно. Для деревянных кораблей это оружие, получившее название «греческий огонь», представляло смертельную опасность, и с его помощью дважды были отбиты нападения осаждавших Константинополь в VII и VIII веках мусульман-арабов. В первую очередь победы были достигнуты за счет применения греческого огня против флота мусульман. Таким образом Константинополь еще на семь веков отстоял свое право быть христианским городом, пока в конце концов не пал-таки под натиском мусульман (на этот раз — турок) в 1453 году.
Но для горения греческого огня, как и любого другого горючего, требовался воздух (точнее, содержащийся в воздухе кислород).
Так что настоящая революция произошла с открытием пороха, для горения которого воздух уже не является необходимым. Каким-то образом (скорее всего, опять же благодаря случайности) выяснилось, что если смешать горючие вещества (уголь и серу) с селитрой (нитратом калия) и нагреть смесь, то произойдет мгновенное мощное возгорание, даже при отсутствии воздуха. Мы-то сейчас можем объяснить, что это происходит потому, что в нитрате калия уже содержится кислород, которого достаточно для реакции горения, но люди Средневековья этого знать не могли.
Кажется, впервые в истории орудия — конечно же самые примитивные — были использованы в 1346 году в битве при Креси. В последующие века значение артиллерии все возрастало; постепенно появлялось и индивидуальное огнестрельное оружие. Эти процессы изменили и саму структуру европейского общества.
Среди других великих изобретений эпохи Средневековья можно назвать компас, в котором использовалась энергия, именуемая «магнетизмом» (от названия греческого города Магнезия, в окрестностях которого греки находили первые природные магниты).
Именно с помощью компаса мореплаватели получили возможность ориентироваться в открытом море вдали от суши, даже тогда, когда тучи скрывали от них привычные ориентиры — Солнце и звезды. Появление этого прибора подтолкнуло человека к изучению океанов. Без компаса великие путешествия Колумба и последующих первооткрывателей, скорее всего, не состоялись бы.
Казалось бы, значение этих двух изобретений — пороха и компаса — настолько велико, что других равных им достижений в средневековую эпоху и искать бессмысленно. Однако мы все же вспомним еще одно, важнее и пороха, и компаса, хотя, в отличие от них, не имевшее прямого отношения ни к какому из видов физической энергии.
Приблизительно в середине XV века, когда Средневековье уже заканчивалось и на горизонте уже маячила современная эпоха (которую часто отсчитывают от открытия Колумбом Америки), немецкий монах Иоганн Гутенберг изобрел книгопечатный станок.
Ни одно изобретение за всю предыдущую историю человечества не получило такого мгновенного распространения. Не прошло и одного поколения, а печатное слово уже полилось потоком по Европе. Знания стали доступны каждому (по крайней мере, теоретически). Теперь ученые могли распространять свои мысли не через неторопливо передаваемые из рук в руки и долго переписываемые трактаты, а с помощью быстро разлетающихся печатных книг.
Для того чтобы сто лет спустя произошла революция в астрономии, недостаточно было одних идей Коперника. Для того чтобы коренным образом изменить представления об анатомии, мало было одних идей Везалия. Необходимо было кристаллизовать их представления в книгах (обе книги были напечатаны в один год — 1543) в таком количестве, чтобы с ними успели ознакомиться все ученые Европы прежде, чем власти спохватились и начали репрессии.
Книгопечатание стало как бы ферментом для развития знаний, оно высвободило некую мыслительную энергию. Появились новые воззрения о природе Вселенной — впервые в полном объеме их продемонстрировал итальянский ученый Галилео Галилей, и суть их заключалась в необходимости точного измерения всех физических явлений. На смену простому наблюдению в науку пришли количественные отношения, имеющие строгие математические выражения.
Разумеется, в новых условиях такие явления, как энергия и работа, тоже не могли не подвергнуться измерению. Так огонь, за сотню тысяч лет до того выделивший человека из мира животных, помимо применения, подвергся еще и изучению. Результатом этих научных опытов стали изменения в образе жизни человека, по сравнению с которыми померкли даже последствия изобретения пороха и компаса.
Овладение огнем принесло человечеству совершенно новые вещи — металлы, кирпич, стекло; если бы огня не было, человечеству пришлось бы обходиться без всего этого. Мышечная энергия никоим образом не может заменить огонь для получения всего вышеперечисленного. Однако, несмотря на все эти дары, в обыденной жизни человеку приходилось заниматься все той же работой — таскать, поднимать, толкать и рубить, и подмогой ему оставались разве что верные домашние животные.
Использование энергии неживой природы привело к появлению новых видов работы — опять же грубой работы мышц человека. Возьмем хотя бы водяные мельницы. Вода течет сверху вниз, и чем больше разница в высоте между этими «верхом» и «низом», тем быстрее поток и тем больше в нем энергии. А чем мощнее поток, тем активнее будут вращаться лопасти колеса, приводящего в движение мельничные жернова. Проблема в том, что речки, к примеру в Англии, как правило, тихие и спокойные. Чтобы добавить их течению энергии, воду необходимо поднять на определенную высоту, чтобы она уже оттуда падала на лопасти. А поднимать ее приходилось посредством все той же мышечной силы.
Проблема подъема воды приобрела большую остроту, когда в Англии стали рыть глубокие угольные шахты, которые необходимо было защищать от опасности затопления. Человеку пришлось задуматься над решением вопроса об откачке воды.
Это уже напоминало порочный круг. На подъем воды требуется затратить энергию, а лучшим способом получения этой самой энергии в те времена было как раз использование падающей воды. Для того чтобы разорвать круг, необходимо было полагаться на некий сторонний источник энергии: либо на непостоянный и ненадежный ветер, который вращает лопасти ветряных мельниц, либо на жестко ограниченные ресурсы мышечной силы людей или животных.
Однако в ходе работы над проблемой откачки воды ручными насосами родилось новое решение, позволившее не только разорвать порочный круг, но и вообще навсегда освободить человека от крупномасштабного физического труда.
По мере того как шахты становились все глубже и насосам приходилось выкачивать воду на все большее расстояние, выяснилось, что выше чем на 10 метров поднять ее просто невозможно, с какой силой и яростью ни налегай на ручку помпы.
Вопрос о том, чем же обусловлен такой предел возможностей насосов, пытался решить еще Галилео, но самому ученому сделать это не удалось. Зато его ученик, Эванджелиста Торричелли, вскоре после смерти учителя выдвинул предположение о том, что при работе насоса воду на самом деле толкает вверх вес воздуха, давящего на поверхность водного зеркала. В природных условиях давление воздуха на поверхность воды везде одинаково, но при использовании насоса в момент вытягивания поршня внутри насоса создается вакуум и равновесие нарушается. Внутри насоса воздух перестает давить на воду, а снаружи — давление продолжается с прежней силой. Поэтому по закону сообщающихся сосудов жидкость начнет перетекать в насос, и уровень воды в нем будет подниматься.
Однако, когда столб поднимающейся по трубе или шлангу воды достигнет высоты в 10 метров, его вес сравняется с весом воздуха, давящего на водную поверхность снаружи насоса, и вода перестанет подниматься дальше. Система снова придет в равновесие. Тогда жидкость менее плотную, чем вода, удастся поднять на большую высоту, а более плотную — не удастся поднять и на 10 метров.
В качестве материала для эксперимента, призванного проверить справедливость своей теории, Торричелли выбрал самую плотную из известных ему жидкостей, которая, предположительно, должна была прекратить подниматься, достигнув весьма малой высоты. Этой жидкостью была ртуть. И вот в 1643 году Торричелли залил жидким металлом стеклянную колбу длиной в 1 метр и в перевернутом виде опустил ее в чашу с ртутью, после чего открыл колбу под поверхностью ртути. Давления воздуха на чашу с ртутью оказалось недостаточным, чтобы уравновесить давление метрового столба ртути. Ртуть начала выливаться из колбы в чашу и остановилась лишь на отметке 30 дюймов (76,2 см).
На этом уровне ртутный столбик застыл, наглядно демонстрируя количественное значение силы давления воздуха. Над столбиком образовался вакуум, который до сих пор называют «торричеллиевой пустотой», и это был первый настоящий рукотворный вакуум (рис. 2). Торричелли изобрел барометр, который и по сей день используют в практически неизменном виде, измеряя с его помощью слабые перемены атмосферного давления и пытаясь на основе этих данных предсказать погоду.
Торричелли показал, что воздух имеет вес, а значит, может оказывать давление. На самом деле на уровне моря атмосферное давление составляет чуть более 1 кг/см2, то есть на нас с вами оказывается давление весом около 22 тонн. Мы не чувствуем этого только потому, что давление воздуха одинаково во всех направлениях, и давление снаружи нас равняется давлению внутри нас — внутреннее и внешнее давление уравновешено.
Рис. 2. Барометр
Любому, кто сомневался в силе искусственно создаваемой разницы давлений, следовало бы побывать на демонстрации, которую устроил в свое время немецкий физик Отто фон Герике (по совместительству — мэр Магдебурга). Работа Торричелли очень заинтересовала фон Герике, и он разработал насос для откачки не воды, но воздуха. Поршни, приводимые в движение вручную, плотно прилегая к стенкам трубок, по которым двигались, захватывали в своих трубках и выталкивали наружу одну за другой порции воздуха из герметично запаянного контейнера (примерно так же, как это делает велосипедный насос, захватывая воздух из атмосферы и выталкивая его в камеру велосипеда) до тех пор, пока внутри воздух не становился настолько разреженным, что вполне мог сойти уже и за вакуум.
Вот что сделал фон Герике: он совместил воедино два металлических полушария, но не скреплял их при этом ни болтами, ни какими-либо иными застежками. В одном из полушарий при этом имелся клапан, через который насосом откачали воздух, так что внутри полушарий (впоследствии их будут называть «магдебургскими полушариями») образовался тот самый вакуум. После того как воздух откачали, полушария удерживало воедино только атмосферное давление — более килограмма на каждый квадратный сантиметр. Фон Герике хотел показать, как могуча сила атмосферного давления; с этой целью к каждому полушарию он прикрепил по упряжи, в которую запрягли по четверке лошадей (то есть всего восемь!) и дали им команду тянуть в разные стороны. Но разъединить полушария животным не удалось. Когда же внутрь состоящего из двух частей шара вновь впустили воздух, полушария развалились под собственным весом.
Вы и сейчас можете воспроизвести подобный эксперимент в уменьшенном масштабе, взяв резиновую присоску и налепив ее на гладкую мокрую поверхность.
В ходе одной из своих последующих демонстраций фон Герике использовал трубку, внутри которой находился плотно прилегающий к краям трубки поршень. Ученый выкачал воздух из трубки с одной стороны от поршня, и поршень пришел в движение, опускаясь в сторону вакуума, несмотря на все усилия пятидесяти здоровых мужчин, которые пытались удержать его на месте с помощью каната.
Все это, конечно, заставляло публику изумляться силе, заключенной в разнице давлений, но поскольку никакого практического использования подобной силе не было придумано, то и воспринимали ее как диковинку, и не более.
Необходимо было разработать способ образовывать вакуум с помощью чего-то более подходящего, чем мышечная сила. А ведь именно мышечная сила приводила в действие и помпы, откачивающие воду из шахт, и насосы фон Герике — да и наши биологические насосы, легкие, работают только благодаря ей. Да, фон Герике действительно показал, что один человек может с помощью ручного насоса получить силу, позволяющую ему перетянуть пятьдесят других человек, но для этого оператору насоса пришлось сначала очень долго поработать, откачивая воздух. Для промышленных масштабов такие темпы явно не годились.
Ответ был найден. Ключом к решению стал пар — обычный пар от кипящей воды. Тут необходимо сделать небольшое отступление.
В 1690 году французский физик Дени Папен обнаружил, что если пар от кипящего котла с водой впустить в сосуд, то он вытеснит из сосуда весь воздух, причем давление в сосуде останется поначалу таким же.
Но какова разница! Для того чтобы удалить из сосуда воздух, требуется приложить усилия и откачать его. А для того чтобы удалить пар — достаточно всего лишь остудить сосуд! И огромный объем пара конденсируется в виде нескольких капель воды, а в сосуде останется практически полноценный вакуум. В качестве источника энергии для всего процесса достаточно некоторого количества древесины, которая, сгорев, вскипятит воду, в результате чего появится пар. Больше не требовалось никакого физического труда, никакого утомительного откачивания воздуха вручную. Кроме того, с помощью ручного откачивания воздуха создание вакуума занимает долгое время, а в сосуде, наполненном паром, вакуум можно создать за несколько секунд, плеснув на его горячие стенки стакан холодной воды.
Папен даже сконструировал механизм, в котором созданный им вакуум вытягивал поршень вниз под действием атмосферного давления и сам, в свою очередь, поднимал вверх воду. Применить это устройство как насос на практике было, конечно, нельзя, но факт его существования доказал, что воду в принципе можно поднимать с помощью вакуума, созданного из пара.
Несколько лет спустя, в 1698 году, английский военный инженер Томас Севери разработал и первое практическое устройство, работавшее по такому принципу. Получившимся из пара вакуумом он поднимал воду на максимально возможный уровень, а затем использовал пар и по-другому: он добился такого высокого давления пара в замкнутом контейнере, что выпущенная из него струя пара могла подтолкнуть поднятый водяной столб еще выше. Главная проблема применения машины Севери заключалась в том, что нагнетание высокого давления в сосудах, созданных с использованием технологий конца XVII века, было делом весьма опасным. Всегда оставался немалый риск того, что сосуд взорвется и работники погибнут. Поэтому устройство Севери хоть и использовалось, но не очень широко, так как риск себя не оправдывал.
Однако еще десять лет спустя английский кузнец Томас Ньюкомен (вряд ли зная о существовании машины Севери) придумал насос, тоже работавший за счет свойств пара при атмосферном давлении. Сосуд наполнялся паром, затем остужался, потом еще раз наполнялся паром и опять остужался, и так постоянно. Иначе говоря, это был аналог ручного насоса, действовавший по принципу, открытому Папеном, где ручной труд по откачке воды заменяла энергия горящей древесины или угля.
Нагнетание высокого давления в этом механизме не использовалось, и благодаря своей сравнительной безопасности машина Ньюкомена стала очень популярной на шахтах, где постоянно требовалось откачивать воду. В 1778 году в одном только Корнуолле работало более семидесяти машин Ньюкомена.
Однако машина Ньюкомена работала медленно и к тому же крайне неэффективно. Топлива ей требовалось очень много, и больше 99 процентов энергии при ее работе просто терялось. В 1760-х годах английский гражданский инженер Джон Смитон доработал машину, удвоив ее эффективность (впрочем, и удвоенная, она оставалась все еще слишком низкой). Однако главный недостаток машины Ньюкомена состоял в ее чрезмерно узкой специализации. Ее нельзя было использовать ни для чего больше, кроме откачки воды.
Требовалось что-то большее, и вот на сцене появляется Джеймс Уатт.
В 1765 году шотландскому механику Джеймсу Уатту принесли в ремонт машину Ньюкомена. Он ее, конечно, починил, но даже после этого все равно остался недоволен работой устройства. Все воскресенье Уатт расхаживал в раздумьях, и вот ему показалось, что он нашел источник проблем с эффективностью. Ведь как работает механизм? Сначала пар нагревает стенки сосуда, потом сосуд охлаждается для получения вакуума — пока все правильно. Но вот уже на следующем цикле пар попадает в охлажденный сосуд и конденсируется на стенках. Лишь когда какое-то количество пара отдаст свое тепло стенкам сосуда, тогда сосуд нагревается настолько, что пар, попадая в него, остается паром. Таким образом, с каждым циклом огромное количество топлива тратится только на ликвидацию последствий действия холодной воды из предыдущего цикла — охлаждения стенок сосуда.
Уатт решил добавить еще один сосуд — «конденсатор», в который следовало впускать пар. Конденсатор следовало всегда оставлять холодным, а первый сосуд, «цилиндр», — всегда горячим. Таким образом, два процесса, нагрев и охлаждение, пере: стали мешать друг другу. К 1769 году Уатт уже создал работающую паровую машину, эффективность которой была гораздо выше, чем у любой из разновидностей машины Ньюкомена. Более того, поскольку при новой схеме исчезли долгие промежутки, требующиеся для нагрева сосуда между циклами, машина Уатта работала не только эффективнее, но и быстрее.
Уатт придумал и воплотил еще немало рационализации — например, пускать пар по очереди по обе стороны поршня. Раньше давление воздуха быстро толкало поршень в одном направлении, а затем постепенное нагнетание пара медленно двигало его обратно. Когда Уатт стал чередовать пуск пара по обе стороны поршня, атмосферное давление стало одинаково быстро толкать поршень в обе стороны, и эффективность машины в целом возросла еще больше. К 1790 году машина Уатта полностью вытеснила устаревшую машину Ньюкомена, и к 1800 году в Англии работало около пятисот машин Уатта.
Уатта принято считать изобретателем паровой машины. В строгом смысле слова это, конечно, не так. Однако подобную славу ему обеспечило не усовершенствование машины Ньюкомена, а тот факт, что Уатт оказался первым, кто сумел сделать из парового механизма нечто большее, чем просто насос. В 1780-х годах он разработал несколько устройств, в которых циклическое поступательное движение поршня преобразовывалось во вращательное движение колеса, и тем или иным образом паровой механизм стал использоваться для самых различных целей. Одними из первых его стали применять железолитейщики для раздувания мехов и снабжения энергией молотов, дробящих руду. Таким образом, паровая машина стала первым из так называемых сегодняшних «основных двигателей» — то есть общих способов извлекать энергию из ее природного состояния и использовать для работы механизмов. Так началась промышленная революция.
Паровую машину еще двести лет после Уатта постоянно дорабатывали и усовершенствовали. Однако в наши дома промышленная революция вошла не напрямую благодаря паровой машине, а через посредничество электричества.
О том, что электричество, как и пар, может содержать в себе энергию, люди знали еще в древности. Но в те времена это воспринималось как любопытная диковинка, не более. Только к 80-м годам XIX века были разработаны методы получения постоянного тока с помощью металлов и химических веществ. Для ученых такой электрический ток был крайне важным достижением, но получать его удавалось лишь в незначительном объеме, и для широкомасштабного использования электричество оставалось слишком дорогим.
В 1831 году английский ученый Майкл Фарадей открыл новый способ производства электрического тока. Он обнаружил, что если между полюсов магнита поместить медный диск, то при вращении этого диска (скажем, вручную) производится электрический ток. Так был изобретен электрогенератор. Оставалось только обеспечить генератору постоянное вращение силой воды или пара, чтобы получить много дешевого электрического тока без какого бы то ни было ручного труда.
Примерно в то же время американский физик Джозеф Генри обнаружил, что можно заставить электрический ток вращать колесо, и изобрел, таким образом, электромотор.
В итоге через несколько десятилетий доработок и усовершенствований стало возможным снабжать жилые дома дешевым электричеством благодаря Фарадею и использовать это электричество с помощью электромоторов благодаря Генри.
Ближе к концу XIX века выяснилось, что электрический ток состоит из частиц, которые можно перебрасывать через вакуум, точно контролируя силу и направление переброски с помощью электрических полей. Открытие этих частиц, получивших название «электроны», привело к появлению уже привычных нам электронных устройств, таких как радио или телевидение.
Если сравнить состояние, в котором пребывало человечество в 1750 году, сначала с каменным веком, а потом с современностью, то неизбежно приходишь к выводу, что, какое бы значение ни имели перемены, произошедшие до 1750 года, последние двести пятьдесят лет принесли изменения еще более радикальные и заметные.
Логично сделать вывод, что изо всех ключевых открытий, совершенных человеком за всю историю его существования, самыми важными были открытие огня и изобретение паровой машины. Первое вручило человеку ключ к энергии горения, второе научило использовать этот ключ для решения множества стоящих перед людьми задач.
Лично я вообще считаю, что история человечества — это в большей степени история развития способов использования энергии, а не список деяний королей и завоевателей.
Глава 3. ИЗМЕРЯЕМОЕ ДВИЖЕНИЕ
В новом научном подходе, выдвинутом Галилео Галилеем незадолго до 1600 года, ничего не говорилось напрямую о развитии прикладных аспектов использования человеком энергии. Так что это развитие можно считать случайным побочным продуктом общей теории.
Ученым этот новый, количественный подход был нужен в первую очередь для удовлетворения своего любопытства касательно принципов устройства Вселенной. Разумеется, если по ходу дела удавалось открыть или изобрести что-нибудь практически полезное — тем лучше.
Начали исследователи с изучения и измерения энергии в ее различных формах — в формах, которые человек и ранее использовал, не понимая их природы, как уже упоминалось. И то, что им удалось обнаружить, оказалось применимым не только к неживой природе, которую ученые столь кропотливо исследовали, но и к самому человеку.
Одним из самых очевидных видов энергии является движение, ведь именно движение напрямую переводится в деятельность, именуемую работой. Движение лопаты, вгрызающейся в землю, движение топора, срубающего ствол дерева, движение транспорта, перевозящего грузы, движение тарана, сокрушающего стену крепости, — все это наводит на мысль о неразрывной связи между движением и работой. Энергию движения принято называть кинетической энергией, от греческого слова, означающего движение.
В 1580-х годах Галилей провел ряд экспериментов с движущимися телами. Точных часов тогда еще не существовало, и ему приходилось выдумывать собственные способы измерения времени, например считать количество капель, вытекающих из сосуда с водой, или количество ударов собственного пульса. Для измерения времени движения свободно падающих тел такие методы не годились, поэтому Галилею пришлось вместо этого изучать движение шаров, скатывающихся вниз по наклонной плоскости. Уменьшая наклон плоскости, ученый добивался уменьшения скорости движения объектов до приемлемой. В остальном движение скатывающихся шаров вполне соответствовало движению падающих вниз предметов.
Результаты его опытов были систематизированы лишь сто лет спустя английским ученым Исааком Ньютоном, который представил миру то, что мы сейчас знаем как три закона Ньютона.
Первый закон основывался на наблюдении Галилеем того факта, что если пустить гладкий шар катиться по ровной гладкой поверхности, то его скорость уменьшается очень медленно, и тем медленнее, чем более ровной и гладкой будет поверхность.
Формулировка первого закона Ньютона гласит: «Всякое тело пребывает в состоянии покоя или равномерного движения, пока его не вынуждает к изменению этого состояния приложение внешних сил».
Но если по ровной поверхности шар катится (в идеальном случае) с неизменной скоростью, то с шаром, скатывающимся по наклонной поверхности вниз, а тем более — со свободно падающим предметом, дело обстоит иначе. Такие тела, как показали опыты Галилея, подвергаются ускорению, то есть по мере движения вниз их скорость постоянно возрастает. Путем точных измерений Галилей показал, что скорость таких тел возрастает прямо пропорционально времени, прошедшему с момента начала движения шара, а проходимое за единицу времени расстояние пропорционально квадрату этого времени.
Для любого изменения сложившейся ситуации требуется приложить усилия. Это, кажется, понятно любому. Чтобы сдвинуть предмет с места, необходимо приложить усилия. Чтобы остановить движущийся предмет, тоже нужно приложить усилия — чтобы понять это, достаточно попробовать бросить или поймать бейсбольный мяч.
Таким образом, любое изменение состояния, описанного в первом законе Ньютона, любое изменение скорости предмета или направления его движения является ускорением, и для его совершения требуется приложение силы. Каждый знает, что быстро летящий мяч поймать труднее, чем летящий медленно, и что бросить мяч так, чтобы он летел быстро, тоже сложнее. Однако каждый знает и то, что тяжелый предмет труднее остановить (и наоборот — сдвинуть с места), чем легкий. Гораздо легче остановить рукой мячик для настольного тенниса, чем летящий с такой же скоростью бейсбольный мяч. Свойство тела, характеризующее его способность ускоряться под действием заданной силы, называется «массой». Первым ясное представление о массе высказал Ньютон. Чем больше масса, тем меньшее ускорение может произвести заданная сила.
Общее представление о действии некоторой силы мы можем получить и из бытового опыта, но только благодаря количественным измерениям, произведенным Галилеем, Ньютон смог сформулировать свой второй закон, гласящий: «Сила, прилагаемая к телу, приводит к ускорению этого тела, прямо пропорциональному величине приложенной силы и обратно пропорциональному массе тела». Математическим языком это выражается так: а = f/m, или f = та, где f — сила, а — ускорение, а m — масса.
Луна хоть и движется непрерывно, но траектория ее движения — не прямая, а замкнутая кривая вокруг Земли. Скорость Луны подвергается постоянному ускорению, поскольку направление ее движения постоянно меняется, значит, на нее столь же постоянно должна действовать некая сила. Поскольку эта сила изменяет направление движения Луны в сторону Земли, то логично сделать вывод, что источник этой силы тоже находится где-то на Земле.
Ньютон сумел показать, что на Луну в ее небесных странствиях действует та же сила, что и на падающее на землю с постоянным ускорением яблоко. Таким образом, стало ясно, небесные тела управляются теми же законами природы, что действуют и здесь, на Земле, — стало быть, законы эти едины для всей Вселенной (по крайней мере, насколько мы ее знаем).
Ньютон предположил, что сила притяжения, влекущая яблоко к земле с равномерным постоянным ускорением и удерживающая Луну на замкнутой орбите вокруг Земли, является частным проявлением общего закона, по которому любой предмет во Вселенной притягивает все остальные предметы во Вселенной (закон всемирного тяготения).
Тогда ученый на основе выведенных им законов (включая третий, гласящий, что «каждое действие встречает равное ему по силе противодействие», пример практического применения которого мы видим всякий раз, когда в космос запускается очередная ракета) рассчитал, что такая всеобщая сила притяжения должна быть прямо пропорциональной массам обоих задействованных тел и обратно пропорциональной квадрату расстояния между их центрами:
f = mm'/d2
Оказалось, что открытый Ньютоном закон всемирного тяготения хорошо объясняет движение различных небесных тел. С его помощью представление о Вселенной стало простым и понятным. Для современной науки это стало важным достижением, навсегда освободившим человечество от благоговения перед достижениями древнегреческих авторов.
Правда, в XX веке была выдвинута другая, более сложная теория строения Вселенной, лучше объясняющая некоторые явления, относящиеся к сфере сверхмалых и сверхбольших частиц. Изменения произошли и в самой концепции силы и притяжения, а также и в концепциях движения, пространства и времени. Тем не менее для подавляющего большинства практических целей вполне достаточно и теории Ньютона.
После того как представление о количественном измерении движения прочно закрепилось в научном сознании, родился закономерный вывод, что работа тоже должна поддаваться измерению. Раз приложение к телу силы выводит его из «естественного состояния», то проще всего показалось измерить количество проделанной работы, умножив приложенную силу на то расстояние, на которое тело было перемещено против какого бы то ни было сопротивления.
Для того чтобы измерять такие явления, как сила и работа, требовалось введение новых, специализированных единиц измерения. Сами эти единицы многим незнакомы, но они выводятся из всем известных единиц измерения массы, расстояния и времени. Ведь все знают, что расстояние измеряется в метрах, сантиметрах и километрах, а масса — в граммах, килограммах и тоннах.
(Массу часто путают с весом, поскольку они имеют одинаковые единицы измерения, а массу определяют таким образом, чтобы ее единица на уровне земной поверхности соответствовала единице веса. Однако на самом деле вес — это то действие, которое оказывает на предметы сила земного тяготения, и по мере удаления от центра земли он уменьшается.
Масса же определяет сопротивляемость тела ускорению под действием заданной силы и никакого отношения к силе земного тяготения не имеет. Соответственно на Луне, где сила тяготения в шесть раз меньше, чем на Земле, предмет, весящий у нас шесть килограммов, будет весить всего один, но при этом масса его все равно будет равна шести килограммам. По весу предмет будет казаться легче, но придать ему заданное ускорение на Луне будет так же тяжело, как и на Земле.)
Скорость — это показатель, описывающий перемещение предмета в заданном направлении за некий промежуток времени. Основными принятыми в науке единицами скорости являются сантиметры в секунду и метры в секунду.
Ускорение — это изменение скорости, происходящее со временем. Предположим, что скорость некоего предмета равномерно увеличивается. Если сейчас он движется со скоростью 1 см/сек, то секунду спустя его скорость будет уже 2 см/сек, еще через секунду — 3 см/сек и т. д. Каждую секунду его скорость возрастает на 1 см/сек, то есть мы можем сказать, что предмет этот движется с ускорением 1 сантиметр в секунду в секунду, или 1 см/сек/сек.
С такими записями позволительно обращаться так, как если бы это были простые математические формулы. То есть, рассматривая см/сек/сек как a/b/b, мы можем привести его к виду a/b ÷ b, то есть а/b х 1/b, или а/b2. Точно так же 1 см/сек/сек можно записать как 1 см/сек2 («сантиметр на секунду в квадрате»). Или если расстояние измерять в метрах, то 1 м/сек2.
Согласно второму закону Ньютона, сила равна массе, помноженной на ускорение (ранее в этой главе я уже указывал, как вы помните, эту формулу: f = ma).
Тогда если ускорение измеряется в см/сек2, то, умножив его на массу ускоряемого тела, измеряемую в граммах, мы и получим искомую силу в таких единицах, как г ∙ см/сек2.
Для краткости эта единица получила название «дина» (от греческого слова, означающего силу). Соответственно 1 дина может быть определена как количество силы, приложение которого к массе в 1 грамм придаст этому телу ускорение в 1 сантиметр в секунду в квадрате. То есть, 1 дина = = 1 г ∙ см/сек2.
А единица кг ∙ м/сек2 получила название «ньютон». Поскольку килограмм — это 1000 граммов, а метр — 100 сантиметров, то 1 кг ∙ м — это 1000 х 100 = = 100 000 г ∙ см. Соответственно 1 кг ∙ м/сек2 = = 100 000 г ∙ см/сек2, то есть 1 н = 100 000 дин.
Теперь перейдем к работе. Работу можно представить как приложение некоей силы на протяжении некоего расстояния. Если взять за единицу силы 1 дину, то есть г ∙ см/сек2, и умножить на расстояние, измеряемое в сантиметрах, то получим единицу измерения в г ∙ см2/сек2. Физики назвали эту единицу «эрг», от греческого слова, означающего работа.
Иными словами, вы выполняете 1 эрг работы, когда прилагаете к некоему телу силу в 1 дину при перемещении на 1 сантиметр. 1 эрг = 1 дин ∙ см = 1 г — см2/сек2.
Если же измерять силу в ньютонах, то есть кг ∙ м/сек2, и умножать ее на расстояние в метрах, то получится единица кг ∙ м2/сек2. Она получила название «джоуль» в честь физика, о котором я еще буду рассказывать.
Один джоуль работы подразумевает приложение силы в 1 ньютон на протяжении 1 метра. То есть 1 дж = 1 Н ∙ м = 1кг ∙ м2/сек2.
Поскольку 1 ньютон равен 100 000 дин, а метр — 100 сантиметрам, то 1 Н ∙ м равен 10 000 000 дин∙см, то есть 1 джоуль равен 10 000 000 эрг.
С переходом таких явлений, как сила и энергия, в количественное русло стало понятно не только каким образом изменяются некоторые явления в природе, но и то, почему они иногда не изменяются.
Очевидно, что движущееся тело совершает работу, а следовательно, обладает кинетической энергией («энергией движения»). Из законов Ньютона, а также из определений силы и работы следует, что кинетическую энергию тела можно представить в следующем виде:
Ek = 1/2 ∙ mv2,
где Ek обозначает кинетическую энергию, т — массу, a v — скорость.
Теперь предположим, что 10-килограммовый железный шар подбросили вверх со скоростью 49 метров в секунду. В момент броска его кинетическая энергия — 1/2 х 10 х 49 х 49 = около 12 000 джоулей.
Однако по мере движения шара вверх давящая его вниз сила тяжести постоянно снижает скорость полета. Секунду спустя он движется уже со скоростью 39,2 метра в секунду, две секунды спустя — 29,4 метра в секунду. Пять секунд спустя, на высоте 122 метра, скорость его станет равной нулю (по крайней мере, по отношению к земной поверхности). На мгновение он зависнет в этой точке.
Вместе со скоростью уменьшается и кинетическая энергия предмета. В тот момент, когда он остановится и зависнет в воздухе, кинетическая энергия его будет равняться 1/2 х 10 х 0 х 0, то есть, разумеется, нулю.
Как же может энергия так резко уменьшаться и в конце концов вообще исчезать по мере продвижения предмета вверх? Она что, навсегда пропадает? Нет, конечно, поскольку железный шар, достигнув вершины своей траектории, начинает падать вниз — сначала медленно, а потом — все быстрее и быстрее, влекомый силой тяжести. Достигнув вновь уровня поверхности земли, он набирает ту же скорость, с которой вылетал вверх (пренебрежем пока сопротивлением воздуха), только направление его движения теперь будет противоположным.
Он снова движется со скоростью 49 метров в секунду и снова обладает кинетической энергией в 12 000 джоулей. К нему вернулась вся кинетическая энергия, которой он обладал вначале. Так где же была эта энергия в верхней точке полета?
Чтобы ответить на этот вопрос, придется представить, что предметы могут обладать энергией просто в силу своего положения. Камень, лежащий на вершине скалы, казалось бы, никакой энергией не обладает. Он может вечность пролежать на одном месте, не выполняя никакой работы. Если же его столкнуть со скалы, он наберет по мере падения скорость (а значит — и кинетическую энергию) и может убить человека. Энергия, происходящая из положения предмета, именуется «потенциальной энергией» (ее можно обозначить как Е), поскольку никак не проявляется, пока ей не предоставят для того условия, то есть является не действительным свойством предмета, а лишь потенциальным.
По мере подъема вверх железный шар (или камень, в общем, любой предмет) теряет кинетическую энергию, приобретая взамен потенциальную. В наивысшей точке подъема вся кинетическая энергия тела переводится в потенциальную. Затем, по мере падения, вся потенциальная энергия постепенно переходит обратно в кинетическую, и в момент приземления вся энергия тела снова приходит в кинетическую форму. На самом деле, если взять любую промежуточную точку на траектории полета шара, то окажется, что, падая с этой высоты, шар наберет к моменту приземления столько же кинетической энергии, сколько он потерял, долетая до этой высоты снизу. То есть в любой точке полета общее количество кинетической и потенциальной энергии тела остается неизменным.
В общем, энергия не появляется ниоткуда и не исчезает никуда. Она все время присутствует в неизменном объеме, переходя из одной формы в другую. Энергия сохраняется. Если объединить понятия кинетической и потенциальной энергий в едином понятии «механической энергии» (Еm), то мы можем говорить о законе сохранения механической энергии.
Перед нами — пример постоянства в природе, который в принципе невозможно было заметить и оценить, пока человек не взялся за точное измерение явлений.
Конечно, это не значит, что прямо так уж вся потенциальная энергия переходит в кинетическую, когда предмет падает на поверхность земли. Может, он больше и не упадет и не проделает никакой работы, но, если выкопать шахту глубиной в тысячу метров, предмет, казалось бы исчерпавший всю потенциальную энергию падения, вдруг обретет способность падать дальше и проделать таким образом еще какой-то объем работы. Эта дополнительная потенциальная энергия — она что, взялась ниоткуда?
Нет, это вопрос точки отсчета. Находящийся на вершине скалы камень обладает большой потенциальной энергией относительно поверхности Земли; но куда большей потенциальной энергией он обладает относительно центра Земли, ведь если бы существовала достаточно глубокая шахта, то после достижения поверхности Земли этот камень мог бы пролететь еще шесть с половиной тысяч километров. И, даже находясь в самом центре Земли, предмет все равно будет обладать потенциальной энергией относительно Солнца, а сам центр Солнца обладает потенциальной энергией относительно центра Галактики. Нигде во всей Вселенной потенциальная энергия предметов не равна полному нулю, и это отсутствие «абсолютных рамок относительности» и является одним из основных положений теории относительности Эйнштейна.
Однако для нас отсутствие абсолютной системы координат не имеет значения. Интерес для физиков, таким образом, представляют не абсолютные значения, а разница потенциальных. То есть предмет на вершине километровой скалы обладает большей потенциальной энергией, нежели такой же предмет, находящийся у подножия этой скалы, и эта разница остается неизменной для нас, находящихся на планете Земля. Для математического удобства примем потенциальную энергию на уровне поверхности Земли за ноль, тогда за потенциальную энергию на любой высоте логично будет принять разность потенциальных энергий на этой высоте и на поверхности Земли, поскольку х — 0 = х.
Кинетическую энергию можно рассчитывать таким же образом, не как абсолютную величину, а как разность величин, и выходит, что механическая энергия сохраняется независимо от выбора точки отсчета.
Еще одним интересным свойством потенциальной энергии является тот факт, что она зависит только от положения, и никоим образом не от того пути, которым это положение было достигнуто! Представьте себе три пушечных ядра одинакового веса, находящиеся на вершине скалы. Одно попало туда путем выстрела из пушки таким образом, что вершина скалы оказалась наивысшей точкой траектории его полета. Второе долго катили вверх по длинной извилистой горной дороге. Третье подняли на самолете на высоту тридцати километров и спустили на вершину скалы на длинном канате.
Если же теперь все три ядра сбросить со скалы, думаете ли вы, что то, которое катили долго и спокойно, будет обладать меньшей потенциальной энергией? Или что то, которое набрало в свое время огромную потенциальную энергию, поднявшись в самолете, будет обладать большей?
Нет, потенциальная энергия всех трех ядер будет одинаковой — на ее количество влияет только их положение в данный момент. Прошлые заслуги тут бессильны.
Точно таким же образом представим, что одно из ядер просто уронили вниз, а второму дали скатиться по длинному пологому спуску (с условием, что трение отсутствует). Катящийся шар будет ускоряться гораздо медленнее, но зато он будет ускоряться и гораздо дольше; так что к моменту достижения поверхности Земли его скорость и кинетическая энергия будут равны скорости и кинетической энергии того ядра, которое просто бросили вниз. Если взять третье ядро и скатить его вниз по неровной горке, на которой спуск перемежается с небольшими подъемами, все равно в нижней точке его кинетическая энергия окажется такой же, как у двух предыдущих.
В отношении любого сохраняемого свойства предмета, каким является и механическая энергия, верно следующее: когда предмет переходит из состояние A в состояние B, изменения в сохраняемом свойстве зависят только от природы состояний A и B и не зависят от того способа, которым предмет перешел из состояния А в состояние В.
Физикам приятно ощущать сохранность определенных свойств, и они всегда ищут примеры таких свойств.
Возьмем два неупругих тела, то есть таких, которые при столкновении не отскочат друг от друга, а сплющатся и останутся на месте. Примерами таких тел могут послужить два комка размягченного воска или сырой глины.
Теперь представим, что два восковых шара одинакового размера катятся навстречу друг другу с равной скоростью (скажем, 2 метра в секунду) по некоей ровной, абсолютно гладкой (то есть лишенной трения) поверхности. Они сталкиваются, слипаются и останавливаются. Очевидно, что скорость движения каждого из них стала нулевой, сложившись со скоростью движения второго.
Приняв скорость одного шара за +2 м/сек, то скорость второго, движущегося в обратном направлении, естественно, надо будет принять за -2 м/сек. Сложение этих двух скоростей дает ноль как до столкновения, так и после него.
Если удовольствоваться одним только этим наблюдением, можно сделать вывод о том, что сохраняющимся свойством в таких условиях является скорость; что алгебраическая сумма скоростей составляющих системы должна оставаться неизменной, вне зависимости от отношений между составляющими внутри самой системы.
Но предположим теперь, что только что упомянутые восковые шары — разного размера. Допустим, что тот, что катится влево, — в три раза тяжелее того, что катится вправо, а скорости их при этом равны и составляют все те же 2 м/сек. Сумма скоростей по-прежнему равна нулю, но после столкновения и слипания эти тела не остановятся. Вместо этого объединенный комок продолжит движение в том же направлении, в котором двигался больший шар, но уже со скоростью 1 м/сек. Общая скорость системы в таком случае не сохранилась.
В 1671 году английский физик Джон Валлис указал, что сохраняющимся свойством в таком случае является не скорость сама по себе, а произведение скорости и массы, mv, и назвал эту величину «импульсом».
Поясним на примере двух разных шаров: допустим, что один из них весит 2 грамма, а второй — 6 граммов. Если они движутся навстречу друг другу со скоростью 2 м/сек каждый, то, несмотря на то что их скорости равны (если не считать разницы направлений движения), импульсы их не равны. Импульс первого шара равен 2 умножить на 2, то есть 4 грамм∙метра в секунду (г∙м/сек), а импульс второго — 6 умножить на 2, то есть 12 г∙м/сек. Возьмем импульс большего шара за положительную величину, импульс второго, движущегося в противоположном направлении, — за отрицательную, тогда суммарный импульс всей системы до столкновения будет равен + 12 — 4, то есть +8 г∙м/сек.
После столкновения объединенный комок воска будет весить 8 граммов и двигаться в направлении движения большего из первоначальных шаров, соответственно его импульс будет положительным и равным 8 умножить на 1, то есть +8 г∙м/сек.
Как доказывают эксперименты, при таких условиях импульс всегда сохраняется. Импульс сохраняется и в том случае, когда сталкиваются два упругих шара (например, стеклянных или стальных, то есть таких, которые не слипаются, а разлетаются в разные стороны), только не надо забывать о том, что если мы принимаем импульс при движении в одну сторону за положительный, то импульс при движении в другую сторону следует принимать за отрицательный. Существуют даже общепринятые геометрические способы разделения движения в любом направлении на положительную и отрицательную составляющие, и при их применении оказывается, что импульс сохраняется даже при столкновении тел, движущихся не лоб в лоб, а под углом, или при столкновении более чем двух шаров, как, например, при разбивании пирамиды в бильярде.
Возьмем, например, такую систему, как заряженное ружье. Если подвесить его на шнуре, момент в покоящемся состоянии будет равным нулю. Однако теперь предположим, что на спусковой крючок очень тихо и незаметно (не покачнув ружья) нажали. Тогда одна часть системы (пуля) вылетит из ствола, имея высокую скорость и достаточно большой импульс. Единственным способом сохранить общий импульс для системы будет движение второй ее части, самого ружья, в противоположном направлении, с импульсом равным импульсу вылетевшей пули. Поскольку ружье во много раз тяжелее, чем пуля, то и придаваемая ему для уравновешивания импульса скорость будет во много раз меньше.
Угловой импульс (произведение массы на вращательное движение) тоже сохраняется. Самой красивой иллюстрацией тому может послужить вращение фигуристки, которая кружится так быстро, как только может. Каждая часть ее тела обладает определенным угловым импульсом, в зависимости от скорости движения этой конкретной части тела — чем дальше от центральной оси вращения, тем быстрее движение. У нашей фигуристки с наибольшей скоростью будут двигаться вытянутые в стороны руки.
Если фигуристка прижмет руки к телу, они потеряют угловой импульс, поскольку окружность, расстояние, которое они преодолевают за один оборот, станет меньше, а значит, и скорость их движения уменьшится. Однако ведь угловой импульс должен быть сохранен! Если одна часть системы его теряет, другая должна приобретать. Так и здесь — если фигуристка прижимает руки к телу, само тело начинает вращаться еще быстрее, и выступающая становится похожей на волчок.
К сожалению, сохранение механической энергии и импульса полностью может осуществляться только в идеальной ситуации, в которой нет ни сопротивления воздуха, ни трения. На Земле такого не бывает нигде. В идеальных условиях отсутствия трения и сопротивления маятник никогда не перестанет качаться, мячик — прыгать, бильярдные шары будут вечно кататься и сталкиваться, а фигуристка продолжит кружиться, пока ей самой не надоест и она не остановится, сознательно приложив к этому усилия.
Ничего подобного мы наблюдать не можем. Когда мяч бросают в воздух, не вся его потенциальная энергия переходит в кинетическую — часть ее потратится на преодоление сопротивления воздуха. А когда он станет падать обратно, опять же не вся его потенциальная энергия перейдет в кинетическую — часть ее съест трение. После того как шар ударится о землю и отскочит от нее, в момент удара еще часть энергии потеряется, поскольку ни шар, ни земля никогда не являются абсолютно упругими. На практике ни одна, даже наилучшим образом продуманная, система не может избежать подобного рода потерь, так что полностью импульс никогда не сохраняется.
Далее, из-за наличия трения вопрос о том, каким именно образом механическая энергия или импульс перешли из состояния А в состояние В, приобретает значение. Ядро, сброшенное со скалы, падая вниз, потеряет небольшое количество энергии из-за сопротивления воздуха. Такое же ядро, которое пустили скатываться вниз по пологому спуску (не идеально гладкому, как я предположил ранее, а реальному, где присутствует трение), прибудет на поверхность земли, обладая меньшим количеством кинетической энергии, чем тело, падавшее свободно. Чем положе спуск и чем длиннее путь качения, тем больше будет трение и тем меньшим станет в итоге количество кинетической энергии тела.
При расходе энергии вырабатывалось тепло, а теплом ученые всерьез заинтересовались лишь тогда, когда появление паровой машины ясно показало, что тепло — это одна из форм энергии, которую можно перевести в работу так же однозначно и безошибочно, как и кинетическую энергию. И только постигнув природу тепла, физики смогли работать с реальным миром, а не с идеальным, существующим только в их воображении.
Глава 4. ИЗМЕРЯЕМОЕ ТЕПЛО
Ученые древности не могли четко уяснить себе, что же такое тепло, кроме того, что это нечто, к чему чувствителен человеческий организм. Что не мешало им, однако, исследовать это явление, причем даже с некоторым успехом.
Прежде всего, они научились измерять силу тепла — то есть температуру. Ведь наши ощущения дают нам некоторое представление о силе тепла, а не о его общем количестве. Мы различаем холодные и горячие предметы, но не можем сказать, сколько в том или ином предмете содержится тепла. Например, его гораздо больше в ванне с холодной водой, чем в капле кипятка, но при этом вода в ванне кажется нам холодной, а капля кипятка — горячей. В капле выше насыщенность теплом — то есть больше тепла содержится в заданном объеме жидкости.
Это крайне важный элемент устройства всей Вселенной, поскольку в ней тепло перетекает от более горячих объектов (с более высокой температурой) к более холодным (с более низкой температурой), а не от объектов, содержащих больше тепла, к объектам, содержащим меньше тепла. Так, если каплю кипятка капнуть в ванну с холодной водой, то тепло перейдет из капли (которая моментально остынет) в ванну (которая нагреется на незаметную величину).
Если вы не уверены, что поняли суть идеи, то представьте себе аналогию с течением воды. В горной речке воды гораздо меньше, чем в океане, но горная речка находится на большей высоте и обладает большей потенциальной энергией, чем океан. И вода течет не из океана, где ее много, в речку, где ее мало, а наоборот — из маленькой речки, находящейся высоко в горах, в океан, находящийся внизу.
Народная мудрость гласит, что вода всегда течет вниз — это частное проявление закона о том, что любое самопроизвольное движение происходит в направлении уменьшения потенциальной энергии.
Температура является для тепла тем же, чем потенциальная энергия — для массы. Тепло переходит от горячих предметов к холодным так же, как вода стекает вниз. Лично я с удовольствием заменил бы слово «температура» на «тепловой потенциал» — называем же мы движущую силу электрического тока «электрическим потенциалом», зная, что электричество всегда течет из точки с высоким потенциалом в точку с низким.
Потенциальную энергию тела мы можем узнать, измерив высоту его положения над уровнем моря. А можно ли как-то измерить температуру? Первым принцип ее измерения придумал Галилей. Практически все вещества расширяются при нагревании и сжимаются при охлаждении. И в 1592 году Галилей изобрел «воздушный термометр», в котором, в зависимости от температуры, измерялся объем воздуха, что приводило к изменению уровня воды в трубке. К сожалению, на уровень воды в трубке влиял также и такой параметр, как атмосферное давление, так что показатели такого термометра были ненадежными.
За этим термометром последовали другие, закрытые, на которые атмосферное давление уже не влияло. В таких термометрах жидкость заливали в колбу, и она частично заполняла тоненькую запаянную капиллярную трубку таким образом, что даже небольшие изменения общего объема жидкости заметным образом сказывались на уровне этой жидкости в трубке. Изменения уровня и отражали изменения температуры.
В 1715 году немецкий физик Габриэль Даниэль Фаренгейт впервые использовал в качестве жидкости, уровень которой изменялся в тщательно градуированной трубке термометра, ртуть. Таким образом и был изобретен инструмент, которые мы до сих пор пользуемся в неизменном виде. В Соединенных Штатах, Великобритании, Канаде, Южной Африке, Австралии и Новой Зеландии до сих пор используется и шкала Фаренгейта, разработанная им самим. На этой шкале температуре таяния льда соответствует показатель 32 градуса (обозначается 32°), а температуре кипения воды — 212°. Шкала обозначается буквой F после цифр.
В других странах, а также в научной среде используется десятичная шкала, которую разработал шведский астроном Андерс Цельсий, где температура таяния льда взята за 0°, а температура кипения воды — за 100°. Шкала Цельсия обозначается буквой С после цифр.
Изобретение термометра позволило получить некоторые данные не только о температуре, но и о количестве тепла, содержащегося в веществе.
Предположим, что литр спирта нагрели до 60°, а затем быстро перемешали с литром воды температурой 20°. Тепло, естественно, перейдет от горячего спирта к холодной воде. По ощущениям понятно, что температура получившейся смеси — «что-то среднее» между горячим спиртом и холодной водой. Естественно предположить, что она будет представлять собой среднее значение, и если бы не было термометра, то исследовать этот вопрос глубже не удалось бы.
Однако, когда оказалось, что температуру можно измерить, «ощущение чего-то среднего» перестало удовлетворять нас как показатель температуры итоговой смеси. Напрашивалось предположение, что, перемешав равные объемы жидкости с температурой 20° и 60°, мы получим в итоге смесь с температурой 40°, однако оказалось, что это не так. Температура получившейся в итоге смеси воды со спиртом оказалась всего 36°.
Почему? Очевидно, что количество тепла, содержащегося в нагретом до определенной температуры спирте, меньше, чем количество тепла, содержащегося при тех же условиях в воде. Другими словами, количество тепла, необходимого для нагрева спирта на 10°, меньше, чем количество тепла, необходимого для нагрева на эту же температуру воды. И наоборот, количество тепла, отдаваемого спиртом при охлаждении на 10°, меньше, чем количество тепла, отдаваемого при этом же процессе водой. Можно использовать аналогию, представив, будто вода и спирт — это широкий и узкий сосуды с водой. Для того чтобы в широком сосуде уровень воды поднялся на 5 сантиметров, нужно больше воды, чем для того, чтобы добиться того же самого в узком. Если уровень воды в обоих сосудах будет одинаковым, то в широком жидкости будет больше. Так и здесь — если нагреть воду и спирт до одной и той же температуры, вода будет содержать при этом больше тепла.
Тогда загадка низкой температуры смеси спирта и воды объясняется. Тепла, высвобождаемого при охлаждении алкоголя на 24° (с 60° до 36°), достаточно ровно для того, чтобы нагреть равный объем воды лишь на 16° (с 20° до 36°), и в итоге мы получаем температуру общей смеси 36°.
Шотландский физик Джозеф Блэк стал первым исследователем данного явления. К 1760 году он провел множество экспериментов по измерению количества тепла, необходимого для того, чтобы нагреть определенное количество различных веществ на определенное количество градусов. Это свойство ученый назвал «удельной теплоемкостью» вещества.
За единицу была взята теплоемкость воды. Для нагревания спирта требуется 2/3 от количества тепла, необходимого для нагревания воды.,. Значит, теплоемкость спирта — приблизительно 0,65. Теплоемкость еще одной жидкости, ацетона, — 0,5 и так далее.
Обнаружилось, что теплоемкость воды очень велика; она оказалась одной из самых высоких вообще. А у большинства металлов теплоемкость оказалась крайне низкой: теплоемкость алюминия — 0,22; меди — 0,093; свинца — 0,031. Мы и из бытового опыта знаем, как быстро раскаляется на газу пустая алюминиевая кастрюля и как долго нагревается даже небольшое количество воды.
Точности ради надо добавить, что на измерение теплоемкости влияет также и температура измеряемого вещества — горячее вещество имеет большую теплоемкость, чем холодное.
Все эти эксперименты не могли не привести к необходимости разработки единиц измерения количества тепла (не путать с температурой!).
За такую единицу было взято количество тепла, необходимое для того, чтобы нагреть 1 грамм воды с 14,5° до 15,5°. Единица эта получила название «калория», от латинского слова, означающего «тепло». Естественно, используется также и более крупная единица — килокалория, это то количество тепла, которое необходимо, чтобы нагреть 1 килограмм воды опять же с 14,5° до 15,5°. Килокалория в тысячу раз больше, чем калория.
Зачастую в обиходе последнюю тоже называют «калорией», и это приводит к путанице. Особенно часто неправильным использованием слова «калория» злоупотребляют диетологи, подразумевая под ним конечно же «килокалорию».
Но вернемся к Джозефу Блэку. Ему принадлежит честь совершения еще одного важного открытия в области изучения тепла. Он обнаружил, что лед при нагревании плавится, но при этом образующаяся в процессе смесь воды и льда не начинает нагреваться до тех пор, пока не растает весь лед. Количество теплоты, затраченной на процесс таяния льда, оказалось таким, что если бы оно пошло на нагревание такого же количества ледяной воды, то вода нагрелась бы почти до точки кипения. На то, чтобы растопить один грамм льда, тратится 80 калорий. Блэк описал эту теплоту как «латентную», то есть «скрытую», «невидимую», поскольку теплозатраты не отражаются на подъеме температуры. Как и слово «потенциальный» в словосочетании «потенциальная энергия», дополнительное определение было введено для обозначения чего-то, что присутствует неочевидным образом. В современной физике эту теплоту называют «теплотой плавления» (в данном случае «плавление» равнозначно «таянию»).
Существует еще одна форма латентной теплоты — это теплота, затраченная на кипячение жидкости. При добавлении теплоты к кипящей жидкости ее температура не растет, жидкость просто кипит, пока не выкипит до конца. На кипячение тратится еще больше тепла, чем на таяние. Так, на выпаривание одного грамма нагретой до 100° воды тратится около 540 калорий, а в результате получается один грамм пара той же температуры. Это «теплота кипения».
Кроме того, Блэк обнаружил, что при замерзании воды (или конденсации пара обратно в воду) латентная теплота выделяется обратно. Вещество поглощает тепло при таянии и выделяет при замерзании, поглощает при испарении и выделяет при конденсации. Этот процесс напоминает переход энергии из кинетического в потенциальное состояние и обратно, что позволило выдвинуть предположение о том, что тепло — это сохраняемое явление или, как минимум, является частью некоего составного сохраняемого явления.
Значит, чтобы изменение температуры можно было представить с помощью измененной объема жидкости, объем жидкости должен изменяться равномерно. Иначе промежутки между градусами на шкале термометра были бы неравномерными. Равномерность изменений объема — ни в коем случае не само собой разумеющееся явление. Например, вода по мере нагревания расширяется неравномерно. На самом деле на промежутке от 0 до 4 градусов вода даже сжимается с повышением температуры. А вот ртуть, как оказалось, расширяется вполне равномерно, и это — одна из причин, по которой именно ртуть используют в градусниках.
Сначала изучению подвергались, естественно, те жидкости, которые используются в градусниках. Неудачная попытка Галилея создать газовый термометр казалась забытой, и последующие двести лет изучению влияния изменения температуры на газы уделялось крайне мало внимания.
Так, в 1660 году английский физик Роберт Бойль первым показал, что давление и объем заданного количества газа находятся в обратно пропорциональном отношении (закон Бойля). Если удвоить давление на газ, его объем уполовинится; если утроить давление — объем сократится втрое, и так далее. Это один из краеугольных камней современной химии, но Бойль забыл указать, что это соотношение верно только при неизменной температуре. Очевидно, температура и ее влияние на объем газов не входили в сферу его интересов.
Примерно в 1680 году французский физик Эдм Мариотт независимо от Бойля заново открыл его закон, и вот он уже отметил, что на объем газа оказывает влияние также и температура. В Европе закон Бойля называют законом Мариотта, в русскоязычной же терминологии этот закон носит двойное название — закон Бойля—Мариотта.
Следующий шаг совершил в 1699 году французский физик Гийом Амонтон, отметив, что изменение температуры на заданную величину приводило к одинаковому в процентном соотношении расширению различных масс воздуха.
Однако лишь в 1787 году этот вопрос подвергся точному измерению. Французский физик Жак Александр Сезар Шарль окончательно продемонстрировал, что газы расширяются и сокращаются равномерно по мере измерения их температуры (закон Шарля) — два века спустя после того, как Галилей интуитивно догадался о том же самом и создал свой термометр.
Шарль выяснил, что газ (а лишь в XVIII веке впервые было установлено существование иных газов, кроме воздуха) расширяется примерно на 1/273 от своего объема при 0° с повышением температуры на каждый градус. Соответственно при понижении температуры на 1º газ сокращался в объеме на 1/273 от своего объема при 0°.
То есть если мы возьмем 273 литра газа при температуре 0° и начнем нагревать, то его объем вырастет до 274 литров при Г, до 275 — при 2°, до 276 — при 3°, и так далее. И наоборот, при -1º объем газа сократится до 272, при -2° — до 271, при -3° — до 270, и так далее.
Если предположить, что закон Шарля верен до самого конца, то при -273° объем газа станет равным нулю, а при более низких температурах величина объема газа примет отрицательное значение, чего быть не может в принципе.
Физиков такие расчеты не особенно изумляли, поскольку основывались на предположении, что закон Шарля верен и для сверхнизких температур, хотя имелись некоторые признаки, позволяющие предположить, что это не так. Во времена Шарля и еще столетие спустя получение действительно низких температур было делом невозможным, и проверить действие закона в таких условиях соответственно было нельзя. Однако уже к 1900 году стало ясно, что задолго до -273° все газы конденсируются в жидкости, а на жидкости закон Шарля не распространяется. Так что — никакого парадокса.
Тем не менее температура в -273° действительно оказалась неким критическим значением, и ученые считают ее абсолютным нулем, точкой, ниже которой температура опуститься не может в принципе. Сейчас самым точным значением абсолютного нуля называют -273,16°, но мы позволим себе округлить это значение. Абсолютный ноль — это температура, при которой тело вообще не содержит тепла. Если принять ее за ноль и отсчитывать от нее привычные нам градусы по Цельсию, то получится, что вода замерзает при 273°, закипает при 373° и так далее. Это — абсолютная шкала температуры (рис. 3).
В 1848 году английский физик Уильям Томсон (позже он получит статус пэра, и нам он сейчас более известен как лорд Кельвин) установил эту систему на прочную теоретическую основу. Поэтому абсолютную шкалу чаще называют «шкалой Кельвина», и, скажем, температуру замерзания воды по ней можно обозначить и как 273 °А, и как 273 °К, причем последнее обозначение встречается чаще.
На шкале Фаренгейта абсолютный ноль — это -460 °F (точнее, -459,69 °F), и можно взять эту точку за ноль, а дальше отсчитывать от нее градусы по Фаренгейту. Первым, кто стал пользоваться такой шкалой, был шотландский инженер Уильям Джон Макуорн Ранкин, и шкала эта теперь называется «шкалой Ранкина». Точка замерзания воды на этой шкале будет равна 492 °Rank, а точка кипения воды — 672 °Rank.
Рис. 3. Различные виды температурных шкал
(Название шкалы не сокращается до «R», как можно было бы ожидать, потому что существует еще шкала температуры по Реомюру, которую разработал французский физик Рене Антуан Фершо де Реомюр в XVIII веке, и буквой «R» обозначается именно она. На шкале Реомюра точка замерзания воды — 0 °К, а точка кипения воды — 80 °R. Шкала Реомюра никогда не пользовалась особой популярностью и сейчас представляет сугубо исторический интерес.)
Когда температура и содержание тепла стали легкоизмеримыми явлениями, ученые радостно приняли их под свое крыло и стали по-новому смотреть на энергию. С наступлением XIX века энергию перестали рассматривать как нечто неотрывное от движения. Усиленное внимание к механической энергии привело к замечательным достижениям в XVII и XVIII столетиях, но теперь требовалось нечто большее.
Паровая машина ясно продемонстрировала, что тепло может совершать работу так же, как и падающее тело, и что теплоту соответственно можно считать одной из форм энергии. Магнетизм тоже был признан одной из форм энергии (собственно, в некоторой степени это было ясно уже в Средние века), а проводимые в XVIII веке эксперименты с электричеством показали, что оно тоже является формой энергии.
Само слово «энергия» ввел в науку в 1807 году английский физик Томас Юнг. Наиболее важные из его исследований касались света — еще одной из форм энергии. За несколько десятилетий термин «энергия» расширился до его сегодняшнего понимания и стал означать все, что может производить работу.
Многие ученые стали понимать, что закон сохранения энергии казался нечетко соблюдаемым просто потому, что при оценке не учитывались некоторые из ее форм, в первую очередь — тепло. Так, например, стало ясно, что потери механической энергии при трении сопровождаются выработкой тепла, а значит, вполне возможно, что потери механической энергии уравновешиваются производством энергии тепловой?
В этом отношении выдающимся экспериментатором был английский физик Джеймс Прескотт Джоуль, занимавшийся изучением того, сколько тепла может произвести тот или иной объем работы. Если закон сохранения энергии действительно верен, то при точном учете всех ее форм заданный объем работы должен приводить к образованию одного и того же количества тепла, независимо от того, какая форма энергии использовалась при совершении работы.
Джоуль начал свои измерения в 1840 году и продолжал их на протяжении десятилетий. Он производил тепло различными способами — путем пропускания электрического тока через проволоку, путем наливания воды в тонкие стеклянные трубки, взбивая лопастями сначала воду, потом масло, потом ртуть, путем трения чугуна, путем пропускания электричества напрямую через раствор, путем вращения проволочной спирали между полюсами магнита…
И каждый раз он подсчитывал количество совершенной работы и количество произведенной при этом теплоты и обнаруживал, что одно и то же количество работы, независимо от источника энергии, всегда приводило к образованию одного и того же количества теплоты. Таким образом Джоуль разработал «механический эквивалент теплоты». Оказалось, что 1 калории тепла соответствует примерно 41 800 000 эрг. работы. В честь Джоуля его именем назвали единицу в 10 000 000 эрг., так что мы можем сказать, что 1 калории соответствует 4,18 джоуля.
Джоулю в 1840-х годах казалось ясным, что в реальном мире энергия действительно сохраняется, если учитывать все без исключения ее формы. По крайней мере, ему не встретилось ни одного случая, где энергия бы не сохранялась. И в течение того же самого десятилетия то же самое поняли и двое немецких ученых — Юлиус Роберт фон Майер и Герман Людвиг Фердинанд фон Гельмгольц.
Сегодня именно Гельмгольцу принято отдавать пальму первенства в отношении точной и однозначной формулировки принципа сохранения энергии. Этот принцип ученый изложил в книге, изданной им в 1847 году. Согласно содержанию этого научного труда энергию невозможно ни создать, ни уничтожить, она может только переходить из одной формы в другую. Иными словами, общее количество энергии во Вселенной неизменно и никогда не было и не будет иным; нельзя сделать его ни на йоту больше и ни на йоту меньше.
Из некоторых замечаний, находимых в трудах Майера, можно сделать вывод, что он принял этот принцип еще в 1842 году. И он пошел дальше, чем Гельмголыд, причем в том аспекте, который крайне важен для нас в рамках нашей книги. Майер решил, что источником всей энергии, которая есть на Земле, являются солнечный свет и тепло. Более того, он решил, что источником энергии, которую тратят все живые существа, включая человека, тоже является исключительно солнечное излучение. Из этого следовало, что закон сохранения энергии распространяется не только на неживые, но и на живые объекты.
Этот вывод Майера является крайне важным. Человечество всегда считало, что между живой и неживой природой — пропасть. Именно с описания этой пропасти я и начал книгу. До XIX века законы, выводимые учеными для описания деятельности Вселенной, распространялись либо на живые существа, либо на неживую природу, но никогда — и на то и на другое вместе. Планеты двигаются в некоем строго определенном и неизменном порядке, а живые существа — по своему усмотрению. Камень всегда падает вниз, дым — всегда поднимается вверх, но человек может и лечь и подпрыгнуть, как сам того пожелает. С другой стороны, человек или мышь могут поддаться страху или гневу, а кирпич — нет.
И вот впервые родилось предположение о том, что закон природы — закон сохранения энергии — применим в равной степени к живой и к неживой природе. Это был важнейший шаг к пониманию жизни как таковой; возможно, вообще первый шаг к тому, чтобы сделать изучение живой ткани чем-то большим, нежели просто описание.
Но кажется, мы уходим в сторону от цели данной книги, как я описал ее в первой главе. Я писал о том, что понятия работы и энергии помогут нам найти более четкую, чем интуитивная, границу между живой и неживой природой. А сейчас мы, кажется, движемся в обратном направлении — стирая эту границу вообще.
Но не сдавайтесь! Изучение энергии в XIX веке подразумевало не только открытие закона ее сохранения, и мы это скоро увидим.
Глава 5. ТЕПЛОВЫЕ ПОТОКИ
Принятие представления о сохранении энергии стало в некоторой степени фундаментальной переменой в системе взглядов человека на Вселенную, переменой, которая даже сейчас не полностью проникла в образ человеческой мысли. Люди всегда верили, что вера может двигать горами; что с помощью волшебной палочки или лампы Аладдина можно построить дворец во мгновение ока; что сапоги-скороходы могут за считаные минуты переносить своего владельца через леса и горы…
А теперь все эти картинки исчезают, стоит лишь задать простой вопрос: где взять на это энергию?
Если уж нам приходится разбить радужные мечты и настоять на том, что все сводится к балансу поступления и потери энергии, то давайте уж убедимся, что мы действительно имеем на это право. Иными словами, насколько мы можем быть уверены в действенности закона сохранения энергии? Можем ли мы доказать, что этот закон действительно существует?
Если честно — нет. По крайней мере, на данный момент. Убедительных причин, которые однозначно не позволяли бы создавать или уничтожать энергию, никто еще не сформулировал. Мы можем утверждать лишь, что ни в одном из тщательнейших наблюдений, ни в одном из самых разнообразных экспериментов, от Джоуля до наших дней, не было зафиксировано ни одного случая, когда энергия возникала бы ниоткуда или исчезала в никуда.
Пока не будет отмечен хоть один такой случай и пока на практике допущение, что закон сохранения энергии действует, приносит неоценимую пользу в неисчислимом количестве сфер деятельности, ученые от него не откажутся. Они не могут доказать существование этого закона, но уверены в нем, как мало в чем другом.
Лишь однажды глубокая убежденность в существовании закона сохранения энергии была поколеблена. Это произошло в 1896 году, когда было открыто явление радиоактивности. Именно тогда обнаружилось, что некоторые элементы, например уран, непрерывно производят энергию, казалось бы, ниоткуда.
Однако уже в 1905 году физик Альберт Эйнштейн опубликовал новую, в огромной степени фундаментальную, теорию строения Вселенной (ныне обычно именуемую «специальной теорией относительности»), где все прояснилось за счет того, что в расчет была включена и масса.
Дело в том, что масса сама по себе также представляет собой сохранное явление. Этот факт ученые с большим удивлением обнаружили только в конце XVIII века. Неискушенному наблюдателю кажется, что, например, горящая свечка постепенно тает и ее масса исчезает. А когда железо ржавеет — оно, наоборот, набирает вес, и это кажется примером «появления» массы. Такие выводы вполне возможно сделать, если упустить из виду переход твердого или жидкого вещества в газ или, в противоположном случае, поглощение газов из атмосферы.
В 1770-х годах французский химик Антуан Лоран Лавуазье возвел в систему применение количественных измерений к химическим экспериментам, и полученные им результаты быстро убедили прочих химиков в необходимости взвешивать и измерять все, что только можно взвесить и измерить. Проводя реакции горения и ржавления в замкнутых емкостях, Лавуазье доказал, что если учитывать массу газов, которые производятся в результате горения или поглощаются в результате ржавления, то каких-либо заметных изменений массы реагентов не происходит!
Таким образом был провозглашен «закон сохранения массы», гласящий, что масса может переходить из одной формы вещества в другую, но не может быть ни создана, ни уничтожена. Иными словами, общее количество массы во Вселенной всегда одинаково.
Законы сохранения массы и энергии формулируются схожим образом, и всю вторую половину XIX века эти два закона считали аналогичными, но независимыми друг от друга обобщениями.
И только Эйнштейн в 1905 году сумел показать, на основе немногих базовых принципов, что массу можно рассматривать как одну из форм энергии. По его теории выходило, что крайне малое количество массы соответствует весьма большому количеству энергии. Этот принцип выражен в знаменитой формуле Эйнштейна е = mс2, где е — это энергия, m — масса, а с — скорость света. Из этой формулы видно, что 1 грамм массы соответствует примерно 21 500 000 000 000 джоулей энергии.
Таким образом, энергия, высвобождаемая при проявлениях радиоактивности, перестала быть загадкой. Стало ясно, что она появляется за счет потерь массы, столь малых, что приборы того времени не могли их зафиксировать. С тех пор появились гораздо более точные приборы, и с их помощью теория Эйнштейна обрела документальное подтверждение.
Высвобождение энергии при взрыве атомных бомб и выработка ее в ядерных реакторах тоже происходит за счет потерь массы. Еще важнее, что таким же образом объясняется и способность Солнца на протяжении множества веков выплескивать в пространство энергию в огромных количествах. Этот вопрос очень интересовал Гельмгольца, и в итоге ученый пришел к предположению, что Солнце постепенно сжимается, таким образом, потенциальная энергия его уменьшается и переходит в тепло и свет. Такая картина не лишена логики, но если бы она соответствовала реальности, то в истории Солнечной системы пришлось бы предположить некоторые факты, которых быть не могло в принципе; астрономы эту теорию принимать отказались.
Когда же выяснилось, что солнечный водород можно превратить в гелий с некоторой потерей массы, а следовательно — с высвобождением большого количества энергии, то феномен солнечного излучения (равно как и феномен излучения звезд вообще) стало возможным объяснить исходя из закона сохранения энергии.
Сейчас уже понятно, что, говоря «энергия», мы включаем в это понятие и массу; чтобы это стало очевидным, зачастую говорят о «законе сохранения массы-энергии».
Таким образом открытие радиоактивности, сперва пошатнувшее закон сохранения энергии, в конечном итоге еще прочнее утвердило его в более стойком и незыблемом виде.
На самом деле практики интуитивно использовали этот принцип еще задолго до того, как физики сумели убедительно доказать его на экспериментальном материале. Еще в 1775 году Парижская академия наук отказалась рассматривать какие бы то ни было проекты устройств, о которых заявлялось, что они будут производить энергии больше, чем потреблять. Такое устройство, если бы его существование было возможным, могло бы производить работу и вместе с тем продолжать работать за счет энергии, производимой им же самим. Получился бы пресловутый «вечный двигатель». И сейчас Патентное бюро США не будет рассматривать вопрос о патентовании устройств, включающих в себя «вечный двигатель», если только податель заявки не предъявит действующую модель своего изобретения. Надо ли говорить, что такого ни разу до сих пор не произошло?
Закон сохранения энергии подвел черту, провозгласив, что ни одно устройство не может вырабатывать больше энергии, чем тратит, однако не исключил надежды на то, что можно хотя бы получать столько же энергии. Если уж нельзя ничего выиграть у природы, то, может быть, получится хотя бы остаться при своих?
Именно эта надежда стала основной движущей силой всех теоретических исследований начала XIX века, связанных с работой паровой машины. В массовом сознании принято недооценивать значение прогресса в области теории, необходимого для того, чтобы изобретатель мог представить работающий механизм. Сам Уатт опирался в своих разработках паровой машины на работы Блэка, посвященные латентному теплу, о которых говорилось в предыдущей главе. А кто из слышавших об изобретении Уатта знает, что оно стало возможным только благодаря теории Блэка?
Эффективность самых лучших машин Уатта, какими бы полезными и незаменимыми они ни были, не превышает 5 процентов. Это значит, что работы они могут производить только на 5 процентов от получаемой ими тепловой энергии. Поэтому казалось очевидным, что, и не нарушая закона сохранения энергии, можно добиться значительного повышения производительности. Даже учитывая неизбежность каких-то потерь на трение, теплопроводность и тому подобное, логично было предположить, что эффективность вполне возможно поднять до близкого к 100 процентам показателя.
Так считали до тех пор, пока французский физик Николя Леонар Сади Карно не принялся всерьез изучать движения тепловых потоков, основав таким образом науку термодинамику (что по-древнегречески и означает «движение тепла»).
В течение всего XIX века значение этой науки все более возрастало, поэтому к тому моменту, как был четко сформулирован закон сохранения энергии, по причине своей фундаментальной важности для всего, что касается перехода энергии в работу и обратно, он получил название «первый закон термодинамики».
Карно основал науку, но времени на то, чтобы внести в нее большой вклад, у него оставалось уже очень мало. Ученый умер в возрасте тридцати шести лет во время эпидемии холеры в Париже. Однако кое-что он все же успел. В возрасте двадцати восьми лет в 1824 году он опубликовал небольшую книжку под названием «Размышления о движущей силе огня», где привел описания своих опытов и собственные рассуждения о том, до какой степени тепло может быть преобразовано в работу. В этой книге Карно ясно показал, что даже при идеальных условиях (то есть при отсутствии трения и потерь энергии в направлении окружающей среды) лишь строго определенная доля тепловой энергии может преобразовываться в работу. Эта доля определялась разностью температур пара и конденсируемой воды по абсолютной шкале температур, выведенной с помощью закона Шарля. Если первую определить как T1 а вторую — как Т2, то наибольшая доля тепла, которую можно перевести в работу, определяется по формуле:
(T2 — T1)/ T2
Доля преобразуемого тепла, то есть, иными словами, эффективность системы, одинакова, независимо от того, какие именно вещества подвергаются нагреву и охлаждению, будь то вода, ртуть или что угодно; важна только его температура. Поэтому формула Карно справедлива для любой «тепловой машины», а не только для паровой.
Допустим, например, что в машине Уатта используется пар, нагретый до 100 °С (373 °К), а температура конденсируемой воды — 5 °С (278 °К). Тогда по формуле Карно получаем:
(373 — 278)/373 = 0,255.
Лишь примерно четверть, и не больше, производимой тепловой энергии может быть преобразована в работу, как бы идеально ни работала машина. Повысить эффективность помогло бы использование раскаленного пара (чтобы Т2 была побольше) или жидкости, имеющей более высокую температуру кипения и более низкую температуру плавления, чем вода. Пробовали и то и другое, но даже современные паровые машины не имеют эффективности выше, чем 0,25.
* * *
Формула Карно не только указала путь к тому, как можно увеличить эффективность паровой машины, но и привела к открытию одного крайне важного обобщения.
Если формула Карно верна, то получается, что машина, в которой горячая и холодная камера имеют одну и ту же температуру, никакой работы произвести не способна. Ведь в таком случае Т2 будет равна Т1 соответственно, формула Карно приобретет вид:
(T2 — T1)/ T2 = 0/ T2 = 0.
Например, представим себе энергию, содержащуюся в океанской воде, пусть даже в ледяной. Когда эта вода замерзает, каждый грамм ее отдает 80 калорий тепла (как показал в свое время Блэк, измеряя латентное тепло). Почему бы тогда, скажем, океанскому лайнеру не собирать это тепло и не использовать для работы своих двигателей? Вода возле лайнера остужалась бы, возможно, вплоть до замерзания, но общий объем воды в океанах, а значит и содержащегося в ней тепла, настолько огромен, что для обеспечения работы всех океанских лайнеров (да и вообще всех механизмов) в мире потребовалась бы крайне незначительная ее доля. К тому же и эту потерю быстро возмещало бы солнечное тепло.
Такое предположение никоим образом не нарушает первого закона термодинамики. Энергия в данной схеме не берется из ниоткуда — она просто переводится из одной формы (из тепла, содержащегося в океанской воде) в другую (кинетическую энергию вращающихся винтов), а переход энергии из одной формы в другую в первом законе термодинамики оговорен отдельно.
Однако ни одна схема такого рода не оказалась работоспособной. Так и не удалось разработать ни одного способа использовать тепловую энергию какого-либо вещества, температура которого была бы равномерной. Иными словами, общий опыт всего человечества свидетельствует о том, что формула Карно справедлива для любых условий, которые когда-либо были испытаны. Для того чтобы тепло можно было преобразовать в работу, где-то в системе должна существовать разность температур.
Лорд Кельвин объяснял это так: «Трансформация, в результате которой должно быть преобразовано в работу тепло, извлеченное из источника, имеющего однородную равномерно распределенную температуру, — невозможна».
Это — одна из формулировок утверждения, получившего название «второй закон термодинамики».
Этот второй закон не кажется таким очевидно неизбежным, как первый. С некоторым сожалением мы чувствуем себя вынужденными признать, что энергию нельзя создавать из ничего (первый закон), но почему же мы не можем использовать ту энергию, которая у нас есть? Пусть мы не можем получить выгоду, но можно же хотя бы остаться при своих?
Давайте рассмотрим этот момент на примере энергии движения, с которой мы имеем дело ежедневно. Должно быть, второй закон термодинамики станет несколько нагляднее, если рассмотреть его по аналогии с падающими телами.
Достигая земли, падающее тело может совершать работу. Оно может убить человека, расколоть орех или просто пробить дырку в земле, но в любом случае — это очевидная работа. Достигнув же поверхности, тело больше никакой работы совершать не способно, по крайней мере до тех пор, пока продолжает лежать неподвижно. Соответственно своей способностью совершить ту работу, которую оно совершило, это тело обязано тому факту, что оно переместилось из точки с большим потенциалом энергии (к примеру — с вершины километровой скалы) в точку с меньшим потенциалом (к подножию той же скалы).
Но и покоящееся на поверхности земли тело тоже обладает некоей энергией. Если под ним выкопать шахту в километр глубиной и сбросить его в эту шахту, то тело вновь сможет проделать работу, такую же как и когда падало со скалы. Это происходит потому, что вновь создана разность потенциалов.
То же самое происходит и в отношении тепла. Тепло, содержащееся в океанской воде, нельзя перевести в работу без помощи камеры, содержащей нечто более холодное или более теплое, чем океанская вода. Если выразиться логичнее, то можно сказать, что работу совершает не камень, а падение камня, не тепло, а тепловой поток.
Далее, как каждому известно на собственном опыте, падающие тела двигаются только в одном направлении — вниз. Если бы тело могло падать в обоих направлениях, то один и тот же предмет мог бы совершать бесконечную работу, просто двигаясь туда-сюда — то с вершины скалы в долину, то из долины на вершину скалы. Однако на самом деле предметы падают только из точки с высоким потенциалом энергии в точку с низким.
То же самое происходит и с другими формами энергии, и в частности с теплом. В 1850 году немецкий физик Рудольф Юлиус Эмануэль Клаузиус дал однозначную формулировку этого процесса, сказав, что при любом спонтанном процессе (то есть таком, который происходит сам по себе, без внешнего вмешательства) тепло всегда переходит от более горячего тела к более холодному и никогда — от более холодного к более горячему.
На самом деле мы все это прекрасно знаем и принимаем как должное, что чайник с водой над горящим газом в итоге закипит, а теплая вода — всегда растопит лед. То есть тот факт, что тепло будет переходить от более горячего тела к более холодному, а не наоборот, нам хорошо известен.
То же самое утверждение и является само собой разумеющимся для формулы Карно, поскольку если бы тепло не перетекало от более горячего тела к более холодному, то оно могло бы перетекать и внутри равномерно нагретого резервуара с водой от одной его части к другой, и из этого перетекания можно было бы получать работу. Таким образом, утверждение Клаузиуса — это одна из формулировок правила Карно—Кельвина о невозможности получения работы из равномерно нагретой системы, то есть одна из формулировок второго закона термодинамики.
Клаузиус не только сформулировал это утверждение по поводу тепловых потоков (суть которого известна нам по бытовому опыту и без каких-либо научных формулировок), но и увидел в нем повод для масштабного обобщения, которое можно распространить на все процессы, в которых используется энергия, при любых условиях и в любом месте Вселенной. По этой причине именно ему приписывают честь «открытия» второго закона термодинамики.
Это подводит нас к интересному моменту. Любой тепловой машине для преобразования тепла в работу требуется некоторое время. Ни одна из них не способна производить работу мгновенно. За время работы тепло перетекает из горячей камеры в окружающую среду (которая, как правило, сама по себе холоднее, чем горячая камера) и никогда — наоборот. Таким образом', горячая камера охлаждается, а холодная камера нагревается. Разность температур становится со временем все меньше и производит все меньше работы по сравнению с изначальной разностью температур[2].
Можно придумать тепловую машину, в которой и горячая и холодная камеры имели бы более высокую температуру, чем окружающая среда, но в этом случае горячая камера теряла бы тепло быстрее, чем холодная. Если же, наоборот, температура обеих камер будет ниже температуры окружающей среды, то горячая камера будет нагреваться медленнее холодной. И в том и в другом случае разность температур будет уменьшаться. На самом деле в любой системе, переводящей в любой форме энергию в работу, со временем разность потенциалов уменьшается, или, иначе говоря, часть потенциально выполнимой разностью потенциалов энергии работы остается невыполненной на практике из-за необходимости преодолевать трение или иные формы сопротивления естественному потоку энергии.
Клаузиус еще в 1875 году изобрел параметр, включающий в себя и неизбежно теряемую энергию, и абсолютную температуру, — параметр этот получил название «энтропия системы».
Можно, конечно, представлять себе совершенные тепловые машины, настолько хорошо изолированные, что тепло не будет ни перетекать в них извне, ни тратиться на нагревание окружающей среды, машины, в которых будут отсутствовать потери на трение, и так далее. При таких условиях выполняться будет вся работа, на которую способна заданная разность температур. Энергия будет тратиться полностью, без потерь. Однако в реальности и трение, и теплообмен с внешней средой всегда имеют место, а значит — и энергопотери, причем их объем будет увеличиваться со временем (рис. 4).
В свете теории Клаузиуса можно сказать: при любом спонтанном процессе энтропия либо остается неизменной (в идеальном случае), либо возрастает (в реальных случаях).
Однако забудем об идеале — приходится признать, что в реальном мире вокруг нас энтропия всегда увеличивается.
Поскольку все это — неизбежные последствия однонаправленности тепловых потоков, то существует еще один способ выражения второго закона термодинамики.
Строго говоря, отдавая должное законам термодинамики, мы всегда должны помнить о том, что эти законы применимы только к замкнутым системам — то есть к тем частям Вселенной, которые можно рассматривать как не испытывающие никакого влияния извне со стороны других ее частей. Если же рассматривать открытые системы, то часто может казаться, что законы термодинамики нарушаются.
Рис. 4. Изменение количества доступной энергии со временем
Например, предположим, что вы ведете наблюдения за котелком с водой, стоящим на плите. Вы видите, что энергетическое содержание воды в котелке постепенно возрастает, пока вода не начнет кипеть и пока, наконец, вся не выкипит. Если рассматривать один лишь котелок с водой, вне его связей с плитой, то может показаться, что энергия, дерзко нарушая первый закон термодинамики, появилась из ниоткуда. Однако вы прекрасно понимаете, что это не так, поскольку под котелком находится горячая плита или газовый рожок. Если принять во внимание, что система складывается из обеих этих частей, то вопрос о том, почему на закипающий котелок не действует первый закон термодинамики, снимается сам собой.
Что касается второго закона термодинамики в отношении открытых систем, то представьте себе — тело действительно может подниматься с земли на высоту, а тепло — перетекать от более холодных тел к более горячим. В быту вы часто являетесь свидетелем подобных «феноменов», и если сосредоточить внимание только на поднимающемся теле или только на тепловом потоке, то вполне возможно сделать вывод о нарушении второго закона термодинамики.
Однако рассматривать систему надо в целом. Тело может подниматься с земли на крышу дома только тогда, когда оно находится, скажем, в лифте, движимом электрическим мотором. Тепло утекает из холодной камеры холодильника в более теплую окружающую среду тоже благодаря электрическому двигателю. Если включить в расчет двигатель и поток энергии внутри его, то вы увидите, что имеется и поток энергии в «правильном» направлении, причем превышающий по объему поток в «неправильном», действие которого мы видим как подъем тела или охлаждение камеры.
Другими словами, локальное уменьшение энтропии (являющееся результатом потока энергии в направлении, противоположном указанному вторым законом термодинамики) в одной из частей системы всегда более чем уравновешивается возрастанием энтропии в другой части системы. Если брать в расчет всю систему целиком, то общие изменения всегда происходят в направлении увеличения энтропии.
На самом деле, если мы имеем дело не с воображаемыми системами, существующими только в умах физиков-теоретиков, а с реальностью, то представить себе действительно замкнутую систему очень сложно. Внешняя среда всегда оказывает некоторое действие, которое необходимо учитывать.
Все вышеописанное справедливо и в отношении человеческого организма. Если его вдруг сделать замкнутой системой, лишенной энергообмена с окружающей средой, то он умрет в течение нескольких минут (ведь воздух — тоже часть окружающей среды). Направление естественных изменений в человеческом организме, сопровождающихся, как уже было сказано, возрастанием энтропии, ведет к смерти. Мы, конечно, живем, не умирая, иногда по целой сотне лет, но это происходит только потому, что наш организм является не замкнутой системой, а частью большей системы, в которую входят и воздух, которым мы дышим, и пища, которую мы едим. Сложность общего взаимодействия всех форм жизни и всей неодушевленной окружающей среды на планете, на которой мы живем, не позволяет считать замкнутой системой что-либо меньшее, чем всю Землю в целом.
Но и этого мало. Если бы Земля была замкнутой системой, то жизнь на ней очень быстро закончилась бы, поскольку поверхность планеты остыла бы, океаны — замерзли и так далее. Это тоже естественные изменения, соответствующие возрастанию энтропии. Этого не происходит только благодаря тому, что Земля является частью более крупной системы, в которую входит еще и Солнце, тепло которого и не дает Земле замерзнуть.
Даже Солнечная система не является полностью замкнутой. На нее действует сила притяжения со стороны других тел Галактики и много других не так ярко выраженных сил. Каждая часть Вселенной тем или иным образом влияет на остальные, и логично предположить, что на свете существует только одна действительно замкнутая система — это сама Вселенная. Если же рассматривать любую ее часть, то появляется вероятность того, что в этой отдельно взятой части энтропия может уменьшаться — за счет еще большего ее увеличения во всей остальной Вселенной.
Ясно, что если общее количество тепла во Вселенной ограниченно, а энтропия продолжает возрастать, то в конце концов она достигнет максимума, то есть такого состояния, что никакой разности температур не будет вообще. Вся энергия во Вселенной станет недоступной для совершения работы — все спонтанные процессы прекратятся и какие-либо изменения перестанут происходить вообще. Эта картина получила название «тепловая смерть Вселенной», и теория о тепловой смерти приобрела большую популярность во второй половине XIX века.
Теперь давайте вернемся к началу нашего повествования и посмотрим, можно ли выразить в терминах термодинамики то различие между живой и неживой материей, которое я высказал в первой главе. Я сказал, что живые существа могут совершать усилия, а неживые — нет.
Понятно, что «совершение усилия» подразумевает локальное уменьшение энтропии. Для того чтобы опустить висящий в воздухе камень вниз, усилия не требуется — его достаточно отпустить, и он упадет. А вот для того, чтобы поднять его вверх, усилие необходимо.
Сам по себе камень может двигаться только вниз, в том направлении, где усилия не нужно. Он не может совершить усилие, чтобы подняться наверх. С точки зрения термодинамики это будет звучать так: камень сам по себе может быть подвержен только увеличению энтропии, но не ее уменьшению.
Живой же организм способен совершать усилия по уменьшению энтропии по крайней мере на одном участке системы, частью которой он является (разумеется, за счет еще большего ее увеличения в других частях системы). Даже простейшие живые существа способны создавать локальное уменьшение энтропии, когда они прыгают, летят, лезут, идут, ползут или плывут вверх, против силы притяжения. Даже не сдвигающиеся с места организмы, например устрицы, тоже могут производить локальное уменьшение энтропии различными другими способами.
Удовлетворимся ли мы заявлением, что различие между живыми и неживыми организмами заключается в том, что живые организмы могут производить локальное уменьшение энтропии, а неживые — нет?
Что ж, выдвинув это утверждение, мы явно встали на верный путь, но, к сожалению, такого определения пока недостаточно. Солнечное тепло тоже может вызывать локальное уменьшение энтропии, когда выпаривает воду из океана, то есть поднимает в воздух огромные массы водяного пара. Силы, задействованные в геологических процессах, происходящих в земной коре, способны воздвигать горы в несколько миль высотой, что тоже подразумевает масштабное уменьшение энтропии. Однако ни Солнце, ни Земля не являются живыми ни в одном из смыслов, которые вкладывает в это понятие человек.
Надо еще поработать над нашим определением. Итак, продолжим.
Глава 6. ДВИЖУЩИЕСЯ ЧАСТИЦЫ
Еще со времен Джоуля, Кельвина, Майера, Гельмгольца и Клаузиуса, со времен открытия двух великих законов термодинамики, точного представления о том, что же такое тепло, не существовало. По крайней мере, такого, которое удовлетворило бы работающих с теплом ученых.
Это совершенно не означает, что законы термодинамики неполноценны, — они основаны на наблюдениях и не зависят от природы тепла. Однако с практической точки зрения этот факт осложнял применение законов термодинамики к каким-либо иным энергетическим устройствам, кроме тепловых машин, — к тем, где отсутствует тепловой поток.
Например, человеческий организм — главный предмет рассмотрения данной книги — определенно работает, и при этом температура его (37 °С) однородна и постоянна.
Разве это не является нарушением второго закона термодинамики? Мы уверены, что не является, но для того, чтобы четко понимать, почему именно не является, надо понять новую концепцию тепла как такового, выдвинутую впервые около 1800 года, а окончательно принятую научным сообществом только в 1860 году.
Начнем с того, что среди прочих над природой тепла размышляли и такие ученые, как Галилей и Ньютон. Они (и не только они) представляли себе тепло как движение мельчайших частиц материи. Для них это было вполне естественное предположение, поскольку эти великие ученые, исследуя в первую очередь законы движения и представляя тепло одной из форм движения, стремились вписать его в рамки своих грандиозных обобщений.
Однако в XVIII веке принято было представлять тепло как невесомый нематериальный ток. Такую точку зрения впервые выдвинул голландский физик Герман Бургаве примерно в 1700 году. В общем-то никаких объективных причин считать, что тепло представляет собой движение или вибрации, либо предполагать, что в горячих телах это движение или эти вибрации происходят быстрее, чем в холодных, не было. Разговоры о том, что, мол, существуют некие микрочастицы, слишком маленькие для того, чтобы их можно было увидеть, и вибрирующие слишком быстро и малоамплитудно для того, чтобы это можно было заметить, дети «эпохи рассудка» могли воспринимать только как заумную фантасмагорию.
Точнее говоря, в 1738 году профессор-математик из Санкт-Петербурга, столицы России, которого звали Даниил Бернулли, показал, что если представить газы состоящими из крошечных частиц, то из этого можно сделать вывод, что за давление газа отвечает движение этих частиц. Более того, предложенная им математическая модель, при которой скорость этих частиц возрастает по мере повышения температуры, в точности описывала реальные данные наблюдений. Однако его современники сочли эту теорию не более чем забавной спекуляцией. Большинство ученых предпочли принять на вооружение теорию теплорода — невесомого флюида, содержащегося в веществах, поскольку уже тогда было известно (по крайней мере, в представлении общественности) немало подобных флюидов в других областях: свет, электричество, магнетизм и т. п. Все были уверены в существовании такого явления, как «флогистон», — считалось, что его испускает в воздух любое вещество, сгорая или ржавея. Почему бы теплу не быть чем-то подобным? Так и сочли, и флюид тепла получил название «теплород».
Представление об одном из таких флюидов было торжественно похоронено в 1770-х годах, когда Лавуазье опроверг гипотезу о существовании флогистона, заменив ее тем представлением о природе горения и ржавления, которое мы разделяем и сейчас. Он показал, что при этих процессах не теряется или приобретается флогистон, а происходят химические реакции с содержащимся в воздухе кислородом. Однако существование теплорода тот же Лавуазье подтвердил, подкрепив эту теорию собственным авторитетом величайшего химика своего времени. Благодаря его заступничеству теория теплорода продержалась еще полвека, несмотря на лавинообразный рост фактов, свидетельствующих против нее.
Первые эксперименты, результаты которых однозначно указывали на ошибочность поддерживаемой Лавуазье теории теплорода, провел эмигрант из Америки Бенджамин Томпсон. Томпсон был тори и бежал из Америки во время Войны за независимость. Впоследствии, в 1791 году, курфюрст Баварский пожалует ему графский титул, и новоиспеченный граф вскоре женится, как ни забавно, на вдове самого Лавуазье. В историю он попал под именем графа Рамфорда.
В 1798 году граф Рамфорд наблюдал за высверливанием пушечного жерла в одной из оружейных мастерских курфюрста. В процессе погружения сверла в металлический цилиндр выделялось очень много тепла. Чтобы избежать перегрева, отверстие, в котором работало сверло, заливали водой и постоянно подливали ее по мере выкипания.
Сторонники теории теплорода не могли отрицать, что при такого рода трении вырабатывается тепло, и объясняли это так: металлический предмет всегда содержит тепло, а когда сверло вскрывает поверхность предмета, тепло выходит наружу. Рамфорд отметил в связи с этим два факта. Во-первых, количество содержащегося в металле тепла кажется бесконечным — сколько его ни сверли, тепло не перестает вырабатываться. А во-вторых, даже сточившееся сверло, уже практически не углубляющееся в металл, все равно производит не меньше тепла — а строго говоря, даже больше.
Рамфорду пришло в голову лишь одно вразумительное объяснение, почему при сверлении вырабатывается тепло — потому что в него переходит производимая работа. Рамфорд даже придумал единицу измерения механического эквивалента тепла на полвека раньше Джоуля, но выбранное им значение было слишком уж велико. Граф решил, что работа и тепло — тесно взаимосвязанные явления, и, поскольку работа, за которой он наблюдал, представляла собой механическое движение, Рамфорд заключил, что тепло тоже должно представлять собой одну из форм механического движения.
Через год, в 1799 году, близкий по сути эксперимент провел английский химик Гемфри Дэви. Он взял два куска льда и стал тереть их друг о друга с помощью механического устройства при температуре чуть ниже точки замерзания воды. Согласно господствовавшей на тот момент теории теплорода, при такой температуре лед просто не мог содержать в себе достаточно теплорода, чтобы растаять. Однако в процессе трения лед все же начинал таять. Дэви, как и граф Рамфорд, сделал вывод, что энергия движения переводится в тепло, а значит, тепло — это одна из форм движения.
Несмотря на это, теория теплорода господствовала в умах еще несколько десятков лет.
Поколебать ее господство удалось не путем изучения тепла как такового, а путем изучения материи. XVII и XVIII века стали периодом постепенного накопления знаний о свойствах газов. В четвертой главе уже упоминалось о законах Бойля и Шарля. Все эти знания просто взывали к тому, чтобы свести их в единую теорию вроде той, которую безуспешно пытался продвинуть Бернулли.
И вот в 1803 году английский химик Джон Дальтон продвинулся еще дальше. Он предположил, что не только газы, но и вообще любое вещество состоит из крошечных частиц, слишком маленьких, чтобы их можно было увидеть, неделимых и неразрушимых. Он назвал такие частицы «атомами». Этот термин происходит из древнегреческой философии, поскольку еще среди древних греков были философы, которые придерживались сходных взглядов. Однако греки в свое время не увидели в этих теориях ничего, кроме пустых рассуждений, и отвергли их. А Джон Дальтон — и это принципиальная разница! — положил в основу своих выводов строгие экспериментальные данные.
Несмотря на это, теория Дальтона не сразу овладела умами химиков — скорее всего, из-за того, что уложить в голове представление о существовании каких-то частиц, слишком малых для того, чтобы быть заметными в принципе, очень сложно. Но мало-помалу стало выясняться, что эта теория в силах дать ответ на многие вопросы. В ее рамках описывались не только свойства газов (как в теории Бернулли), но и многие свойства химических реакций твердых и жидких веществ. Все реакции обретали единую логику, если рассматривать их как взаимодействие различного рода атомов, связанных в определенные группы (позже их назовут «молекулами»), которые распадаются, чтобы дать возможность образовавшим их атомам связаться уже по-другому. Сами по себе атомы так и продолжали оставаться невидимыми, но преимущества, которые несла с собой теория атомов в отношении понимания свойств вещества, понемногу заставляли ученых ее принять.
Датировать завершение этого процесса можно 1858 годом, когда итальянский химик Станислао Канниццаро опубликовал трактат, где химические явления объяснялись через теорию атомов. Приводимые им объяснения были столь четкими и ясными, что непонимания не осталось уже ни у кого. Два года спустя на конференции химиков в Карлсруэ (Германия) Канниццаро активно отстоял эту теорию, убедив присутствующих как фактическими свидетельствами, так и силой собственного авторитета. С этого момента теория атомов стала единственной господствующей и продолжает оставаться таковой по сей день, хотя на сегодня об атомах известно уже, что они сами по себе гораздо сложнее тех неделимых маленьких шаров, лишенных собственных свойств, какими описывали их Дальтон и Канниццаро.
Взирая на материю, и в первую очередь на газы, как на совокупность одиночных атомов или, чаще, групп атомов, именуемых молекулами, логично было вернуться к давнишним рассуждениям Бернулли о том, как свойства газов можно объяснить через движение составляющих их частиц. Были проведены дополнительные эксперименты, результаты которых интерпретировались уже в свете теории атомов.
К примеру, Джоуль, проводя в 1840-х годах свои эксперименты по превращению всеми возможными способами работы в тепло, исследовал расширение газов такими способами, при которых работа не была задействована. Расширяясь, газы не толкали никаких поршней и не приводили в движение никаких предметов. Они просто расширялись в пустоту. Когда это происходило, Джоуль замерял температуру газов и сперва не обнаруживал ни ее повышения, ни понижения, как и ожидалось от процесса, в котором не задействована работа.
Однако в 1852 году, работая вместе с Томсоном (который позже станет лордом Кельвином), он установил, что на самом деле в таких случаях все же происходит небольшое понижение температуры. Это явление до сих пор называют «эффектом Джоуля—Томсона». Понижение температуры свидетельствует о том, что расширение газа на самом деле не является процессом, где не задействовано никакой работы. Молекулы газа испытывают друг к другу слабое притяжение, и движение против силы этого притяжения и есть тот момент, где совершается работа. Энергия, необходимая для совершения этой работы, берется из теплового содержания газа, так что в результате температура несколько падает.
Наличие этой силы межмолекулярного притяжения несколько усложняет расчеты, которыми должны описываться свойства газа, но химики-теоретики упростили себе жизнь, взяв за материал для своих формул некий воображаемый «идеальный газ», в котором сила притяжения между молекулами равна нулю, как и суммарный объем самих молекул.
Строго говоря, описываемая таким образом ситуация невозможна, но ее изобретение настолько упрощает расчеты, что позволяет теоретикам выводить из них простые законы. Эти законы приблизительно справедливы для реальных ситуаций и, будучи однажды сформулированными, в дальнейшем могут подвергаться всевозможным уточнениям для каждого конкретного случая. Это явно более благодарный подход, чем пытаться с самого начала математически просчитывать все детали реальных ситуаций.
И закон Бойля, и закон Шарля в точности применимы только к идеальному газу, и если свести их воедино, то мы получим простое «уравнение состояния газов», которое описывает состояние таких параметров газа, как температура, давление и объем. Зная любые два из этих параметров, можно сразу же высчитать третий. В отношении реальных газов результат таких расчетов будет соответствовать действительности лишь приблизительно (хотя порой очень близко к точному). Однако уравнение состояния газов вполне можно модифицировать таким образом, чтобы в нем учитывались и сила межмолекулярного притяжения, и объем молекул. Голландский физик Йоханнес Дидерик ван-дер-Ваальс с большим успехом привел одну из таких модификаций в 1873 году.
Я надеюсь, что это объяснит тот факт, что в течение 1850-х годов множество исследователей (в том числе и Клаузиус), прекрасно зная, что на самом деле это не так, продолжали дорабатывать работу Бернулли исключительно для газов с нулевым объемом частиц, не оказывающих друг на друга никакого воздействия. В результате родилась кинетическая теория газов, то есть теория, рассматривающая частицы в движении.
До совершенства эту теорию довели шотландский математик Джеймс Кларк Максвелл и австрийский физик Людвиг Больцман в 1859 году и за несколько последующих лет. Итогом их математического подхода (в условия которого входило, что молекулы газа движутся по прямой в случайно выбранных направлениях и сталкиваются друг с другом и со стенками камеры с абсолютной упругостью, не теряя при столкновении энергии) стало установление связи скорости движения молекул с температурой газа.
Представьте себе, что две молекулы газа столкнулись. Они отскакивают в разные стороны, изменив после столкновения направление движения и, вероятнее всего, скорость. Однако суммарный импульс системы остается при этом постоянным (см. главу 3), так что скорости, которые обе частицы могут иметь после столкновения, далеко не произвольны.
Но даже в этом случае распределение скоростей частиц после столкновения может быть различным. Если, к примеру, быстро движущаяся молекула сталкивается с медленно движущейся, то может получиться так, что медленная остановится, а быстрая отлетит в сторону еще быстрее, чем раньше, обладая всем суммарным импульсом обеих молекул до столкновения. Возможно также (причем куда более вероятно), что в результате скорости обеих молекул изменятся в сторону усреднения — быстро движущаяся молекула станет двигаться медленнее, а медленно движущаяся — быстрее.
Это можно наблюдать на примере бильярдных шаров. Во времена Максвелла атомы и молекулы так и представляли в виде сверхмалых бильярдных шаров. Сейчас их представляют уже не так; на самом деле сейчас уже известно, что строение их настолько сложно, что их невозможно представить в виде чего бы то ни было нам знакомого, не покривив при этом душой. Однако для описаний в рамках кинетической теории газов аналогии с бильярдными шарами вполне достаточно.
Предсказать, как именно перераспределятся скорости двух конкретных молекул после их столкновения, невозможно. Однако в отношении бессчетного множества квинтиллионов столкновений (а именно столько их и происходит каждую секунду в любом объеме газа, достаточно большом, чтобы его можно было увидеть) вполне допустимо использовать статистические методы для установления среднестатистического распределения скоростей. С их помощью можно показать, что молекулы любого заданного объема газа имеют некую «наиболее вероятную» скорость, к которой в той или иной степени тяготеют все молекулы этого объема. В любой отдельно взятый момент времени одни молекулы будут двигаться чуть (или значительно) быстрее этой «наиболее вероятной» скорости, другие — чуть (или значительно) медленнее.
Рис. 5. Скорость молекул и температура
Довольно сложное математическое выражение, получившее название «статистический закон распределения Максвелла—Больцмана» (рис. 5) в честь разработавших его ученых, позволило подсчитать процентное соотношение молекул любого заданного объема газа, относящихся к группам с различным значением скорости (при условии, что известны температура газа и масса составляющих его молекул). Если изобразить эту формулу в виде графика отношения скорости к процентному соотношению обладающих данной скоростью молекул, то получим плавную кривую, достигающую пика на значении равном «наиболее вероятной» скорости, а затем — так же плавно снижающуюся.
Теперь можно провести прямую связь между температурой и движением молекул газа. В любом газе, при любой температуре скорость отдельных молекул может принимать значения от нуля до крайне высокой. Однако наиболее вероятная скорость оказалась находящейся в прямой пропорции к квадратному корню от абсолютного значения температуры. По мере повышения температуры наиболее вероятная скорость молекул газа увеличивается. Если абсолютная температура возрастает в четыре раза, то наиболее вероятная скорость молекул — в два.
Так что для любого отдельного газа температура является величиной, тесно привязанной к наиболее вероятной скорости молекул. Однако для того, чтобы корректно обобщить это правило для любых газов, надо принять в расчет массу молекул этого газа. При любой заданной температуре, согласно формуле Максвелла—Больцмана, наиболее вероятная скорость обратно пропорциональна квадратному корню этой массы. Чем массивнее молекулы, тем медленнее они движутся. Молекула кислорода в шестнадцать раз массивнее молекулы водорода, поэтому молекула водорода движется в четыре раза (четыре — квадратный корень из шестнадцати) быстрее, чем молекула кислорода при любой заданной температуре.
Но кинетическая энергия, как уже объяснялось в главе 3, равняется произведению половины массы на квадрат скорости, и вкупе со всеми только что приведенными данными мы получаем, что при любой заданной температуре средняя кинетическая энергия молекул всех газов одинакова. Молекулы одного газа могут быть массивнее молекул другого, но тогда они обладают меньшей скоростью; если же их масса меньше, то и скорость их соответственно выше. Так или иначе, произведение массы на квадрат скорости будет во всех случаях одинаково. А поскольку скорость увеличивается пропорционально квадратному корню температуры, то и кинетическая энергия, пропорциональная квадрату скорости, является прямо пропорциональной температуре (см. рис. 5).
То есть можно сказать, что словом «температура» мы называем среднюю кинетическую энергию молекул, из которых состоит газ.
Оказалось, что это отношение справедливо для всех веществ, не только для газов. Точнее, для жидкостей и твердых тел сильно отличаются только условия. Молекулы, составляющие газ, находятся далеко друг от друга и движутся независимо. В жидкостях молекулы находятся в постоянном контакте и могут лишь скользить друг по другу, а в твердых телах — вообще жестко закреплены в общей структуре и даже скользить не могут. Тем не менее молекулы жидкостей начинают скользить друг по другу, а молекулы твердых тел — вибрировать на своих жестко установленных местах с большей энергией по мере возрастания температуры.
Аналогичным образом по мере понижения температуры все вещества теряют энергию, и при абсолютном нуле энергетическое содержание всех веществ сводится к минимуму. Собственно, до последнего времени принято было считать, что этот минимум равен нулю, но современная теория говорит о том, что даже при абсолютном нуле в веществе остается некий неизвлекаемый минимум энергии. Это объясняет, в частности, странные свойства гелия при температурах близких к абсолютному нулю.
Теперь давайте представим, что некий объем горячего газа вошел в соприкосновение с другим объемом холодного газа. Кинетическая энергия молекул горячего газа в среднем выше, чем молекул холодного газа. При столкновении двух молекул из разных объемов, скорее всего, кинетическая энергия «горячей» молекулы будет больше, чем «холодной», несмотря на то что вполне возможны и противоположные сочетания. Если вас смущает последняя оговорка, представьте себе такую аналогию: уровень жизни в США выше, чем уровень жизни, скажем, в Египте, так что наугад выбранный американец с преобладающей вероятностью окажется богаче наугад выбранного египтянина, хотя, конечно, в Египте можно найти людей, которые будут богаче многих американцев.
Точно таким же образом, не исключено, что в результате столкновения «горячая» молекула получит еще больше энергии за счет «холодной» молекулы и станет еще «горячее». (Понятно, почему я взял слова «холодная» и «горячая» в кавычки, — потому что отдельная молекула в принципе не может быть ни холодной, ни горячей, эти понятия применимы только в целом к системам, состоящим из огромного числа молекул.) Однако с большей вероятностью «горячая» молекула энергию потеряет, а «холодная» — получит, и обе останутся с неким усредненным количеством энергии, а значит — и температуры.
При большом количестве столкновений лишь единицы приведут к увеличению разности энергий участвовавших в них молекул, а подавляющее большинство — к уменьшению этой разности. Вероятность того, что при единичном столкновении «горячая» молекула приобретет энергию, а «холодная» — потеряет, мала, но вероятность того, что такая случайность повторится многократно, еще меньше.
Следовательно, в ходе множества случайных столкновений средняя кинетическая энергия молекул, а значит и температура, горячего газа (как и любого другого горячего предмета) уменьшится при контакте с холодным газом (или любым другим холодным предметом), а температура холодного, — наоборот, увеличится. Тепло будет перетекать от горячего предмета к холодному, пока средняя кинетическая энергия всех молекул обоих предметов не приобретет некое общее усредненное значение.
В чем отличия такого представления от старой теории тепла, как нематериального тока? Согласно старой теории, тепло перетекало от объектов с высокой температурой к объектам с низкой, повинуясь второму закону термодинамики, не подразумевающему ни исключений, ни модификаций. Согласно же кинетической теории, поток тепла есть среднестатистический результат случайных столкновений, который теоретически может оказаться и иным, так что второй закон термодинамики больше не может считаться абсолютно неизбежным. В принципе не исключено такое стечение обстоятельств, что множество «горячих» молекул наберут энергию из «холодных» и тепло перетечет, таким образом, из холодного предмета к горячему. То есть кинетическая теория не считает невероятным, что вода в чайнике, поставленном на огонь, не закипит, а замерзнет и огонь станет еще жарче.
Вероятность такого события (просчитанная на основе уравнений Максвелла) настолько ничтожно мала, что даже если бы вся Вселенная состояла только из стоящих на огне чайников, то шансов дождаться, чтобы хоть один из них замерз за все время существования Вселенной, у нас все равно не было бы практически никаких.
Разница между неизменным потоком тепла и потоком, испытывающим постоянные колебания, с философской точки зрения, конечно, огромна, но с практической настолько незначительна, что Максвеллу пришлось специально изобретать способ ее хоть как-то подчеркнуть. Поэтому он придумал крошечное существо, которое с заслонкой сидит на трубе, соединяющей две камеры с газом, температура в которых сначала одинакова. Существо, выдуманное Максвеллом, занималось следующим: когда к трубе подлетала из правой камеры быстро движущаяся молекула, оно пропускало ее через трубу, а медленные — не пропускала. Из левой же камеры оно, наоборот, пропускало все медленные молекулы, а быстрые — нет. Таким образом, в левой камере собирались быстро движущиеся молекулы, и сама камера нагревалась, а в правой — медленно движущиеся, и камера остывала. Таким образом, тепло перетекало бы из холодной камеры в горячую, что для старой теории тепла было неприемлемо, а для кинетической — вполне допустимо. Это воображаемое существо было названо «демоном Максвелла», и с тех пор этот «демон» известен как идеальный борец с энтропией.
Впрочем, подобные демоны водятся не только в наших фантазиях. В реальной жизни тоже существует некий аналог «демона Максвелла». Среднестатистические свойства молекул столь близки к неизменным только потому, что при обычных обстоятельствах мы имеем дело с телами, состоящими из огромного количества молекул. По мере уменьшения количества молекул в системе шансы наткнуться на заметное отклонение от среднестатистической вероятности возрастают. Когда речь идет о действительно малых количествах, ровное единообразие полностью пропадает.
В качестве такого примера можно назвать наблюдение, которое произвел в 1827 году шотландский ботаник Роберт Броун, отметивший, что цветочная пыльца, будучи распыленной в воде, как-то странно шевелится то в одном, то в другом направлении, очевидно, случайным образом. Сначала он решил, что пыльца движется сама, поскольку в ней скрыта живая сила, но вскоре обнаружилось, что подобным образом шевелятся и любые другие маленькие предметы (например, распыленные красители). В честь первооткрывателя это явление было названо «броуновским движением».
Примерно в 1890 году Больцман продемонстрировал, что броуновское движение можно объяснить с помощью кинетической теории. Он отметил, что любой находящийся в воде предмет со всех сторон подвергается бомбардировке молекулами окружающей его воды. Статистически количество ударов, получаемых им с одной стороны, будет уравновешиваться количеством ударов, получаемых с другой, и в итоге предмет будет оставаться неподвижным.
Понятно, что точно равным количество ударов с обеих сторон не будет, но при обычных обстоятельствах это не важно, разница будет незначительна. Если с одной стороны предмет получил квинтиллион ударов, а с другой в этот же момент — квинтиллион и двенадцать, то такое неравенство останется незамеченным. Однако при уменьшении размеров находящегося в воде тела общее число ударяющих по его площади одновременно молекул тоже уменьшится, и то же самое небольшое неравенство станет ощутимее. Если взять настолько маленькое тело, что одновременно в него будут ударять лишь сто молекул с одной стороны и сто двенадцать — с другой, эти двенадцать ударов разницы, незаметные в первом случае, теперь могут оказать вполне реальное воздействие. Больцман продемонстрировал, что применительно к очень малым телам случайное движение молекул, при котором возникает перевес ударного воздействия то в одну, то в другую сторону, вполне может привести к поведению характеризуемому броуновским движением.
Таким образом, мы имеем дело со своего рода демоном Максвелла, шевелящим тела, которым по прежней теории предназначено было пребывать в неподвижном состоянии. Поскольку движения частиц строго хаотичны, то никакой направленности в долгосрочной перспективе в отношении крупных тел в них просматриваться не может.
В 1905 году Альберт Эйнштейн разработал точную математическую модель броуновского движения, а в ходе точных экспериментов 20-х и 30-х годов XX века были измерены даже скорости движения молекул в газах, и оказалось, что их распределение в точности соответствует расчетам кинетической теории.
Энтропию тоже можно рассматривать в свете кинетической теории. Однако сначала разберемся в значениях слов «порядок» и «хаос».
Интуитивно мы называем «порядком» любое положение вещей, в котором присутствует некая математическая или логическая закономерность. Если же никакой системы в положении вещей вычленить невозможно, мы называем это хаосом.
Можно сказать так: порядок — это когда одну часть системы можно отличить от другой, а хаос — когда четкой границы нельзя провести нигде. Чем более четки различия между частями системы, тем более она упорядоченна.
Часто используемым примером упорядоченной системы является колода карт, где все карты сгруппированы по мастям и карты каждой масти расположены по старшинству. Заранее известно, что первая карта — пиковый туз, вторая — пиковый король и так далее по всем остальным мастям. Можно точно определить порядковый номер любой карты в колоде.
Если же разбивка колоды по мастям сохраняется, но в пределах каждой масти карты не расположены по старшинству, такая система уже менее упорядоченна. В отношении любой пиковой карты можно сказать только то, что она находится «где-то в первой четверти колоды», но точнее определить ее местонахождение уже невозможно.
Если же колода хорошо перетасована, то вообще ничего невозможно сказать ни об одной из карт. В этом случае мы имеем дело со «случайным распределением», то есть с хаосом.
Теперь давайте представим себе ситуацию возрастающей энтропии, например перехода тепла от горячего тела к холодному (это классический пример увеличения энтропии). По мере перетекания тепла горячее тело охлаждается, а холодное — нагревается, пока оба они не будут иметь некую среднюю температуру.
Во время этого процесса увеличивается не только энтропия, но и хаос. В частности, до начала теплопередачи оба тела (горячее и холодное) легко отличить друг от друга хотя бы по их температуре, если даже они и являются совершенно одинаковыми во всех остальных отношениях. По мере перетекания тепла от одного к другому разница между ними становится все меньше и в конце концов исчезает полностью.
Опять же, если свести вместе объем кислорода и объем водорода, температура и давление в которых равны, то они перемешаются, пока общий объем не будет содержать равномерную смесь обоих газов. Поскольку это спонтанный процесс, значит, при нем происходит возрастание энтропии. И поскольку в результате два легко различимых объекта становятся неразличимы, то, значит, хаос при этом тоже возрастает.
На самом деле в каждом конкретном случае можно провести параллели между возрастанием энтропии и возрастанием хаоса. Энтропия и хаос — это аналогичные явления.
Поскольку все спонтанные процессы подразумевают увеличение энтропии, то, значит, они подразумевают и увеличение хаоса. Странно было бы ждать, что тепло будет само по себе переходить от холодного тела к горячему, а смесь газов — сама по себе рассортировываться на составляющие.
Это утверждение справедливо и в отношении самого первого из наших примеров — колоды карт. Сложенная упорядоченным образом колода сама по себе, конечно, не перетасуется, но это лишь потому, что она вообще не будет подвергаться никаким изменениям. Но предположим, что мы создадим некие условия, при которых колода будет подвергаться неким изменениям, причем таким, которые будут определяться исключительно случайным образом. Например, если мы сбросим карты с крыши дома на мостовую. Тогда колода разлетится на отдельные карты. Если теперь эти карты собрать, не глядя на их достоинство, то в результате мы получим совершенно случайную последовательность, несмотря на то что начинали они свой полет в строгом порядке. Таким образом, мы имеем очередной спонтанный процесс, в котором возрастают и энтропия, и хаос.
Перетасовывание карт — тоже пример спонтанного процесса (в том смысле, что карты при нем распределяются случайным образом), при котором возрастают как энтропия, так и хаос. На самом деле честное перетасовывание карт случайным образом — обязательное условие для честной игры в карты.
Для того чтобы перевести колоду карт обратно из хаотичного в упорядоченное состояние, необходимо сесть и разложить ее, уделяя внимание каждой карте (то есть, в терминологии нашей первой главы, необходимо «совершить усилие», уменьшая энтропию). Глупо было бы ждать, что колода вдруг придет в упорядоченное состояние сама собой, если ее долго перетасовывать или подбрасывать в воздух.
Точнее, существует ненулевая вероятность, что перетасовывание колоды может привести к образованию где-то в ней коротенькой упорядоченной последовательности или даже длинной — ведь бывает же, что при сдаче на руках у одного играющего оказывается тринадцать пик. Это явление того же порядка, что и замерзание воды в поставленном на огонь котелке. Разница лишь в масштабах вероятности — увидеть на руках тринадцать пиковых карт вполне возможно лишь потому, что их в колоде всего пятьдесят две. Если бы карт в колоде было столько же, сколько молекул в котелке с водой, то и шансы вытащить случайным образом четверть из них так, чтобы все вытянутые карты оказались одной масти, были бы такими же ничтожными, как и увидеть замерзающую воду в котелке.
Из всех форм энергии тепло больше всех тяготеет к хаосу. То есть вещества, отличающиеся друг от друга только тепловым содержанием, труднее различить, чем вещества, отличающиеся количеством излучаемого света или положением в гравитационном или электромагнитном поле. Следовательно, во всех спонтанных процессах, где используется нетепловая энергия, часть энергии всегда переходит в тепло, что само по себе является примером возрастания энтропии.
По той же логике, все содержащееся в системе тепло никогда не может быть полностью переведено в нетепловую энергию, поскольку такой процесс подразумевал бы уменьшение энтропии. В действительности же если часть тепла переводится в другую форму энергии, то энтропия в оставшейся части возрастает настолько, что более чем компенсирует свое снижение, получившееся в процессе перехода тепловой энергии в нетепловую.
Таким образом, очевидно, что кинетическая теория газов, разработанная во второй половине XIX века, удовлетворительным образом объясняет термодинамические явления, зафиксированные в наблюдениях первой половины столетия под влиянием теории теплорода.
Однако, как уже упоминалось в начале главы, в рамках этой новой теории объясняется и то, как человеческий организм может производить работу, сохраняя при этом свою температуру неизменной, чего прежняя теория объяснить не могла. Я этого не забыл, и мы методично движемся к выполнению обещанного. Важнейшими понятиями теперь для нас станут «атом» и «молекула» — понятия, которых в прежней теории не было, но в новой являющиеся краеугольными.
Глава 7. ЧАСТИЦЫ, УДЕРЖИВАЕМЫЕ ВМЕСТЕ
Соблазнительно было бы думать о человеческом организме (и вообще о живой ткани) как о механизме, извлекающем работу из равномерно нагретой системы просто в силу каких-то особых своих свойств, позволяющих противодействовать энтропии. Ведь в конце пятой главы я уже начал было описывать живую материю в терминах энтропии.
Однако давайте не будем сосредоточиваться на тепле исключительно как на источнике работы только потому, что этим занимались на заре возникновения термодинамики. Формулировка второго закона этой науки, выдвинутая Кельвином, гласила, что тепло невозможно перевести в работу при условии отсутствия разности температур, но ведь, помимо тепла, существуют еще и другие виды энергии! Падающий камень совершает работу, несмотря на тот факт, что температура его в точности равняется как температуре вершины скалы, на которой он лежал, так и температуре подножия, на которое он падает. Важна не разность температур, а разность потенциалов энергии.
В таком случае остается установить, какую же именно энергию используют живые организмы, извлекая из нее работу. Но жизнь — слишком сложное явление, чтобы постичь его с наскоку, и для начала надо взять что-нибудь попроще.
Вернемся к тепловым машинам и зададимся вопросом: откуда берется энергия для изначального нагрева горячей камеры? Ответ прост — она получается в процессе горения. Дерево, уголь, нефтепродукты или газ сжигаются, и полученная в этом процессе энергия нагревает воду до состояния пара, что и делает возможным функционирование тепловых машин. Да, для того, чтобы запустить процесс горения, любое топливо надо сначала поджечь, но количество энергии, получаемой во время горения, во много раз больше, чем количество энергии, изначально затраченной на поджигание. Так откуда же берется эта энергия?
Это крайне важный для нас вопрос, поскольку, как я расскажу позже, достаточно давно было подмечено, что между горением угля и дыханием живых существ есть что-то общее. Казалось, что, если удастся найти источник энергии, таящейся, скажем, в холодном угле, нашедший его окажется на прямом пути к открытию источника энергии человеческого организма.
Так или иначе, давайте попробуем.
В XVIII столетии, на пике популярности теорий неуловимых флюидов, считалось, что уголь — это пример вещества полного флогистона. Считалось, что в процессе горения флогистон высвобождается и именно этот процесс и порождает выделение тепла и света, составляющих горение. Однако эта теория содержала в себе неустранимые внутренние противоречия, за что Лавуазье ее и разгромил.
Теперь требовалось новое объяснение того, каков же источник высвобождаемой при горении энергии, и до появления теории атомов этот пробел так и не был заполнен.
Ключевую подсказку к правильному ответу я уже привел в предыдущей главе, там, где упоминал эффект Джоуля—Томсона. (Напомню: газ, расширяющийся в вакууме, производит работу, поскольку молекулам при центробежном движении приходится преодолевать существующую между ними слабую силу притяжения.)
Значит, между молекулами существует сила притяжения, так же как и между небесными телами. Как существование силы гравитационного притяжения является основой для самого понятия о «потенциальной энергии», так и существование межмолекулярного притяжения является основой для некоего понятия, которое можно по аналогии назвать «химической энергией».
Возьмем, скажем, лед. Он состоит из молекул воды, находящихся в непосредственном контакте друг с другом и расположенных в строгом порядке. (Я не буду углубляться в доказательство этих фактов, упомяну лишь, что такой порядок атомов или молекул называется «кристаллическим» и что большую часть твердых веществ можно привести к кристаллическому виду.)
При заданной температуре ниже 0 °С отдельные молекулы в составе кристалла вибрируют в рамках выделенного им места. Однако кинетической энергии подобных вибраций недостаточно, чтобы преодолеть силу межмолекулярного притяжения, которое удерживает молекулы вместе так, что все молекулы продолжают оставаться на своих местах.
Если лед начать нагревать, молекулы будут вибрировать все быстрее и кинетическая энергия, которой они обладают, будет становиться все больше. По достижении температуры в 0 °С кинетическая энергия молекул становится достаточно мощной, чтобы преодолеть силу межмолекулярного притяжения, и кристалл льда распадается. Отдельные молекулы начинают свободно перемещаться по общему объему вещества — они больше не привязаны к конкретному месту в общей структуре. Короче говоря, твердый лед начинает таять и превращается в жидкую воду.
По мере дальнейшего нагревания тающего льда поступающее тепло не переходит в увеличение кинетической энергии отдельных молекул и, соответственно, температура не повышается. Вместо этого вся поступающая тепловая энергия тратится на преодоление силы межмолекулярного притяжения, так что лед продолжает таять. Молекулы талой воды в образующейся слякоти не обладают большей кинетической энергией, чем те молекулы воды, что еще связаны в кристаллической структуре, так что температура образующейся жидкости не выше температуры еще не растаявших кристаллов льда. Тем не менее в какой-то форме вода все же должна содержать больше энергии, чем лед, ведь молекулы воды сумели преодолеть силу, удерживающую их в кристалле, а молекулы льда — нет. Эта форма энергии и есть та «химическая» энергия, о которой я упомянул.
Таким образом, молекулы жидкой воды при температуре 0 °С содержат больше химической энергии, чем молекулы льда при той же температуре. Когда лед тает, получаемое тепло переводится в химическую энергию, а не в кинетическую, поэтому в процессе таяния температура льда не повышается. Лишь после того, как весь лед растает, получаемое тепло снова будет переходить в кинетическую энергию и приводить к дальнейшему повышению температуры.
На процесс перевода грамма льда с температурой 0 °С в грамм воды с той же температурой тратится 80 калорий, так что каждый грамм жидкой воды содержит на 80 калорий химической энергии больше, чем грамм льда с той же температурой. Именно это латентное тепло плавления открыл Блэк в период господства теории теплорода. Он не сумел внятно объяснить этот феномен (хотя и совершил героическую попытку сделать это), поскольку в своей теоретической базе использовал лишь «невесомые флюиды». Нам в этом отношении повезло больше.
Но ведь это еще не все. В жидкой воде (как и в любой жидкости) составляющие ее молекулы не закреплены в каком-либо определенном месте, но продолжают оставаться в непосредственном контакте, скользя друг по другу. От обретения дальнейшей независимости молекулы все же удерживаются некими силами. Дальнейшее нагревание жидкости приводит к двум следствиям. Часть тепла переводится в кинетическую энергию, так что молекулы начинают вибрировать быстрее, и температура жидкости повышается. Другая часть переходит в химическую энергию, придавая молекулам способность оторваться от остальных без повышения температуры. Так образуется пар.
При любой температуре вода (как и любая жидкость) в тех или иных масштабах испаряется. Если жидкость находится в закрытом сосуде, то часть пара обязательно конденсируется обратно в жидкость и устанавливается некое равновесие, так что при каждой заданной температуре существует свойственное ей определенное давление пара. Чем выше температура, тем выше это давление.
В обычных обстоятельствах атмосферное давление выше, чем давление водяного пара, и оно не дает молекулам воды масштабно отрываться от жидкости. Однако при температуре 100 °С давление пара сравнимо по силе с атмосферным, и вода, преодолев атмосферное сопротивление, начинает испаряться с максимальной интенсивностью — мы называем этот процесс кипением. Естественно, при более низком атмосферном давлении давление пара уравнивается с ним при более низкой температуре. Поэтому на большой высоте вода кипит при меньших температурах, и задача сварить яйцо вкрутую там приобретает особую сложность.
Пока вода кипит, все получаемое тепло переходит в химическую энергию, и вода с температурой 100 °С переводится в пар с такой же температурой. И опять же, грамм пара с температурой 100 °С содержит на 540 калорий больше, чем один грамм воды с той же температурой. Это латентное тепло кипения.
Естественно, когда пар конденсируется обратно в воду, он должен вернуть эту химическую энергию, которая переводится при этом снова в тепло. Поскольку грамм конденсирующегося пара отдает при этом 540 калорий, а грамм воды, остывающей затем со 100 °С до 0 °С, — всего 100, становится понятно, что большая часть работы, производимой паровым двигателем, получается за счет конденсации пара, а не за счет последующего остывания воды.
Водяной пар при любой температуре содержит больше химической энергии, чем жидкая вода при той же температуре. Именно поэтому при потении тело охлаждается. Химическая энергия, необходимая для испарения пота, берется из тепловой энергии тела, так что тело в результате остывает. Когда влажность воздуха так высока, что конденсация влаги практически уравновешивает ее испарение, пот собирается в капли, и мы говорим: «Проблема не в жаре, а во влажности».
Но и это еще не все. Молекула воды сама по себе не является простейшей частицей — нет, она состоит из трех атомов. Два из них — атомы водорода, один — кислорода. Три атома удерживаются воедино с помощью сил гораздо более крепких, чем те, что обеспечивают притяжение между соседними молекулами, настолько более крепких, что на ум сразу же приходят аналогии с веревками и канатами. Поэтому внутримолекулярные силы притяжения называют «химическими связями».
По мере нагревания воды (рис. 6) не только молекулы набирают кинетическую энергию и ускоряют вибрации — то же самое происходит и с составляющими эти молекулы атомами. Но даже когда вода нагревается достаточно для того, чтобы молекулы смогли разорвать все соединяющие их связи, полученной энергии еще недостаточно атомам, составляющим молекулу, чтобы разорвать куда более прочные внутримолекулярные связи. Даже водяной пар продолжает состоять из целых молекул воды.
Однако при температуре в несколько тысяч градусов энергия вибрации атомов приобретает достаточную силу, чтобы разорвать химические связи, и вода начинает разлагаться на водород и кислород. При температуре 3000 °С около четверти молекул воды распадаются на водород и кислород. Соответственно смесь водорода и кислорода содержит в себе больше химической энергии, чем аналогичная масса воды при той же температуре.
Рис. 6. Химическая энергия и распад молекул воды
Но и водород с кислородом, образующиеся из распавшейся воды, тоже еще не являются простыми частицами! Пока что это газы, молекула каждого из которых состоит из двух связанных между собой атомов. Связи между этими атомами тоже могут распасться, если вещество нагреть еще больше. При температуре около 3500 °С около четверти молекул кислорода распадается на единичные атомы (с получением так называемого «атомного кислорода»), а доля молекул водорода, распадающихся при той же температуре на атомный водород, — еще больше, около трети. И опять же, в атомной форме водород и кислород содержат больше химической энергии, чем молекулярный водород и кислород при той же температуре.
При еще более высоких температурах атомы и водорода и кислорода могут распадаться на еще более мелкие частицы, но в рамках нашей книги мы на этом остановимся.
Из всего сказанного видно, что связи межатомного и межмолекулярного притяжения имеют различную силу и что при разрыве или образовании одной конкретной связи или ее замещении на другую всегда происходит некое изменение (в ту или иную сторону) содержания в веществе химической энергии. В случаях, когда химическая энергия набирается, надо учитывать энергию, поступающую в других формах (чаще всего в тепловой), чтобы не создавалось впечатления нарушения первого закона термодинамики.
Теперь мы можем дать ответ на вопрос, откуда же берется энергия горящего угля. Тепло и свет, испускаемые при горении, возникают за счет потерь химической энергии, причиной которых являются изменения в природе химических связей в угле и атмосферном кислороде.
Для того чтобы дальше говорить о подробностях типов взаимодействий с учетом изменений в природе химических связей (то есть о химических реакциях), при которых производится энергия в форме тепла и света, нам необходимо выучить язык химических записей. Это нужно не для того, чтобы «наукообразить» наше повествование, а, наоборот, для того, чтобы читать было удобнее. К счастью, язык химических записей очень логичен и прост.
Начнем с того, что на данный момент известно 103 различных химических элемента, то есть 103 различных вида атомов. В рамках этой книги все 103 нам не понадобятся. Достаточно будет около дюжины самых важных.
У каждого элемента есть конечно же собственное название, будь то простое, например «железо», или сложное, например «празеодимий». Кроме названия, известного всем химикам в мире, у каждого элемента есть еще и всемирно принятое краткое обозначение. Это одна-две буквы латинского алфавита — первая буква названия элемента по-латыни плюс, в большинстве случаев, еще одна буква из названия.
Уже самые первые исследования структуры атомов показали, что основной параметр, по которому атомы разных видов различаются между собой, — это их масса. То есть отдельный атом углерода всегда в двенадцать раз массивнее отдельного атома водорода; отдельный атом магния в два раза массивнее отдельного атома углерода и так далее. Поэтому атомам различных химических элементов присвоены также номера, отражающие их относительную массу. Массе атома кислорода было произвольно присвоено значение 16,0000, исходя из чего с учетом пропорций и все прочие атомы получили свой «атомный вес»[3].
В таблице 1 я привожу несколько химических элементов, с которыми мы будем дальше иметь дело в этой книге, — их символические обозначения и атомные веса. Для последних приводятся самые точные значения по новым, 1961 года, стандартам. Однако нет никакой необходимости запоминать все десятые, сотые и тысячные доли. Большая часть значений атомных весов с легкостью округляется до целых единиц, и принято считать, что атомный вес водорода — 1, углерода — 12, натрия — 23, серы — 32 и так далее. Пожалуй, единственными случаями, когда десятичные цифры стоит брать в расчет, являются хлор с его 351/2 и магний с его 241/2.
Писать «С» вместо «углерод» или «Н» вместо «водород» быстрее и проще, особенно это важно для химиков, которые тратят большую часть времени
Таблица 1
СИМВОЛИЧЕСКИЕ ОБОЗНАЧЕНИЯ И АТОМНЫЕ ВЕСА
Элемент …… Обозначение … Атомный вес
Водород …… Н … 1,00797
Углерод …… С … 12,01115
Азот …… N … 14,0067
Кислород …… О … 15,9994
Натрий …… Na … 22,9898
Магний …… Mg … 24,312
Фосфор …… Р … 30,9738
Сера …… S … 32,064
Хлор …… Cl … 35,453
Калий …… K … 39,102
Железо …… Fe … 55,847
Йод …… I … 126,9044
при написании своих работ на указание названий элементов. Когда же речь заходит об обозначении молекул, состоящих из различных сочетаний атомов, экономия становится просто невероятной. Здесь использование символики перестает уже быть вопросом одной лишь экономии сил и времени, а становится важной составляющей ясности подхода; вы и сами поймете это по ходу книги.
Возьмем, к примеру, кислород. В нормальных условиях это газ, состоящий из молекул, каждая из которых состоит, в свою очередь, из 2 атомов кислорода. Следовательно, если мы просто говорим «кислород», то непонятно, что именно мы имеем в виду: атомы или молекулы. Можно, конечно, вносить ясность путем добавления уточняющих определений — говорить «атомный кислород» или «молекулярный кислород», но опять же, мало того что мы при этом чрезмерно усложняем речевой оборот, так к тому же цель еще и остается при этом не полностью достигнутой. Ведь есть еще, например, такая форма молекулярного кислорода, как озон, в котором молекула состоит не из двух, а из трех атомов.
Для упрощения и конкретизации вопроса нужно всего лишь дописать к символу — обозначению элемента циферку, и мы получаем химическую формулу вещества, которая сама по себе говорит нам о строении молекулы. Таким образом, просто О обозначает атомный кислород (совсем уж дотошные педанты могут записывать его как О2 но по умолчанию и так принято считать, что если символ написан без дополнительных цифровых обозначений, то подразумевается «1»).
Молекулярный кислород обычного типа пишется O2, а озон — О3.
Точно так же азот, водород и хлор — все они в обычном виде тоже представляют собой газы, состоящие из двухатомных молекул, и записываются так: N2, H2 и Cl2.
Не всегда предмет состоит из молекул четко определяемого состава. Например, кусок углеродного материала (например, угля) состоит из множества атомов углерода, объединенных между собой очень сложными химическими связями. В принципе кусок угля можно рассматривать как единую огромную молекулу. Однако для простоты химические элементы в твердом состоянии обозначает просто как атомы, игнорируя при этом реальные связи между этими атомами. Поэтому углерод в его твердом естественном состоянии обозначается просто как С.
Буквенно-цифровую систему можно использовать и в том случае, если молекула состоит из атомов нескольких разновидностей (такие вещества называют «сложными»). Так, например, формула сложного вещества хлороводорода (это газ, состоящий из двухатомных молекул, один из атомов которой — водород, а второй — хлор) записывается так: НСl.
Молекула воды, состоящая из 2 атомов водорода и 1 атома кислорода, записывается как Н2O (эту формулу знают все, даже те, кто не имеет ничего общего с химией), а формула углекислоты, состоящей из 1 атома углерода и 2 — водорода, обозначается как СO2.
Каждая молекула имеет свой молекулярный вес, равный сумме атомных весов всех составляющих ее атомов. Молекулярный вес молекулы кислорода, O2, равняется 16 + 16, то есть 32. Молекулярный вес углекислоты — 12 + 16 + 16 то есть 44, и так далее.
Формулы можно использовать для описания химических реакций более быстрым и точным образом, чем в словесном рассказе. Например: уголь, представляющий собой практически чистый углерод, при горении вступает в соединение с содержащимся в воздухе кислородом, в результате чего получается углекислота. Химическая реакция в данном случае записывается так:
С + O2 → СO2.
Это можно перевести как «углерод плюс кислород равно углекислота», и является прекрасным примером химического выражения.
Таким же образом, водород вступает в соединение с кислородом, в результате чего получается вода. Это можно записать таким образом:
Н2 + O2 → Н2O.
Рис. 7. Уравновешенные химические выражения
Но химиков такая запись не может полностью удовлетворить, и вот почему.
В первой из двух вышеприведенных реакций, где речь шла о сочетании углерода и кислорода, видно, что ни один атом не «остался без дела», все они закономерно перешли из левой части уравнения в правую. У нас изначально имеется 1 атом углерода (представляющий собой уголь) и 2 атома кислорода (представляющие собой молекулу кислорода), а в результате мы получаем 1 молекулу углекислоты, в которой содержатся и тот самый атом углерода, и те самые 2 атома кислорода.
Но вот во втором выражении, где речь идет о соединении водорода и кислорода, дело обстоит иначе. Здесь у нас с самого начала имеется 2 атома водорода (представляющие собой молекулу водорода) и 2 атома кислорода (представляющие собой молекулу кислорода), но в результате мы получаем молекулу воды, включающую в себя оба атома водорода, но при этом лишь один из двух атомов кислорода. Такая «неуравновешенная» запись процесса может ввести в заблуждение, поскольку позволяет предположить, что 1 атом кислорода просто исчез, чего на самом деле, понятно, случиться не могло. Более того, для того, чтобы использовать такие выражения для количественного расчета, они должны быть уравновешенными (рис. 7).
Для того чтобы уравновесить выражение, надо указать соответствующее количество для каждого участвующего в реакции элемента. Вот как выглядит уравновешенное выражение для соединения водорода и кислорода:
2Н2 + O2 → 2Н2O.
В этом случае мы изначально берем 4 атома водорода и 2 атома кислорода и в результате имеем те же 4 атома водорода и 2 атома кислорода. Все сходится!
Конечно, можно написать
4Н2 + 2O2 → 4Н2O
или
12Н2 + 602 → 12Н2O
и, таким образом, тоже уравновесить выражение, но принято все же использовать наименьшую цифру из возможных.
Впрочем, если и принято использовать только целые числа в химических выражениях, то это правило не является универсальным. Когда речь идет о вырабатываемой в ходе химической реакции энергии (а именно об этом я и собираюсь рассказывать), часто удобнее бывает обозначать единый атом кислорода как 1/2O2. Это не совсем хорошо, поскольку может навести на мысль о том, что «полумолекулы» существуют на самом деле, а это не так. Однако с таким отображением удобнее вести энергетические расчеты, так что выражение для соединения водорода и кислорода можно записать и так:
H2 + 1/2O2 → H2O.
В этом выражении мы изначально имеем 2 атома водорода и 1 атом кислорода (полмолекулы), а в результате получаем 2 атома водорода и 1 атом кислорода, так что выражение получается сбалансированным.
Можно привести пример подобного выражения и без участия кислорода. Водород и хлор вместе могут образовывать хлороводород, а натрий и хлор — хлорид натрия (это привычная нам поваренная соль). Эти процессы описываются такими выражениями:
Н2 + Cl2 → 2НСl,
2Na + Cl2 → 2NaCl.
Очевидно, что использование целых чисел — простейший способ записать выражения в уравновешенном виде.
Итак, ход химических реакций благодаря применению специальных обозначений стал нам понятнее, и теперь мы можем, как я уже говорил, использовать эти выражения для различного рода вычислений.
Возьмем, к примеру, выражение, представляющее соединение водорода и хлора:
Н2 + Cl2 → 2НСl.
Оно показывает, что в ходе химической реакции одна молекула водорода реагирует с 1 молекулой хлора для создания 2 молекул хлороводорода. В реакцию вступают равные количества молекул водорода и хлора — один к одному, два к двум, десять к десяти, миллиард к миллиарду. Однако это не значит, что и массы вступающих в реакцию газов будут одинаковы, поскольку одна молекула хлора гораздо тяжелее, чем одна молекула водорода; соответственно и масса участвующего в реакции хлора будет больше, чем реакция участвующего в ней же водорода.
Поскольку атомный вес водорода равен 1, а хлора — 351/2, то молекулярный вес Н2 равен 1 + 1, то есть 2, а молекулярный вес Cl2 равен 351/2 + 351/2, то есть 71. Вне зависимости от того, сколько пар молекул — по одной молекуле хлора и водорода — вступают в реакцию, отношение их масс всегда будет составлять 2:71. Так, две унции водорода вступят в реакцию с 71 унцией хлора; два фунта водорода — с 71 фунтом хлора; две тонны водорода — с 71 тонной хлора и так далее.
Удобнее всего, конечно, рассматривать, как и принято в химической науке, 2 грамма водорода и 71 грамм хлора.
Еще до того, как были установлены подробности касательно атомного строения молекул, химики уже выяснили путем точных измерений, что 2 грамма водорода вступают в реакцию с 71 граммом хлора. И только после того, как в результате долгих наблюдений они поняли, что хлор с водородом соединяются 1:1, был сделан вывод о том, что молекула хлора в 351/2 раза тяжелее молекулы водорода и что атом хлора в 35У2 раза тяжелее атома водорода. Именно отношение весов в сочетаниях и позволило впервые установить значения атомных весов различных химических элементов.
Впоследствии оказалось, что количество молекул водорода в 2 граммах этого вещества равняется примерно 6O2 000 000 000 000 000 000 000.
Это огромное число принято называть «числом Авогадро», поскольку установлено оно было в ходе исследований, которые проводил итальянский химик Амадео Авогадро примерно в 1810 году. Число Авогадро обычно обозначают N, и, поскольку это гораздо проще, чем писать его целиком, именно так я и буду его в дальнейшем приводить.
Таким образом, можно сказать, что N молекул Н2 весят 2 грамма. Поскольку отдельная молекула Cl2 в 351/2 раза массивнее, чем отдельная молекула Н2, то N молекул Cl2 тоже должны весить в 351/2 раза больше, чем N молекул Н2. Поэтому вес N молекул Cl2 должен составлять 2 х 351/2, то есть 71 грамм.
Подобные рассуждения справедливы для любых молекул. Вес N молекул любого вещества относится к весу N молекул водорода как вес одной молекулы этого вещества к весу N молекул водорода.
Число N было выбрано по той причине, что вес N молекул водорода равняется молекулярному весу водорода в граммах. То есть молекулярный вес водорода — 2, а вес N молекул водорода — 2 грамма. И, согласно описанным в предыдущем абзаце пропорциям, N молекул любого вещества будут иметь вес равный молекулярному весу этого вещества, выраженному в граммах. Как уже быkо установлено, N молекул Cl2 весит 71 грамм, а молекулярный вес хлора — 71.
Поскольку молекулярный вес воды, H2O, равен 1 + 1 + 16, то есть 18, то мы сразу же можем сказать, что N молекул воды будут весить 18 граммов, а N молекул углекислоты (молекулярный вес которой — 44) будут весить 44 грамма.
Вес равный молекулярному весу вещества, только в граммах, называют «грамм-молекулярным», или «молярным», а количество вещества в таком случае получило название «моль». Так что N молекул любого вещества — это 1 моль этого вещества. Один моль водорода весит 2 грамма, 1 моль воды — 18 граммов, 1 моль углекислоты — 44 грамма и так далее. Веса во всех этих случаях различны, но количество вещества определяется не весом, а количеством молекул.
Естественно, все вышеизложенное справедливо и для отдельных атомов. Так, N атомов углерода (С) весят 12 граммов, а N атомов серы (S) весят 32 грамма. Атомный вес, выраженный в граммах, правильнее было бы называть «грамм-атомным» весом. Однако простоты ради я буду использовать термин «моль» применительно и к грамм-молекулярному, и к грамм-атомному весу.
Таким образом, химические выражения могут трактоваться двояко. Они описывают как поведение одного атома или одной молекулы, так и поведение N атомов или молекул. К примеру, выражение
2Н2 + O2 → 2H2O
можно читать как «две молекулы водорода плюс одна молекула кислорода переходят в две молекулы воды», а можно как «два моля водорода плюс один моль кислорода переходят в два моля воды». Поскольку молекулярные веса водорода, кислорода и воды составляют 2,32 и 18, то 1 моль каждого из них весит соответственно 2 грамма, 32 грамма и 18 граммов. Так что вышеприведенное выражение можно прочесть и так: «4 грамма водорода плюс 32 грамма кислорода переходят в 36 граммов воды».
Как видно, закон сохранения материи при этом не нарушается. Изначально мы имеем 36 граммов водорода и кислорода, а в итоге — 36 граммов воды. Это справедливо только тогда, когда выражение записано в уравновешенной форме.
Еще раз: видя перед собой выражение типа
С + O2 → CO2,
мы можем прочесть его трояко:
а) «один атом углерода плюс одна молекула кислорода переходят в одну молекулу углекислоты»;
б) «один моль углерода плюс один моль кислорода переходят в один моль углекислоты»;
в) «12 граммов углерода плюс 32 грамма кислорода переходят в 44 грамма углекислоты».
Вот мы и освоили язык химических формул в том объеме, который будет необходим нам для рассуждений об изменении энергетического содержания веществ в ходе химических реакций аналогичных (хочется верить) тем, что происходят в организме человека.
Глава 8. ТЕПЛО И ХИМИЧЕСКИЕ РЕАКЦИИ
Способа напрямую измерить химическую энергию не существует, но тепловую энергию измерить несложно. Предположим, что некоторую реакцию проводят в замкнутой камере, запуская ее, скажем, через электрический провод. Со всех сторон камера омывается определенным количеством воды, которая тщательно перемешивается. Вся система «камера плюс вода» изолирована во избежание теплообмена с окружающей средой.
Предположим, что в камере электрический ток поджигает смесь водорода с кислородом. В результате происходит вспышка и образуется вода. Химическая энергия, представленная связями между атомами водорода и кислорода в молекулах соответствующих газов, больше, чем представленная связями в молекуле воды. Поэтому при переходе от кислорода и водорода к воде химическая энергия теряется. Но эта потеря химической энергии строго уравновешивается выработкой равного количества энергии в форме тепла.
Когда в камере появляется это тепло, температура окружающей камеру воды повышается. Перемешивание воды обеспечивает ее равномерный и как можно более быстрый прогрев. Изоляция системы гарантирует, что повышение температуры воды происходит исключительно за счет повышения температуры в камере.
Измерение повышения температуры заранее известного объема воды позволяет подсчитать количество калорий тепла, вырабатываемого в ходе реакции («теплоту реакции»), что автоматически свидетельствует об аналогичном изменении в содержании химической энергии. Строго говоря, при обычной реакции горения не вся вырабатываемая в ее ходе энергия уходит в тепло, поскольку, как правило, кроме тепла вырабатывается еще и значительное количество света. Однако в замкнутой камере любой вырабатываемый свет быстро поглощается стенами и переводится в тепло. Есть крайне малая вероятность того, что реакции будет сопутствовать увеличение химической энергии, и тогда для уравновешивания этих изменений должно будет исчезнуть эквивалентное количество тепла, и, следовательно, температура окружающей камеру воды понизится.
Рис. 8. Калориметр с бомбой
Такую камеру называют калориметром (от латинских слов «тепло» и «мерить»), а исследования, проводимые с ее использованием, — калориметрическими. Реакции, производимые в камере калориметра, обычно происходят со скоростью взрыва, поэтому саму камеру иногда называют «бомбой» (рис. 8).
История современных способов калориметрии началась с экспериментов датского химика Юлиуса Томсена и французского физика Пьера Эжена Марселена Бертло, которые произвели сотни калориметрических измерений во второй половине XIX века.
Измеряя теплоту реакций превращения смеси водорода и кислорода в воду, невозможно установить абсолютное количество химической энергии, присутствующей в смеси водорода и кислорода, или в воде. Можно измерить лишь разницу химических энергий до и после реакции — разность уровней химической энергии воды и смеси водорода и кислорода. Но только эта разность и может представлять практический интерес для химика, поскольку, согласно второму закону термодинамики, количество работы, которое можно извлечь из химической реакции, зависит только от разности уровней химической энергии, так же как и количество работы, которое можно извлечь из тепловой машины, зависит только от разности уровней тепловой энергии (то есть температур).
В физике и математике любую разность часто представляют греческой буквой «дельта» (Δ) перед самим значением. Таким образом, если мы обозначаем энергию буквой Е, то разность энергий будет обозначаться как ΔЕ, что читается как «дельта Е». Применительно к реакции получения воды из водорода и кислорода, ΔЕ может представлять как потерю химической энергии во время этого процесса, так и получение тепловой. Естественно, в обоих этих случаях она будет иметь одно и то же значение.
Однако измерение теплоты реакции можно проводить двумя способами. Вещества, вступающие в химическую реакцию, можно брать в определенных количествах, как это делается в калориметрах. Объем бомбы калориметра в ходе реакции не меняется. Если в результате реакции увеличивается количество газа (а калориметрические эксперименты проводят чаще всего именно с газами или парами), занимаемый им объем все равно остается прежним и соответственно давление возрастает. И если количество газа уменьшается, объем все равно остается прежним и давление падает. Обозначение ΔЕ специально относится к изменению энергии именно в данных условиях сохранного объема и переменного давления. (Иногда используется обозначение ΔU, но я буду придерживаться ΔЕ.)
С другой стороны, можно представить себе и ситуацию, когда реакция проводится в сосуде, верх которого представляет собой поршень, способный сдвигаться вверх и вниз без трения, герметично прилегая при этом к стенкам сосуда. В таком сосуде давление меняться не будет, поскольку оно всегда будет оставаться ровно таким, чтобы держать вес поршня. При возрастании давления поршень будет двигаться вверх, пока объем той части сосуда, где произошла реакция, не вырастет настолько, что давление опять приобретет прежнее значение. Если же давление упадет, то и поршень двинется вниз, что приведет к уменьшению объема и увеличению давления до уравновешивающего значения. В таких условиях, независимо от того, как меняется в ходе реакции количество газа, давление останется неизменным, а меняться будет только объем. Тогда реакция будет происходить при постоянном давлении и переменном объеме.
Один моль любого газа при нормальном атмосферном давлении занимает всегда один и тот же объем (22,4 литра), поскольку размер молекул не влияет на их количество в заданном объеме. В реакции водорода и кислорода
2Н2 + O2 → 2H2O
2 моля водорода соединяются с 1 молем кислорода для образования 2 молей воды (разумеется, при той температуре, при которой происходит эта реакция, вода образуется в единственно возможной форме — газообразной, то есть получается водяной пар). Иначе говоря, на входе реакция имеет 3 моля газов, а на выходе — только 2. (Разумеется, масса участвующего в реакции вещества не меняется; просто в воде атомы сгруппированы плотнее, чем в водороде и кислороде.)
Рис. 9. Реакция соединения водорода и кислорода при постоянном давлении и при постоянном объеме
В камере с поршнем это уменьшение объема тут же вызовет втягивание поршня, и давление восстановится на прежнем уровне. В бомбе калориметра, где объем уменьшиться не может, вместо этого на треть уменьшится давление (возможно, это проще понять, рассмотрев рис. 9).
В первом и во втором случаях будет зафиксировано разное количество изменения энергии. При постоянном давлении оно будет больше, чем при постоянном объеме. Символ, которым обозначают изменение энергии при постоянном давлении, — ΔН, где Н — тепловое содержание, иначе именуемое «энтальпия». Таким образом, для нашей конкретной реакции ΔН больше, чем ΔЕ. Это отношение можно выразить и математически, и одно можно без проблем вывести из другого.
В природе химические реакции происходят обычно при постоянном давлении — это атмосферное давление, и оно практически всегда одинаково. Поэтому из двух названных нами величин больше практической ценности имеет ΔН, и получаемую с помощью калориметра ΔЕ переводят в ΔН.
Возникает вопрос и о том, для какого количества материала подсчитывается ΔН. Очевидно, что если в кислороде сжечь 10 граммов водорода, то будет произведено в десять раз больше тепла, чем если сжечь 1 грамм. Более того, каким образом сравнивать тепло от сжигания водорода с теплом от сжигания углерода? Если сжечь для сравнения по грамму того и другого, то как учесть при этом тот факт, что 1 грамм водорода содержит в двенадцать раз больше атомов, чем 1 грамм углерода?
Химики решили, что полезнее всего с практической точки зрения определять тепло реакции на молярной основе, то есть сравнивать теплоту реакции 1 моля водорода, сжигаемого в кислороде, с теплотой реакции 1 моля опять же сжигаемого в кислороде углерода. Тогда веса участвующих в реакции веществ будут разными, но количество молекул — одинаковым, а это важнее.
Поэтому ΔН, как правило, принято понимать как «молярную теплоту реакции при постоянном давлении». Это та величина, на которую изменяется тепловое содержание 1 моля интересующего нас вещества при его вступлении в реакцию.
Вернемся к примерам. Вот еще одно соединение — углерода и кислорода:
С + O2 → CO2.
Молярная теплота данной реакции — 94,03 килокалории. Поэтому для полноты уравнения это значение тоже следует указать в выражении, поскольку в полном значении этого слова соединение углерода и кислорода производит не только углекислоту, но и энергию в виде света и тепла. Поэтому в полном виде наше выражение будет выглядеть так:
С + O2 → СO2 + 94,03 ккал.
Это можно прочесть так: 1 моль углерода плюс 1 моль кислорода производят 1 моль углекислоты плюс 94,03 килокалории. Или так (что то же самое): 12 граммов углерода плюс 32 грамма кислорода производят 44 грамма углекислоты плюс 94,03 килокалории.
Чаще же теплоту реакции не вписывают в само уравнение, а указывают сбоку, как отдельный параметр, таким образом:
С + O2 → CO2
ΔН = -94,03 ккал.
Обратите внимание, что значение ΔН в данном случае приведено как отрицательная величина. Дело в том, что при соединении углерода с кислородом химическая энергия системы уменьшается, а тепловая — увеличивается. Если рассматривать этот процесс с точки зрения химической энергии, то изменения в энергетическом содержании покажутся отрицательными, а если с точки зрения тепловой — то положительными. Количество энергии, естественно, остается неизменным, независимо от точки зрения, при условии, что в процессе рассмотрения различных реакций сама точка зрения тоже остается неизменной. В течение некоторого периода одни химики расценивали изменения в энергии, при которых отдается тепло, как положительные, а другие — как отрицательные. В результате получалась путаница, и сейчас решено в этом случае использовать всегда отрицательное значение.
Далее, рассмотрим процесс горения водорода. Этот процесс можно, как я уже говорил, описать двумя способами, каждый из которых будет уравновешенным:
2Н2 + O2 → 2H2O,
Н2 + 1/2O2 → H2O,
Химиков интересует, как правило, тепло, вырабатываемое при сжигании 1 моля водорода, так что второе выражение, при котором используется 1 моль водорода, является для них предпочтительным. (Для любых же других химических целей, за исключением подсчета теплоты реакции, предпочтительным является первое выражение.)
Итак, идем дальше: данные калориметрических измерений позволяют нам написать
Н2 + 1/2O2 → H2O,
ΔН = -68,37 ккал.
Это то значение теплоты реакции, которое получается, если дать получаемой воде остыть до жидкого состояния, иначе говоря, в нее включается и отдаваемая при остывании латентная теплота парообразования. Если же вода остается в газообразном состоянии, то без латентной теплоты парообразования ΔН становится равной только -57,8 килокалории. Однако такого рода уточнения, как бы важны они ни были для химиков, для нас сейчас не будут представлять особого интереса.
Сравнивая теплоту реакции горения углерода с теплотой реакции горения водорода, мы сравниваем их моль к молю. Один моль горящего углерода отдает почти в два раза меньше тепла, чем 1 моль горящего водорода. Но моль углерода весит 12 граммов, а моль водорода — всего 2 грамма. Если мы будем сравнивать эти вещества грамм к грамму, мы увидим, что 1 грамм углерода при сжигании отдает 94,03/12, то есть 7,8 килокалории, а грамм водорода — 68,37/2, то есть 34,2 килокалории. Соответственно при весовом подходе (который является естественным для всех, кроме химиков) логично сделать вывод, что при сжигании водорода вырабатывается почти в 41/2 раза больше энергии, чем при сжигании углерода. Так что всегда важно знать, что именно предстоит сравнивать.
Уголь представляет собой практически чистый углерод, а водород — он и есть водород. Однако существуют важные виды топлива, молекулы которых содержат более одного вида элементов. В состав молекул различного вида нефтепродуктов — бензина, керосина, дизельного топлива — входят и водород, и углерод. В состав древесины входят молекулы, содержащие и углерод, и водород, и кислород. Такие молекулы, хоть и гораздо более сложны, подчиняются тем же самым законам. Возьмем для примера метан, основную составляющую так называемого «природного газа», используемого в газовых плитах и газовом отоплении. Молекула метана состоит из 1 атома углерода и 4 атомов водорода (СН4). Вот так выглядит выражение, описывающее соединение метана с кислородом:
СН4 + 2O2 → СO2 + 2H2O
ΔН — -210,8 ккал.
Как видно из формулы, при этом образуются и углекислота, и вода.
Если оценивать молярно, то метан способен вырабатывать больше тепла, чем и углерод, и водород по отдельности. Однако молекулярный вес метана — 16 складывается из 12 — веса атома углерода и 4 — веса 4 атомов водорода. Соответственно 1 грамм метана выделяет при горении 210,8/16, то есть 13,2 килокалории. Это больше, чем тепло, высвобождаемое при горении 1 грамма углерода, но меньше, чем тепло, высвобождаемое при горении 1 грамма водорода. Собственно, этого и следовало ожидать от вещества, состоящего частично из углерода, частично из водорода.
Пример еще более сложной молекулы — этиловый спирт (известное вещество, присутствующее в пиве, вине и виски и других алкогольных напитках). Его молекула состоит из 2 атомов углерода, 6 атомов водорода и 1 атома кислорода (С2H6O).
Так выглядит выражение для реакции его горения:
С2H6O + 3O2 → 2СO2 + 3H2O
ΔН = —327,6 ккал.
Молекулярный вес этилового спирта — 46 (24 — 2 атома углерода, 6 — 6 атомов водорода, 16 — 1 атом кислорода), так что при сгорании 1 грамма этилового спирта высвобождается 3276/46, то есть 7,1 килокалории. Это гораздо меньше, чем при сгорании грамма водорода или метана. Это даже меньше, чем при сгорании 1 грамма углерода. Дело в том, что в молекуле спирта уже имеется 1 атом кислорода, поэтому такую молекулу можно рассматривать, так сказать, как уже частично сгоревшую. Один из 7 атомов кислорода, необходимых для связывания всех имеющихся атомов углерода и водорода в углекислоты и воду, уже присутствует в молекуле.
Участие в реакции кислорода не является обязательным условием выделения при ней тепла (хотя именно реакции такого плана с участием кислорода стали первыми известными человечеству). На самом деле любые химические изменения имеют некоторую теплоту реакции. К примеру, в предыдущей главе уже приводились выражения для реакции формирования хлороводорода из водорода и хлора и хлорида натрия — из натрия и хлора.
ΔН первой из этих реакций 22,6 килокалории (для создания 1 моля хлороводорода из половины моля водорода и половины моля хлора), а второй 98,3 килокалории (для создания 1 моля хлорида натрия из 1 моля натрия и половины моля хлора).
Существует такой тип веществ, как кислоты, характеризующийся определенным набором свойств, который может вступать в реакцию с другим типом веществ, так называемыми основаниями, обладающими свойствами прямо противоположными кислотным. В результате этих реакций образуются вещества, чьи свойства не близки ни кислотам, ни основаниям. Такие реакции называются «реакциями нейтрализации», и мы приведем пример одной из них. Вот как реагирует хлороводород, раствор которого имеет кислотные свойства, с гидроксидом натрия, раствор которого является основанием (в результате реакции получаются хлорид натрия и вода):
НСl + NaOH → NaCl + H2O
ΔН = -137,4 ккал.
Даже такие процессы, которые химическими можно назвать лишь с некоторой натяжкой, например растворение некоего вещества в воде, могут выделять тепло реакции. Это вполне логично, поскольку при растворении вещества происходит замена сил, удерживающих его молекулы вместе, на силы, удерживающие его молекулы посреди молекул воды. Так, если в воде растворить карбонат натрия (пищевую соду), то ΔН этого процесса (именуемого в данном случае «молярной теплотой растворения», а не «молярной теплотой реакции») составит около -5,64 килокалории.
Остановимся поподробнее на карбонате натрия. Формула этого вещества — Na2CO3, молекулярный вес — 106 (46 — вес 2 атомов натрия, 12 — вес углерода и 48 — вес 3 атомов кислорода), так что растворение 1 грамма карбоната натрия приведет к выделению 564/106, то есть 0,053 килокалории. Это 53 калории, то есть меньше тепла, чем выделится при замерзании 1 грамма воды, так что неудивительно, что факт выделения тепла при растворении соды остается незамеченным.
Изменения химической энергии не должны нарушать законы термодинамики. Я уже упоминал об этом, когда подчеркивал, что изменение уровня химической энергии должно компенсироваться противоположным изменением уровня тепловой энергии, чтобы не оказался нарушенным первый закон термодинамики. Но это еще не все.
Самый первый закон о свойствах химической энергии вывели в свое время Лавуазье и другой французский ученый, Пьер Симон де Лаплас, который в 1780 году на основании достаточно грубых (по позднейшим меркам) измерений сделал вывод, что тепло, поглощаемое при разложении вещества на составляющие, равняется теплу, затрачиваемому на то, чтобы создать это же вещество из этих же составляющих.
Вот пример. Я уже говорил, что при соединении водорода и кислорода выделяется 68,37 килокалории тепла на моль сгоревшего водорода, или (что то же самое, как видно из уравнения) на моль получившейся воды:
Н2 + 1/2O2 → H2O,
ΔН = -68,37 ккал.
Следовательно, согласно закону Лавуазье—Лапласа, разложение 1 моля воды на водород и кислород (выражение для этого действия можно получить, просто обратив вспять выражение для создания воды из составляющих) потребует приложения 68,37 килокалории энергии, то есть
H2O → Н2 + 1/2O2,
ΔН = +68,37 ккал.
В данном случае значение ΔН положительно, поскольку вода в ходе реакции получает, а не отдает химическую энергию за счет того, что для того, чтобы реакция разложения молекулы воды оказалась возможной, к ней прилагают энергию тепловую или (что чаще) электрическую.
Рис. 10. Механическая энергия и химическая энергия
Можно провести аналогию между химической энергией и механической. В механике кинетическая энергия движущегося вверх предмета полностью преобразуется в потенциальную энергию в верхней точке подъема, а затем — обратно в изначальную кинетическую энергию в нижней точке падения. Точно таким же образом нехимическая энергия, которую получает вода, переводится в химическую путем распада на смесь водорода с кислородом, а затем вновь переходит в нехимическую, когда водород с кислородом снова соединяются, образуя воду (рис. 10).
Разумеется, полное равенство достижимо только в идеальных условиях. В отношении механической энергии — это отсутствие трения и сопротивления воздуха, в отношении химической — это отсутствие теплопотери. В реальности, когда воду разлагают с помощью электрического тока, часть электрической энергии всегда теряется, переходя в тепло; а если энергию сразу подают в воду в тепловом виде, то часть ее обязательно уходит в окружающее пространство. В любом случае сначала приходится тратить больше энергии, чем ее удастся получить в итоге. Однако это лишь отражение увеличения энтропии, а в целом же данный факт только лишний раз подтверждает, что в отношении химической энергии законы термодинамики соблюдаются так же, как и а отношении любой другой.
Еще один важный закон открыл в 1840 году физик по имени Герман Иванович Гесс в Санкт-Петербурге (Россия). Проведя множество экспериментов в области теплоты реакций, он сделал вывод, что в общем случае, если реакция происходит в несколько стадий, то общий объем теплоты реакций в цепочке будет тот же, что и в том случае, если производить реакцию в один прием. Этот закон был назван именем открывшего его ученого и оказался столь важным, что Гесса сейчас принято считать отцом термохимии (тепловой химии).
В качестве простого примера (хоть и не попавшего в число тех, что наблюдал сам Гесс) можно привести опять же горение углерода. Углерод может соединяться с кислородом и в пропорции атомов 1:1 — в таком случае получается угарный газ, СО. Соответственно мы можем написать такое выражение:
C + 1/2O2 → CO
ΔН = -26,4 ккал.
Угарный газ способен гореть, то есть объединяться еще с одним атомом кислорода в более распространенный углекислый газ:
CO + 1/2O2 → CO2,
ΔН = -67,6 ккал.
Если мы сложим оба этих выражения (как будто бы это были просто математические уравнения), то по закону Гесса мы должны будем получить суммарную теплоту реакции.
С + 1/2О2 + СО + 1/2О2 → СО + СО2
ΔН = (-26,4) + (-67,6) ккал.
Преобразовав получившееся выражение опять же по законам математики, то есть сократив находящийся по обе стороны уравнения СО и сложив две половинки молекулы кислорода в одну целую, мы получаем
С + О2 → СО2
ΔН = -94 ккал,
то есть именно то же самое выражение, которое мы вывели бы, если бы просто сжигали углерод, получая при этом в один прием углекислоту.
Более общая формулировка закона Гесса звучит так: при преобразовании химическим образом вещества А в вещество В итоговое изменение энергетического содержания будет одним и тем же, независимо от того, каким путем вещество было преобразовано. Здесь можно снова провести аналогию с механической энергией, где совершенно не важно, каким образом и по какому маршруту тело было перемещено из одного положения в другое; на изменение его потенциальной энергии влияет только само изменение положения.
Должен признаться, что, приведя в качестве самого простого примера действия закона Гесса процесс горения углерода, я несколько погрешил против истины. Измерить напрямую количество тепла, получаемого при сжигании углерода с образованием угарного газа, невозможно, поскольку нельзя построить эксперимент таким образом, чтобы углерод, соединяясь с кислородом, образовывал только угарный газ. Чистый угарный газ можно получать, но по-другому.
Однако термохимик способен произвести из углерода углекислоту и измерить теплоту этой реакции (получится -94 килокалории). Может он и путем сжигания сделать из угарного газа углекислый, снова измерив при этом теплоту реакции (получится -67,6 килокалории). Затем, положившись на закон Гесса, он вычтет из первой теплоты реакции вторую и сделает вывод, что молярная теплота реакции перевода углерода в моноксид углерода, угарный газ, составит -26,4 килокалории, хотя доказать это экспериментально ученый окажется не в состоянии.
Важность закона Гесса заключается в том, что он означает следующее: теплоту любой реакции, даже той, которую по каким-то причинам невозможно измерить, можно высчитать исходя из теплоты других, более доступных для экспериментатора реакций.
Например, существует такой углеводород, как этилен, — это газ, молекулы которого состоят из 2 атомов углерода и 4 — водорода (С2Н4). Один моль этого газа, сгорая в кислороде, выделяет 340 килокалорий. Выражение для этой реакции выглядит так (я пронумерую выражения для удобства отсылки к ним в дальнейшем):
1) С2Н4 + 3O2 → 2СO2 + 2H2O
ΔН = -340 ккал.
Я уже описывал процессы горения углерода и водорода, но сейчас я снова выпишу выражения для этих реакций, потому что они нам понадобятся:
2) С + O2 → CO2
ΔН = -94 ккал.
3) Н2 + 1/2О2 → Н2О
ΔН = -68 ккал.
Теперь давайте проведем математические преобразования этих химических выражений. Если вы из тех, кого тошнит от математики, то можете смело пролистнуть остаток этой главы; остальным же, думаю, должно понравиться.
В выражении 3 перенесем 1/2O2 из левой части уравнения в правую с переменой знака (на теплоте реакции это никак не скажется), получим:
4) Н2 → H2O — 1/2O2
ΔН = -68 ккал.
Теперь удвоим обе части выражения 4, при этом удвоится и теплота реакции:
5) 2Н2 → 2H2O — O2
ΔН = -136 ккал.
Сделаем то же самое с выражением 2 — переместим O2 в правую часть уравнения с переменой знака и удвоим все значения, включая теплоту реакции:
6) 2С → 2CO2 — 2O2
ΔН = -188 ккал.
Обратим выражение 1 без перемены знаков; в этом случае, согласно закону Лавуазье—Лапласа, изменится знак у теплоты реакции:
7) 2СO2 + 2H2O → С2Н4 + 3O2
ΔН = +340 ккал.
В выражении 7 переместим 2СO2 и 2H2O в правую часть с переменой знака — знак теплоты реакции останется при этом неизменным:
8) Ноль → С2Н4 + 3O2 — 2СO2 — 2H2O
ΔН = +340 ккал.
(Я написал здесь «ноль» вместо 0, чтобы его не путали с обозначением кислорода — О.)
Теперь же давайте сложим выражения 5, 6 и 8, не забывая складывать и значения теплоты реакций. Мы получим следующий результат:
9) 2Н2 + 2С → 2H2O — O2 + 2СO2 —
— 2O2 + С2Н4 + 3O2 — 2СO2 — 2H2O
ΔН = (-136) + (-188) + (+340) ккал.
Проведя все возможные математические сокращения правой части, мы увидим, что сократилось все, кроме С2Н4, так что все выражение теперь сводится к
10) 2Н2 + 2С → С2Н4
ΔН = +15,2 ккал.
Таким образом, мы обнаружили, что если мы хотим 2 моля водорода заставить вступить в соединение с 2 молями углерода для получения 1 моля этилена, то для того, чтобы реакция состоялась, необходимо затратить 15,2 килокалории энергии. Иными словами, 1 моль этилена содержит на 15,2 килокалории больше химической энергии, чем составляющие его углерод и водород. Или можно сказать так: молярное тепло формирования этилена равняется + 15,2 килокалории.
На самом деле напрямую измерить это тепло формирования невозможно, поскольку не существует такой химической реакции, в ходе которой можно было бы за один шаг создать этилен из углерода и водорода. Тем не менее вышеприведенная цифра не вызывает у химиков никаких сомнений. Во-первых, все математические действия, произведенные нами, обоснованы вторым законом термодинамики, которые не оспаривает никто из химиков, а во-вторых, во всех тех случаях, где математические расчеты можно проверить практикой, они подтверждаются.
По этим причинам теплота формирования этилена и многих других соединений рассчитывается на бумаге ко всеобщему удовлетворению, и тот факт, что получаемые значения не проверены на практике и никогда не будут проверены, никого не смущает.
Глава 9. НАПРАВЛЕНИЕ РЕАКЦИИ
Закон Гесса является выражением первого закона термодинамики применительно к химическим реакциям, и теперь мы переходим к дальнейшему. Несколько глав назад мы сделали попытку определить жизнь через энтропию, а также предположили, что жизнь как процесс в чем-то сродни горению и, следовательно, должна потреблять химическую энергию. Теперь мы попытаемся установить, как же действует второй закон термодинамики применительно к химическим реакциям.
В отношении механической энергии мы уже знаем, что второй закон термодинамики требует, чтобы предметы спонтанно перемещались из положения с большей потенциальной энергией (в данном случае она называется «гравитационным потенциалом») к положению с меньшей, и не наоборот. Вода течет по склону горы вниз, а не вверх. В отношении тепловой энергии второй закон термодинамики требует, чтобы тепло спонтанно переходило только от горячих тел (обладающих большей температурой — «тепловым потенциалом») к холодным, а не наоборот. Продолжая аналогию, можно предположить, что и химические реакции будут проходить таким образом, чтобы вещество переходило из состояния с большим «химическим потенциалом» в состояние с меньшим, и не наоборот.
Соответственно возникает вопрос: что же это за химический потенциал и как его измерить?
Бертло, которого я упоминал в предыдущей главе, как автора множества экспериментов по измерению теплоты реакции, считал, что ответ может крыться в самих этих измерениях. Он высказывал мнение, что спонтанными можно считать те реакции, которые характеризуются снижением химической энергии и соответственно выделением тепла, то есть те, ΔН которых отрицательна. С другой стороны, реакции, при которых химическая энергия увеличивается, так что тепло извлекается из окружающей среды (иными словами, ΔН которых имеет положительное значение), не будут протекать спонтанно.
Бертло назвал реакции первого типа (с выделением тепла в окружающую среду) «экзотермическими» (от греческого «тепло наружу»), а реакции второго типа (с поглощением тепла из окружающей среды) — «эндотермическими» (что означает «тепло внутрь»). По мнению Бертло, спонтанными могут быть только экзотермические реакции.
Существует множество примеров, которые подтверждают это правило. Например, смесь водорода с кислородом, если ее поджечь, возгорится мгновенно и даже взрывообразно, соединяясь в воду, — это экзотермическая реакция. С другой стороны, вода может вечно находиться в стабильном состоянии, не выказывая ни малейшего желания разлагаться на водород и кислород, — если бы этот процесс начался, он был бы эндотермическим. Точнее, если воду как следует нагреть, она начнет разлагаться, но ведь и вода может течь вверх, если ее качать насосом.
Тут можно возразить, что смесь водорода с кислородом тоже может вечно находиться в стабильном состоянии, совершенно не собираясь вступать в реакцию, пока в систему, опять же, не добавят избыточное тепло. Однако есть принципиальная разница. После того как некоторое количество избыточного тепла подожжет смесь водорода с кислородом, дальше реакция продолжается сама сколь угодно долго. Если же, с другой стороны, добавление дополнительного тепла, или электрического тока, запускает реакцию разложения воды на водород и кислород, то прекращение подачи тепла или электричества тут же приведет к остановке реакции на любом этапе.
Короче говоря, экзотермическая реакция соединения водорода и кислорода в принципе может продолжаться спонтанно, а эндотермическая реакция разложения воды — не может.
Однако, к огорчению Бертло, это правило оказалось недостаточно всеобъемлющим. Все экзотермические реакции действительно происходят спонтанно, а все эндотермические, как правило, не происходят спонтанно. Однако все же есть несколько реакций, которые являются эндотермическими и при этом все же происходят спонтанно. Лучшим примером такого рода реакций является растворение некоторых веществ в воде. Если аммиачную селитру высыпать в воду, то она спонтанно растворится, хотя АН этого процесса и будет положительна. При этом происходит набор химической энергии, а тепловая — извлекается из воды, которая становится ледяной на ощупь. И не важно, скольким количеством примеров подтверждается теория Бертло, для того, чтобы опровергнуть ее, достаточно и единственного исключения.
Однако на самом деле ущербность теории Бертло доказывается не только фактом наличия нескольких опровергающих ее исключений. Против нее имеются и некоторые более тонкие возражения, подводящие нас к идее «химического равновесия».
Реакции, которые вызывают наибольший интерес термохимиков — реакции горения, — кажутся однонаправленными. То есть углерод и кислород соединяются навсегда для образования углекислоты, водород и кислород — для образования воды, соединения, имеющие в своем составе и углерод, и водород, соединяются навсегда с кислородом для образования углекислоты и воды. Более того, никогда вода в сколь-либо заметных количествах не разлагается на водород и кислород, а углекислота — на углерод и кислород. И вода никогда не соединяется с углекислотой для образования этилена или других углеводородов. Такие однонаправленные реакции также называют необратимыми.
Однако положение дел обстоит таким образом далеко не со всеми химическими реакциями. Например, посмотрим на одну из реакций с участием водорода и йода. При обычной температуре йод представляет собой синевато-серое твердое вещество, но плавное нагревание его приводит к появлению фиолетового газа, а при температуре выше 184 °С он существует исключительно в виде газа. В газообразном состоянии йод состоит из двухатомных молекул (I2).
Если же смешать йод с водородом при температуре, скажем, 445 °С, будет образовываться соединение йодоводород (HI):
H2 + I2 → 2HI.
Однако в соединение вступают не весь йод и не весь водород. Сколько бы времени ни протекала реакция, все равно часть йода и часть водорода не будут в ней участвовать.
Если же, наоборот, произвести некоторое количество чистого йодоводорода и нагреть его до тех же 445 °С, то он начнет разлагаться на йод и водород:
2HI → Н2 + I2.
И опять же, независимо от того, сколько времени протекает реакция, распадется не весь йодоводород. На самом деле, что бы мы ни взяли изначально — смесь ли йода и водорода или йодоводород, в итоге мы получим одно и то же соотношение: около 80% йода и водорода будут находиться в соединенном виде HI; около 20% — в разрозненном. Такие реакции, способные протекать в обоих направлениях, называют обратимыми.
Очевидно, происходит следующее: водород и йод, будучи смешанными при высокой температуре, быстро соединяются, образуя йодоводород. Образуемый йодоводород имеет тенденцию к распаду при такой температуре, но так много йода и водорода задействовано в процессе соединения, а йодоводорода еще так мало, что наблюдателю заметен только эффект соединения, и количество йодоводорода в эксперименте только увеличивается.
Однако по мере увеличения количества йодоводорода все больше и больше соединившихся молекул начинает распадаться, а одновременно с этим количество все еще продолжающих объединяться молекул водорода и йода сокращается, и скорость образования йодоводорода снижается. По мере того как скорость распада йодоводорода возрастает, а скорость образования — снижается, должен наступить момент, когда эти два процесса уравновесят друг друга. Эксперимент показывает, что этот момент наступает при соотношении йодоводорода к смеси йода и водорода 80: 20. Дальше никаких изменений мы уже не увидим, и не потому, что все процессы на этом останавливаются, а потому, что одновременно происходят два противоположно направленных и взаимно уравновешивающих друг друга процесса.
Теперь предположим, что изначально у нас имеется не смесь, а чистый йодоводород (рис. 11). Некоторые его молекулы начинают распадаться сразу же. По мере накопления водорода и йода в общем объеме в этих газах начинают проявляться тенденции к воссоединению, сила которых возрастает по мере накопления самих газов. И наоборот, по мере того, как количество молекул йодоводорода в общем объеме снижается, скорость распада оставшихся молекул также уменьшается. И опять же, как показывают наблюдения, в итоге наступает некий момент равновесия.
Когда два противоположно направленных процесса уравновешивают друг друга, это называется «состоянием химического равновесия». Само слово «равновесие» рисует в воображении картинку некоего замершего под действием разносторонне направленных сил положения дел. Это — статическое равновесие, но химическое равновесие — совсем не такое. Оба противоположно направленных процесса происходят со всей доступной им скоростью, но при этом аннулируют эффект друг друга. Это — динамическое равновесие.
Рис. 11. Отношения между скоростью реакции и химическим равновесием
Ситуация химического равновесия, такого как в нашем примере с водородом и йодом, обычно обозначается таким образом: двумя противоположно направленными стрелочками:
Н2 + I2 ↔ 2HI.
Таким же образом можно записать и любое количество других реакций.
Ключевой момент здесь следующий: каждой реакции, при определенных условиях, присуща своя ΔН. Обратной реакции, при тех же условиях, присуща та же самая ΔН, но с обратным знаком. Об этом свидетельствует закон Лавуазье—Лапласа и, что еще важнее, первый закон термодинамики.
Следовательно, в любой обратимой реакции, если реакция в одну сторону является экзотермической, то реакция в противоположную сторону должна быть эндотермической. Применительно к водороду, йоду и йодоводороду распад йодоводорода на водород и йод — экзотермическая реакция с ΔН -6 килокалорий. Соответственно соединение водорода и йода — реакция эндотермическая, с ΔН +6 килокалорий.
Если бы теория Бертло, согласно которой спонтанными могут быть только экзотермические реакции, была верна, то йодоводород сам по себе мог бы только распадаться и не соединяться обратно. Однако наблюдения показывают совсем иную картину. Йодоводород на самом деле соединяется, причем с большим размахом, чем распадается.
Если бы Бертло был прав, такого понятия, как обратимая реакция, вообще не существовало бы — все реакции были бы однонаправленными. Поскольку наблюдения прямо опровергают это предположение, то все идеи Бертло были очень быстро преданы забвению. Вообще непонятно, почему Бертло сам не увидел очевидного и не удержался от публичного высказывания своих предположений, — но легко быть крепким задним умом.
* * *
Итак, мы продолжаем пребывать в поисках химического потенциала. Итак, один фактор, вроде бы имеющий влияние на направление, принимаемое обратимой реакцией, — это процентное соотношение соединений в общем объеме. Если количественно преобладают водород и йод, то всеохватывающее значение примет тенденция к соединению. Систему можно сбить с положения устоявшегося химического равновесия, если просто добавить в нее либо йодоводород либо смесь водорода и йода.
Первым, кто четко сформулировал это наблюдение, был французский химик Клод Луи Бертолле в 1803 году (не путать с Бертло, которого я упоминал в предыдущей части — тот жил на полвека раньше!).
Примерно с полвека теория Бертолле о влиянии массы на направление реакции не находила общего признания химиков, хотя один за другим они пробовали ее на зуб. Наконец, в 1863 году норвежские химики Като Максимилиан Гульдберг и Петер Вааге тщательно разработали этот вопрос и сформулировали правило, которое мы сейчас называем «законом сохранения массы». К сожалению, они опубликовали свою работу на норвежском языке, и ведущие немецкие и французские ученые смогли прочитать ее только пятнадцать лет спустя.
Яснее всего продемонстрировать важность этого закона можно, если представить себе обратимую реакцию в общем случае, без указания конкретных реагирующих веществ. Ее можно записать так:
А + В ↔ С + D.
Предположим, реакция осуществляется слева направо, тогда А и В переходят в С и D. Но для этого надо, чтобы эти два вещества встретились. Чем их больше в общем объеме, тем легче им встретиться и тем быстрее протекает этот процесс. Важно не общее количество, а количество в определенном объеме, то есть концентрация вещества. Можно провести такую аналогию: для юной леди, стремящейся выйти замуж, гораздо больше вариантов для выбора можно найти в сельском штате Невада, чем в массачусетском городке Холиоке, но вот беда — все кандидатуры в Неваде разбросаны по территории штата, и получается, что в Холиоке концентрация выше, а значит — выше и шансы подобрать себе подходящий вариант.
Если концентрация А удваивается, то вместе с ней удваивается и частота встреч молекул А и В, а соответственно — скорость их реакции между собой. Аналогичным будет результат удваивания и концентрации В. Если одновременно удвоится концентрация и А и В, то частота встреч молекул этих двух веществ, а значит, и скорость реакции возрастет вчетверо. Соответственно скорость реакции соединения этих веществ равна произведению концентрации одного на концентрацию второго. Для обозначения концентрации некоего вещества принято изображать его заключенным в квадратные скобки, и мы можем сказать, что
скорость реакции слева направо ~ [А][В].
Известно, что если некая величина, х, прямо пропорциональна другой величине, у> то пропорциональность можно перевести в равенство, если умножить х на некое третье число, k, именуемое в таком случае коэффициентом. Иными словами, если х ~ у, то x = ky.
Итак, получаем:
скорость реакции слева направо = k [А][В].
Конкретное значение k для той или иной реакции можно установить только в ходе эксперимента.
Но сейчас нам и не нужно конкретное значение. Достаточно просто знать, что k — это фиксированная величина.
Теперь давайте перейдем к реакции справа налево, то есть к обратной реакции слева направо, когда соединение С и D приводит к образованию А и В.
Вся вышеприведенная логика относится и к реакции справа налево, поэтому понятно, что ее скорость зависит от концентрации С и D:
скорость реакции справа налево = k’ [C][D],
где k’ — другой коэффициент, скорее всего не равный первому и поэтому отмеченный штрихом.
По достижении химического равновесия скорость реакций в обоих направлениях одинакова (первым это установил английский химик Александр Уильям Уильямсон в 1850 году), что можно описать так:
k [А][В] = k’ [C][D],
соответственно, применив математические преобразования, получим
[C][D]/ [А][В] = k’/k.
Поскольку и k/k' — константы, то и отношение одного к другому тоже будет константой, назовем ее К. Следовательно,
[C][D]/ [А][В] = K,
где K — «постоянная равновесия», значение которой четко описывает те концентрации веществ, при которых скорость противоположно направленных реакций будет одинакова.
Допустим, к примеру, что к смеси, пребывающей в состоянии химического равновесия, добавляют некоторое количество С. В таком случае произведение [C][D], являющееся числителем дроби, увеличится. Чтобы К осталось постоянным, необходимо увеличить также и знаменатель дроби, [А][В]. Как это может произойти? Только одним образом — часть С и D должны вступить в соединение и образовать А и В. То есть [C][D] несколько уменьшится, а [А][В] — несколько увеличится, так что соотношение их снова приобретет значение К, при котором опять будет достигнуто химическое равновесие. То же самое произойдет и в том случае, если в исходную смесь добавить D, а не С.
Можете сами проверить, что случится, если в исходную смесь добавить А или В (или и то и другое) или, наоборот, из исходной смеси удалить любое из веществ.
Я подскажу. Неизменным свойством обратимых реакций является следующее: реакции типа
A + B ↔ C + D
начинают осуществляться в направлении слева направо при добавлении к изначальной смеси А или В или устранении из нее С или D и справа налево при добавлении С или D или устранении А или В.
(В 1901 году американский химик Гилберт Ньютон Льюис внес изменения в формулировку этого закона, получившего название «закон действия масс», указав, что на направление осуществления обратимой реакции влияет не концентрация веществ, а фактор, который ученый назвал «активностью» этих веществ. Это родственный концентрации фактор, часто практически равный ей, особенно когда концентрация невысока. Но нас это уточнение волновать не будет.)
Тот факт, что обратимая реакция именно таким образом реагирует на изменения концентраций участвующих в ней веществ, французский химик Анри Луи Ле Шателье в 1888 году положил в основу более общего закона, сформулировав его так: «В любой системе, находящейся в состоянии равновесия, любые изменения условий приводят к сдвигу положения равновесия в направлении частичного аннулирования произведенных изменений».
Этот закон называют принципом Ле Шателье.
Иными словами, если в набор веществ, участвующих в описанной нами обратимой реакции, добавляется А или В, то равновесие сдвигается в том направлении, в котором используется именно добавленное вещество. В более общем выражении, если смесь реагирующих веществ нагревать, то и равновесие будет сдвигаться в том направлении, в котором часть тепла поглощается, то есть в эндотермическом. Точно таким же образом, если смесь остудить, то равновесие сдвинется в направлении экзотермической реакции. Таким образом, можно сразу сказать, что нагрев системы, состоящей из йода, водорода и йодоводорода, приведет к смещению равновесия в сторону формирования большего количества йодоводорода, а остывание системы — в противоположном направлении. Аналогичным образом увеличение давления в системе приведет к сдвигу равновесия в том направлении, результатом которого станет уменьшение объема.
На самом деле вполне возможно рассматривать принцип Ле Шателье как универсальный, распространяющийся даже на поведение людей. Среднестатистический человек всегда поддерживает некое равновесие между доходами и расходами таким образом, чтобы ни накопления, ни долги не разрастались до слишком больших объемов. Если ему увеличивают зарплату или богатый дядюшка оставляет ему наследство, то уровень жизни этого человека, как правило, увеличивается настолько, чтобы компенсировать полученное увеличение дохода. Если же, наоборот, зарплату человеку урезают или он остается без работы, то он начинает экономить, урезать расходы, таким образом частично компенсируя этим уменьшение дохода.
* * *
После всеобщего утверждения закона действия масс все еще оставалась потребность в том, чтобы связать его с законами термодинамики, что показало бы, что химическая энергия подчиняется всем тем же законам, что и любая другая.
Еще в 1869 году немецкий химик Аугуст Фридрих Хорстманн использовал законы термодинамики для разложения вещества под названием «хлорид аммония», более известного нам как нашатырный спирт, а в течение 70-х и 80-х годов XIX века ряд других химиков тоже работали над этой проблемой.
Самых важных результатов смог добиться американский химик-теоретик Джозайя Уиллард Гиббс. Работая в Йельском университете, в 1876 и 1878 годах он опубликовал доклады в «Протоколах Коннектикутской академии наук», где подробно излагались законы термодинамики применительно к химическим реакциям. Он продемонстрировал, что закон действия масс — это неизбежное следствие из законов термодинамики. Его исследование оказалось столь совершенным, что ни о какой «термохимии» с тех пор и речи быть не могло, осталась только «химическая термодинамика».
К несчастью для Гиббса, в его дни весь мир импортировал науку из Европы и американских ученых ценили мало. Американские научные журналы никто не принимал всерьез, и работа Гиббса попала в поле зрения европейских ученых лишь два десятилетия спустя.
Наконец, в 1890-х годах Ле Шателье сам перевел труды Гиббса на французский язык, а немецкий специалист по физической химии Вильгельм Оствальд — на немецкий. И лишь тогда Гиббсу воздали должное. К тому времени Гельмгольц, первооткрыватель первого закона термодинамики, и датский физик Якоб Хендрик Вант-Гофф уже и сами независимым образом открыли принципы химической термодинамики, но первооткрывателем в итоге все же был признан Гиббс. В 1901 году Гиббс получил официальное европейское признание своих заслуг и был награжден медалью Коплея — самой почетной международной наградой Лондонского королевского общества, — и хорошо, что успел, потому что дожил он лишь до 1903 года.
По сути, все рассуждения Гиббса вертелись вокруг того факта, что при любой спонтанной химической реакции энтропия должна возрастать, как и при любых других энергетических изменениях. Поскольку общее количество задействованной энергии изменяться не может, а возрастание энтропии — это способ измерить энергию, которую невозможно перевести в работу, то, следовательно, количество энергии, которую можно перевести в работу, должно снижаться.
Количество энергии доступной для перевода в полезную работу в ходе химической реакции может быть различным, в зависимости от того, проходит ли реакция при постоянном давлении или при постоянном объеме. Как я объяснял в предыдущей главе, системы с постоянным давлением дают нам более приближенную к реальности картину. Количество энергии, доступной для перевода в работу в ходе химической реакции, называли в честь Гиббса «энергией Гиббса». В начале 1920-х годов Льюис назвал эту энергию «свободной энергией», — и это название тоже было принято, так что теперь используются оба названия, и обозначение этой энергии тоже может быть одним из двух: иногда ее обозначают F (по первой букве от англ. free — свободная), а иногда — G (по первой букве фамилии Гиббса). Сейчас «свободная энергия» является все же более распространенным названием, так что я в дальнейшем буду использовать обозначение F.
Гиббс показал, что в любой реакции, проходящей при неизменной температуре (Е), соблюдается простое отношение между изменениями теплового содержания (ΔР), изменениями свободной энергии (ΔF) и изменениями энтропии (ΔS). Это отношение таково:
ΔH = ΔF + TΔS.
В термодинамике всегда используются значения температуры по абсолютной шкале (см. главу 4), в которой нет отрицательных величин. Поэтому Т — всегда положительное число. Из второго закона термодинамики нам известно, что при любой спонтанной реакции энтропия возрастает, так что значение изменений в энтропии (ΔS) тоже должно быть положительным. А поскольку произведение двух положительных чисел тоже всегда положительно, то мы знаем, что значение TΔS всегда положительно.
С другой стороны, по мысли Гиббса, свободная энергия всегда уменьшается при любой спонтанной химической реакции, так что изменение свободной энергии (ΔF) всегда должно быть отрицательно.
Получается, что значение ΔН — это сумма отрицательного и положительного чисел. Но термодинамика, хоть и указывает нам, что одно из слагаемых — положительно, а второе — отрицательно, не позволяет выяснить, какое из них больше по модулю. Если модуль отрицательного ΔF больше, чем положительного TΔS, то мы получаем экзотермическую реакцию, если меньше — то эндотермическую.
В любом случае, какой бы реакция ни была — эндотермической или экзотермической, энтропия возрастает, количество свободной энергии снижается и реакция происходит спонтанно.
Соответственно надо обращать внимание не на то, выделяется или поглощается в ходе реакции тепло, а на то, какие изменения происходят со свободной энергией. Реакция всегда будет проходить в направлении, способствующем снижению уровня свободной энергии, по тому же закону, по которому тепло перетекает от горячего предмета к холодному, а шар — скатывается вниз.
Далее, Гиббс показал, что количество свободной энергии, присутствующей в любом химическом веществе, изменяется в зависимости от концентрации этого вещества. Меняя концентрацию вещества, возможно влиять на изменение свободной энергии таким образом, чтобы оно становилось отрицательным для одного направления реакции, хотя до этого оно было отрицательным же для противоположного. Именно поэтому на ход обратимой реакции можно влиять, добавляя в систему тот или иной компонент или удаляя его.
Это похоже на ситуацию с шаром, лежащим на гладкой ровной поверхности, которую можно слегка покачивать то в одну сторону, то в другую. Шар сам будет катиться в нужном направлении.
Гиббс составил выражение для расчета величины, в которой учитывались и свободная энергия, и концентрация, и назвал эту величину «химическим потенциалом». Ученый определил, что каждая реакция проходит в сторону уменьшения химического потенциала.
Глава 10. ЭЛЕКТРИЧЕСКИЙ ПУТЬ
При оценке действия изменений свободной энергии на химические системы ход химической реакции проще рассматривать по аналогии с движением в гравитационном поле. Это вполне разумное решение, поскольку на всем протяжении предыдущей главы мы доказывали, что химические реакции производятся под воздействием химического потенциала, так же как падающие тела движутся под воздействием гравитационного потенциала. А движение падающих тел нам настолько хорошо знакомо по бытовому опыту, что для нас вполне естественно визуализировать все по аналогии с ним.
Рассмотрим, к примеру, соединение водорода и кислорода, при котором формируется вода. Смесь водорода и кислорода содержит в себе определенное количество свободной энергии на моль смеси («молярная свободная энергия»), и вода тоже. Судя по тому факту, что водород с кислородом стремительно бросаются соединяться, стоит их лишь чуть-чуть подтолкнуть, — уровень свободной энергии смеси водорода и кислорода выше, чем образуемой при их соединении воды. Это можно представить в виде схемы (не претендуя при этом на использование каких-либо реальных цифр) — рис. 12. Точка А представляет собой уровень свободной энергии чистой смеси водорода и кислорода, а точка В (размещенная на оси ниже, чем точка А) представляет собой уровень свободной энергии чистой воды, образовавшейся при их соединении.
Рис. 12. Изменения свободной энергии при образовании воды (вверху) и йодоводорода (внизу)
По мере того как водород и кислород соединяются для образования воды, все большее количество молекул этих веществ в нашей воображаемой замкнутой системе уступает место молекулам воды. Постепенно смесь с высоким содержанием свободной энергии вытесняется веществом с более низким ее содержанием, так что общая свободная энергия системы постепенно снижается.
Самый простой способ продемонстрировать это — провести на диаграмме прямую линию от точки А до точки В. Таким образом мы получаем картинку наклонной плоскости, и общий жизненный опыт с легкостью подсказывает нам единственное направление, по которому будет осуществляться спонтанное движение по такой плоскости. Соединение водорода с кислородом для образования воды можно рассматривать как «скатывание вниз» по наклонной плоскости начиная с точки с высоким уровнем свободной энергии. Обратная же реакция — расщепление воды — отражает требующее усилий движение вверх по наклонной.
Точнее, нарисованный мной график в виде прямой линии был бы полностью справедливым только в том случае, если бы молярная свободная энергия водорода и кислорода не менялась вместе с концентрацией. Однако на самом деле уровень молярной свободной энергии по мере концентрации незначительно, но меняется, так что изображенная выше прямая линия в действительности не является совсем прямой. В данном конкретном примере отличие от прямой достаточно мало, чтобы им можно было пренебречь, но в тех случаях, где общая свободная энергия системы значительно меньше, чем у системы, состоящей из смеси водорода с кислородом, упомянутый параметр приобретает действительно важное значение.
Возьмем для примера реакцию соединения водорода и йода в йодоводород. В данном случае уровень свободной энергии, используемой в реакции, сравнительно невелик. Визуально это можно изобразить, как в нижней половине рис. 12, отметив значение уровня свободной энергии С смеси чистого водорода с чистым йодом лишь немного выше уровня свободной энергии D чистого йодоводорода, образуемого в ходе полного соединения водорода и йода.
Первое, что хочется сделать в подобной ситуации, — это снова провести прямую линию от одной точки до другой, так чтобы получилась еще одна наклонная плоскость, угол наклона которой был бы меньше, чем предыдущей, но в остальном аналогичная первой. Тогда реакция снова «катилась бы под уклон» — от смеси водорода и йода до йодоводорода, и образовавшийся в ее ходе йодоводород так и оставался бы неразлагаемым «у подножия», пока с помощью приложения некоторого усилия его не подняли бы «вверх». По такой логике смесь водорода и йода отличалась бы от смеси водорода и кислорода лишь скоростью и силой реакции, но не общим рисунком ее хода.
Но мы знаем, что на самом деле это не так. Водород и йод вступают в соединение не в полном объеме, а значит — не «скатываются вниз до конца». Более того, и чистый йодоводород до некоторого уровня будет сам по себе распадаться, что соответствовало бы по нашей схеме «движению вверх». Значит, график с прямой линией был бы неправильным.
Ответ кроется в том факте, что молярная свободная энергия снижается вместе с концентрацией вещества. Если концентрация смеси водорода и йода уменьшится на 10 процентов за счет образования йодоводорода, то уровень свободной энергии смеси снижается сильнее чем на 10 процентов. Это значит, что график изменения уровня свободной энергии, начинаясь от точки С, будет опускаться сильнее, чем прямая линия.
То же самое справедливо и в отношении йодоводорода. При разложении части его уровень свободной энергии оставшейся части окажется меньше, чем можно было бы ожидать. Поэтому от точки D график изменения уровня свободной энергии тоже будет опускаться вниз.
Рис. 13. Изменения уровня свободной энергии
Так что график будет напоминать не наклонную доску, а скорее подвесной гамак и на протяжении большей его части уровень свободной энергии будет меньше, чем на любой из крайних точек.
Этот факт надо подчеркнуть особо. Из-за зависимости молярной свободной энергии от концентрации свободная энергия заданной реакции не достигает минимума ни в одной из крайних точек, в которых реакция была бы завершена либо в одну, либо в другую сторону. Вместо этого минимум достигается в некоторой средней точке, в которой снижение концентрации всех составляющих приводит к максимальному снижению общей свободной энергии.
Следовательно, реакция, приведя к минимальному уровню свободной энергии, оказывается в положении равновесия. Более того, реакция останавливается в одной и той же точке с минимумом свободной энергии, независимо от того, с чего она начинается — со смеси йода с водородом или с чистого йодоводорода.
Поэтому для полноты аналогии с движением под влиянием силы тяжести надо представить себе не одну, а две наклонные плоскости, или, более образно — два горных склона, между которыми находится долина. Если шар отпустить с вершины С, он скатится в ту же самую нижнюю точку долины, что и в случае, если его отпустить с вершины D.
Чем меньше разность уровней свободной энергии между двумя крайними точками графика, тем ближе будет точка равновесия находиться к его середине. Чем выше разность уровней энергии между двумя крайними точками, тем ближе точка равновесия сдвигается в сторону той крайней точки, свободная энергия которой меньше.
В случае соединения водорода с кислородом точка равновесия сдвигается так далеко в сторону воды, что практически неотличима от точки, обозначающей чистую воду. В этой точке равновесия уровень свободной энергии будет, конечно, ниже, чем в точке чистой воды, но настолько неощутимо ниже, что эту разницу практически невозможно измерить (можно только высчитать из сведений о свободной энергии).
Это значит, что в замкнутой системе водород и кислород никогда не соединятся в воду полностью — всегда будет оставаться неизмеримо малое количество свободного водорода и кислорода, не вступивших в реакцию. Более того, если изначально мы имеем чистый водяной пар, то при тех же условиях (температуре и давлении) неизмеримо малое количество этой воды будет разлагаться на водород и кислород.
С точки зрения термодинамики получается, что все реакции обратимы. Однако с практической точки зрения можно продолжать расценивать в качестве необратимых те реакции, в которых точка равновесия неотличимо близка к одной из крайних точек.
Поскольку положение равновесия напрямую зависит от изменений уровня свободной энергии при переходе от одной стороны химического выражения к другой, то это изменение можно очень просто вычислить, исходя из постоянной равновесия. Проблема только в том, что саму постоянную равновесия определить бывает очень сложно, особенно в отношении реакций, которые принято считать необратимыми. Поэтому ученые долго искали другие способы подсчета изменений уровня свободной энергии — и находили. Один из таких способов заслуживает особого рассмотрения, поскольку это поможет осветить важные положения химии. В этом способе используется электричество.
Однако, перед тем как приступить непосредственно к описанию этой методики, нам надо чуть глубже взглянуть на атом. До сих пор, описывая кинетическую теорию газов, я рассматривал атомы как крошечные бильярдные шары. Однако на самом деле они представляют собой гораздо большее. Атомы сами по себе состоят из еще меньших частиц. Это открытие, совершенное в 1890-х годах, произвело поистине революцию в науке.
Эти элементарные частицы принадлежат к трем основным категориям: протоны, нейтроны и электроны. Протоны и нейтроны относительно массивны и плотно сгруппированы в единое тело (так называемое «ядро атома»), находящееся в самом центре атома. Они в обычных химических реакциях не участвуют.
Все остальное пространство атома, за исключением ядра, занимают электроны, представляющие собой очень легкие частицы. Количество электронов в каждом атоме равно количеству протонов в ядре этого атома, и число это свое у каждого химического элемента. Его так и называют — «атомное число». Самый простой атом — атом водорода — содержит всего один протон и один электрон, атомы остальных элементов содержат больше. У некоторых сложных атомов, искусственно создаваемых в последние годы в лабораториях ученых, атомное число превышает сотню. В таблице 2 приведены атомные числа некоторых наиболее распространенных элементов.
Каждый электрон имеет свой «электрический заряд»[4], так же как и каждый протон. У нейтронов электрического заряда нет, и поэтому хотя их значение и крайне велико, но нас в ходе дальнейшего рассмотрения они интересовать не будут. Величина заряда электрона и протона одна и та же, но природа этих зарядов различна. Один протон будет отталкивать другой протон и, наоборот, притягивать электрон. Точно так же и электрон будет отталкивать другой электрон и притягивать протон.
Совершенно произвольно было решено назвать электрический заряд электрона отрицательным, а протона — положительным. Поэтому заряд одного электрона обозначается как -1, а заряд одного протона — как +1. Кроме того, установлен закон, что одинаковые заряды отталкиваются, а противоположные — притягиваются.
В обычном атоме, как я уже сказал, количество протонов ядра (атомное число) в точности уравновешивается количеством удаленных от ядра электронов, так что атом в целом ведет себя как лишенный заряда, или «электрически нейтральный». Однако в отличие от протонов, хорошо укрытых в ядре от воздействия межатомных и межмолекулярных столкновений, легкие электроны, существующие на «внешних рубежах» атома, чувствуют эти события на себе в полной мере. И при химических реакциях неизбежно осуществляется некоторое перераспределение электронов между участвующими в реакции атомами. На самом деле именно наличие перераспределения электронов отличает химические реакции от изменений иного рода.
Таблица 2.
АТОМНЫЕ ЧИСЛА
Элемент — Атомное число
Водород (Н) — 1
Гелий (Не) — 2
Углерод (С) — 6
Азот (N) — 7
Кислород (О) — 8
Фтор (F) — 9
Натрий (Na) — 11
Магний (Mg) — 12
Алюминий (Al) — 13
Фосфор (Р) — 15
Сера (S) — 16
Хлор (Cl) — 17
Калий (К) — 19
Кальций (Са) — 20
Хром (Cr) — 24
Марганец (Mn) — 25
Железо (Fe) — 26
Кобальт (Со) — 27
Никель (Ni) — 28
Медь (Си) — 29
Цинк(Zn) — 30
Серебро (Ag) — 47
Олово(Sn) — 50
Йод (I) — 53
Вольфрам (W) — 74
Платина (Pt) — 78
Золото (Au) — 79
Ртуть (Hg) — 80
Свинец (Pb) — 82
Радий (Ra) — 88
Торий (Th) — 90
Уран (U) — 92
Плутоний (Pu) — 94
Лоуренсий (Lw) — 103
На электрическую нейтральность атома эти изменения могут влиять, а могут и не влиять. К примеру, два атома, столкнувшись, могут поделиться друг с другом электронами вполне стабильным образом (подробнее об этом чуть позже). Это «предоставление» электронов одним атомом другому сохраняется только до тех пор, пока атомы сохраняют контакт между собой. Для того чтобы разъединить атомы, необходимо теперь будет разорвать их стабильную связь, а на это потребуется значительное количество энергии. Без получения этой энергии атомы, имеющие общие электроны, будут неопределенно долго оставаться вместе, и именно это и есть основа тех химических связей, о которых я говорил в предыдущих главах. В молекулах водорода, кислорода, воды, углекислоты, йодоводорода и многих других соединений атомы удерживаются вместе с помощью «общих» электронов.
При подобного рода перераспределении электронов атомы продолжают оставаться электрически нейтральными.
Однако бывает и так, что определенные электроны в атомах некоторых элементов держатся крайне слабо. К примеру, в атоме натрия самый удаленный электрон не слишком-то прочно привязан к своему атому. Поэтому при соседстве с атомом хлора (который все собственные электроны удерживает очень крепко) самый удаленный атом натрия не то что становится «общим», а вообще переходит из атома натрия в атом хлора.
После такого перехода в атоме натрия остается всего 10 электронов, то есть на один электрон меньше, чем требуется, чтобы нейтрализовать положительный заряд 11 протонов ядра. Атом натрия теряет электрическую нейтральность. Теперь он несет общий заряд значением в +1, это заряд протона, потерявшего уравновешивающий его электрон. С другой стороны, у атома хлора теперь 18 электронов, то есть на один электрон больше, чем требуется для нейтрализации 17 протонов ядра. Поэтому его общий заряд теперь равняется заряду этого лишнего электрона, то есть составляет -1.
Такие атомы, несущие электрический заряд по причине избытка или нехватки электронов, называют «ионами». Естественно, ионы делят на положительные и отрицательные. Ионы обозначают приставляя к обычному символу элемента маленький плюс или минус, отражающий заряд иона. То есть ион натрия обозначается как N+, ион хлора — как Сl-.
Некоторые атомы могут терять в ходе химической реакции по два или даже три электрона, а могут и вести себя по-разному в разных условиях — при одной реакции терять два электрона, а при другой — три. Бывает даже так, что группа атомов, удерживаемая воедино с помощью обычных связей из «общих» электронов, теряет или приобретает электроны. Атомы остаются соединенными, но все вместе приобретают электрический заряд и становятся «сложными ионами». Мы не будем вдаваться в пущие подробности; однако на всякий случай приводим здесь список самых распространенных ионов (табл. 3).
Таблица 3.
ИОНЫ
Положительные
Название … Обозначение
Ион водорода … Н+
Ион натрия … Na+
Ион калия … К+
Ион магния … Mg2+
Ион кальция … Са2+
Ион цинка … Zn2+
Одновалентный ион меди … Cu+
Двухвалентный ион меди … Cu2+
Двухвалентный ион железа … Fe2+
Двухвалентный ион железа … Fe3+
Ион аммония … NH4+
Отрицательные
Ион фтора … F-
Ион хлора … Сl-
Ион йода … I-
Ион серы … S2-
Карбонат-ион … СО32-
Нитрат-ион … NO3-
Сульфат-ион … SO42-
Фосфат-ион … PO43-
Примечание. Когда атом или группа атомов теряют или приобретают более одного электрона, то этот факт отмечают приписывая перед плюсом или минусом соответствующий индекс.
Закон о том, что противоположно заряженные частицы притягивают друг друга, распространяется и на ионы. Поскольку ионы натрия и хлора формируются путем перехода электрона от атома натрия к атому хлора, то ионы остаются вместе, связанные силой притяжения между положительным и отрицательным зарядами двух ионов. В итоге получается соединение хлорид натрия — привычная нам поваренная соль.
Такие вещества, как хлорид натрия, удерживаемые воедино ионными связями, не состоят из молекул в том же понимании, что и углекислота или вода.
В кристалле поваренной соли любой отдельный ион натрия не является прочно соединенным с каким-то конкретным ионом хлора в единую двухатомную частицу. Нагляднее всего это видно на примере растворения поваренной соли. Ионы натрия и хлора свободно перемещаются в растворе. Точнее, существует всеобщее притяжение между положительными и отрицательными зарядами, но любой отдельный ион натрия может передвигаться, не таща за собой какой-то конкретный ион хлора. На самом деле под воздействием электрического тока оба набора ионов можно заставить двигаться в противоположных направлениях.
Некоторые химические реакции лучше всего рассматривать именно в свете такой вот ионной независимости; тогда проще всего описывать их, сосредоточившись на одном из ионов и упуская из виду второй.
К примеру, возьмем цинк (Zn) и медный купорос, молекула которого состоит из одного атома меди (Cu), одного атома серы (S) и четырех атомов кислорода и обозначается CuSO4. Если в раствор медного купороса добавить металлический цинк, то произойдет спонтанная реакция, в ходе которой цинк войдет в состав раствора, который станет теперь раствором сульфата цинка (ZnSO4), а медь выйдет из состава раствора и выпадет в осадок в виде знакомого нам красноватого металла.
Записанное обычным образом выражение для этой реакции будет выглядеть так:
Zn + CuSO4 → ZnSO4 + Cu.
При этом создается впечатление, что сульфатная группа (SO4) отделяется от меди и прикрепляется к цинку. На самом же деле сульфатная группа ничего подобного не совершает. Изо всех компонентов системы она играет самую пассивную роль. Взглянем на происходящее, исходя из ионной картины.
Медный купорос удерживают воедино ионные связи (по крайней мере, частично), и в растворе он существует не в виде отдельных молекул, а в виде смеси ионов меди (Cu2+) и сульфат-ионов (SO2). В ходе реакции атом цинка (его можно записать как Zn0, чтобы лишний раз подчеркнуть его нейтральность в металлической форме) теряет два электрона и становится ионом цинка (Zn2+), и эти два электрона приобретает ион меди, становясь, таким образом, нейтральным атомом меди (Cu0) и оседая в этом виде.
Выражение можно записать так:
Zn0 + Cu2+ → Zn2+ + Cu0.
Эта реакция подразумевает изменение в природе ионной связи. Изначально мы имеем ионную связь между ионом меди и сульфат-ионом, а в итоге — между ионом цинка и сульфат-ионом. Изменения ионных связей подразумевают и изменение уровня свободной энергии, как и любые другие изменения химических связей. В этом случае реакция проходит спонтанно в направлении, указанном в вышеприведенной формуле, так что мы можем быть уверены в том, что при переходе от металлического цинка и иона меди к иону цинка и металлической меди уровень свободной энергии снижается.
Теперь давайте предположим, что два реагента разделены. В одной камере находится полоска цинка, погруженная в раствор сульфата цинка, в другом — полоска меди, погруженная в раствор медного купороса. Между двумя камерами — пористая перегородка, сквозь которую ионы могут проникать в обе стороны, но, при обычных условиях, очень медленно. В такой системе сами по себе обсуждаемые реакции не будут проходить в каком бы то ни было значительном объеме.
А происходит в ней следующее: атомы цинка в полоске цинка начинают терять электроны и превращаться в ионы цинка. Ионов меди, которые могли бы перехватить эти электроны, поблизости нет, так что в растворе происходит накопление «свободных электронов». Этот процесс не заходит слишком далеко, поскольку срабатывает следующий механизм: все отрывающиеся электроны, обладая одинаковым зарядом, стараются оттолкнуться друг от друга как можно дальше, создавая, таким образом, в растворе нечто вроде «электронного давления». Любому электрону, который хочет в этих условиях оторваться от атома цинка, приходится теперь преодолевать это давление, которое с отрывом каждого нового свободного электрона становится все сильнее, и так продолжается, пока электроны не перестают отрываться вообще. На этом этапе количество накопившихся в растворе свободных электронов относительно мало. То же самое происходит и в «медной» камере, поскольку атом меди тоже имеет склонность терять электроны. И все же в «цинковой» камере электронное давление выше, поскольку склонность атома цинка к потере электронов сильнее, в ней накапливается больше свободных электронов.
Теперь предположим, что полоска цинка соединена с полоской меди металлической проволокой. Тогда мы станем наблюдателями нового для нас и крайне интересного процесса. Обычные атомы по проволоке перемещаться не могут — этому мешают атомы, уже находящиеся в ней. А вот электрон — гораздо меньше и легче, чем атом. Его масса в 1837 раз меньше массы самого легкого атома (имеется в виду конечно же водород). Поэтому электрон может скользить между атомами, из которых состоит металлическая проволока. Способность электрона проходить сквозь вещество зависит от электронного строения самих атомов этого вещества. Электронная структура многих веществ — серы, стекла, резины, например, — не позволяет электронам свободно проходить сквозь них.
Электронное давление в обеих камерах становится движущей силой, запускающей перемещение этих микрочастиц по проволоке. Поскольку в «цинковой» камере электронное давление выше, то электроны будут вылетать из «цинковой» камеры активнее, чем из «медной». Таким образом, общее движение электронов будет происходить в направлений из точки с большим электронным давлением в точку с меньшим электронным давлением, по тому же принципу, по которому камень катится вниз (из точки с высоким уровнем потенциальной энергии — в точку с более низким), а тепло переходит от горячих предметов к холодным (из области с высокой температурой — в область с низкой). Эта разность электронных давлений, служащая движущей силой электронного потока, называется «электрическим потенциалом», или «электродвижущей силой».
По мере того как электроны покидают «цинковую» камеру, электронное давление в ней понижается и находящиеся в ней атомы цинка начинают активнее избавляться от электронов. Эти освобождающиеся электроны тоже покидают камеру, и атомы цинка продолжают испускать электроны в прежнем темпе. Так продолжается неопределенно долго, и этот непрерывный поток электронов и есть знакомый нам электрический ток.
По мере того как электроны перетекают из «цинковой» камеры в «медную», их подхватывают ионы меди, окружающие медную полоску, превращаясь, таким образом, в нейтральные атомы меди. Дальше по мере притока электронов атомы цинка на одном конце проволоки превращаются в ионы и переходят из твердого состояния в раствор, а ионы меди на другом конце превращаются в атомы меди и выпадают из раствора в осадок. Общее количество положительных ионов в обеих камерах не изменяется, как и общий размер положительного заряда. Точнее, положительный заряд собирается в той части раствора, которая окружает цинк, и исчезает из той части, которая окружает медь; однако отрицательно заряженный сульфат-ион может перемещаться сквозь пористую перегородку из «медной» камеры в «цинковую» и поддерживает, таким образом, электрическое равновесие.
Поток электронов — это вид энергии, и его можно использовать для выполнения работы. Электрическая энергия возникает за счет снижения химической энергии, которое происходит в процессе превращения ионов меди и цинка в ионы цинка и медь.
Такое устройство, переводящее свободную энергию химической реакции в электрическую энергию, называют химической батареей, или электрической батареей, или электрохимической батареей, элементом питания или даже «гальваническим элементом», или «вольтовой цепью» (рис. 14), по имени Алессандро Вольта, итальянского ученого, который впервые изготовил химическую батарею в 1800 году. Описанная нами конкретная схема с использованием меди и цинка называется «элементом Даниеля» по имени разработавшего ее в 1836 году английского химика Джона Фредерика Даниеля.
Рис. 14. Поток электронов в гальваническом элементе
Обратите внимание — эти батареи уже изготавливали и использовали за столетие до того, как были открыты электроны! Однако именно с 1890-х годов отсчитывается невероятный рост применения потока электронов благодаря работе физиков, трудившихся в области электроники. Мораль тут такова: чтобы использовать некое явление — совершенно не обязательно его понимать, но если все же его удастся понять, то польза от него возрастет многократно!
Чем больше снижается уровень свободной энергии, задействованной в химической реакции, запускающей поток электронов, тем больше движущий электроны электрический потенциал. Электрический потенциал легко измерить; единицей измерения его служит «вольт», а прибор, которым его измеряют, называется «вольтметр» — опять же в честь Вольта. Математические выкладки Гиббса показали, что из этого потенциала можно высчитать уменьшение свободной энергии. Таким образом, Гиббс увязал с термодинамикой, которая изначально разрабатывалась в общем-то для тепловых машин, не только химическую, но и электрическую энергию.
Некоторые очень важные химические реакции остаются, таким образом, за пределами возможностей прямого изучения. Реакция соединения углерода и кислорода в углекислоту имеет точку равновесия настолько близкую уже к самой углекислоте, что снижение уровня свободной энергии, связанное с ней, подсчитать, исходя из точки равновесия, невозможно. Невозможно создать и химическую батарею на основе реакции соединения углерода и кислорода. Это была бы «топливная батарея», которая позволила бы производить дешевое электричество и представляла бы собой очень ценное и полезное устройство, если бы только ее возможно было создать.
К счастью, здесь можно воспользоваться эквивалентом закона Гесса. Как вы помните, закон Гесса позволяет обращаться с химическими выражениями так, как будто это выражения математические, и это распространяется на значения ΔН (см. главу 8). То же самое справедливо и для ΔF. Манипулируя выражениями, для которых можно измерить изменения уровня свободной энергии напрямую, можно вывести из них и значения для тех реакций, для которых напрямую их измерить нельзя.
Таким образом, можно сказать с полной уверенностью, насколько в науке вообще можно что-то говорить с полной уверенностью, что
Н2 + 1/2О2 → Н2О
ΔF = -54,6 ккал,
СН4 + 2O2 → CO2 + 2H2O
ΔF = -195,6 ккал
и так далее для множества других реакций.
Глава 11. КАК ПОДТОЛКНУТЬ РЕАКЦИЮ
Триумфальное вторжение термодинамики в химию в 70-х и 80-х годах XIX века, описанное в двух предыдущих главах, проходило не всегда гладко.
Я уже говорил, и еще не раз повторюсь, что реакции соединения водорода с кислородом (как и углерода с кислородом) сопутствует сильное снижение теплового содержания и свободной энергии; эта реакция является спонтанной. Однако я уже упоминал, хотя и не заостряя на этом внимания, что для того, чтобы смесь водорода с кислородом воспламенилась, ее надо поджечь, то есть, чтобы началось это, предположительно, спонтанное соединение, реакцию надо подтолкнуть. В отношении реакции соединения углерода с кислородом это положение еще более справедливо. Ни одному хозяину загородного дома не приходит в голову волноваться, что уголь в его подвале вдруг начнет самостоятельно вступать в реакцию с атмосферным кислородом, пока не окажется в камине. И даже в камине изначально разжечь огонь не так-то просто.
Почему так происходит? Если графики изменения свободной энергии, которые я приводил в предыдущей главе, хоть в какой-то степени отражают реальность, то, по идее, реакция водорода с кислородом должна начаться немедленно, как только они вступают в соприкосновение. Если провести аналогию с механикой, то шар, будучи положенным на верхнюю точку наклонной плоскости, должен сразу же покатиться вниз, не нуждаясь в дополнительном толчке. Почему же тогда спонтанной химической реакции нужен толчок в тепловом виде? Что не так с принципами динамической термодинамики?
Один из ответов на этот вопрос заключается в том, что термодинамика может указать направление, в котором пойдет та или иная химическая реакция, но не ее скорость. Иными словами, водород и кислород, содержащиеся в воздухе, на самом деле все же соединяются, и уголь в подвале тоже вступает в соединение с атмосферным кислородом. Однако и тот и другой процессы происходят настолько медленно, что не влекут за собой никаких заметных внешних изменений даже за очень долгий период времени.
Это звучит как принципиально непроверяемая гипотеза, теоретическая отговорка, но, к счастью, имеются и подтверждающие эту теорию факты. Бумага, состоящая из сложных молекул, в состав которых входят атомы углерода, водорода и кислорода, вступает с кислородом в реакцию, при которой происходит снижение уровня свободной энергии. В случае, когда она горит, испуская тепло и свет, это очевидно, и понятно, что реакция эта спонтанна. Однако без предварительного поджигания бумага, кажется, в соединение с кислородом не вступает — по крайней мере, мы этого не видим. Но действительно ли не вступает? Может быть, стоит приглядеться повнимательнее, и мы сможем обнаружить эту реакцию?
Страницы любой книги со временем желтеют и крошатся. Края страниц, которые больше всего контактируют с воздухом, выглядят желтее и более хрупкими, чем внутренняя их часть. В целом бумага выглядит слегка опаленной. Она и является опаленной — все десятилетия неторопливого соединения с кислородом она очень медленно «горит».
Или вот еще более наглядный пример. Маслянистые вещества, молекулы которых состоят но большей части из углерода и водорода, вступают в соединение с кислородом в ходе реакции, которая приводит к снижению свободной энергии и, разумеется, к производству тепла. Без поджигания эта реакция происходит слишком медленно, чтобы быть замеченной.
Однако сами по себе маслянистые вещества плохо проводят тепло. Если хранить кучу промасленных тряпок в плохо проветриваемом помещении, то тепло, вырабатывающееся с микроскопической скоростью в результате вялотекущих реакций соединения масла и кислорода, не удаляется ни с потоком воздуха, ни через теплопроводность среды. Оно потихоньку, очень медленно, начинает накапливаться. По мере его накопления и подъема температуры возрастает и скорость, с которой проходит реакция. В результате этого тепло начинает накапливаться уже быстрее, температура повышается тоже быстрее, и в конце концов тряпки действительно загораются. Склад охватывает пожар, с ним вместе может сгореть и дом, а пожарные впоследствии скажут — «самовозгорание» и прочтут очередную лекцию о правилах пожарной безопасности при хранении горючих материалов.
Так что, похоже, спонтанные реакции действительно спонтанны. Необходимость объяснять их очевидное «нежелание» начинаться не свидетельствует о некоей принципиальной погрешности термодинамики как таковой, а лишь является проявлением принципа, который станет нам ясен после более тщательного изучения скоростей прохождения реакций (эта область называется «химической кинетикой»). Почему реакция происходит просто незаметно при одних условиях и со взрывообразной скоростью при других?
Первый закон, открытый в области химической кинетики, гласит, что чем выше температура, тем быстрее проходят все химические реакции. Это знакомо каждому на основе личного опыта, и даже в доисторическую эпоху люди знали, что чем жарче огонь, тем быстрее могут выполняться работы по приготовлению пищи, металлургии, изготовлению стекла и так далее. В области менее высоких температур можно указать, что, например, фруктовый сок гораздо быстрее забродит в теплой комнате, чем в снежном сугробе. Однако от «общих знаний» еще далеко до формулировки принципа на основе точных измерений при контролируемых условиях — а ведь только последнее что-то значит в науке.
В 80-х годах XIX века разные химики проводили эксперименты по осуществлению различных химических реакций при различных температурах и измеряли точное время реакции. Оказалось, что повышение температуры на 10° приводит к ускорению реакции приблизительно вдвое.
В рамках кинетической теории это звучит разумно. Химическая реакция между двумя веществами не сможет толком происходить, если молекулы этих веществ не будут сталкиваться. По мере повышения температуры движение молекул ускоряется (см. главу 6), и каждую секунду происходит большее количество столкновений, поэтому и вся реакция в целом проистекает быстрее.
Но подождите-ка! Мы знаем, что средняя скорость движения молекул возрастает пропорционально квадратному корню абсолютной температуры. Скажем, повышение ее с 20 °С до 30 °С по абсолютной шкале будет означать лишь повышение с 293 °К до 303 °К, то есть всего на несколько процентов'. А если скорость движения молекул повышается так мизерно, почему вдруг скорость реакции должна при этом удвоиться?
Кроме того, возникает и другой вопрос. Если медленно нагревать смесь водорода и кислорода, то практически ничего не изменится, пока температуpa смеси не достигнет 600 °С. А тогда мы вдруг становимся свидетелями взрывообразной реакции!
На первый взгляд странно. Если скорость реакции при повышении температуры на 10° увеличивается примерно вдвое, то логично предположить, что по мере нагревания водород с кислородом будут вступать в соединение с равномерно увеличивающейся скоростью. Да, при столь высокой температуре она вполне может достигать наблюдаемой скорости, но и на подходе к ней реакция ведь тоже должна протекать, причем все быстрее? А вместо этого скорость реакции скачкообразно переходит от состояния «слишком медленная, чтобы измерить» к состоянию «слишком быстрая, чтобы измерить». Почему так?
Давайте еще раз взглянем на составляющие химической реакции — это можно сделать на примере все той же реакции соединения водорода и кислорода в смеси двух газов.
До сих пор, говоря о соединении водорода с кислородом, я не затрагивал особых подробностей. Я только сказал, что на входе мы имеем смесь газообразных водорода и кислорода с одним содержанием свободной энергии, а на выходе получаем воду с другим, значительно более низким содержанием. Этих сведений до сих пор было достаточно, но теперь надо разобраться и в самом процессе реакции. Понятно ведь, что молекулы водорода и кислорода не превращаются в молекулы воды по мановению волшебной палочки. Разумеется, это процесс, состоящий из нескольких этапов, каждый из которых требует определенного времени.
Представим себе, что исходный водород — это газ, состоящий из молекул, каждая из которых представляет собой два атома водорода, соединенных химической связью. Такую молекулу можно обозначить как НН. Точно таким же образом и кислород состоит из молекул, каждая из которых представляет собой два атома, удерживаемые воедино такой же химической связью, — обозначим их как ОО. А получаемая в итоге вода, как показывает практика, состоит из молекул, где один атом кислорода находится между двумя атомами водорода (НОН).
Но для того чтобы поместить атом кислорода между двумя атомами водорода, необходимо сначала, чтобы связь этих двух атомов между собой распалась. И для того, чтобы этот единственный атом кислорода смог встроиться в молекулу воды, он тоже должен сначала оторваться от своего собрата по молекуле кислорода.
Соответственно, прежде, чем речь зайдет об образовании воды, должны произойти следующие реакции:
Н2 → 2Н,
O2 → 2O.
Но при подобном разложении молекул на свободные атомы, как уже указывалось в главе 7, уровень свободной энергии заметным образом возрастает.
Если посмотреть на соединение водорода и кислорода с этой точки зрения, то станет ясно, что на самом деле речь идет о двух различных реакциях. Первая из них — это превращение молекул водорода и кислорода в свободные атомы этих же элементов, а вторая — соединение этих свободных атомов в молекулы воды. При этом изменение уровня свободной энергии происходит так, как изображено на рис. 15.
Если посмотреть на рис. 15 на уровень свободной энергии смеси молекулярного кислорода и молекулярного водорода (А) и сравнить его с уровнем свободной энергии воды (В), то кажется, что этот уровень должен в ходе реакции равномерно снижаться. Однако если принять во внимание наличие промежуточной стадии смеси атомного водорода с атомным кислородом, то станет очевидно, что на этой стадии мы будем иметь уровень свободной энергии значительно более высокий (X), чем и в начальной (А), и в конечной (В) точках. Неудивительно, что заставить водород и кислород соединиться — непростая задача. Используя аналогии из мира механики, можно сказать, что это то же самое, что заставить шар скатиться вниз из точки А в точку В не по ровной наклонной плоскости, а минуя на своем пути гору, вершина которой находится выше исходной точки.
Рис. 15. Соединение водорода с кислородом: две стадии
Тогда возникает следующий вопрос. Почему же тогда водород с кислородом вообще вступают в реакцию? В главе 7 я упоминал, что даже при температуре 3500 °С менее половины молекул водорода и кислорода распадаются на атомы — а смесь газов почему-то вступает во взрывообразную реакцию уже при 600 °С.
Рис. 16. Энергия активации
Ответ прост: а нам и не надо, чтобы вообще все молекулы водорода и кислорода в смеси распались на атомы. Для запуска процесса реакции достаточно образования лишь небольшого количества свободных атомов обоих веществ.
На самом деле на графике не будет наблюдаться острого пика, поскольку точка X будет достигнута лишь в том случае, если смесь полностью будет состоять из отдельных атомов водорода и кислорода. В реальности при обычных условиях молекулярные водород и кислород в процессе образования воды никогда не проходят через такое состояние. Даже в самом приближенном к идеалу случае лишь малая часть системы состоит из свободных атомов, поэтому этот промежуточный пиковый уровень свободной энергии на самом деле проходит куда более плавно. На графике (рис. 16) ему будет соответствовать скорее не горный пик, а покатый бугорок. Но если вернуться к нашей аналогии, то для катящегося шара и покатый бугорок — достаточно серьезная преграда. Шар придется хорошенько толкнуть, чтобы он закатился на бугорок, прежде чем покатиться вниз самостоятельно уже до самого конца. То же самое относится и к химической реакции.
В 1889 году шведский химик Сванте Август Аррениус вывел общую математическую формулу для описания подобных процессов, и оказалось, что подобный «бугорок» наблюдается при описании не только реакции соединения водорода с кислородом, но и вообще всех химических реакций. Энергию, которую необходимо привнести в систему для того, чтобы общего уровня свободной энергии оказалось достаточно для поднятия реакции «на вершину», по достижении которой далее она будет протекать уже спонтанно, сейчас принято называть «энергией активации».
Самый простой способ привнести в систему дополнительную энергию для запуска реакции — это нагреть реагирующие вещества. Если смесь водорода и кислорода нагреть до соответствующей температуры, она взрывается; если бумагу или промасленные тряпки нагреть до соответствующей температуры, они загораются. С этого момента реакция живет собственной жизнью и протекает спонтанно, не требуя более никакого приложения внешних усилий.
Из наших рассуждений может показаться, что химические реакции происходят по принципу «все или ничего», то есть до тех пор, пока энергии системы недостаточно для преодоления пика, реакция вообще не будет идти, а потом, по мере добавления необходимого количества тепла, внезапно начинается реакция. Это вполне логичное предположение, которое можно сделать исходя из того, что смесь водорода с кислородом при одной температуре пребывает в стабильном состоянии, а при другой — внезапно взрывается, а бумага и промасленная ветошь при одной температуре спокойно лежат себе, а при чуть более высокой — вдруг вспыхивают ярким пламенем.
Но это упрощенная точка зрения. Я уже говорил о том, что на самом деле и бумага, и промасленная ветошь все-таки вступают в реакцию соединения с кислородом при комнатной температуре, просто очень медленно, и что так же ведут себя, по-видимому, и водород с кислородом. А ведь при комнатной температуре энергетическое содержание системы гораздо ниже, чем требуется для достижения энергии активации. Почему же в этих случаях тем не менее происходит соединение?
Давайте еще раз рассмотрим смесь водорода с кислородом, четко обозначив при этом температуру равную комнатной — скажем, около 25 °С.
Формулы Максвелла—Больцмана (которые я уже упоминал в главе 6) можно использовать для расчета наиболее вероятной скорости и, соответственно, наиболее вероятной кинетической энергии молекул газа при заданной температуре. Произведя этот расчет, мы удостоверимся, что энергии имеется гораздо меньше, чем требуется для разрыва связей между атомами в молекулах водорода или кислорода. Две молекулы, имеющие среднюю для температуры 25 °С энергию, после столкновения просто разлетятся в стороны. Какое-то количество энергии может перейти от одной из них к другой, но обе останутся целыми.
Однако нельзя забывать, что формулы Максвелла—Больцмана позволяют узнать лишь наиболее вероятную энергию молекул — они не могут универсальным образом описывать энергию каждой из них. При любой температуре разброс энергетического содержания между молекулами одного и того же вещества огромен. Энергия большинства молекул близка к средней, но некоторое меньшинство может обладать энергией гораздо больше средней. И в любом множестве молекул всегда найдется немного таких, которым посчастливилось набрать достаточно энергии для самопроизвольного расщепления на атомы. Энергия, имеющаяся у этих молекул, явно не меньше энергии активации. Атомы, высвобождающиеся из этих молекул, вполне могут принимать участие в реакциях как друг с другом, так и, что более вероятно, с еще целыми молекулами для образования воды.
Поэтому даже при комнатной температуре имеется некоторое количество молекул водорода и кислорода, проходящих порог энергии активации и предоставляющих в итоге свободные атомы для образования молекул воды. Процент таких молекул настолько мал, что скорость образования воды оказывается неизмеримо более медленной.
Однако по мере повышения абсолютной температуры среднее энергетическое содержание молекул пропорционально возрастает. Повышение температуры с 20 °С до 30 °С, как я уже говорил, в процентном соотношении выражается в крайне незначительном увеличении средней скорости молекул, но при этом количество молекул, обладающих энергией больше пороговой, увеличивается вдвое, а то и втрое (рис. 17). Можно провести такую аналогию: если лето выдается жарким, то, подсчитав среднесуточную температуру, мы обнаружим, что она всего на 1 °С выше, чем обычно, но при этом жарких дней, то есть таких, когда температура достигала бы 32 °С, по подсчетам окажется в два-три раза больше.
Скорость реакции зависит не от среднего уровня энергии молекул, а от количества молекул, обладающих энергией не меньшей, чем энергия активации. Поэтому она и удваивается с повышением температуры на каждые 10 градусов.
Рис. 17. Температура и скорость реакции
Если говорить конкретно о реакции соединения водорода с кислородом, то при комнатной температуре скорость реакции настолько мизерна, что ее можно очень долго удваивать путем повышения температуры без того, чтобы она достигла сколько-нибудь заметного уровня. Однако далеко не для всех реакций энергия активации столь велика. Для многих реакций уже при комнатной температуре энергия значительной части молекул участвующих в них веществ окажется достаточной для того, чтобы преодолеть этот довольно невысокий порог, и реакция протекает с вполне измеримой скоростью. Именно на материале таких реакций с низким порогом химики 1880-х годов получили те данные, которые были им необходимы для измерения возрастания скорости реакции по мере увеличения температуры.
Что ж, допустим, что такое объяснение может оказаться удовлетворительным ответом на вопрос о «слишком медленных» реакциях, но что же сказать в таком случае о реакциях взрывообразных? Чем обусловлен внезапный перескок от реакции «слишком медленной для измерения» к реакции «слишком быстрой для измерения»?
Загадочным такое положение дел будет казаться лишь до тех пор, пока мы не обратим внимание на тот факт, что тепло может поступать в систему не только извне. Образование молекул воды из свободных атомов — реакция экзотермическая, при ней тоже выделяется тепло. Правда, вырабатывается его немного, температура в результате выделения тепла повышается незначительно, к тому же смесь газов быстро избавляется от излишков тепла через излучение, и общая температура системы остается стабильной.
Однако если систему начать подогревать снаружи, то ее температура станет возрастать, количество соединений — увеличиваться, а с ними вместе и объем вырабатываемого при соединениях тепла. В определенный момент количество вырабатываемого за секунду тепла превысит возможности газа по излучению тепла за ту же секунду, и излишек вырабатываемого при реакции тепла будет теперь оставаться в той же системе, повышая тем самым температуру системы еще больше. Это, в свою очередь, приведет к дальнейшему ускорению реакции, и получится замкнутый круг — чем выше температура, тем интенсивнее реакция, а чем интенсивнее идет реакция, тем выше поднимается температура.
То есть стоит один раз нарушить равновесие, и система уже сама начнет уходить от него все дальше. До определенного порогового уровня смесь водорода с кислородом кажется спокойной; по его достижении, когда излучение уже не справляется с теплоотводом и равновесие оказывается нарушенным, темпы реакции внезапно ускоряются настолько, что экспериментатор даже не успевает отключить внешний источник тепла.
По тому же принципу, только в меньшем масштабе, запускается и процесс горения бумаги. Предположим, что к уголку бумаги поднесли спичку. На этом уголке бумага получила энергию активации, и реакция горения оказалась запущенной, молекулы, из которых состоит бумага, принялись активно соединяться с кислородом, производя при этом тепло. Этого тепла оказывается вполне достаточно, чтобы придать энергию активации соседним молекулам бумаги, которые, в свою очередь, сгорая, тоже вырабатывают тепло, и так далее. Спичка давно уже догорела, но ее пламя к этому моменту уже не нужно. Бумага продолжает гореть уже самостоятельно и будет гореть, пока не закончится. Все прекрасно знают, что один-единственный непогашенный окурок может предоставить изначальное количество энергии достаточное, чтобы спалить много гектаров леса.
Энергию активации той или иной реакции участвующие в ней вещества могут получить не только посредством притока в систему тепла. Вот пример: смесь водорода с хлором, будучи нагретой, взорвется еще охотнее, чем смесь водорода с кислородом, но при комнатной температуре она является вполне инертной, но только… в темноте! Если же на смесь водорода с хлором попадут лучи света, особенно яркого — например, дневного солнечного света или вспышки магниевой лампы, — то она взорвется и при комнатной температуре.
Такое действие света на смесь водорода с хлором первым подметил в 1801 году английский химик Уильям Крукшенк, и разрозненные наблюдения по поводу этого феномена отмечались на протяжении всего XIX века. Однако для полного его понимания необходимо было сначала получить правильное представление о природе света как такового, чего у физиков XIX века еще не было. Тут необходимо сделать небольшое отступление.
Современный подход к изучению света был заложен еще Исааком Ньютоном в 1660-х годах. Ньютон показал, что солнечный свет можно разложить на разноцветные полоски (получившие название «спектр») с помощью треугольной призмы. Ньютон придерживался мнения о том, что свет — это поток бесконечно малых частиц, с огромной скоростью разлетающихся во все стороны прочь от своего источника. (Впервые скорость света более-менее точно установил в 1671 году датский астроном Оле Рёмер. Сейчас известно, что она равняется 300 000 километров в секунду.)
Современник Ньютона, датский астроном Кристиан Гюйгенс выдвинул другую точку зрения, что свет — это волновое движение.
В XVIII веке большей популярностью обладала ньютоновская «корпускулярная» теория. Однако ряд экспериментов, проведенных в начале XIX века, позволил сделать четкий вывод о том, что свет все же состоит из волн, и, таким образом, прочно утвердилась «волновая» теория.
Длина каждой отдельной волны света крайне мала и меняется от одного цвета к другому. Точную «длину волны» можно высчитывать разными способами, и все они сходятся в том, что длина волны красного света лежит приблизительно около значения в 0,0000007 метра.
Понятно, что метр — слишком большая величина для измерения длины световых волн. Для этого используются единицы микрон (одна миллионная, 0,000001, метра) и миллимикрон (одна тысячная микрона, или одна миллиардная метра, 0,000000001). Шведский астроном Андерс Йонас Ангстрем, занимавшиися изучением света в середине XIX века, использовал единицу в одну десятую миллимикрона, или одну десятимиллиардную (0,0000000001) метра. Эта единица получила в его честь название «ангстрем», что записывается как Å, и, таким образом, длина волны красного света равняется примерно 7000 Å (рис. 18).
Рис. 18. Спектр видимого света
Длина волны света постоянно колеблется, и цвет ее неуловимо меняет оттенки. При длине волны 6000 Å свет четко оранжевый, при около 5700 Å — уже желтый, при 5300 Å — зеленый, при 4800 Å — синий, при 4200 Å — фиолетовый. Конечно, значения, которые здесь приведены, — средние. Все цвета плавно и незаметно переходят друг в друга, а крайние цвета спектра — в темноту, красный — где-то после 7600 Å, а фиолетовый — после 4000 Å.
Кроме длины волны, не менее важен такой параметр, как «частота», то есть количество волн, попадающих в глаз (или в прибор) в секунду. За секунду свет проходит 300 000 километров, или около 3 000 000 000 000 000 000 ангстрем. Соответственно количество волн самой большой длины (красных), находящихся на этом участке, равняется 3 000 000 000 000 000 000 / 7600, то есть около 400 000 000 000 000. Значит, за секунду на глаз попадает около четырех триллионов волн красного света — такова его частота.
Понятно, что чем меньше длина волны, тем большее количество волн попадает в этот отрезок. То есть чем короче волна, тем выше ее частота. Частота волны фиолетового спектра, самой короткой из видимых световых волн, равна примерно 730 000 000 000 000, то есть почти в два раза выше, чем частота волны красного света.
Приблизительно в 1860 году Максвелл принялся за изучение электрических и магнитных сил, которые проявляют свое действие на некотором расстоянии от магнитного или электрического заряда. Его выводы показали, что электричество и магнетизм неразрывно связаны и создают в пространстве единое электромагнитное поле. Более того, он продемонстрировал и то, что любой колеблющийся электрический заряд излучает энергию («электромагнитное излучение») в волновой форме с частотой равной частоте своих колебаний. Эта энергия движется в пространстве со скоростью света.
Для Максвелла сходство между этой теоретически выведенной скоростью электромагнитного излучения и уже известной скоростью света оказалось слишком разительным, чтобы рассматривать его как случайное совпадение. Он решил, что свет — это одна из разновидностей электромагнитного излучения.
Конечно, возникает вопрос — каким же должен быть заряд, чтобы создавать колебания частотой в сотни триллионов, и на это Максвеллу ответить было нечего. Ответить на подобный вопрос смогли лишь в 90-х годах XIX века, когда было открыто внутреннее строение атома. Именно тогда голландские физики Хендрик Антон Лоренц и Питер Зееман смогли продемонстрировать, что генераторами колебания служат несущие электрический заряд электроны, вращающиеся по внешним орбитам атомов. Именно изменения уровня энергии этих электронов и запускают световые волны.
Далее. Максвеллу показалось логичным, что заряды могут колебаться с любой частотой, а следовательно, и электромагнитные колебания могут быть любой частоты. Отсюда следовал вывод о существовании излучений с меньшей частотой и большей длиной волны, чем у красного света, и, наоборот, с большей частотой и меньшей длиной волны, чем у фиолетового.
Сейчас уже действительно открыты и инфракрасный, и ультрафиолетовый спектры излучения. Глаз их не воспринимает, так что свет этих спектров для нас невидим, но в физическом отношении эти излучения вполне реальны. Примерно в 1800 году английский астроном немецкого происхождения Уильям Гершель поместил градусник под облучение невидимым глазу светом частотой чуть меньше красного, и градусник стал нагреваться даже быстрее, чем при облучении видимым светом, из чего стало ясно, что излучение содержит энергию.
Примерно в то же время немецкий физик Иоганн Вильгельм Риттер обнаружил, что воздействие синего и фиолетового света приводит к распаду нитрата серебра на металлическое серебро и вещество становится из белого черным; но, кроме того, оказалось, что невидимые лучи той части спектра, которая находится сразу за фиолетовой, приводят к тому же результату еще быстрее! Так было доказано содержание энергии и в ультрафиолетовой части спектра.
Однако и инфракрасное и ультрафиолетовое излучения лежат все же достаточно близко к видимой части спектра, а по теории Максвелла предполагалось существование излучения и в удаленных от нее частях. При его жизни существование таких видов излучения экспериментально установлено не было.
Максвелл, умерший в 1878 году в возрасте всего сорока восьми лет, не дожил до дня подтверждения своей теории на практике. Однако уже через восемь лет, в 1886 году, немецкий физик Генрих Рудольф Герц построил электрическую цепь, в которой электрический ток вызывал колебания с крайне низкой частотой, что, по теории Максвелла, должно было привести к образованию излучения с такой же низкой частотой и соответственно большой длиной волны. И Герцу действительно удалось зафиксировать такое излучение — нам оно известно под именем радиоволн.
Частота радиоволн — от 1 000 000 и ниже. Частота коротких радиоволн доходит до 10 000 000 000 (десяти миллиардов). Радиоволны постепенно переходят в микроволны, те — в волны инфракрасного спектра, а те, в свою очередь, — в волны видимой части спектра. Все переходы происходят плавно и незаметно, разрывов, то есть таких значений частоты, для которых не существовало бы волны, в этой цепочке нет.
Что же мы можем сказать про вторую половину спектра излучения? В 1895 году немецкий физик Вильгельм Конрад Рентген открыл новый вид излучения. Он называл его «лучами X», а нам оно известно под названием «рентгеновского излучения», по имени первооткрывателя. Частота этого излучения оказалась гораздо выше, чем частота излучения ультрафиолетового, порядка миллионов триллионов. Как выяснилось позже, источник этого излучения запускался изменением энергетического уровня электронов, вращающихся на внутренних орбитах атома. А год спустя обнаружилось, что элемент уран испускает неизвестное до тех пор излучение, оказавшееся тоже разновидностью электромагнитного излучения с частотой еще выше, чем у рентгеновского, — порядка миллиардов триллионов. Это излучение получило название «гамма-лучей». Его источником оказалось изменение энергетического уровня заряженных частиц самого ядра атома.
Рис. 19. Электромагнитный спектр
В этой части спектра мы видим ту же картину, которая описывалась выше для «низкочастотного» излучения: гамма-лучи плавно переходят в рентгеновское излучение, рентгеновское — в ультрафиолетовое, а ультрафиолетовое — в видимую часть спектра. Полностью весь электромагнитный спектр (рис. 19) содержит около 60 октав (октава — это отрезок, на протяжении от начала до конца которого частота удваивается). Из них видимая часть спектра — это всего лишь одна октава. К 1900 году теория Максвелла подтвердилась полностью.
Свет — это форма энергии, но, как стало ясно с наступлением XIX века, энергетическое содержание света различных участков спектра не одинаково. Привести к распаду серебросодержащих соединений с образованием металлического серебра может только действие «высокочастотного» синего и фиолетового света. Сколько ни облучай нитрат серебра «низкочастотным» красным светом, ничего не произойдет.
Этот и множество других примеров ясно показывают, что энергетическое содержание высокочастотных световых волн выше, чем низкочастотных. Ультрафиолетовое излучение было обнаружено только благодаря тому, что еще эффективнее, чем любой свет видимой части спектра, разлагало серебросодержащие элементы. Кроме того, ультрафиолетовые лучи могут обжечь кожу. Рентгеновские лучи проникают в вещество глубже, а гамма-лучи — еще глубже, и оба этих вида излучения вызывают в организме реакции (очень вредоносные), требующие приложения большого количества энергии.
Тот факт, что излучение с высокими частотами несет больше энергии, подтверждается и свойствами нагретых предметов. Часть энергии, приобретаемой ими с теплом, отдается наружу посредством излучения. Чем выше поднимается температура, тем выше частота испускаемого излучения. Таким образом, нагреваемый кусок металла начинает испускать излучение (и поднесенная к нему рука будет чувствовать тепло или даже жар), оставаясь при этом абсолютно невидимым в темноте. Испускаемое им излучение лежит в инфракрасной части спектра. По мере повышения температуры он начинает излучать уже и в видимой части, и мы замечаем исходящее от него тускловатое красное свечение. Для того чтобы «раскалиться докрасна», металлу необходимо нагреться примерно до 650 °С.
При еще более высоких температурах частота излучения продолжает возрастать, так что при температуре в 2000 °С металл, миновав стадию ярко-красного, станет уже желтым. Солнце, температура на поверхности которого равна 5700 °С, «раскалено добела» и испускает в достаточно большом количестве ультрафиолетовые лучи. Некоторые звезды (правда, их немного среди общего числа) излучают в основном в синей и ультрафиолетовой частях спектра. Солнечная корона, температура которой более миллиона градусов, испускает даже рентгеновские лучи.
Интерес к подробностям излучения тел при различной температуре к концу XIX века становился все больше. Для упрощения было введено представление о существовании тела, которое поглощает все попадающие на него лучи, какую бы частоту они ни имели. Такой предмет не отражал бы никакого излучения и представлял бы собой, таким образом, идеально «черное тело». Если такое черное тело нагреть, оно стало бы с одинаковой легкостью испускать излучение всех частот. (Тело, не являющееся «черным», то есть поглощающее излучение лишь определенных частот, именно на этих частотах и будет излучать, если его нагреть.)
Но если черное тело при нагревании действительно будет с одинаковой легкостью излучать на всех частотах, то возникает парадокс, нуждающийся в объяснении. Высокочастотных видов излучения существует гораздо больше, чем низкочастотных (так же, как чисел более триллиона существует гораздо больше, чем чисел менее триллиона). Поэтому если свет может с равной вероятностью «выбирать» среди всех доступных частот, то практически все излучение должно происходить в высокочастотном спектре, а на долю немногочисленных низкочастотных значений должно приходиться очень мало. Однако при нагревании предметов, приближенных к идеальному «черному телу», такого не происходило. Даже при сравнительно высоких температурах большая часть излучения оказывалась лежащей в видимой и более низкочастотных частях спектра. Для получения высокочастотного излучения в более-менее значительном объеме требовалось нагреть тело до весьма значительных температур.
Объяснения этому явлению не существовало вплоть до 1900 года, когда немецкому физику Максу Карлу Планку пришла в голову идея. А что, если излучение, как и материя, не является непрерывной и однородной субстанцией? Что, если излучение, как и материя, состоит из крошечных неделимых единиц? Для объяснения того факта, что высокочастотное излучение содержит больше энергии, чем низкочастотное, только и остается предположить, что оно состоит из единиц большего объема.
Планк назвал эти единицы энергии «квантами», от латинского «quantum» — «сколько», и предположил, что энергетическое содержание одного кванта пропорционально частоте излучения. Обозначив энергию как е, а частоту заданного излучения как ν (греческая буква «ню»), мы получим математическую формулу гипотезы Планка в виде
е = hν,
коэффициент пропорциональности которой h известен нам сейчас как «постоянная Планка».
Соответственно, не следует предполагать, что при нагревании предмета, будь это даже идеально черное тело, он будет с одинаковой вероятностью излучать на всех частотах. Частота гамма-лучей в миллиард раз больше частоты инфракрасных лучей, значит, на образование кванта гамма-излучения требуется в миллиард раз больше энергии, чем на образование кванта инфракрасного излучения. При низких температурах, когда энергетическое содержание предмета невелико, в нем могут образовываться вообще одни только кванты инфракрасного света. По мере роста температуры, а следовательно, и доступной для формирования квантов энергии в предмете начинают образовываться все более и более крупные кванты все более и более высокочастотного излучения. Вообще, только с использованием квантовой теории оказалось возможным точное описание свойств испускаемого черным телом излучения — ничто другое не позволяло добиться такого результата.
Теория эта оказалась настолько революционной, что в течение некоторого периода лишь немногие физики решились принять ее на вооружение. А затем в 1905 году Альберт Эйнштейн с помощью квантовой теории сумел объяснить механизм, путем которого некоторые металлы под воздействием света начинают испускать электроны.
Еще в конце XIX века было отмечено, что под лучами света некоторые металлы испускают электроны. Энергия испускаемых электронов зависела при этом не от силы света, а от его частоты. К примеру, красный свет, не важно, сколь сильный, не приводил к испусканию электронов вообще. Облучение желтым светом вызывало испускание лишь небольшого количества электронов с малым содержанием энергии. Если желтый свет был ярче и сильнее, электронов испускалось чуть больше, но их энергетическое содержание по-прежнему оставалось небольшим. А вот облучение синим светом уже приводило к испусканию достаточно энергичных электронов. Если синий свет был очень слабым, то и электронов испускалось мало, но энергетическое содержание их было при этом все таким же высоким.
Эйнштейн указал, что такое положение дел становится вполне логичным, если предположить, что энергия может поглощаться только целыми квантами. Энергии маленького кванта красного света не хватает на то, чтобы вытолкнуть электрон, и, сколь сильным ни делай красный свет, испускания электронов не добьешься, потому что перед поглощением каждого следующего кванта атом всегда успевает избавиться от предыдущего. Чуть более крупные кванты желтого света при поглощении могут выбить электрон, обладающий слабой энергией, а еще более крупные кванты синего света — электрон с еще большим энергетическим содержанием.
И только тогда ученые наконец признали и приняли квантовую теорию Планка.
* * *
Вернемся же к нашей смеси водорода с хлором, чтобы посмотреть в свете свежеобретенного знания, что же делает с ней свет. Если смесь газов просто нагревать с помощью горячей плиты или даже пламени горелки, то излучение, с помощью которого в газ поступает тепло, будет в основном инфракрасным — в случае с горелкой лишь небольшая часть его будет находиться в видимой части спектра. Поэтому кванты его будут невелики. Расщепление молекул начнется лишь тогда, когда они наберут достаточно этих квантов для приобретения определенного уровня кинетической энергии.
А кванты сравнительно высокочастотных фиолетовых и ультрафиолетовых лучей, содержащихся в солнечном свете или магниевой вспышке, гораздо крупнее. Молекула хлора, два атома которой связаны слабее, чем в аналогичных молекулах водорода или кислорода, поглотив такой квант, сразу же набирает достаточно энергии для распада. Если обозначить квант за hν, то мы можем записать это так:
hν + Cl2 → Сl + Сl.
Каждый высвобожденный таким образом атом хлора может тут же вступить в реакцию с молекулой водорода для образования хлороводорода.
Но если бы это было все, то действием каждого кванта становилось бы образование двух молекул хлороводорода и общее количество квантов, необходимое для превращения смеси двух газов в хлороводород, равнялось бы количеству имеющихся в смеси молекул хлора.
На самом же деле излучения требуется гораздо меньше. Тщательное изменение количества поставляемой энергии и образуемого хлороводорода показало, что подача одного кванта энергии может привести к образованию от 10 000 до 1 000 000 молекул хлороводорода.
Поскольку энергии одного кванта для выполнения такой задачи явно недостаточно, то остается сделать вывод, что здесь не все так просто. Общепринятое сейчас объяснение этого факта впервые выдвинул специалист в области физической химии немец Вальтер Герман Нернст. Он предположил, что расщепление молекулы хлора квантом с высоким энергетическим содержанием — это лишь первый шаг. Каждый полученный таким образом атом хлора далее вступает в реакцию с молекулой водорода, в результате чего получается не только молекула хлороводорода, но и свободный атом водорода:
Сl + Н2 → HCl + Н.
Этот свободный атом водорода, в свою очередь, вступает в реакцию с молекулой хлора, в результате которой образуется опять один свободный атом хлора:
Н + Cl2 → HCl + Сl.
Этот атом хлора опять вступает в реакцию с молекулой водорода, полученный в ее результате атом водорода — в реакцию с молекулой хлора и так далее; и на каждом повторении этого цикла будет образовываться молекула хлороводорода.
Задача полученного системой кванта энергии — лишь запустить эту цепную реакцию.
Возникает вопрос: почему же тогда цепная реакция не продолжается до тех пор, пока не обработает все до единой молекулы водорода и хлора и не превратит в хлороводород всю смесь без остатка? Дело в том, что цепная реакция не бессмертна. Рано или поздно очередная итерация реакции совершится не с положенной по счету молекулой водорода или хлора, а с какой-нибудь примесью — скажем, водой или кислородом. Необходимый для продолжения цепной реакции свободный атом хлора или водорода в этом случае образован не будет, и цепочка прервется.
Даже при полном отсутствии в реагирующих газах каких-либо примесей (а очистить смесь до такого состояния, чтобы цепная реакция продлилась достаточно долго, — весьма сложная задача!) все равно остается вероятность того, что высвобожденный атом вступит в реакцию, скажем, с молекулой вещества, из которого состоит стенка камеры, или с другим таким же свободным атомом, объединившись с ним обратно в такую же молекулу, из которой они изначально распались. То есть даже при идеальных условиях цепная реакция не будет длиться вечно.
Понятно, что смесь газов, в которой вероятность длительного существования цепной реакции мала, останется в целом инертной при любом световом облучении. К примеру, на смесь водорода с кислородом световое облучение никакого заметного эффекта не оказывает. Даже если молекула газообразного кислорода и получит достаточно большой квант энергии, чтобы распасться, то получившиеся в результате свободные атомы кислорода присоединятся каждый к одной молекуле водорода, и на том все и кончится:
О + Н2 → H2O.
В подробности природы света и его воздействия на химические реакции я углубился лишь потому, что ближе к концу книги эти свойства света приобретут для нас решающее значение. Однако сейчас путь, которым мы терпеливо продвигаемся, уводит нас в сторону от этого предмета — навстречу другим, не менее интересным.
Глава 12. СТИМУЛЯЦИЯ БЕЗ ПРИЛОЖЕНИЯ ЭНЕРГИИ
Остановимся на мгновение и подведем промежуточные итоги. Мы начали с поисков различий между живыми существами и неживыми предметами и перешли от них к термодинамике тепловых машин.
Затем мы пришли к выводу, что живые существа тепловыми машинами не являются, но при этом вполне вероятно, что энергию они получают в результате процесса, сходного с горением. От этого повествование закономерно перешло к химической энергии и к тому, что она представляет собой с точки зрения законов термодинамики. Это соображение, в свою очередь, вынудило нас объяснить, почему именно реакции типа задействованных при горении и предполагаемых в участии в процессах жизнедеятельности называются в терминах термодинамики «спонтанными», внешне таковыми не являясь.
Таким образом, мы перешли к предмету обсуждения предыдущей главы — энергии активации, необходимой для того, чтобы «запустить» спонтанную реакцию.
Так чем же теперь это может нам помочь в нашей основной задаче — исследовании природы живой материи? Предположим, что в организме человека происходят такие же реакции, как и при горении. Соответственно они должны обладать энергией активации, которую организм должен предоставить прежде, чем эти реакции начнут спонтанно протекать, снабжая при этом, в свою очередь, организм энергией, необходимой для его функционирования. И кажется, что все описанное в предыдущей главе к живой ткани никоим образом относиться не может.
Я описал два способа, которыми реагенты могут получить энергию активации, — с помощью тепла и с помощью света, но в живом организме явно не используется ни то ни другое. Температура живой ткани практически никогда не поднимается выше 37 °С, чего явно недостаточно для запуска реакций, сходных с горением. То же самое со световым излучением — живая ткань в принципе может быть источником света (примером тому служат светлячки), но это никогда не бывает излучение с высоким содержанием энергии, достаточным для активации химических процессов. Так как же решают живые организмы задачу предоставления энергии активации?
Может быть, перед нами наконец-то пример неподчинения живой материи законам термодинамики? Может быть, вот он наконец-то, тот четкий критерий, что позволит нам провести границу между живой и неживой материей?
Перед тем как перейти к непосредственному ответу на вопрос, давайте посмотрим, существуют ли в мире неживой природы явления, в которых спонтанная реакция запускается без поступления энергии активации, необходимой в большинстве случаев. Ведь если они существуют, то и в живой ткани вполне может происходить нечто подобное.
Первый значительный пример такого рода был обнаружен в связи с производством серной кислоты.
Серная кислота, как и ряд других сильнодействующих кислот, была открыта в Средние века, став одним из очень важных, хотя и недооцененных, продуктов алхимических опытов. Алхимики слишком концентрировались на поиске рецептов производства золота и слишком мало внимания обращали на действительно важные результаты своих исследований.
Серная кислота действует во много раз сильнее, чем самая сильнодействующая кислота из известных древним (уксусная кислота виноградного происхождения). Она вступает в ряд химических реакций, которые более слабые кислоты или не могут повторить вообще, или повторяют гораздо медленнее. Таким образом, сильнодействующие кислоты в целом и серная кислота в частности явили собой очень действенный химический инструмент, как для исследовательского, так и для промышленного применения. Даже сегодня серная кислота является самым используемым в химической промышленности веществом, если, конечно, не считать повсеместно присутствующих воздуха и воды, да еще, быть может, соли. Ежегодно изготавливается около пятнадцати миллионов тонн серной кислоты, и иногда даже считается, что масштаб индустриализации страны можно определить по количеству потребляемой ею серной кислоты.
Понятно, что важное значение приобрела разработка технологий дешевого и массового производства серной кислоты. На заре современности ее производство было сложным и дорогим процессом с ограниченным объемом.
Причиной тому были не трудности с добычей исходного сырья. Им служит сера (S) — вещество известное еще в древности, широко распространенное и веками добываемое в достаточном количестве и сравнительно легко, например, в Сицилии.
Сера хорошо горит, вступая в соединение с кислородом и образовывая при этом удушливый газ, сернистый ангидрид (SO2). Именно этот газ и дает знаменитый «запах серы», а не сама сера, которая запаха как раз не имеет.
Сернистый ангидрид растворим в воде, соединяясь затем с молекулой воды в «сернистую кислоту» — H2SO3.
S + O2 → SO2,
SO2+H2O → H2SO3.
Действие сернистой кислоты имеет лишь умеренную силу, и к тому же она не очень стабильна. Это не то же самое, что необходимая нам серная кислота, имеющая в своем составе на один атом кислорода больше — H2SO4.
И вот самое сложное — это именно добиться присоединения этого самого последнего атома. Точнее, сернистый ангидрит может и дальше соединяться с кислородом, образовывая при этом серный ангидрид (SO3), а он уже при растворении в воде и даст вожделенную серную кислоту:
2SO2 + O2 → 2SO3,
SO3 + Н2О → H2SO4.
На бумаге все выглядит гладко, но проблема состоит в том, что реакция соединения сернистого ангидрида с кислородом, хоть и приводит к снижению уровня свободной энергии, а значит — является спонтанной, вместе с тем требует столь высокой энергии активации, что путем прямого соединения сернистого ангидрида с кислородом удается получить очень мало серного ангидрида. Поэтому на протяжении всего XVII и начала XVIII века серную кислоту производили лишь по чуть-чуть и использовали крайне редко. На получение двух фунтов серной кислоты уходила неделя тяжкого труда.
Затем, в 40-х годах XVIII века, один из производителей серной кислоты, Джошуа Уорд, вдруг обнаружил, что при сжигании стандартной упаковки серы удается произвести гораздо больше серной кислоты, если примешать к ней селитру (азотнокислый натрий). Выяснилось ли это случайно, или изначально планировалось подмешать в серу селитры, чтобы она быстрее сгорала, на манер пороха (который состоит, как известно, из серы, селитры и порошкового угля), я не знаю. Так или иначе, Уорд запатентовал свою технологию, и стоимость производства серной кислоты резко упала.
Масштабы производства этого химиката соответственно возросли, и сам технологический процесс стали осуществлять уже не в хрупких стеклянных колбах, а в больших свинцовых камерах.
На протяжении полувека производители продолжали подмешивать селитру в серу, так и не понимая, зачем именно они это делают. Никаких азотсодержащих веществ в результате реакции никогда не образовывалось. По окончании процесса селитра так и оставалась в камере нетронутой, так что ее можно было использовать снова и снова. В ходе реакции она ничего не отдавала (по крайней мере, этого не обнаруживалось) и не расходовалась. Так в чем же заключалась ее роль?
В 1806 году два французских химика, Шарль Бернар Дезорм и Николя Клеман, выдвинули предположительное объяснение, принцип которого принят и по сей день. При сгорании серы и селитры образуются два газа, сернистый ангидрид (SO2) и перекись азота (NO2). По предположению ученых, перекись азота отдает затем один из своих атомов кислорода на образование серного ангидрида, а сама превращается в простой оксид азота (NO):
SO2 + NO2 → SO3 + NO.
Сам оксид азота после этого забирает один атом из атмосферного кислорода и снова становится перекисью азота:
2NO + O2 → 2NO2
Таким образом, перекись азота выполняет роль посредника, отдавая атом кислорода сернистому ангидриду, забирая на его место другой из воздуха и снова передавая его другой молекуле сернистого ангидрида, и так далее. На всем протяжении этой активной работы перекись азота остается сама собой, превращаясь в конце реакции обратно в селитру, как будто ничего с ней и не происходило.
Со времен Дезорма и Клемана эта картина уточнялась и усложнялась. Сейчас уже известно, что перекись азота и сернистый ангидрид соединяются вместе с водой и кислородом в единый сложный «продукт присоединения», который в итоге распадается, в частности, на серную кислоту и селитру. Однако принцип происходящего остается неизменным — сначала селитра участвует в реакции, а затем восстанавливается в прежнем виде.
С точки зрения энергии при такой схеме удается избежать момента приложения мощной энергии активации, необходимой для непосредственного соединения сернистого ангидрида и кислорода (рис. 20). Да и самого непосредственного соединения при такой схеме тоже не происходит. Вместо этого сернистый ангидрид соединяется с перекисью азота, образовывая с ним «продукт присоединения», в ходе реакции, требующей значительно более низкой энергии активации, а образование серной кислоты и восстановление перекиси азота происходит в ходе другой реакции, тоже требующей невысокой энергии активации.
Рис. 20. Как избежать приложения энергии активации
Здесь нет получения чего-либо «ниоткуда». Законы термодинамики не нарушаются. Свободная энергия имеющегося на входе сернистого ангидрида и получаемого на выходе серного ангидрида (или серной кислоты) остается прежней. Общее направление движения реакции на обоих этапах — «вниз», от высокого уровня энергии к низкому. Однако вместо перехода от сернистого ангидрида непосредственно к серному через высокий порог благодаря добавлению селитры путь прокладывается иным образом — через два последовательных низких порога. В терминах энергии активации эта интерпретация впервые прозвучала в отношении всех явлений подобного рода в 1894 году из уст немецкого физика Вильгельма Оствальда.
Если рассматривать реакцию сернистого ангидрида с кислородом для образования серного ангидрида как путь по железной дороге из одной долины в другую, ниже расположенную, через перевал, то добавление селитры равносильно открытию нового пути, через более низкие перевалы. Если поездам хронически не хватает топлива, то через высокий перевал переберутся лишь немногие, и успешное завершение переезда из одной долины в другую станет делом редким и удивительным. Но открытие нового пути позволит облегчить и сделать более массовым движение между долинами даже без поставок дополнительного топлива.
В течение XIX века обнаруживались все новые и новые примеры того, что примешивание определенных веществ в небольших количествах помогало ускорять реакции больших объемов реагентов, при том что сами вещества в процессе реакции не расходуются. В 1812 году русский химик Готлиб Сигизмунд Кирхгоф обнаружил, что если при варке крахмала в воде добавить чуть-чуть разведенной серной кислоты, то крахмал распадается с образованием сахара, полностью идентичного тому, что содержится в винограде (позже его назовут глюкозой).
Если же кислоты не добавлять, а просто варить крахмал в воде — этого не происходит. Более того, при распаде крахмала с помощью кислоты сама кислота не расходуется — окончательный раствор сахара содержит не меньше кислоты, чем исходный раствор крахмала.
А английский химик Гемфри Дэви в 1816 году обнаружил, что наличие проволоки из некоторых металлов стимулирует соединение различных паров, например спиртового, с кислородом. Это оказалось особенно справедливым в отношении редких и инертных металлов, платины и палладия.
Исследования в этом направлении привели к тому, что немецкий химик Иоганн Вольфганг Дёберейнер установил, что участие порошка платины приводит к соединению водорода с кислородом при комнатной температуре. Он изобрел даже автоматическую зажигалку (известную как «лампа Дёберейнера») за много лет до того, как были придуманы спички для практического использования. Основу его «лампы» составляла емкость с кислотой, сконструированная таким образом, чтобы кислоту можно было подавать во внутреннюю камеру, в которой содержалась цинковая полоска. В ходе реакции между цинком и кислотой высвобождался водород и выходил в отверстие в верхней части емкости. Там поток водорода попадал в камеру с платиновым порошком и мгновенно загорался.
Разумеется, платиновый порошок, во-первых, дорог, а во-вторых, быстро теряет свои свойства при подобном использовании из-за наличия посторонних примесей в поступающем водороде. Так что «лампе Дёберейнера» была уготована судьба всего лишь химической игрушки. Однако сам факт ее работы очень наглядно продемонстрировал уникальные свойства платины. Кроме того, стало ясно, что реакции, происходящие при горении (и, возможно, в человеческом организме), можно заставить происходить и при комнатной температуре без обязательного внесения энергии активации (что мы и собирались выяснить в начале главы).
В 1836 году этот факт, а с ним — и ряд других привлекли внимание шведского химика по имени Йене Якоб Берцелиус. В свое время этот человек железной рукой правил миром химии, проявляя интерес (причем с весьма плодотворными результатами!) ко всем разделам этой стремительно развивавшейся науки.
Берцелиус свел воедино все разрозненные факты, которые были ему известны, указал на их значение и предложил дать описываемому явлению название «катализ», от греческого слова, означающего «распад», — в честь первого факта распада крахмала на сахар в присутствии кислоты. Термин был принят и используется до сих пор.
Любое вещество, обладающее свойством, присутствуя в небольших количествах (иногда — в совсем малых), ускорять реакцию между большими количествами других веществ, не расходуясь при этом в ходе реакции, называется катализатор. Кислота — это катализатор реакции распада крахмала на сахар. Платина — это катализатор реакции соединения водорода с кислородом при комнатной температуре. Перекись азота — это катализатор создания серной кислоты.
Кстати, сам процесс производства серной кислоты в свинцовой камере сошел на нет благодаря тем же новым открытиям, благодаря которым и появился. В 1831 году английский химик Перегрин Филлипс обнаружил, что платина является более продуктивным катализатором превращения сернистого ангидрида в серный, чем селитра, и запатентовал свое открытие. К середине XIX века, когда были разработаны методы продления активной жизни дорогого платинового катализатора, новый «контактный процесс», где для соединения с кислородом сернистый ангидрид должен вступить в контакт с платиной, повсеместно вытеснил старую технологию производства кислоты в свинцовой камере.
Сразу хочется назвать свет и тепло также катализаторами, поскольку добавление небольшого количества тепла ускоряет любую реакцию, а добавление небольшого количества света приводит к взрывообразной реакции до того инертной смеси водорода с хлором. На самом деле реакции по типу последней часто так и называют — катализируемыми светом.
Однако термин «катализатор» используют, как правило, только по отношению к веществам.
Понятно, что на самом деле такие катализаторы, как перекись азота или кислота, все же участвуют в реакции, восстанавливаясь впоследствии. Это активные вещества, принимающие полноценное участие в химических реакциях, когда им создают соответствующие условия.
Вот платина — другое дело. Это самый замечательный катализатор из всех открытых в начале XIX века, инертный металл, крайне тяжело вступающий в реакцию с другими веществами лишь под воздействием совсем уж непреодолимых обстоятельств. В чем же тогда заключается его участие во множестве реакций, в результате которых получаются катализированные соединения? Ведь немыслимо же, чтобы платина просто оказывала на молекулы реагирующих веществ какое-то мистическое воздействие.
В 1833 году английский ученый Майкл Фарадей выдвинул на эту тему следующее предположение. Он обнаружил, что кусок чистой платиновой фольги катализирует реакцию соединения водорода с кислородом, но при добавлении к смеси небольшого количества угарного газа (СО) действие катализатора прекращается. Угарный газ как бы «отравляет» платину. (Тут можно увидеть интересную аналогию: стоит подмешать немного угарного газа к нашему собственному запасу кислорода — и он с таким же успехом отравит и нас.)
Фарадей предположил, что кислород с водородом образовывают пленку на поверхности платины. В этой пленке оба вещества гораздо плотнее примыкают друг к другу, чем в исходной смеси газов. В общем, можно сказать, что эффект катализатора в данном случае сходен с эффектом нагнетания давления, ведь известно, что повышение давления в смеси газов зачастую ускоряет их реакцию. Затем Фарадею осталось указать, что угарный газ, даже в малых количествах, тоже склонен образовывать пленку на платине, но поскольку он, в отличие от водорода и кислорода, никуда с нее не девается, то в итоге он полностью закрывает платину и от того и от другого, на чем катализ и заканчивается.
Представление о том, что в некоторых катализируемых реакциях ведущая роль принадлежит поверхности катализатора, до сих пор не опровергнуто, оно лишь периодически уточняется. Так, само по себе наличие газовой пленки на такой поверхности ничего не объясняет, поскольку уже после Фарадея выяснилось, что высокое давление, казалось бы равносильное по механизму действия катализатору, не приводит к столь же резкому ускорению реакции.
В 1916 году американский химик Ирвинг Ленгмюр видоизменил теорию Фарадея и внес в нее предположение о том, что молекулы газовой пленки удерживаются на поверхности настоящими химическими связями с атомами платины.
Крайние атомы платины, находящиеся на поверхности, не со всех сторон окружены другими атомами платины, так что их способность образовывать химические связи задействована не полностью. В сторону открытого пространства атомы платины (Pt) способны образовывать связи с чужими атомами. Соответственно тот факт, что платиновый порошок имеет гораздо более выраженные каталитические свойства, чем просто кусок платины, можно объяснить тем, что на единицу веса порошок имеет гораздо большую площадь поверхности и гораздо больше атомов могут вступать в реакцию с образованием химических связей.
Так что можно рассматривать платину как вещество, все-таки вступающее в полноценную реакцию с кислородом. Все атомы с поверхности платины, вцепляясь в атомы кислорода, образовывают некое подобие «продукта присоединения» — оксид платины. Энергия активации для образования этого оксида крайне мала, как и энергия активации следующей реакции — соединения водорода с кислородом из этого оксида (в отличие от соединения с кислородом из его двухатомных молекул, составляющих газ). Соединение происходит очень быстро, поскольку кинетической энергии молекул газа при комнатной температуре более чем достаточно для того, чтобы предоставить необходимую энергию активации.
После того как соединение произошло, атом платины оказывается соединенным с молекулой воды. Но связь между ним и молекулой достаточно слаба, и бомбардировка молекулами газа легко разрывает ее. Атом платины, таким образом, высвобождается для образования новой связи со следующим атомом кислорода.
«Отравление» поверхности платины угарным газом происходит по причине способности атома платины связываться как с молекулой кислорода, так и с молекулой угарного газа. Но угарный газ, в отличие от кислорода, присоединившись к платине, не вступает в реакцию с водородом (как и ни с чем другим, что бы ни присутствовало в системе) для образования слабо удерживаемой молекулы. Он крепко застревает на своем месте. Каждый атом платины, занятый молекулой угарного газа, так и остается занятым, и так происходит со всеми атомами поверхности, пока платина полностью не утратит свои каталитические свойства.
Даже поверхностный катализ не отменяет и не изменяет основных законов энергообмена в химических реакциях. Он может лишь перенаправить ход реакции таким образом, чтобы она проходила через промежуточные реакции с низким уровнем энергии активации, и ускорить тем самым ход реакции в целом, но катализ не влияет на общие изменения энергии в ходе реакции, и в принципе не может этого сделать.
В частности, это значит, что катализатор не может обратить спонтанную реакцию вспять. Если водород спонтанно соединяется с кислородом, образовывая при этом воду, то катализатор может ускорить этот процесс за счет снижения уровня энергии активации. Но никакой катализатор не может вызывать массовое разложение воды на водород и кислород при комнатной температуре без приложения дополнительной энергии.
Далее, в любой обратимой реакции положение точки равновесия (как вы помните — это точка, в которой уровень свободной энергии минимален) никак не смещается по причине присутствия катализатора. Катализатор может лишь ускорять реакцию в обоих направлениях и способствовать скорейшему достижению точки равновесия. Однако изменить значение самой точки равновесия катализатор не способен ни на йоту.
Теперь, разобравшись с катализаторами и обретя необходимый багаж базовых знаний, мы можем перейти наконец к живой материи. Во второй части книги я постараюсь показать, насколько принципы справедливые и незыблемые для неодушевленного мира применимы к процессам, происходящим в человеческом организме.
Часть вторая. ОРГАНИЗМ
Глава 13. И СНОВА О ЖИВОЙ И НЕЖИВОЙ МАТЕРИИ
Все открытия и выводы о сохранении энергии и возрастании энтропии, о свободной энергии и катализе были получены на основе изучения неодушевленного мира. Всю первую половину книги я описывал и объяснял эти механизмы лишь для того, чтобы теперь с их помощью попытаться объяснить работу живых клеток.
Но для этого надо сначала удостовериться, что все законы, справедливые для явлений неживой природы, справедливы и для процессов живой ткани. А так ли это? Свойства камня и ящерицы — определяются ли они одними и теми же законами или все-таки разными?
На протяжении всей истории человечества сама постановка такого вопроса казалась делом странным, и очевидно было, что ответ должен заключаться в гордом «ни в коем случае!». Я только что потратил множество страниц на тщательные поиски оснований, на которых можно было бы провести четкую границу между живой и неживой природой, и оказалось, что это не так-то просто, но еще сто лет назад о таких сложностях никто и не подозревал. Вместо этого считалось, что живая материя принципиально, безоговорочно и явно отличается от неживой. Право же, каким дураком надо быть, чтобы не видеть принципиальной разницы между камнем и ящерицей.
И действительно, вполне естественным кажется четкое, без сомнений и оговорок, разделение всех объектов во Вселенной на три категории: мир неживой, состоящий из воды, земли, гор, песка и воздуха; мир растительный, к которому принадлежат объекты, рождающиеся, живущие и умирающие, но при этом укорененные в почве и не умеющие передвигаться самостоятельно; и мир животный, к которому принадлежат объекты, рождающиеся, живущие и умирающие, но при этом обладающие способностью передвижения. Это необходимо учитывать, прежде чем мы начнем игру в угадайку и будем пытаться определить, «животное это, растение или минерал».
Стоит немного задуматься, и становится ясно, что различие между животными и растениями гораздо меньше, чем между ними обоими и минералами. Например, человек может употреблять в пищу как животных, так и растения. Когда же в XVII веке был изобретен микроскоп, то с обнаружением микроорганизмов граница между этими двумя категориями оказалась еще более размытой, поскольку многие микроорганизмы непонятно было куда отнести.
Поэтому более логичным казалось разделение надвое: на живую природу (куда входят и животные, и растения) и неживую.
Таким образом, мир кажется совершенно четко разделенным на категории объектов с абсолютно различными свойствами, и неизбежно было предположить, что для каждой категории существуют свои законы природы. Даже в XIX веке существование различия между живой и неживой материей и между законами, управляющими бытием той и другой, казалось само собой разумеющимся.
Такие представления распространялись не только на сами объекты, такие как камень или ящерица, но и на составляющие их химические вещества.
Раскрошите камень, и получите недвижимую инертную пыль и крошку. Оставьте их на несколько лет, и с ними не произойдет никаких перемен. Размешайте каменную пыль в воде, потом выпарите воду — каменная пыль снова станет прежней. Нагрейте каменную крошку докрасна, потом остудите ее — и снова никаких следов.
С другой стороны, если нашинковать ящерицу, то получится куча мягкого кровавого мяса, которое за короткий промежуток времени испортится, начнет вонять и в нем заведутся личинки мух. Нагрейте мясо, и оно зашипит, обуглится и изменится до неузнаваемости. И сколько его потом ни охлаждай, прежним оно уже не станет.
Эти разительные отличия в свойствах наблюдаются и если рассматривать чистое химическое вещество, выделив его из общей массы. Из камня можно извлечь чистый силикат алюминия или чистую медь. Из живого организма можно извлечь чистый сахар или чистое растительное масло. И силикат алюминия, и медь можно нагревать, потом остужать, и никаких следов этих процессов на веществе не останется. Если же нагреть сахар — он обуглится, если нагреть масло — оно загорится; и в том и в другом случае обратно в сахар и масло эти вещества уже не превратятся.
Это различие между веществами, принадлежащими к двум разным группам, довлело над химиками с самого зарождения науки. К примеру, в XVII веке немецкий химик Иоганн Рудольф Глаубер занимался исследованием веществ, получаемых как из живых, так и из неживых предметов. Из царства минералов он получил кристаллы сульфата натрия, в которых, как нам сейчас известно, каждая молекула имеет слабые связи с десятью молекулами воды. Такие слабые связи в формулах принято обозначать точками, и формула этого вещества, именуемого иногда «глауберовой солью», выглядит как Na2SO4∙10H2O. Из мира живой материи Глаубер выделил такие вещества, как ацетон и бензол.
Все эти вещества под действием плавного нагревания подвергаются изменениям. Однако есть принципиальное различие. Глауберова соль при нагревании теряет слабо прикрепленные к ней молекулы воды, так что остается только «обезвоженный» сульфат натрия; но если к этому «обезвоженному» веществу добавить воду, то снова образуются кристаллы глауберовой соли идентичные изначальным.
С другой стороны, если нагреть ацетон или бензол, он вспыхнет и после этого вся королевская конница и вся королевская рать уже не смогут собрать горячие пары в изначальный ацетон или бензол, используя какие-то простые средства вроде охлаждения или добавления воды.
Казалось, что химические вещества, получаемые из неживой материи, разделяют инертность и стабильность камней, из которых они выделены, а вещества, получаемые из живых организмов, так же хрупки и тонки, как сама жизнь. Или наоборот — можно было заявить, что камни мертвы и бесчувственны потому, что состоят из мертвых и бесчувственных материалов, а живые существа состоят из нестабильных и хрупких составляющих, и поэтому сами переменчивы, тонки и чувствительны.
К 1807 году Берцелиус окончательно закрепил эти различия в терминологии, назвав все вещества, получаемые из живых существ или из их мертвых тел, «органическими». Понятно, что вещества, имеющие неживое происхождение, стали «неорганическими». В соответствии с представлениями о том, что существует два свода законов природы, один — для живой материи, а другой — для неживой, и химия была разделена на две части — на химию органическую и неорганическую.
Поскольку органические химические вещества производятся только живыми организмами и никогда не встречаются в неживой природе, то казалось логичным предположить, что для их создания требуется некая «искра жизни», или «жизненная сила». Если бы это оказалось правдой, то химики со всеми своими горелками и мехами, со всеми своими кислотами никогда не сумели бы создать органическое вещество из неорганических, потому что одно дело — инструменты и химикаты, а совсем другое — мистическая «жизненная сила».
Самым главным сторонником такой теории был сам Берцелиус, и он был, должно быть, просто шокирован, когда его ученик, немецкий химик Фридрих Вёлер, в 1828 году разрушил всю теорию, как карточный домик. Вёлер занимался неорганической химией, именно он впервые сумел получить чистый алюминий и бериллий и разработал новые методики выделения никеля. Во время совершения своего выдающегося открытия он занимался нагреванием цианата аммония — вещества, традиционно рассматриваемого как совершенно неорганическое. К собственному изумлению, Вёлер обнаружил, что в процессе нагревания свойства цианата аммония разительно изменяются. Вещество, полученное в итоге, обладало всеми свойствами мочевины — самой что ни на есть органической субстанции, основного вещества, растворенного в моче млекопитающих.
Таким образом, из неорганического вещества удалось создать органическое путем простого нагревания. Никакой «жизненной силы» при этом приложено не было (если не считать жизненную силу самого Вёлера). Вёлер еще много раз повторил свой эксперимент, прежде чем осмелился объявить о нем публично, но когда это наконец-то было сделано, то вскоре, как это часто случается в науке, и другие химики повсеместно стали объявлять о синтезе органических веществ из неорганических.
С химической точки зрения открытие Вёлера не имеет столь уж большого значения — он провел достаточно тривиальную реакцию, но психологическое значение этого достижения было безмерно. Он сломал казавшийся незыблемым барьер между живой и неживой материей. Теории о «жизненной силе» был нанесен смертельный удар, и ученые впервые готовы были поверить в существование неких всеобщих законов природы, единых для всего на свете — живого и неживого.
С уничтожением границы между живой и неживой материей в научном мышлении важное место заняли различные моменты сходства между этими двумя видами веществ. Эти моменты были известны людям с незапамятных времен. Главным из этих общих моментов была роль воздуха.
Человек, как и другие сухопутные животные, для поддержания жизнедеятельности должен вдыхать воздух, и воздух этот должен быть хотя бы относительно свежим. Уже древние люди знали, что в закрытом помещении животные впадали в сонливость и умирали, как будто исчерпав запас чего-то жизненно необходимого, что содержится в воздухе (хотя в самом воздухе при этом не отмечалось никаких заметных невооруженным глазом изменений).
Так же ведет себя и огонь. Он ярко вспыхивает при порыве ветра, а в закрытой камере гаснет. Это можно было бы списать на то, что топливом для огня являются все же органические вещества — дерево или уголь, и именно их свойства диктуют свойства пламени, если бы не существовало неорганических горючих веществ, таких как сера или водород, огонь от которых ведет себя точно так же.
Еще в 200 году нашей эры римский физик Гален указал, что если человек поймет механизм горения, то он поймет и механизм дыхания. И его предсказание оправдалось, как стало ясно с появлением трудов Лавуазье.
Когда в конце 70-х годов XVIII века Лавуазье показал, что воздух состоит из азота и кислорода, он также ясно дал понять, что именно кислород и является веществом необходимым как для горения, так и для жизнедеятельности. Затем он обнаружил, что выдыхаемый воздух не только сравнительно беден кислородом, но и сравнительно богат при этом углекислотой. Но более тщательный анализ привел его к выводу о том, что не весь вдыхаемый кислород уходит на образование углекислоты. Некоторое количество кислорода должно тратиться и на что-то еще.
Когда в 1781 году английский химик Генри Кавендиш продемонстрировал, что при сжигании водорода в кислороде образуется вода, для Лавуазье все встало на свои места. Выдыхаемый воздух — заметно влажный, а в пище, потребляемой человеком, определенно содержится водород. В процессе дыхания кислород может соединяться как с водородом, так и с углеродом и производить как воду, так и углекислоту. То же самое происходит при сгорании древесины: кислород потребляется, а вода и углекислота — производятся.
Несомненно, в те времена было бы еще слишком смелым выдвигать предположение о столь тесном сходстве между живой и неживой материей, но после того, как Вёлер синтезировал мочевину и резкое разграничение между живой и неживой материей пропало, такое сравнение стало неизбежным.
Когда возобладало представление о том, что законы органической химии схожи с законами химии неорганической, а то и вовсе совпадают с ними, интерес к органической химии сильно возрос. Химики принялись анализировать органические вещества и с помощью новой теории атомного строения составлять для них формулы, точно так же, как это делалось для веществ неорганических.
Стало ясно, что органические вещества, содержащиеся, к примеру, в пище, состоят по большей части из углерода, водорода и кислорода, в пропорции в среднем два атома углерода на четыре атома водорода на один атом кислорода. Конечно, присутствует в этом перечне в небольших количествах и азот, и, в еще меньших, сера, фосфор и прочие, но ими пока можно пренебречь. Если взять усредненную «формулу пищи» за С2Н4O, то процессы, происходящие в организме человека, можно представить так:
2С2Н4O + 5O2 → 4СO2 + 4H2O.
Состав древесины, как правило, не слишком отличается от среднего состава пищи (хотя его, пожалуй, вернее было бы представить как С2Н4O2), и древесина тоже вступает в соединение с кислородом для образования углекислоты и воды. Так стало ясно, что и человеческий организм, и тепловая машина получают энергию из одного и того же источника — из соединения атомов углерода и водорода с кислородом.
Сам по себе этот факт должен был огорчить тех, кому хотелось бы видеть живой организм чем-то совершенно непохожим на бездушную машину и принципиально превосходящим ее. Строго говоря, аналогия здесь, конечно, не совсем полная. Горящая древесина испускает жар и свет, а «горящая» в организме пища света не производит вообще, а тепло — в достаточно ограниченном количестве.
Возникает вопрос: не свидетельствует ли эта разница о некоем еще более серьезном различии? Если форма энергии, производимой человеческим организмом (и любым другим живым организмом), отличается от формы энергии, производимой пламенем, то, может быть, организм использует более эффективные способы? Может быть, живая материя способна подняться над ограничениями, установленными для неодушевленной тепловой техники такими учеными, как Карно? Должен ли живой организм подчиняться законам термодинамики, разработанным в XIX веке, или мудрость природы даровала ему в виде пищи источник энергии, который паровая машина никогда не обретет ни в виде дров, ни в виде угля?
Остановимся более подробно на пище.
С давних пор люди не могли не замечать, что при приготовлении пищи используется несколько типов материалов с различными свойствами.
Например, есть белое безвкусное вещество, получаемое из зерновых, таких как пшеница или рис. Главной составляющей муки является крахмал.
Во фруктовом соке или, скажем, меде содержится другое, сладкое вещество. Из соков некоторых, особо богатых им, растений это вещество — сахар — можно получать напрямую в твердом виде. Впервые это было проделано в Индии примерно в IV веке до нашей эры. В древности эта технология добралась до Рима, где и сложилось латинское слово «saccharum», происходящее, по всей вероятности, от названия индийского растения. И лишь в Средневековье, вместе с возвращающимися из походов крестоносцами, сахар попал в Европу.
XIX век принес открытие о том, что сахар бывает разный. В 1802 году французский химик Жозеф Луи Пруст (работал он в Испании) объявил об обнаружении вещества, которое выглядит как сахар, такое же белое и кристаллическое, сладкое и легкорастворимое в воде, но при этом не является обычным сахаром, уступая последнему как по сладости, так и по растворимости. Поэтому Пруст провел различие между «тростниковым сахаром» и «виноградным сахаром». Другую разновидность сахара, выделенную за десять лет до того из меда и еще более сладкую, чем тростниковый сахар, Пруст назвал «фруктовым сахаром».
Сейчас принято давать различным сахарам названия, заканчивающиеся на «-оза». Тростниковый сахар — это «сахароза», фруктовый — «фруктоза». Что же касается виноградного сахара, то он получил название «глюкоза», от греческого слова, означающего «сладкий», хотя и является изо всех трех наименее сладким. Сахар, выделяемый из молока (и больше нигде не встречающийся), называют «молочным сахаром», или «лактозой», от латинского слова, означающего «молоко». Однако чаще всего, говоря «сахар», подразумевают именно сахарозу.
В 1812 году, как я уже писал в предыдущей главе, Кирхгоф совершил изумительное открытие: крахмал можно превратить в виноградный сахар, стоит лишь поварить его в растворе кислоты. Это значит, что молекулу крахмала можно рассматривать как состоящую из некоторого количества молекул глюкозы, каким-то образом собранных воедино. Кипячение в кислоте разрывает связь между ними и приводит к высвобождению глюкозы.
К 1819 году французский химик А. Браконно успел прокипятить древесные опилки, холстину, древесную кору, солому и ряд других материалов растительного происхождения в растворе кислоты, и оказалось, что во всех случаях получается глюкоза. Оставалось только сделать вывод, что все эти продукты царства растений состоят из некоего вещества, которое, как и крахмал, состоит из глюкозы, но, в отличие от самого крахмала, несъедобно. Поэтому для нового вещества надо было придумать другое имя. Французский химик Ансельм Пайен назвал его «целлюлозой», от английского «cell» — «клетка», поскольку оказалось, что функция этого твердого вещества — предохранять и защищать уязвимые клетки растения. Именно с этого термина пошел обычай заканчивать названия Сахаров на «-оза».
Французский химик Жозеф Луи Гей-Люссак, проанализировав химический состав сахара и близких к нему веществ, обнаружил, что на каждый атом углерода в молекуле приходится по два атома водорода и одному атому кислорода. Он решил, что, поскольку соединение двух атомов водорода с атомом кислорода — это вода, то молекула сахара должна представлять собой цепочку атомов углерода, к каждому из которых прикреплено по молекуле воды. Поэтому он назвал всю группу веществ — крахмал, целлюлозу, различные сахара — «углеводами». В дальнейшем выяснилось, что на самом деле молекулы их имеют более сложное строение, но название к тому времени уже прижилось, и отменять его никто не стал.
Оказалось, что молекула глюкозы состоит из шести атомов углерода, поэтому ее формула выглядит так: С6Н12О6, и можно сказать, что это типичная формула углевода.
Кроме углеводов, из пищи с давних пор извлекали вещества еще одной категории — жиры и масла. Главное различие между ними заключается в том, что жиры — это твердые тела (хотя и достаточно мягкие), а масла — жидкие; по остальным же свойствам они очень близки, поэтому термин «жиры» принято распространять и на жиры как таковые, и на масла. Жиры нерастворимы в воде и на ощупь дают характерное жирное ощущение.
Примерно в то же время, когда Браконно изучал химию углеводов, другой французский химик, Мишель Эжен Шеврёль, взялся за изучение жиров. Из его трудов в конце концов стало ясно, что жиры, как и углеводы, состоят из трех элементов — углерода, водорода и кислорода, с той лишь разницей, что сравнительное содержание кислорода в них оказалось очень небольшим. Как нам сейчас известно, типичная молекула жира имеет общую формулу C57H104O6.
И еще одна, третья, типичная составляющая пищи, не похожая ни на жиры, ни на углеводы, была обнаружена, в растворенном виде, в яичном белке. Такие вещества, как правило, образовывают вязкие растворы, подобные яичному белку, а при нагревании — сворачиваются и больше не восстанавливаются. Достаточно слабое нагревание приводит к необратимому изменению их свойств.
К концу XVIII века был открыт целый ряд таких «белкообразных» веществ, формировавших вязкие растворы и почти всегда сворачивавшихся при нагревании. Их выделяли из крови, из молока и даже из растительных продуктов.
Главным отличием этих веществ от углеводов и жиров является тот факт, что в их состав входят не только углерод, водород и кислород, но еще и азот, а иногда — сера и фосфор. Уже одного этого было достаточно, чтобы понять, что формула «белкообразных» веществ окажется сложнее, чем других составляющих пищевых продуктов, и в течение XIX века задача по составлению их общей формулы так и оставалась нерешенной.
В 1838 году голландский химик Герард-Иоганн Мёллер попытался разработать схему молекулы-составляющей, в состав которой были включены 88 атомов, и показать, что различные белкообразные вещества могут состоять из различного количества таких «молекул-кирпичиков», возможно, с добавками в виде небольших серо- и азотосодержащих молекул. Эта гипотеза с треском провалилась, но благодаря ей в мировой научной терминологии появился новый термин. По предложению Берцелиуса Мёллер назвал свою молекулу-составляющую «протеином», от греческого слова, означающего «важнее всего», поскольку ученому показалось, что именно этот «кирпичик» является важнейшей составляющей «белкообразных» веществ. В итоге термин стал использоваться для всей молекулы целиком, и теперь на международном научном языке весь класс подобных веществ называется «протеинами». В русской же терминологии их принято называть скромнее: в честь того природного вещества, в котором они впервые были обнаружены, — яичного белка. Так что слова «протеин» и «белок» являются в русском языке полными синонимами.
К 1827 году английский химик Уильям Прут (не путать с Прустом, французским химиком того же периода!) уже выдвинул предположение о том, что органическое вещество пищевых продуктов, а значит — и живых организмов, состоит в основном из веществ трех классов, которые мы сейчас называем углеводами, жирами и белками. Оказалось, что это действительно так. Конечно, не вся живая ткань на 100 процентов состоит только из них. В ней есть и неорганические составляющие (например, в костях), есть, разумеется, вода. Существуют также и органические составляющие, например нуклеокислоты, необходимые для всего живого и при этом не относящиеся ни к одной из трех перечисленных категорий.
Но все же углеводы, жиры и белки — это почти все органические составляющие живой ткани, и давайте теперь сосредоточимся именно на них.
Анализ органических веществ в первой половине XIX века привел к провозглашению принципиально нового различия между органическими и неорганическими веществами. Оказалось, что в состав всех веществ, выделяемых из живой ткани, входят водород и углерод, очень часто — кислород, часто — азот, иногда — сера и так далее. А вот в состав типичных неорганических веществ водород, кислород, азот, сера и многие другие атомы входят тоже очень часто, но углерод — крайне редко, за редкими исключениями вроде известняка.
Этим и объясняется горючесть органических веществ, ведь и углерод, и, разумеется, водород горючи сами по себе. Любое вещество, молекула которого включает в себя атомы водорода и углерода, тоже является горючим. Так что на этот фактор влияет банальный химический состав вещества, а не мистическая «жизненная сила».
Вторым важным отличием органических веществ от неорганических оказался размер молекул. Даже самые крупные неорганические молекулы — достаточно невелики, состоят из десятка-двух атомов. А вот у органических веществ, напротив, такое количество атомов характерно лишь для самых крошечных молекул. В молекуле глюкозы, для органических веществ достаточно маленькой, содержится 24 атома, а в средней молекуле жира — 170. Молекулы крахмала или белков состоят из тысяч и даже миллионов атомов.
И именно размер и хрупкость строения органических молекул, а не какие-то таинственные «свойства жизни», приводят к тому, что они легко распадаются при высоких температурах и теряют свои свойства даже при слабом нагревании.
Подтверждение тому было впервые получено в 50-х годах XIX века, когда химики научились синтезировать не просто вещества, идентичные выделяемым из живой ткани, но и множество других веществ с крупными молекулами, состоящими из углерода, водорода и других элементов, — вещества в природе не встречающиеся. Эти вещества, не являясь частью ни одной живой ткани на Земле, вели себя точно так же, как и природные, — легко воспламенялись, оказались капризно-нестабильными и во всех остальных отношениях — тоже «органическими».
Постепенно, ближе к концу XIX века, разграничение между органическими и неорганическими веществами перестало быть привязанным к фактору «живое — неживое» и стало основываться исключительно на химических свойствах. Поскольку в конце концов стало понятно, что возможность для создания огромных органических молекул кроется в неких особых свойствах углерода, то самым простым критерием отделения органической химии от неорганической стало наличие углерода в молекулах изучаемого вещества.
Кажется, что такое деление несправедливо, да так оно, собственно, и есть на самом деле, но не в том отношении, которое впервые приходит в голову. Способность углерода вступать в неограниченно большое количество соединений приводит к тому, что веществ, имеющих в своем составе углерод, обнаруживается гораздо больше, чем веществ, его лишенных, и с каждым годом этот разрыв все увеличивается.
Разобравшись, в первом приближении, с химическим составом пищи, теперь мы можем правильно истолковать все количественные измерения касательно дыхания.
К примеру, Лавуазье, чья величайшая заслуга перед химией состоит в первую очередь в том, что он всегда настаивал на проведении точных измерений, был первым, кто попытался установить точное количество вдыхаемого кислорода и выдыхаемого углекислого газа. Приборов, которые позволили бы ученому получить точные результаты, у него еще не было, но даже если бы Лавуазье их и получил, то сделать с ними все равно бы ничего не смог — разве что записать.
Сейчас же, после того как стал известен состав молекул веществ, обнаруживаемых в пище, можно сделать определенные выводы относительно исчезающего кислорода и появляющегося взамен него углекислого газа. Предположим, например, что глюкоза — это горючее и мы сжигаем его на огне. Тогда уравновешенное выражение для соединения глюкозы и кислорода будет выглядеть так:
С6Н12О6 + 6О2 → 6СО2 + 6Н2О.
Из этого выражения (которое невозможно было составить до того, как была установлена формула глюкозы) видно, что на каждый моль используемой глюкозы тратится шесть молей кислорода и производится шесть молей углекислого газа. На каждый моль одного, потребляемого, газа производится один моль другого газа. Поскольку один моль любого газа занимает один и тот же объем, то можно сказать, что на каждый литр одного газа получается один литр другого. В данном случае — на каждый литр потребляемого кислорода производится один литр углекислого газа.
Таким образом, отношение производимого углекислого газа к потребляемому кислороду — 1: 1, то есть 1. Лавуазье и прочие ученые интересовались этим отношением именно в связи с дыханием, так что эту величину назвали «коэффициентом дыхания», и мы говорим, что коэффициент дыхания глюкозы (да и вообще углеводов в целом) — 1.
С жирами ситуация иная. Общая формула типичной жировой молекулы — С57Н104О6, и уравновешенное выражение для соединения ее с кислородом выглядит так:
С57Н104О6 + 80О2 → 57СO2 + 52H2O.
То есть на 80 молей потребляемого кислорода производится 57 молей углекислого газа. Значит, коэффициент дыхания жиров — 57/80, или 0,713. Коэффициент дыхания белков больше, чем у жиров, но меньше, чем у углеводов. Округленные цифры выглядят так:
Коэффициент дыхания углеводов = 1
К. д. белков = 0,8
К. д. жиров = 0,7
Каким же образом мы можем теперь применить эти чисто химические соображения к явлениям живой природы? Ответ на этот вопрос был дан в 1849 году, когда два французских химика, Анри Виктор Реньо и Жюль Рейзе, разработали камеру, куда можно было помещать животных и запускать кислород в строго определенном количестве. Углекислоту, выдыхаемую этими животными, тоже можно было собирать, абсорбировать с помощью определенных химических веществ и взвешивать. Таким образом, ученые смогли измерить и объем вдыхаемого животными кислорода, и объем выдыхаемого углекислого газа. Иными словами, у них получался общий коэффициент дыхания животного, и ученые измерили его для самых разных живых существ — от червяков до собак.
У Реньо и Рейзе получилось, что коэффициент дыхания живых организмов лежит между 0,7 и 1. Более того, в этих пределах он изменялся в зависимости от предоставляемой животному пищи. Если диета животного была по преимуществу углеводной, то и коэффициент дыхания приближался к единице; при преимущественно жировой диете он опускался до 0,7.
Через пару десятков лет немецкий химик Макс фон Петтенкофер со своим товарищем физиологом Карлом фон Войтом создали аналогичное устройство, куда мог поместиться и человек. И коэффициент дыхания человека оказался таким же, как у животных, — от 0,7 до 1, в зависимости от диеты. При нормальном смешанном питании или при голодании, когда организм подчищает внутренние запасы пищи, его значение составляло примерно 0,8.
Итак, к середине столетия стало ясно, что ход реакции горения органических веществ принципиально одинаков, независимо от того, проходит она в живой ткани или вне ее. По крайней мере, соотношение потребляемого кислорода к производимому углекислому газу оказалось в точности соответствующим расчетам, основанным на изучении химических реакций неорганических веществ. Пришлось признать, что и живой организм подчиняется закону сохранения материи. Он не создает углерод из ничего и не обходится крупицами.
Но ведь еще остался закон сохранения энергии, — в то время, когда Реньо и Рейзе проводили свои эксперименты, этот закон еще только-только приобретал всеобщее признание. Окажется ли он таким же справедливым для живой материи, как и для неживой?
Глава 14. С МАЛОЙ СКОРОСТЬЮ
Первым шагом при рассмотрении энергетического баланса живых существ должно стать определение количества химической энергии, высвобождаемой при сжигании пищи в отсутствие какой-либо жизни. Надо сжечь в бомбовом калориметре различные пищевые составляющие и замерить теплоту реакции. Надо сказать, что в этом случае пользоваться значениями молярной теплоты реакции будет неудобно, поскольку молекулы некоторых из наиболее важных составляющих пищи настолько велики, что молярная теплота реакции будет приобретать в их случае астрономические значения.
Если рассматривать только самые простые питательные вещества, то можно сойтись на следующем выражении (см. главу 8):
С6Н12О6 + 6О2 → 6СО2 + 6Н2О
глюкоза
ΔН = -738 ккал.
С57Н104О6 + 80О2 → 57СO2 + 52H2O
жир
ΔН = -8044 ккал.
Как видите, речь идет уже о цифрах порядка тысяч килокалорий. А когда речь заходит о гигантских молекулах крахмала и белков, то с ними еще хуже. Один моль крахмала или белка запросто может иметь массу в несколько сотен фунтов, и молярное тепло реакции горения такой массы, естественно, составит миллионы или даже миллиарды килокалорий.
Но теплоту реакции вполне удобно измерять и на основании массы. При сгорании углеводов в бомбовом калориметре выделяется теплота реакции в 4,1 килокалории на грамм (ккал/г). Это достаточно небольшая цифра, если сравнить ее с показателями других горючих веществ, приведенными мной в главе 8. Чтобы освежить данные, я привожу в таблице 4 теплоту реакции из расчета на грамм для некоторых веществ:
Таблица 4.
ТЕПЛОТА РЕАКЦИИ ГОРЕНИЯ НА ГРАММ ВЕЩЕСТВА
Вещество … Формула … Теплота на грамм
Водород … Н2 … 34,2 ккал.
Метан … СН4 … 13,2 ккал.
Уголь … С … 7,8 ккал.
Этиловый спирт … С2Н6О … 7,1 ккал.
Глюкоза … С6Н12О6 … 4,1 ккал.
Как я уже объяснял в главе 8, водород при сжигании выделяет гораздо больше тепла на грамм, чем углерод; соответственно углеводород, например метан, будет выделять некое промежуточное количество теплоты. Тот факт, что спирт выделяет еще меньше теплоты на грамм, чем даже углерод, хотя в составе его молекулы присутствует и водород, я объяснял присутствием в ней также и атома кислорода. Молекула спирта является уже «частично сгоревшей», и на выделение тепла при сгорании в ней остается меньше молекул. По такой же логике и глюкоза (которую можно принять за типичный углевод), формула которой С6Н12О6, является изначально еще более «сгоревшей», чем спирт. Атомы кислорода составляют четвертую часть всех атомов молекулы глюкозы, а в спирте их доля — всего лишь 1/9. Выходит, нечему удивляться, что при сгорании грамма глюкозы выделяется меньше тепла, чем при сгорании грамма спирта.
А вот с жирами — другое дело. Молекула жира, где кислород составляет всего 1/28 от общего числа атомов, является в гораздо меньшей степени «сгоревшей», чем молекула углевода или даже спирта. Поэтому логично ожидать, что теплота реакции в расчете на грамм у жира будет больше, чем у спирта, но меньше, чем у метана, в молекуле которого кислорода нет вообще. Экспериментальные данные показывают, что при сжигании жиров выделяется 9,45 килокалории на грамм. Белок, молекула которого содержит меньше кислорода, чем молекула углевода, но больше, чем молекула жира, имеет показатели промежуточные между показателями этих двух веществ, и при сжигании белка в калориметре фиксируется выделение 5,65 килокалории на грамм.
Это все в том случае, если из еды разводить костер. А как насчет того процесса, в котором еда используется не в пример чаще, — имеется в виду поглощение ее живым организмом? Измерить, сколько тепла выделяет организм, гораздо сложнее, чем сколько выделяет костер, но тоже возможно. Для начала нужен достаточно большой калориметр, чтобы в него поместился живой организм. Организм ест и выделяет отходы; вдыхает кислород и выдыхает углекислый газ. Если точно измерить все, что организм имеет на входе и выходе в процессах питания и дыхания, то в идеальном случае можно высчитать, сколько в нем в данный момент находится питательных веществ и кислорода. Дальше можно рассчитать, сколько тепла выделили бы эти вещества в этом объеме, будучи сожженными в калориметре. Если измерить тепло, вырабатываемое организмом на самом деле, то логически возможен один из трех вариантов — либо оно окажется равным теплу, которое было бы из того же топлива выработано при сжигании, либо большим, либо меньшим. Каким именно окажется это отношение — принципиально важно для решения вопроса о том, распространяются ли законы термодинамики на живые организмы.
Впервые такой эксперимент с достоверной точностью провел немецкий физик Макс Рубнер в 80-х годах XIX века. Исполнение Рубнера было на редкость методичным. Сначала он подверг тщательному анализу экскременты подопытного животного. Несмотря на то что корм состоял сплошь из легкорасщепляемых жиров и углеводов, часть этих питательных веществ все равно прошла весь пищеварительный тракт, так и оставшись непоглощенной, так что для объективности картины этот процент следовало вычеркнуть из общего количества «сжигаемой» пищи. Среди углеводов процент не подвергнувшихся перевариванию оказался ничтожно малым, но среди жиров — более существенным. С учетом неполноты переработки, энергетическое содержание углеводов и жиров в пище пришлось уменьшить до 4 и 9 килокалорий соответственно.
С белками получилось еще сложнее. Если итоговыми продуктами сгорания углеводов и жиров являются углекислота и вода, будь то сгорание в пламени или в организме, то в отношении белков все не так просто. В калориметре атомы углерода и водорода из молекулы белка превращаются все в те же углекислоту и воду, но нельзя ведь забывать и про атомы азота! Они высвобождаются в калориметре в виде окислов азота. На самом деле в белках еще встречаются атомы серы и других элементов, но их процентное содержание настолько мало, что в данном случае ими смело можно пренебречь.
Однако в организме млекопитающих азотистая составляющая расщепляемых белковых молекул переходит не в окислы азота, а в мочевину (CH4ON2) — растворимое твердое вещество, выводимое из организма с мочой. При сжигании молекул мочевины тоже выделяется некоторое количество энергии, так что, если в живом организме она остается несожженной, значит, энергию ее сжигания тоже следует вычесть из общей энергии сжигания пищи. А в этом случае оказывается, что энергия, получаемая тканью млекопитающих из белка, примерно равна энергии, получаемой из углеводов, — 4 килокалории на грамм.
Факт производства организмом мочевины является полезным для исследователя — сейчас объясню почему. Общее количество пищи, используемой и «сжигаемой» живой тканью за заданный промежуток времени, определяется путем замера количества производимого за это время углекислого газа. Однако количество высвобождаемой при этом энергии зависит от того, какая именно пища поглощалась. Некоторое количество углекислого газа, выделенное при сжигании жира, соответствует большему количеству энергии, чем то же самое количество углекислого газа, выделенное при сжигании углеводов.
Поэтому Рубнер счел необходимым измерять не только количество выделяемого углекислого газа, но и количество потребляемого кислорода. Так он получил коэффициент дыхания и смог установить соотношение потребления организмом углеводов и жиров. Чем выше коэффициент дыхания, тем больше в процентном соотношении организм усваивает углеводов и тем меньше энергии производит в расчете на литр вдыхаемого кислорода. Чем ниже коэффициент дыхания, тем больше организм усваивает жиров и тем больше энергии производит на литр потребляемого кислорода.
Но это верно только в том случае, если углеводы и жиры — это единственные вещества, потребляемые организмом, то есть если белок не потребляется вообще. А это не так — белок потребляется всегда. Средний объем потребления белка — около 10 процентов от суммарного объема жиров и углеводов. Но то средний, а для того, чтобы подсчитать какие-то более-менее правдоподобные значения для коэффициента дыхания, а значит, и поступающей в распоряжение организма энергии, надо знать точное количество потребляемого белка.
Допустим, что коэффициент дыхания — 0,8. Если потребляемая при этом пища состоит исключительно из жиров и углеводов, то соотношение потребляемых веществ — 2 части жиров на 1 часть углеводов, и выход энергии, на основе расчетов, составленных с помощью бомбового калориметра, будет равняться примерно 7 ккал/г.
Теперь предположим, что на самом деле смесь потребляемых питательных веществ содержит 2 части жиров на 1 часть углеводов и 1 часть протеинов. Коэффициент дыхания при этом по-прежнему будет равен 0,8 (поскольку именно таков коэффициент дыхания чистого белка, то он не будет изменяться, сколько белка ни подмешивай к смеси жиров и углеводов 2:1). Однако производство энергии на основе этой новой смеси упадет по сравнению с предыдущим случаем примерно до 6 ккал/г, поскольку белок — энергетически бедный материал по сравнению со смесью жиров и углеводов.
Однако мочевина производится только из белка. По данным анализа мочи (еще одно изобретение Рубнера) можно установить и количество потребляемого протеина. Кормление животных строго взвешенными порциями пищи, анализ мочи и кала, измерение количества потребляемого ими кислорода и производимого углекислого газа — все это позволяло Рубнеру совершенно четко знать, сколько и каких питательных веществ употребило то или иное животное за определенный отрезок времени.
А измерение количества вырабатываемого животными тепла привело его (как и исследователей позднейшего времени) к вполне ожидаемому выводу: в живом организме вырабатывается ровно столько же энергии, сколько ее высвободилось бы в бомбовом калориметре, если бы всю эту пищу просто сожгли.
К концу века уже всем стало ясно, что никакого волшебного источника энергии в живых существах нет; никто не может извлечь из системы больше энергии, чем в ней заключено. Короче говоря, первый закон термодинамики оказался так же справедлив для ящерицы, как и для камня.
Конечно, сам по себе закон, согласно которому количество калорий, поглощаемых живым организмом с пищей, уравновешивается количеством расходуемых им калорий, еще не значит, что и то и другое не может в значительной степени колебаться. Были созданы калориметры, куда мог помещаться человек, и замерялись данные при разных его состояниях и занятиях — люди в них сидели, стояли, печатали-Разрабатывались и методики косвенного изменения расхода энергии во время бега, лазания, катания на велосипеде, езды верхом и так далее.
Неудивительно, что чем более активной деятельности предается человек, тем сильнее увеличивается производство его организмом энергии, а значит, тем больше жиров ему требуется. Если получать их в достаточном количестве с пищей не удается, то организм начинает расходовать внутренние резервы тела, что приводит к потере веса.
На самом деле все вопросы потери или набора веса косвенно завязаны на законе сохранения энергии. Для того чтобы сбросить вес, необходимо сократить потребление калорий до уровня ниже их расхода — либо начать меньше есть (сесть на диету), либо начать больше их тратить (заняться спортом), а еще лучше — и то и другое. А для того чтобы набрать вес, надо повести себя прямо противоположным образом.
Для уровня расхода энергии существует как верхняя, так и нижняя планка. Прыгая через три ступеньки вверх, или активно орудуя топором в лесу, или с азартом играя в теннис, человек может тратить энергию со скоростью 10 килокалорий в минуту. Все мы знаем, что долго это продолжаться не может.
С другой же стороны, полностью подавив любую сознательную деятельность, можно урезать расход энергии в пятнадцать раз, не больше. Не важно, насколько удобно мы уляжемся, расслабившись, все равно определенное количество энергии необходимо тратить на работу сердца, легких, печени, почек и т. п. Так же и двигатель автомобиля должен работать в некоем минимальном темпе, чтобы не заглохнуть. Разница лишь в том, что заглохший мотор можно запустить заново, а если «заглохнет» и остановится жизнедеятельность человеческого организма, то ее запустить уже ничто будет не в силах.
Меньше всего энергии расходуется человеком, разумеется, во сне, но замер расхода энергии спящего человека — вообще говоря, дело неблагодарное. Хотя бы потому, что и во сне активность человека может различаться очень сильно, он может спать крайне беспокойно, а объяснять спящему, что он должен спать крепко, — по понятным причинам бесполезно.
Следующий после сна способ сэкономить энергию — это бодрствовать, но лежать при этом неподвижно. Расход энергии при самом пассивном поведении в состоянии бодрствования процентов на 10 выше, чем при идеальном сне, но для эксперимента выбирать приходится все же бодрствование.
Совокупность химических процессов, происходящих в живом организме и, в частности, приводящих к производству в нем энергии, называют «метаболизмом», или «обменом веществ». Термин «метаболизм» ввел в обиход немецкий натуралист Теодор Шванн, произведя его от греческого слова, означающего буквально «перебросить на другое место», а в более широком значении — «изменить». Минимальному расходу энергии (ровно достаточному, чтобы не прерывать процесс жизнедеятельности) соответствует минимальная, или основная, интенсивность обмена веществ. Соответственно эту интенсивность называют «интенсивностью основного объема».
Условия для определения интенсивности основного объема таковы: прежде всего, обследуемый должен находиться в лежачем положении. Даже сидение требует постоянного расхода дополнительной энергии, поскольку большие мышцы туловища постоянно скоординированно сокращаются, поддерживая равновесие. Обследуемый должен быть голодным, после ближайшего к моменту измерения приема пищи должно пройти не менее двенадцати часов, чтобы гарантировать, что энергия не расходуется на пищеварение. В комнате должна быть комфортная температура, чтобы не повышать уровня энергии, расходуемой на выработку тепла (в случае, если в комнате холодно) или потение (если в комнате жарко). Обследуемый должен быть спокоен внутренне, во избежание энергозатрат на сокращения мышц, которые непроизвольно сопровождают любую сильную озабоченность. Самый лучший способ достичь этого состояния — дать обследуемому спокойно полежать полчасика в тишине.
Интенсивность основного обмена точнее всего определяется по количеству потребляемого кислорода, производимого углекислого газа и содержанию мочевины в моче. В упрощенном варианте мочу можно проигнорировать, пренебрегая, таким образом, белковой составляющей как незначительной. Упрощая еще дальше, можно сосредоточиться вообще на одном лишь потреблении кислорода, приняв коэффициент дыхания за средний — приблизительно 0,82 для голодного человека.
В среднем интенсивность основного объема человека составляет около 43 килокалорий в час, то есть — около 1000 килокалорий в день. Это значение очень сильно зависит от веса обследуемого, поскольку чем больше общая масса тела, тем больше энергии приходится тратить просто на поддержание в нем жизни. Так, если у человека весом в 115 килограммов интенсивность основного объема в среднем 68 килокалорий в час, то у 70-килограммового — вышеупомянутые 43, а у 30-килограммового ребенка — всего 20.
Чтобы избежать такого значительного разброса, интенсивность основного обмена следует пересчитывать на килограмм массы тела, и тогда получится, что 115-килограммовый человек тратит около 0,59 ккал/кг/час, а 70-килограммовый — около 0,61. У 30-килограммового ребенка этот показатель окажется несколько выше, около 0,67 ккал/кг/час, но это и неудивительно — ведь ребенок растет, а построение новых тканей организма — это весьма энергоемкий процесс.
Кроме того, в 1883 году Рубнер установил, что интенсивность основного обмена можно представить с еще меньшими вариациями, если сделать поправку не на вес тела, а на площадь его поверхности.
Установление интенсивности основного обмена у других млекопитающих тоже обошлось без сюрпризов. У более крупных, чем человек, животных и интенсивность основного обмена оказалась выше, у более мелких — ниже. В пересчете на массу тела этот показатель уменьшается по мере увеличения массы животного, так же как и у людей.
К примеру, интенсивность основного обмена у человека — 1000 килокалорий в день, у мыши — только 3, а у слона — 50 000 килокалорий в день. Однако один килограмм мышиного организма потребляет в день 158 килокалорий, человеческого — 15, а слоновьего — всего 10.
Памятуя о том, что крупные животные, как правило, живут дольше, чем мелкие, нельзя не задаться вопросом: не связано ли это с интенсивностью обмена веществ? Не в том ли дело, что мелкие зверьки, так сказать, живут быстрее и быстрее изнашиваются?
Недостаток этой теории в том, что животный мир предоставляет нам слишком много исключений, слишком много случаев, когда более мелкие животные живут дольше, чем более крупные. Взять хотя бы самого человека.
Человек живет дольше, чем любая крупная обезьяна, даже горилла, гораздо более крупная, чем человек. Человек живет дольше, чем даже огромный слон. Не существует достоверных сведений о том, чтобы какой-нибудь слон прожил хотя бы до семидесяти лет, как бы хорошо о нем ни заботились; в то же время мы знаем, что в цивилизованных странах половина населения доживает до этого возраста, а многие — и до столетнего юбилея. Даже киты, чью продолжительность жизни оценить сложно, и то вряд ли живут столько же, сколько и люди, поскольку даже самые крупные киты обретают способность к деторождению в возрасте трех лет — а ведь известно, что продолжительность жизни коррелирует с возрастом биологического взросления. Сравните три года кита с тринадцатью годами человека.
Единственные животные, о которых известно, что они живут дольше людей, — это гигантские черепахи, чей возраст может достигать двухсот лет. Но черепахи известны неторопливостью своей жизни. А среди быстро живущих существ никто и близко не стоит рядом с человеком.
Интенсивность основного обмена не представляла бы никакого особого интереса, если бы не было обнаружено, что при некоторых обстоятельствах она может очень сильно изменяться. Перед тем как перейти к подробностям, я должен сначала остановиться на термине «железа».
Железы еще могут называть гландами, от латинского слова «glans», что означает «желудь» — изначально им называли любые узловатые образования живой ткани в организме, например лимфатические узлы. (Это небольшие вытянутые образования, расположенные на некоторых из сосудов, по которым течет лимфа — жидкость, поступающая из крошечных кровеносных сосудов и омывающая клетки.) «Желудь» — это естественная метафора для чего-нибудь маленького; на людей всегда производило сильное впечатление сравнение крошечного желудя с огромным дубом.
Впоследствии и другие, более крупные органы похожей формы, например поджелудочную железу, стали называть этим же термином. В 1642 году немецкий анатом Иоганн Георг Вирсунг обнаружил в организме проток, ведущий от поджелудочной железы в верхнюю часть тонкого кишечника. Так выяснилось, что поджелудочная железа выделяет что-то в тонкий кишечник.
Это открытие произвело на общественность столь сильное впечатление, что железами стали называть любой орган, выделяющий какие-либо соки, даже крупные, например печень, производящую желчь. А ткани, ничего не выделяющие, железами именовать перестали — в частности, те самые лимфатические узлы, с которых все началось.
Первыми как железы были классифицированы те органы, которые, как печень или поджелудочная железа, имеют крупные, четко различимые протоки, по которым выводятся производимые ими вещества. В этом ряду можно назвать потовые железы, молочные железы и ряд мелких желез, находящихся во внутренней оболочке желудка и кишечника.
Однако в начале XIX века выяснилось, что существуют небольшие органы, которые, производя жидкости, выбрасывают их напрямую в кровь безо всяких протоков. После некоторых споров (о том, распространять ли на эти органы термин «железы», возобладала либеральная точка зрения. Немецкий анатом Иоганн Фридрих Меккель разделил все железы на две категории — имеющие проток и не имеющие его. Это деление сохраняется по сей день; железы, имеющие проток, называются экзокринными, а выводящие производимые ими вещества напрямую в кровоток — эндокринными.
Рис. 21. Щитовидная железа
Одна из эндокринных желез окружает трахею сразу же под гортанью (рис. 21). Сама гортань состоит из хряща и впереди у нее вилкообразная выемка, которую можно прощупать пальцем, похожая по форме на выемки в щитах греческих солдат эпохи Гомера, через которые солдаты могли видеть врага, не высовывая голову из-за укрытия. Ввиду такого подобия и сам хрящ назвали щитовидным, в 1646 году английский врач Томас Уортон перенес это название с хряща на расположенный рядом маленький мясистый орган, известный нам ныне как «щитовидная железа».
Иногда щитовидная железа распухает, образуя так называемый «зоб». В древности и в Средневековье на это смотрели достаточно благодушно, и в тех частях Европы, где такое встречалось достаточно часто, небольшое распухание шеи считалось даже неким дополнением к женской красоте. Однако к 1800 году врачи подметили, что зачастую наличию зоба сопутствуют симптомы заболевания, из которых самым заметным, если не самым важным, является выпучивание глаз.
Однако уменьшение щитовидной железы оказалось еще опаснее. В некоторых горных местностях Европы часто рождались слабоумные карлики, которых прозвали «кретинами» (это диалектный вариант произношения французского слова, означающего «христианин», — логика происхождения слова сродни логике происхождения русского термина «убогий»). Оказалось, что это явление непосредственно связано с функцией щитовидной железы. Более того, к концу XIX века было обнаружено, что удаление щитовидной железы у животных приводило к проявлению у них симптомов кретинизма, от которых удавалось избавиться только путем инъекции растолченной щитовидной железы.
Что именно в щитовидной железе оказывает такое мощное влияние на организм, оставалось полнейшей загадкой вплоть до 1896 года, когда немецкий химик Эуген Бауманн выяснил, что в щитовидной железе содержится редкий элемент — йод. Йода там обнаружилось очень мало, так что открытию Бауманна особого значения не придали. Ни химики, ни врачи того времени не понимали, что некоторые элементы могут иметь решающее значение для жизнедеятельности организма, присутствуя в нем в минимальных количествах (так называемые «рассеянные элементы», или «следовые элементы»).
Тем не менее уже в 1905 году американский врач Дэвид Марин, после обучения на Востоке поселившийся на Среднем Западе, подметил, что зоб — крайне распространенное явление как у людей, так и у животных в Кливленде, а на Востоке случаев зоба встречалось мало. Марину пришло в голову предположение, что это как-то связано с низким содержанием в местной почве йода, в результате чего его содержание в воде и в растительной пище, поедаемой как животными, так и людьми, под Кливлендом оказывается гораздо ниже, чем на Восточном побережье, куда ветер доносит богатую йодом водную пыль из океана. Если йод необходим щитовидной железе для нормальной работы, то можно предположить, что ее увеличение — это попытка компенсации организмом нехватки йода.
Марин попробовал посадить животных на диету, обедненную йодом, и действительно у них стал образовываться зоб; после обогащения диеты йодом зоб опять исчезал.
Тогда ученый развернул кампанию по искусственному обогащению йодом питьевой воды в городском водопроводе и после долгой борьбы (вызванной сопротивлением, близким к тому, какое сейчас встречают призывы к аналогичному обогащению питьевой воды фтором) добился-таки своего. Добавление йода в питьевую воду и соль (сейчас йодированная соль продается в каждом магазине) привело к тому, что проблемы образования зоба в цивилизованных странах сейчас практически сняты. Практически, но не полностью, ибо еще даже полвека спустя после открытия йодотерапии зоба все еще около 200 000 000 человек по всему миру еще страдают этим заболеванием. 30 000 000 из них живут в Латинской Америке, и даже в определенных местностях в Соединенных Штатах таких больных очень много — особенно в штатах Вашингтон и Орегон.
В то же самое время, когда с помощью химии была обнаружена важность йода для функционирования щитовидной железы, клинические исследования привели к открытию не менее важного фактора.
В 1895 году немецкий врач А. Магнус-Леви провел ряд экспериментов по установлению интенсивности основного обмена у людей, страдающих различными заболеваниями. У большинства обследуемых значения интенсивности основного обмена оказывались такими же, как и у прочих, но вот у больных с нарушениями функционирования щитовидной железы дело обстояло иначе. Интенсивность обмена веществ у больных с повышенной активностью щитовидной железы была выше, а у людей с пониженной — ниже, чем у здоровых.
Соответственно возникло предположение, что именно щитовидная железа и управляет «минимальной скоростью работы» человеческого организма, являясь чем-то вроде энергетического термостата. (Точный механизм этого контроля так и неизвестен до сих пор.) Теперь интенсивность основного обмена приобрела четкое практическое значение. Из любопытного физиологического курьеза она превратилась в инструмент диагностики расстройств щитовидной железы.
Повышение активности щитовидной железы на 10 процентов выше нормы приводит к тому, что человек становится гиперактивным, дерганым, нервным, то что называется «весь на эмоциях». Ее понижение — к тому, что больной теряет интерес к миру вообще. С помощью экстракта щитовидной железы и ингибиторов, подавляющих ее активность, стало возможным регулировать активность этого органа произвольным образом.
Однако после полувекового использования в качестве повсеместного диагностического инструмента замер интенсивности основного обмена постепенно исчезает из медицинской практики.
Предпосылки к тому появились еще в 1914 году, когда американский биохимик Эдвард Кельвин Кендалл выделил из экстракта щитовидной железы сравнительно небольшую молекулу, которой дал название «тироксин». Оказалось, что это и есть действующее вещество экстракта. Действующие вещества эндокринных желез английский врач Эрнест Генри Старлинг назвал «гормонами», от греческого слова, означающего «возбуждать», так что можно сказать, что тироксин — это гормон щитовидной железы.
Молекула тироксина необычна тем, что в ее состав входят четыре атома йода. В 1952 году английские биохимики Гросс и Питт-Риверс открыли еще одно вещество, производимое щитовидной железой, «трийодтироксин», отличие которого от тироксина заключается в том, что в состав его молекулы входят не четыре, а три атома йода. Действие его оказывалось схожим с действием тироксина. Похоже, что характерные свойства как тироксину, так и трийодтироксину придает именно йод, больше в организме практически нигде не встречающийся.
Щитовидная железа выбрасывает гормоны прямо в кровь. Там они соединяются с белковыми молекулами, которые в норме находятся в плазме (жидкой составляющей крови). Если выделить соответствующую белковую фракцию, то можно проанализировать ее на содержание йода. Таким образом можно установить, какой объем гормона вырабатывается щитовидной железой (поскольку ее гормон — единственный источник йода в организме), а это, в свою очередь, будет свидетельствовать об активности щитовидной железы, из которой можно высчитать и интенсивность основного обмена. При этом не нужно голодать, неподвижно лежать целый час и дышать в шланг, и нет необходимости в дорогостоящих лабораторных комнатах — достаточно просто сдать небольшое количество крови.
Проблема оказалась только в том, чтобы на самом деле суметь проанализировать содержание йода в крови — ведь речь шла о точном установлении цифр порядка 1/20 000 000 грамма. Это стало возможным только в середине 50-х годов XX века.
Для точного измерения столь малых величин пришлось прибегнуть к явлению катализа. После того как йод, связанный с белком, отделяют и собирают в растворе, напрямую измерить содержание растворенного вещества крайне маловероятно. Поэтому в раствор добавляются химические вещества, о которых известно, что под каталитическим воздействием йода они вступают в реакцию. Вещества эти добавляются в строго измеренном количестве, а скорость их реакции очень сильно зависит даже от малейших колебаний концентрации йода, так что именно по ней содержание йода и измеряется.
Следить за ходом реакции очень удобно, потому что она сопровождается изменением цвета раствора, которое можно точно измерить с помощью соответствующих приборов. Чем сильнее меняется цвет, тем интенсивнее проходит реакция, тем больше концентрация йода, тем выше уровень активности щитовидной железы, тем больше значение интенсивности основного объема. Очень удобно!
Глава 15. КАТАЛИЗАТОРЫ ЖИЗНИ
Удобно также рассматривать дыхание и горение как родственные процессы, а человеческий организм — как аналог костра, раздуваемого кислородом и производящего углекислый газ. Но на самом деле между огнем и живым организмом существуют и значительные различия.
Во-первых, огонь — механизм однонаправленный: он превращает дерево или иное топливо в углекислый газ и воду, оставляя лишь пепел, и синтезировать новое топливо не способен. А живой организм, извлекая энергию из распада углеводов, жиров и белков в ходе реакций, схожих с горением, в то же время умеет и создавать запасы новых жиров и углеводов, а также — строить новые белки взамен старых (этот процесс я опишу позже). В растущем организме все эти сложные молекулы строятся даже быстрее, чем поглощаются, ведь в организме десятилетнего ребенка перечисленных веществ содержится больше, чем в организме семилетнего, хотя вроде бы они активно расходовались с того момента на протяжении трех лет.
При создании сложных молекулярных составляющих ткани уровень свободной энергии увеличивается (как мы вскоре увидим), и энтропия соответственно уменьшается. То есть происходит процесс обратный тому, какой в терминологии термодинамики называется спонтанным.
Еще в конце главы 5 я выдвинул предположение о том, что, возможно, принципиальное различие между живой и неживой материей заключается в возможности первой вызывать локальное уменьшение энтропии. Тогда я упоминал только об энтропии механической энергии («совершение усилий») и приводил в качестве примера способность живых существ двигаться против силы тяжести. Теперь мы видим также, что живая материя может вызывать уменьшение энтропии и относительно энергии химической, обладая способностью сформировывать крупные сложные молекулы из более простых, хотя все спонтанные реакции протекают, наоборот, от большого к малому.
Связь между жизнью и уменьшением энтропии становится еще нагляднее, но до четкого определения нам пока еще далеко. В главе 5 я уже указывал, что солнечное тепло испаряет океанскую воду, а силы, действующие в земной коре, воздвигают горы, и ни в первом, ни во втором случае явно не задействовано никаких структур, которые можно было бы отнести к «живым».
Помимо этих «безжизненных» примеров из области механической энергии можно найти аналогичные и из области энергии химической. Облучение растворов простых молекул ультрафиолетом приведет к образованию более сложных молекул, и множество фактов свидетельствует о том, что в первые миллионы лет существования Земли именно так и происходило в массовом порядке — жизни еще не было в принципе, а Солнце яростно облучало ультрафиолетом Мировой океан. На самом деле именно этим «безжизненным» процессам уменьшения энтропии применительно к химической энергии, скорее всего, и обязана своим возникновением сама жизнь.
Так искомый принцип различения снова ускользает от нас.
Однако не стоит обескураживаться. Ведь между огнем и живым существом есть и еще одно очевидное различие.
Огонь — очень горячий, а человек — нет. Да, человек поддерживает некоторое тепло в своем организме, но эти 37 °С ни в какое сравнение не идут с температурами пламени — 700 °С и выше. А в организмах холоднокровных животных процесс поглощения кислорода и производства углекислоты может проходить и при температурах около 0 °С.
Соответственно тут же вспоминаются условия, при которых реакции подобные горению могут запускаться при низких температурах. Вряд ли горючее, используемое организмом, воспламеняется легче, чем обычное топливо костра. Если взять те же самые пищевые продукты и просто положить их на стол при комнатной температуре, они не загорятся никогда и процесс соединения с кислородом будет происходить в них не быстрее, чем в древесине или угле. А вот в организме реакции соединения почему-то происходят достаточно легко и при температурах, которые никогда не поднимаются выше просто теплых.
Ученым XIX века оставалось только сделать единственно логичный вывод о существовании в живой ткани неких катализаторов, работающих по схеме, которую я описал в главе 12. На самом деле именно те катализаторы, которые вызывают горение в лабораторных условиях — палладий и платина, — в живой ткани не встречаются, но это может означать лишь то, что существуют и другие. И опять можно было задаться все тем же вопросом: являются ли эти биологические катализаторы таковыми в полном смысле слова и в соответствии с законами термодинамики, действуя так же слепо, как и порошок платины, или все же в данном случае нам удастся обнаружить некую «жизненную силу», стоящую над термодинамикой.
В среде химиков XIX века этот вопрос вызвал ожесточенные споры, и только благодаря ряду реакций, известных человечеству с доисторических времен, опыт перевесил аргументы сторонников существования «жизненной силы».
Во фруктовых соках, как и в замоченном зерне, как правило, со временем происходят некоторые изменения. Не всегда они оказываются желательными, но в некоторых случаях — и это обнаружили еще доисторические люди — человек, выпивший такую «подпортившуюся» жидкость, чувствовал приятное тепло и легкость. Со временем люди выяснили, что можно не просто выставлять сок и надеяться, что получится нужный результат, а добавлять в емкость с соком небольшое количество уже достигшей нужного состояния жидкости из предыдущей порции, и тогда изменения, во-первых, идут в нужном направлении, а во-вторых — гораздо быстрее.
Так же и в тесте, из которого пекут хлеб, иногда происходят реакции, приводящие к формированию углекислого газа. Пузырьки газа образуются по всей массе теста, и получающиеся в результате лепешки разительно отличаются от обычных — плотных и тяжелых. И в этом случае тоже перенос кусочка теста с пузырьками в емкость с обычным тестом приводит к распространению реакции по всему объему теста.
Все эти изменения вызываются такой вещью, как дрожжи. Образование пузырьков газа как в вине, так и в тесте очень похоже на «медленное кипение» вещества. В связи с этим в современной терминологии процесс, при котором поднимается тесто, фруктовый сок превращается в вино, а закваска зерновых — в пиво, называется «ферментацией», от латинского слова, означающего «кипеть».
С точки зрения химика XIX века действие дрожжей очень похоже на действие катализаторов. Кроме того, они явно отличаются от обычных лабораторных катализаторов своей органической природой и тем, что катализируют реакции близкие к происходящим в живой ткани. Логично было предположить, что если в живой ткани и предполагается обнаружить какие-то катализаторы, то они должны быть сродни скорее дрожжам, чем платине.
Но дрожжи оказались не просто катализатором — они сами по себе до странного походили на живое существо. Они не только оставались нерасходуемыми в ходе реакции, как обычные катализаторы, — они ухитрялись при этом еще и увеличиваться в объеме! В Первом послании к коринфянам о том же говорит и апостол Павел: «Малая закваска квасит все тесто».
Так и есть — а когда все тесто заквашено, то достаточно отщипнуть от него маленький кусок, чтобы с его помощью заквасить другое тесто, и так далее.
Но, несмотря на все свидетельства, принять дрожжи действительно за живое существо оказалось очень сложно. Широкое население запросто верило в существование множества невидимых глазу живых существ (ангелов, демонов, эльфов и прочих), но вот представление о том, что вполне обычные, не сказочные существа могут оказаться невидимыми только из-за своих крайне малых размеров, почему-то оказалось для общества гораздо менее приемлемым.
Но вот в XVII веке был изобретен микроскоп, и в 1675 году величайший из первых микроскопистов, голландский купец Антони ван Левенгук, сумел разглядеть в него «микроскопических животных». Это были одноклеточные существа, ныне именуемые «простейшими», длиной 0,005 см и менее, но не менее живые, чем мы с вами. Открытие Левенгука взбудоражило все научное сообщество до такой степени, что торговца-иностранца даже приняли в Лондонское королевское общество — элиту ученых джентльменов.
В 1680 году Левенгук, с неизмеримым терпением и любовью изучавший под микроскопом все вокруг, обратил свой взор и на дрожжи и выяснил, что они состоят из крошечных шариков. Факт существования микроорганизмов в то время просто заставлял искать жизнь где угодно, но дрожжевые шарики уж совсем никак не были похожи на активно плавающих простейших.
Рис. 22. Этапы размножения дрожжевых клеток почкованием
Однако в 1837 году французский физик Шарль Каньяр де Латур, изучая все те же дрожжи под микроскопом (а это был уже не тот примитивный микроскоп, с которым работал Левенгук), сумел застать эти крошечные шарики в момент отпочковывания (рис. 22). Почкование — это размножение, а где размножение, там и жизнь! Таким образом было получено свидетельство тому, что дрожжи — это одноклеточные существа, более близкие растениям, нежели животным, потому и неподвижные.
В 50-х и 60-х годах XIX века французский химик Луи Пастер в ряде своих классических опытов показал, что ферментизация — это результат жизнедеятельности таких микроорганизмов. Порча продуктов — например, образование кислого вина — это результат деятельности одних видов дрожжей, а получение нужных — например, хорошего вина — других. Да и гниение мяса Пастер наконец-то смог убедительно приписать результату жизнедеятельности микроорганизмов (не то чтобы до него об этом никто не догадывался, но никому не удавалось предоставить убедительных доказательств).
Короче говоря, реакции, которые раньше принято было объяснять работой «органических катализаторов», теперь оказались результатом деятельности живых существ. Сторонники теории «тайны жизни» воспрянули духом.
Конечно, занять старые позиции и вновь утверждать, что «жизненная сила» — это принципиальный критерий различения органической и неорганической материи, было уже невозможно, но вот вторая линия обороны уже казалась вполне надежной. Нельзя было отрицать, что химик в своей лаборатории может искусственно воспроизвести синтез органического вещества, но оставалась вера в то, что он не может сделать это тем же путем, что и природа. Химик прибегает для этого к помощи высоких температур и давлений, сильнодействующих химических веществ или не встречающихся в природе катализаторов. И лишь существа, наделенные жизненной силой, могут формировать те же органические вещества при нормальных условиях с использованием весьма слабых химикатов.
Опасность для таких воззрений появилась с другой стороны. Кроме газообмена кислорода и углекислоты при дыхании к числу наиболее доступных для изучения химических процессов, происходящих в человеческом организме, принадлежат процессы пищеварения.
Причиной тому факт, что организм по форме своей похож на булочку для хот-дога. И пищеварительный тракт — как отверстие для сосиски — пронизывает его насквозь, от начала до конца. Поскольку поместить что-то в отверстие для сосиски — это не то же самое, что заковырять это что-то в булочку, то и процессы пищеварения, проходящие в пищеварительном тракте, можно считать «внешними» для организма.
Практическая ценность этого факта заключается в том, что анализ содержимого пищеварительного тракта можно производить через ротовое отверстие без нанесения обследуемому каких-либо повреждений.
Еще в 1752 году Реомюр, изобретатель температурной шкалы Реомюра, занимался изучением процессов пищеварения у сокола. Целью его работы было установить, что же именно совершается в желудочно-кишечном тракте: просто ли механически перетирается пища или происходят какие-то более тонкие изменения. Ученый заставлял сокола глотать металлические трубочки, внутри которых находились кусочки мяса. Металлическая трубочка была призвана защищать мясо от любого механического воздействия; по торцам трубки были закрыты проволочными сетками, сквозь которые легко мог проходить желудочный сок.
После того как сокол отрыгивал трубки (хищные птицы, как правило, заглатывают пищу целиком, а потом отрыгивают непереваренное), Реомюр видел, что мясо растворилось, а трубки полны чистой жидкостью. При этом запаха гниения не наблюдалось, так что ученый сделал вывод, что здесь имеет место некая другая реакция, не гниение, а что-то сродни ферментации.
Другие исследователи в течение последующих десятилетий установили, что содержание желудка — кислотная среда, а в 1824 году Уильям Прут выяснил, какая именно кислота в нем представлена — соляная. К тому времени было уже хорошо известно, что кислота — это хороший катализатор таких реакций, как распад крахмала и белков на мелкие молекулы, так что ответ на вопрос о механизмах пищеварения родился сам собой — это кислотный катализ.
Однако дальнейшие исследования показали, что в желудочном соке содержатся и другие вещества, раствор которых оказывает разлагающее действие на мясо и которые не являются при этом кислотами. В 1835 году немецкий натуралист Теодор Шванн выделил из желудочного сока порошок, не являющийся кислотой, но при этом очень активно разлагающий мясо. Ученый назвал его «пепсином», от греческого слова, означающего «переваривание».
Это открытие оказалось новостью. Пепсин представлял собой одновременно и катализатор, и вещество совершенно органической природы. Такой органический катализатор назвали ферментом, поскольку тогда казалось, что ферментизация и пищеварение — явления одной природы.
В это же время двое французских ученых, Ансельм Пайен и Ж.-Ф. Персо, произвели нечто подобное в отношении экстракта из солода (вымоченного ячменя). В 1833 году они получили фермент, способный расщеплять крахмал на сахар. Сахар этот получил название «мальтоза», от английского «malt» — «солод», а сам фермент — «диастаза». Пайен оказался первопроходцем в деле присвоения имен классам химических веществ. Введенный им термин «целлюлоза» завел моду на окончание «-оза» для Сахаров, а со введением названия «диастаза» и все остальные ученые стали давать открываемым ферментам названия, заканчивающиеся на «-аза» (правда, в течение какого-то периода ферментам, задействованным в пищеварении, все же давали окончания на «-ин», по аналогии с пепсином).
А выделение различных ферментов — продолжалось. Немецкий химик Юстус фон Либих, вместе с Вёлером, занимался изучением экстрактов горького миндаля — к тому моменту было уже известно, что его действие приводит к распаду вещества растительного происхождения под названием «амигдалин». К 1837 году ученые решили, что в экстракте содержится некий фермент, которому было дано название «эмульсин». Тогда же французский химик Опост Пьер Дюбранфо сумел выделить из дрожжей экстракт, с помощью которого можно было вызывать распад сахарозы на более простые сахара — глюкозу и фруктозу. Он назвал это вещество «инвертазой».
Как оказалось, механизмы действия ферментов, как и катализаторов, совершенно не нарушают законов термодинамики. Ферменты изменяют лишь скорость реакции, но никак не положение точки равновесия (см. главу 9). В этом отношении оказалось, что живые организмы не имеют особенных свойств, которых был бы лишен мир неживой природы.
Однако позицию сторонников «жизненной силы» такие рассуждения могли лишь пошатнуть, но не разрушить. Да, все эти выделенные ферменты — органические вещества, и они способны катализировать определенные реакции, но лишь те (по крайней мере, так казалось в тот момент), которые сходны с расщеплением продуктов в пищеварительном тракте. А все процессы, происходящие в пищеварительном тракте, нельзя рассматривать как «жизненные» в полном смысле слова, поскольку они проходят вне живых тканей.
Далее сторонники «жизненной силы» настаивали на том, что изолированные ферменты не способны и никогда не будут способны катализировать реакции, происходящие внутри самих тканей, например превращать раствор сахара в спирт. На такое способны только цельные живые клетки дрожжей, и внутриклеточный энергообмен все еще оставался делом загадочным.
Для того чтобы еще больше подчеркнуть важность «духа жизни», они ввели разделение ферментов на две категории — на участвующие и не участвующие в процессах жизнедеятельности, назвав первые «организованными ферментами», а вторые, соответственно, «неорганизованными».
В 1876 году немецкий физиолог Вильгельм Кюне продвинулся еще на один шаг дальше. Он предложил оставить термин «фермент» только для жизненных процессов, а все неорганизованные ферменты, действующие и в отсутствие какой-либо жизни, назвать по-другому, «энзимами», что по-гречески означает «в дрожжах», поскольку одним из источников добычи этих ферментов могут служить дрожжи.
Итак, сторонники «жизненной силы» мудро отступали, сдавая одну позицию за другой, но сохраняя при этом нетронутым сам принцип своей веры, на протяжении всего XIX века. Принцип же этот заключался в том, что живая материя вследствие присутствия в ней «жизненной силы» подчиняется иным законам, нежели те, что известны нам из наблюдений и экспериментов над неживой природой.
Но вот в 1897 году немецкий химик Эдуард Бухнер решил как-то раз приготовить себе для экспериментов как можно более цельный дрожжевой экстракт. Для этого ученый тщательно перемолол дрожжевые клетки песком и профильтровал полученную массу, получив таким образом чистый сок дрожжей без единой живой клетки.
По принятым в те годы воззрениям сторонников «жизненной силы», такой дрожжевой сок являлся мертвым, а значит — и неспособным к ферментированию сахара. Так что Бухнер решил, что лучшим способом предохранить экстракт от бактериального заражения будет залить его насыщенным раствором сахарозы, известной своим свойством консервировать продукты. Однако, к его вящему удивлению, добавленная в экстракт сахароза принялась ферментироваться. Сначала в растворе стали заметны пузырьки углекислого газа, а потом — обнаружился спирт.
Процесс такой ферментации, до того считавшийся прерогативой исключительно живых существ, в данном случае оказался вызванным мертвыми химическими веществами, и именно этот факт оказался смертельным ударом по представлениям о «жизненной силе». Оказалось, что с точки зрения энергетического обмена поведение «организованных» и «неорганизованных» ферментов ничем не различается. Так стало очевидно, что законы термодинамики работают и в клетках, и вне клеток, и вообще везде.
Ферменты производятся, как правило, живыми существами, но сами по себе они таковыми не являются, и действие их не имеет никакого отношения к жизни.
Но просто назвать органические катализаторы, являющиеся свойством живой материи, «ферментами» или «энзимами» — явно недостаточно, чтобы объяснить механизм их действия.
Умы биохимиков конца XIX — начала XX века были заняты вопросом о том, какова же на самом деле природа ферментов. Как свидетельствует накопленный к этому времени уже в достаточном количестве опыт работы с катализаторами реакций неорганической химии, для осуществления реакции требуется присутствие крайне малого количества катализатора, так что вполне вероятно было предположить, что экстракты ферментов способны полноценно катализировать реакции, содержа при этом слишком мало самого фермента, чтобы его можно было полноценно проанализировать. (Впоследствии оказалось, что так оно и есть.) Кроме того, любая вытяжка из живой ткани содержит столько различных веществ сложнейшего строения, что надо обладать терпением Иова и мудростью Соломона, чтобы понять, какое же из них является ферментом, если он вообще присутствует.
Так что оставалось только изобретать непрямые подходы. Если реакция идет, значит, фермент присутствует, если реакция не идет, значит, фермент отсутствует; тогда любое условие, при котором реакция останавливается (кроме, конечно, замены самих реагирующих веществ), можно трактовать как выключение действия фермента.
К примеру, слабое нагревание до температур, еще далеких до температуры кипения воды, как правило, приводит к тому, что через несколько минут катализируемая ферментом реакция останавливается. На реагирующие вещества при этом никакого эффекта не оказывается, поскольку если их отдельно нагреть, потом остудить, а потом опять добавить к ним раствор фермента, то реакция сразу же начнется снова. А вот если нагреть, а потом остудить раствор фермента и добавить его к реагирующим веществам, то никакой реакции не произойдет. Значит, нагревание однозначно воздействует как-то на молекулу фермента, которая обладает слабой устойчивостью к высоким температурам.
Таким свойством обладают вещества одной группы — белки. Значит, ферменты — это белки? Начался сбор данных, свидетельствующих в пользу этого предположения. Стали пробовать другие виды воздействий, известных свойством приводить к распаду сложных белковых молекул (например, повышение кислотности среды или механическое взбивание раствора), и все они тоже приводили к прекращению реакций, катализируемых ферментами. Тот же эффект на реакцию оказывало и воздействие химических веществ, имеющих свойство связывать белки. Часто к прерыванию реакций, катализируемых ферментами, приводило и воздействие других ферментов, катализирующих распад белков. На основе всех этих косвенных данных в начале XX века общепринятым стало представление о том, что ферменты — это белки.
Однако в 1920 году немецкий химик Рихард Вильштеттер результатами своих работ заставил усомниться в справедливости такого воззрения. Он задался целью получить как можно более концентрированную вытяжку фермента, очистить ее от всего, от чего только получится. В итоге у ученого получился раствор с высокой каталитической активностью (что свидетельствует о наличии высокой концентрации фермента), но полностью лишенный какой бы то ни было белковой составляющей. Вильштеттер использовал все известные тесты на наличие белка в полученном растворе — и все они давали отрицательный результат. Белка не было.
Конечно, можно было предположить, что сам фермент содержится в растворе в неуловимо малом количестве, или сослаться на несовершенство тестов того времени (собственно, и то и другое впоследствии подтвердилось), но Вильштеттер оказался не столь скрупулезен. Он сделал четкий вывод: чем бы ни был фермент, это уж точно не белок. Ко мнению Вильштеттера — известного химика, лауреата Нобелевской премии — не могли не прислушаться, и представление о том, что фермент — это белок, исчезло из научной картины мира лет на десять.
А между тем в Америке мирно работал биохимик по имени Джеймс Батчеллор Самнер, занимаясь изучением растения под названием «карна-валия мечевидная». Из этого растения ученый извлек вытяжку, которая катализировала распад мочевины на аммиак и углекислоту. По общепринятым правилам, новооткрытый фермент получил название «уреаза». Дальше Самнер выделил из уреазы маленькие кристаллики, раствор которых в чистой воде, как обнаружил химик, к своему удивлению, оказывал то же действие, что и сама уреаза.
Как ни старался Самнер в дальнейшем добиться действия вытяжки в отсутствие кристаллов, этого сделать не удалось. Разрушались кристаллы — прекращалось и действие, и в конце концов Самнер решил, что в кристаллической форме ему удалось выявить сам фермент. А поскольку результаты всех тестов свидетельствовали о том, что кристаллы состоят из белкового вещества, то пришлось признать, что как минимум один конкретный фермент — уреаза — все же является белком.
Авторитет Вильштеттера был так велик, что сперва открытию Самнера особого значения никто не придал. Но в 1930 году еще один американский биохимик, Джон Говард Нортроп, объявил, что ему с коллегами удалось выделить в кристаллической форме еще несколько ферментов, и среди них — пепсин. Тут же последовал ряд аналогичных достижений со стороны других ученых, и всякий раз выделенные кристаллы оказывались белками.
Так теория Вильштеттера рассыпалась под напором фактов, и в 30-х годах XX века навсегда было установлено, что ферменты принадлежат к белкам. Так что сейчас мы смело можем говорить о том, что ферменты — это «белковые катализаторы», или «катализирующие белки».
Глава 16. ПОДРОБНЕЕ О БЕЛКАХ
В свете всего описанного в предыдущей главе мы можем еще раз попробовать провести разграничение между живой и неживой природой, между ящерицей и камнем. Давайте попробуем.
Живой организм отличается способностью производить локальное и временное уменьшение энтропии путем химических реакций, катализируемых ферментами.
«Временной» эта способность названа с учетом того, что ящерица не пробудет живой дольше нескольких лет, даже если полностью удовлетворять все ее потребности. Лишь несколько видов животных (человек и некоторые черепахи) живут по сто лет, и лишь некоторые деревья — по тысяче, тогда как неживой предмет, скажем скала, может оставаться неизменным миллиарды лет, а то и бесконечно.
Таким образом, химические реакции, катализируемые ферментами, представляют собой важную часть определения. Именно их наличие отличает живой организм от систем, в которых локальное уменьшение энтропии достигается за счет подключения внешних источников энергии, таких как солнечный свет или внутреннее тепло Земли, и от рукотворных механизмов, в которых локальное уменьшение энтропии достигается за счет тепловых машин, химических батарей и т. п.
В некотором смысле, конечно, наше определение условно. Зачем подчеркивать важность ферментов? Рукотворные компьютеры и технические средства становятся с каждым годом все ближе и ближе к живым существам и даже к самому человеку. Скоро им станут доступны даже такие абстракции, как мышление, суждение, обучение… Можно ли поручиться, что рукотворные предметы никогда не поднимутся на уровень сложности, равный уровню сложности живых существ? А если это произойдет — сможем ли мы отказать им в праве называться «живыми» на том основании, что они не имеют никакого отношения к реакциям ферментации? А если на каком-то этапе разработки искусственных механизмов в них будут включены и ферменты? Достаточно ли этого, чтобы счесть машины живыми?
Или — с другой стороны (не с такой уж и невероятной, как показывают события последних лет): что, если на других планетах обнаружатся объекты, обладающие всеми свойствами, которые принято приписывать живым существам, — возможно, даже разумом? Если химическая природа этих предметов не будет иметь ничего общего с ферментами или даже с белками вообще, если в них не будет происходить совсем никаких химических реакций — сможем ли мы счесть их живыми?
Задумываясь над этими вопросами, остается только пожалеть, что гипотеза о «жизненной силе» оказалась несостоятельной. Вот если бы она была верна, и действительно существовало бы два отдельных свода законов природы — один для живых существ, другой для неживой материи, — то тогда действительно можно было бы составить точное, корректное и безошибочное определение. Живой организм — это тот, который подчиняется таким-то законам, а неживой предмет — таким-то.
Увы, все объекты во Вселенной — и живые, и неживые — существуют по одним и тем же правилам, и поэтому так трудно провести разграничительную линию. Если сделать определение слишком широким — то под него обязательно подпадет какая-нибудь звезда или даже Солнечная система, а чересчур сужая определение, можно сделать его слишком антропоморфным.
Один из вариантов решения этой проблемы — признать саму задачу принципиального различения между живой и неживой материей несущественной. Понятно, что любая попытка провозгласить принцип разделения, прежде всего, окажется попыткой выражения личных пристрастий провозглашающего. Ведь уже само представление о том, что все объекты должны строго делиться на две категории, живых и неживых, — это предрассудок, не имеющий под собой реального обоснования. На самом деле суть в том, что материя может организовываться как простыми, так и сложными способами, и часть сложных способов, которыми самоорганизовывается материя, принято называть «жизнью», а принципиальной границы между этими способами и близкими к ним провести невозможно.
Лично я считаю именно так, но беда в том, что для целей нашей книги эти рассуждения являются «абсолютно верными и абсолютно бесполезными». Условные определения не обязаны представлять собой Истину с большой буквы, главное — чтобы они помогали мыслить и чтобы их условность не отрицалась и не скрывалась. Вот, например, разделение химии на органическую и неорганическую до сих пор соблюдается не потому, что оно истинно, а просто потому, что это удобно.
Таким образом, признавая условность и возможную несостоятельность нашего определения перед лицом будущих успехов человека на ниве роботостроения и космических исследований, я выделил приведенное определение курсивом как пример адекватного ситуации и полезного принципа разделения живых и неживых существ. Оно коротко, просто, ясно и охватывает все примеры, которые вы или я можем встретить в мире на данном этапе развития человечества.
Итак, придя к удовлетворительному, с моей и, надеюсь, с вашей точки зрения, определению разницы между живой и неживой материей, одной из поставленных целей мы добились. Но было бы странно этим и ограничиться, поскольку ряд волнующих вопросов так и остался пока без ответа.
В конце концов, ведь химические реакции и катализаторы встречаются во множестве явно неживых систем. Реакции, происходящие в живых и неживых системах, в основном похожи и подчиняются одним и тем же законам природы. Так почему же разница в катализаторах приводит к таким кардинальным различиям, какие мы видим между живой и неживой природой?
Никто не спорит с тем, что пчела — более тонкий и сложный механизм, чем самолет, а мышь — более удивительная конструкция, чем гора.
Если такую разницу создает одно лишь присутствие фермента, то давайте же присмотримся к нему пристальнее.
Если сравнивать ферменты с обычными катализаторами из неорганических систем, то в глаза бросается множество различий. Ферменты гораздо более хрупки, их легче отключить, они более требовательны к условиям функционирования — им нужны строго определенный уровень температуры и кислотности, присутствие в небольших количествах одних ионов, полное отсутствие других и так далее.
Кроме того, ферменты в высшей степени специализированы. Если неорганические катализаторы, подобные платине или кислотам, способны ускорять множество реакций, то ферменты могут катализировать их лишь строго ограниченное количество. Очень часто один фермент проявляет способность катализировать лишь одну-единственную реакцию, никак не влияя на ход других, как бы они ни были на нее похожи.
Причиной этих различий (скорее количественных, чем качественных, но тем не менее бросающихся в глаза) является различие в строении неорганических катализаторов и ферментов. Ферменты — это белки, а другие катализаторы — нет. И естественно предположить, что необычные свойства ферментов — следствие их белковой природы.
С этого и начнем.
На протяжении XIX века про молекулы белков точно знали только одно — что они большие.
Так, в 1860 году шотландский химик Томас Грэм обнаружил, что если с помощью листа пергамента разделить раствор некоего вещества в воде на участки с собственно раствором и чистой водой, то частицы растворенного вещества часто все же могут проникнуть через бумажную мембрану в «очищенную» часть. Химические тесты того времени позволяли легко обнаружить их.
Но оказалось, что таким свойством обладают далеко не все растворимые вещества. Поваренная соль и другие неорганические вещества проходят сквозь пергамент без проблем. Такие органические вещества, как сахара, — тоже. А вот растворенный белок так и остается по «свою» сторону пергамента. Грэм разделил все вещества на две категории — те, растворы которых проходят сквозь пергамент, и те, растворы которых не проходят. Поскольку проходящие сквозь пергамент вещества при испарении раствора легко проявляются в виде кристаллов, то он назвал их кристаллоидами, а клееобразные белковые растворы — «коллоидами», от греческого слова «колла» — «клей».
Рис. 23. Диализ с помощью полупроницаемой мембраны
Самое простое (и, за некоторыми уточнениями, верное) объяснение этому явлению кроется в том, что в пергаменте есть микроскопические поры, сквозь которые маленькие молекулы пролезают, а большие — нет. В результате пергамент и подобные ему мембраны — в первую очередь мембраны, окружающие живые клетки, — стали называть полупроницаемыми.
Так появился один из самых распространенных ныне способов очистки белковых растворов. Раствор белка помещали в мешок из полупроницаемой мембраны (в те времена самым распространенным материалом такого рода оказывалась колбасная оболочка — кишка) и подвешивали в проточной воде. Все вещества с малым молекулярным весом просачивались сквозь мембрану и смывались, а большие белковые молекулы оставались в мешке. Этот процесс носит название «диализ», или «мембранная сепарация» (рис. 23).
Тот факт, что белки не проходят сквозь полупроницаемую мембрану, устанавливает нижнюю планку размера белковой молекулы; тот факт, что белки все же растворяются, — верхнюю. Последний момент надо объяснить подробнее.
На каждую растворенную в воде частицу действуют две противоположно направленные силы. Первая — это сила тяжести, тянущая частицы вниз (предположим, что их плотность больше плотности воды; как правило, это так и есть), а вторая — это бомбардировка молекулами воды, постоянные случайные удары, поддерживающие вещество в равномерно растворенном состоянии. (Если частицы несут электрический заряд, то есть еще притягивающие и отталкивающие электрические силы, но этого момента мы сейчас касаться не будем.)
Для частиц любого видимого размера самой важной является сила тяжести, поэтому в конечном итоге они тонут. Однако чем меньше частица, тем большее значение приобретает бомбардировка молекулами и тем меньше становится скорость осаждения вещества. Описанное мной распределение явно видно, если горсть земли бросить в миску с водой. Любые камушки, если таковые там окажутся, тут же опустятся на дно. Чуть позже осядут и частицы чуть покрупнее, потом — помельче, наконец, — самые крохотные. В итоге в воде останется взвесь, поскольку какие-то частицы так и не опустятся на дно, потому что они настолько малы, что молекулярная бомбардировка нивелирует действие силы тяжести, сводя скорость их осаждения до крайне малых значений, а то и до нуля.
На самом деле частицы, чей размер достаточно мал, чтобы они оставались во взвешенном состоянии вечно, глазом неразличимы. Однако для того, чтобы рассеивать свет, их размера вполне достаточно — это явление обнаружил в 70-х годах XIX века британский физик Джон Тиндаль, и в его честь оно называется «эффект Тиндаля». Если пропустить через такой раствор луч света и посмотреть на емкость с раствором под прямым углом к лучу, то луч будет выглядеть как светлый туннель, проходящий сквозь туман. Именно благодаря взвеси мельчайших частиц, рассеивающих свет в направлении глаза наблюдателя, и виден луч.
Если же вместо человеческого глаза за происходящим наблюдает специальный микроскоп («ультрамикроскоп»), то через него видны и сами частицы в виде ярких точек.
Чем меньше частицы, тем слабее эффект рассеивания света, и когда их размер уменьшается настолько, что они уже могут проходить сквозь полупроницаемую мембрану, то эффект становится незаметным, и физики говорят, что раствор «оптически чист».
В растворах белков эффект Тиндаля наблюдается. С учетом того, что белковые молекулы достаточно велики, чтобы полупроницаемые мембраны оказывались для них непреодолимыми, и при этом достаточно малы, чтобы пребывать во взвешенном состоянии, в целом можно сказать, что они «коллоидных размеров».
«Коллоидные размеры» включают от 1 до 1000 миллимикронов в диаметре (напомню, миллимикрон — это одна миллиардная метра). Даже самые маленькие из коллоидных частиц должны состоять, соответственно, из тысяч атомов, а самые крупные — из триллионов. А средний вес одного атома молекулы белка — 7. Соответственно, можно сказать, что молекулярный вес белков, раз они лежат на отрезке «коллоидных размеров», — от 7000 до 7 000 000 000 000.
Столь большой разброс никак не может нас устроить в качестве «точных данных», но даже его достаточно, чтобы понять, что молекулы белка гораздо крупнее, чем молекулы таких веществ, как поваренная соль (молекулярный вес 58,5) или глюкоза (180).
В последней четверти XIX века ученые взялись за проблему установления точных значений молекулярных весов огромных молекул вроде белков. Один из способов добиться этого — диализ. Если с одной стороны полупроницаемой мембраны находится белковый раствор, а с другой — чистая вода, то молекулы воды могут свободно перемещаться сквозь мембрану в обоих направлениях. Однако со стороны раствора крупные молекулы белков «забивают» микропоры, через которые могла бы пройти вода.
В результате молекулы воды из половины с чистой водой в половину с раствором белка переходят активнее, чем наоборот, и получается течение из одной половины в другую, отчего и образуется разность уровней воды между двумя половинами. Из-за этой разности уровней давление в половинке с раствором становится выше, и его компенсирующее действие прекращает перетекание воды.
Такое неравномерное перетекание воды получило название «осмос» (от греческого слова, означающего «толкать»), а создаваемое им давление — «осмотическое» (рис. 24). Величина осмотического давления зависит от количества крупных молекул, блокирующих поры, — чем их больше, тем выше давление.
Теперь предположим, что у нас имеется некое количество белка, точный вес которого известен. Чем крупнее его молекулы, тем меньше их будет в образце вещества одного и того же веса. То есть для образца белка, вес которого известен, чем ниже осмотическое давление, тем больше молекулярный вес.
Рис. 24. Устройство для определения осмотического давления и молекулярных весов белковых молекул
Первым измерить осмотическое давление в различных коллоидных растворах попытался в 1877 году немецкий ботаник Вильгельм Пфеффер. К 1885 году голландский специалист в области физической химии Якоб Хендрик Вант-Гофф вывел точную формулу зависимости осмотического давления от молекулярного веса вещества, и началась полномасштабная доработка методики.
К 1917 году методы определения молекулярного веса через измерение осмотического давления стали уже вполне надежными. В этот год датский химик Серен Петер Лауриц Сёренсен объявил, что молекулярный вес яичного белка (того самого первого белка, который дал название всем остальным!) — 34 000. Вскоре после этого было установлено, что молекулярный вес гемоглобина (главного белка красных кровяных телец) — 67 000.
К сожалению, когда молекулярный вес вещества доходит до сотен тысяч, осмотическое давление падает до столь малых значений, что получение каких-либо точных данных становится делом уже невозможным. Поэтому установить молекулярный вес многих важных белков так и не смогли. Однако уже к 1925 году стало ясно, что молекулярный вес белков редко опускается ниже 10 000, а у многих важных белков — превышает 100 000.
Одновременно с исследованиями проникновения через мембрану шло и параллельное наступление на тайны белков — со стороны изучения их осаждения. Как я уже говорил, чем мельче частицы, тем медленнее они осаждаются. К сожалению, все белковые молекулы достаточно малы, чтобы скорость их осаждения равнялась нулю, так что большие белковые молекулы от маленьких белковых молекул таким образом отличить невозможно — по крайней мере, при обычных условиях.
Чтобы сделать возможным практическое использование скорости осаждения, надо сделать что-то равносильное усилению силы тяготения (до такого уровня, при котором белковые молекулы все же начинают осаждаться, каждая со своей скоростью, определяемой ее размером). Изменить силу тяготения как таковую человек пока еще не в силах, но того же результата можно добиться и с помощью другого явления. Если сосуд с жидкостью быстро вращать, то его содержимое будет сдвигаться от центра вращения в сторону стенок. Во многих отношениях этот центробежный эффект сродни силе тяготения, и, как и сила тяготения, он тоже приводит к осаждению взвесей. Но для центробежной силы, в отличие от силы тяготения, ничего не стоит установить желаемую величину.
В 1925 году шведский химик Теодор Сведберг разработал «ультрацентрифугу», которая могла производить столь быстрое вращение, что белковые молекулы под его действием принимались осаждаться из раствора (сейчас возможно создание центрифуг, имитирующих силу тяжести в 500 000 раз больше действительной).
С помощью оптических устройств можно отследить изменения скорости осаждения по мере разгона центрифуги. Если в растворе присутствует более одного белка, то можно отслеживать скорость осаждения каждого из них в отдельности. (Скорость осаждения зависит не только от веса, но и от формы молекулы, вытянутая молекула будет осаждаться быстрее, чем круглая, при одинаковом весе, так что для того, чтобы по скорости осаждения можно было адекватно судить о молекулярном весе вещества, надо сначала отдельно установить форму молекулы.)
С началом использования ультрацентрифуги количество белков с известным молекулярным весом пошло в гору. Выяснилось, что молекулярный вес белка фибриногена (присутствующего в крови и обеспечивающего свойство сворачиваемости) — 330 000, гемоцианина (синеватого белка, присутствующего в крови морских животных) — 4 000 000, а белков, из которых состоят вирусы, — более 10 000 000.
Однако сейчас нас интересуют ферменты, а это — не самые крупные из белковых молекул. Молекулярный вес подавляющего большинства ферментов — от 10 000 до 500 000, и очень немногие ферменты лежат вне этих рамок.
Но сам по себе большой размер молекулы фермента по сравнению с молекулами других катализаторов еще не может служить объяснением его необычных свойств. Многие органические молекулы других типов тоже имеют огромные размеры — крахмал, целлюлоза, резина, множество синтетических пластмасс, — но свойствами ферментов они при этом не обладают.
Одно из основных различий между белками (в том числе ферментами) и другими огромными молекулами заключается в том, как легко белки разрушаются. Можно, конечно, сказать, что чем крупнее молекула, тем сложнее удержать ее в целостности в условиях вибраций или высоких температур. Но почему на белки это правило распространяется, а на другие огромные молекулы — нет? Сам по себе размер не означает хрупкости. Древесина состоит из огромных молекул, но она достаточно прочна, чтобы служить строительным материалом и выдерживать сильнейшие вибрации без каких-либо видимых последствий.
Так что дело явно в чем-то другом.
Две структуры одинакового размера могут иметь разную стабильность, в зависимости от природы своих составляющих. Трехметровой высоты дом из деревянных блоков — это просто воплощение стабильности, особенно по сравнению с такой же высоты строением из игральных карт. Можем ли мы сравнить составляющие белков с глюкозой, из которой состоят крахмал и целлюлоза, и выяснить, в чем же между ними разница?
Установить составляющие единицы белка оказалось сложнее, чем других огромных молекул, хотя французский химик А. Браконно взялся за это довольно рано. Успешно разложив с помощью методов Кирхгофа (нагреванием с использованием кислоты) ряд углеводов, в 1820 году он обратил внимание на белок желатин.
Это вещество тоже оказалось очень просто разложить с помощью кислоты, и в результате были получены сладковатые кристаллы, которые ученый, разумеется, счел разновидностью сахара. Браконно назвал полученное вещество «желатиновым сахаром». Однако вскоре выяснилось, что из этих кристаллов можно выделить аммиак (NH3), а значит, обычным сахаром они быть не могут, если в них содержатся атомы азота. В итоге вещество получило название «глицин», от греческого слова, означающего «сладкий», с добавлением суффикса «-ин», типичного для азотсодержащих веществ.
Однако это открытие не решило задачу установления структурной единицы белка. Да, другие огромные молекулы состоят из одного и того же структурного элемента, который достаточно определить один раз, но белки — другое дело. Были обнаружены и другие блоки, похожие на глицин. Один из них открыл сам Браконно, назвав его «лейцин», и список этих веществ пополнялся на протяжении всего XIX века и части XX века.
Точное число их назвать нелегко, поскольку некоторые встречаются лишь в нескольких белках, и непонятно, включать ли их в общий список. Общепринято говорить о девятнадцати веществах, присутствующих в числе продуктов распада практически всех крупных белков. Их названия приведены, в порядке открытия, в таблице 5.
Конечно, на самом деле этот список не так уж разнороден, как может показаться. У всех этих веществ много общего. В частности, каждое имеет в своем составе соединение, именуемое «карбоксильной группой» и обладающее кислотными свойствами, и комбинацию атомов под названием «аминогруппа». Последний факт подтолкнул Берцелиуса еще в 1848 году назвать все эти вещества «аминокислотами», — и это название было принято. Соответственно, все белки состоят из аминокислот.
Таблица 5.
ОСНОВНЫЕ СОСТАВЛЯЮЩИЕ БЕЛКОВЫХ МОЛЕКУЛ
Название — Год открытия
Глицин — 1820
Лейцин — 1820
Тирозин — 1849
Серии — 1865
Глютаминовая кислота — 1866
Аспарагиновая —
кислота — 1868
Фенилаланин — 1881
Алании — 1888
Лизин — 1889
Аргинин — 1895
Гистидин — 1896
Цистин — 1899
Цистеин — 1901
Валин — 1901
Пролин — 1901
Триптофан — 1901
Изолейцин — 1903
Метионин — 1922
Треонин — 1935
Во всех случаях карбоксильную группу отделяет от аминогруппы лишь один атом углерода, то есть все молекулы аминокислот, составляющих белки, имеют вот такой «скелет»:
аминогруппа — С — карбоксильная группа.
В состав самой простой (и самой первой из обнаруженных) аминокислоты — глицина — входят два атома водорода, каждый из которых прикреплен напрямую к тому самому центральному атому углерода, и больше в молекуле глицина нет ничего. Во всех прочих аминокислотах к центральному атому углерода тоже прикреплен, помимо карбоксильной и аминогруппы, один атом водорода, а вот вместо второго имеется более-менее сложная углесодержащая группа атомов, именуемая «радикалом». Так что полную схему углекислоты можно записать так:
Как видно, все аминокислоты структурно похожи друг на друга и различаются только тем, что у них разные радикалы.
К концу века, когда из белков уже было выделено с десяток аминокислот, стало понятно, что пора приступить и, наоборот, к синтезу белка из аминокислот. Этой проблеме посвятил свою работу немецкий химик Эмиль Фишер. Он терпеливо создавал аминокислотам одно за другим все условия, которые могли стимулировать соединение органических веществ.
В 1907 году ему удалось собрать молекулу, состоящую из восемнадцати аминокислот — пятнадцати глицинов и трех лейцинов. Сейчас такие короткие цепочки аминокислот называют пептидами, от греческого слова, означающего «пищеварение», потому что они являются продуктами первого шага расщепления белков при пищеварении.
Достижение Фишера навсегда положило конец любым спорам о том, являются ли аминокислоты строительными кирпичиками для белков. Полученное им вещество, состоящее из восемнадцати аминокислот, проявляло все свойства, которые только можно было ожидать от простейшего белка. Ученый продемонстрировал, что при формировании цепочки карбоксильная группа одной аминокислоты соединяется с аминогруппой другой, так что скелет пеп тидов выглядит примерно так:
аминогруппа — С — карбоксильная группа — аминогруппа — С — карбоксильная группа — аминогруппа — С — карбоксильная группа — и так далее.
Центральный атом углерода каждой из участвующих в цепочке аминокислот имеет собственный радикал (в случае с глицином в роли радикала выступает единственный атом водорода), так что пептид можно рассматривать как однородную цепочку, из которой торчат различные радикалы, тип и порядок расположения которых отражает расположение в цепочке различных аминокислот.
Связь между карбоксильной группой и аминогруппой, впервые продемонстрированная Фишером, называется «пептидной», и накопленные с тех пор данные позволяют с наибольшей уверенностью, какую только может позволить себе наука вообще, говорить о том, что все существующие в природе белки состоят из аминокислот, скрепленных между собой пептидными связями.
С тех пор разработано уже много новых методов синтеза пептидных цепочек. С помощью метода, изобретенного в 1947 году израильским ученым Е. Качальским, при котором изначально используются несколько видоизмененные молекулы аминокислоты, можно создавать пептидные цепочки длиной до 200 аминокислот.
Как видите, природа строительных элементов для белков уже сама по себе заставляет видеть в белках нечто принципиально отличное от любых других огромных молекул. Молекулы крахмала и целлюлозы состоят из одинаковых единиц — из глюкозы. Огромная молекула инулина (крахмалоподобного соединения, производимого иерусалимским артишоком) состоит исключительно из фруктозы. Резина — только из углевода под названием «изопрен». Гиалуроновая кислота — скользкое вещество, служащее для уменьшения трения в суставах живого организма и встречающееся в межклеточном пространстве, — состоит из двух равномерно чередующихся разновидностей сахара. Все синтетические пластмассы состоят либо из одинаковых единиц, либо из двух видов единиц, чередующихся в составе вещества равномерно.
Соответственно, молекулы крахмала могут различаться между собой только количеством составляющих их единиц глюкозы; молекулы инулина — количеством единиц фруктозы и так далее. Разумеется, и этого достаточно, чтобы разница между представителями одного и того же вида огромных молекул была гораздо больше, чем между представителями одного вида меньших молекул, но все равно это ничто по сравнению с разнообразием, которое представляют белки.
Молекулы белка состоят из девятнадцати разных аминокислот (плюсминус одна), которые в той или иной молекуле могут быть представлены в любом количестве каждая, и порядок их размещения в пептидной цепочке тоже может быть любым. И любое изменение в размещении аминокислот приводит к появлению молекулы уже с другими свойствами. Белковые молекулы могут различаться между собой не только тем, что в состав одной входит восемнадцать аминокислот, а другой — девятнадцать. Две молекулы, состоящие обе из восемнадцати или девятнадцати аминокислот, могут разительно отличаться порядком расположения аминокислот, а значит, и своими свойствами.
Сколько же возможно в принципе таких вариаций? Допустим, строится молекула, в которой должно присутствовать по одной из каждых девятнадцати видов аминокислот. Начать можно с любой из девятнадцати, это дает нам уже девятнадцать вариантов. Далее продолжить каждый из них можно с помощью каждой из восемнадцати оставшихся аминокислот, так что мы имеем уже 19 х 18 сочетаний, каждое из которых можно продолжить с помощью каждой из 17 оставшихся, и так далее.
Продолжая рассуждать таким образом, мы получаем общее число возможных вариантов 19 x 18 x 17 x 16 x 15 x 14 x 13 x 12 x 11 x 10 x 9 x 8 x 7 x 6 x 5 x 4 x 3 x 2 x 1— такую последовательность называют «19 факториал» и записывают как 19! (цифра, а рядом с ней — восклицательный знак). Факториалы очень быстро достигают невообразимых значений — в данном случае вы и сами можете просчитать величину 19!, а если не хотите — то поверьте мне на слово, что получится число больше сотни квадриллионов (точнее, 121 646 600 408 832 000).
Соответственно, даже если ограничить возможность повторения одной и той же аминокислоты в цепочке одним разом, то из девятнадцати аминокислот можно построить более ста квадриллионов различных веществ с различными же свойствами.
На самом же деле белки состоят из гораздо большего количества повторяемых аминокислот. Гемоглобин, молекулярная масса которого 67 000, состоит из 539 аминокислот. Разумеется, они не могут быть все разными, что в значительной степени снижает количество возможных вариантов, но даже в этом случае получится величина порядка 4 x 10619, то есть четверки с 619 нулями.
Представить себе такое число невозможно. Достаточно просто уяснить себе, что количество различных белков, которые можно построить из девятнадцати аминокислот, как и количество различных книг, которые можно написать с помощью двадцати шести букв латинского алфавита, — для всех практических соображений следует счесть бесконечным.
С точки зрения энергетических соображений значение столь большого числа, с одной стороны, совершенно ясно, а с другой — очень интересно. Сравнительно несложно просто собрать вместе некоторое количество аминокислот, как это сделали Фишер или Качальский. Это равносильно тому, что собрать несколько игральных карт и просто сложить их в стопку не глядя.
Конечно, в стопке карт порядка больше, чем в картах, рассыпанных по полу, то есть и при такой сборке энтропия уменьшается (вспомните отношения между энтропией и порядком, описанные в главе 6). Соответственно, создание пептида из аминокислот — это процесс, связанный с уменьшением энтропии.
Однако образование некоего определенного белка, например гемоглобина, из практически неисчерпаемого набора аминокислот, можно сравнить с упорядочиванием карт в колоде по некоему строго определенному образцу. При этом порядок возрастает (а энтропия, следовательно, уменьшается) многократно. Работа, совершаемая организмом при формировании белка, достойна восхищения, потому что он не просто объединяет аминокислоты в пептидную цепь, но соединяет их в строго заданную пептидную цепь!
Именно поэтому невозможно вывести формулу какого-либо белка путем простого подсчета атомов. Если провести такую попытку, то в результате мы получим что-то вроде C1864H3012O576N468S21. Это, конечно, настоящая формула, и ей соответствует, к примеру, присутствующий в молоке белок беталактоглобулин. Но понять из такого «индекса атомов», из каких аминокислот состоит белок, невозможно, а значит, и пользы в нем практически нет никакой. Молекулу белка надо рассматривать с точки зрения аминокислотного, а не атомного состава.
Простой способ анализа аминокислотного состава белка заключается в том, чтобы путем нагревания в кислоте разложить белок на аминокислоты и проанализировать полученную смесь на наличие каждой из аминокислот по отдельности. К сожалению, смесь получается слишком сложной, а свойства некоторых аминокислот слишком похожи, так что полноценно разделить смесь на отдельные аминокислоты не представляется возможным. До 1940 года анализу аминокислотного состава белков не хватало точности и полноты.
Однако в 1944 году двое английских биохимиков, А. Мартин и Р. Синг, изобрели бумажную хроматографию. Метод заключается в том, чтобы капнуть немного смеси аминокислот на лист очень пористой (фильтровальной) бумаги и дать листу высохнуть, после чего аминокислоты оказываются прочно скованными в листе. Тогда по капиллярам в бумаге начинают вытягивать органическую жидкость, например бутиловый спирт (близкий к известному нам этиловому спирту).
Когда бутиловый спирт проходит через пятно аминокислот, то каждая из них оказывается под действием двух сил: одна — удерживает присохшие кислоты на месте, другая — тянет их двигаться дальше вместе со спиртом. В итоге каждая кислота действует неким компромиссным образом (поскольку каждая из них, благодаря разнице в химическом составе, имеет свой показатель растворимости в воде и в бутиловом спирте). То есть скорость движения аминокислот по листу вместе со спиртом — своя для каждой аминокислоты, и через некоторое время все аминокислоты оказываются «разнесенными» по листу. Вот теперь можно разделить и подвергнуть тщательному анализу составляющие даже очень сложной смеси аминокислот.
С помощью метода бумажной хроматографии большинство белков были проанализированы на аминокислотный состав. К примеру, в таблице 6 приводится количество каждой из девятнадцати аминокислот, обнаруженных в альбумине — белке, встречающемся в плазме крови человека.
Таблица 6.
АМИНОКИСЛОТЫ АЛЬБУМИНА
Аминокислота … Количество в молекуле белка
Глютаминовая кислота … 80
Лейцин … 58
Лизин … 58
Аспарагиновая кислота … 46
Валин … 45
Фенилаланин … 33
Пролин … 31
Треонин … 27
Аргинин … 25
Серии … 22
Тирозин … 18
Цистин … 16
Гистидин … 16
Глицин … 15
Изолейцин … 9
Метионин … 6
Цистеин … 4
Триптофан … 1
Алании … 0
Всего … 510
Разумеется, просто знать количество каждой из аминокислот в молекуле белка недостаточно. Надо было еще установить, в каком порядке они располагаются.
Эта задача казалась вообще неразрешимой. Количество возможных перестановок даже в самых маленьких белковых молекулах так велико, что попытки угадать фактическое их расположение сродни поиску иголки не то что в стоге сена, а в целом поле стогов сена.
Однако в конечном итоге человеческому гению эту задачу удалось решить. Это сделал английский биохимик Фредерик Сенгер со своими коллегами. Сенгер работал с инсулином, молекула которого сравнительно мала — этот белок состоит всего из 50 аминокислот, и его молекулярный вес — всего 6000. (Впрочем, даже и в этом случае количество возможных комбинаций аминокислот, присутствующих в известном соотношении, тоже значительно превышает 10100 — то есть единицу со 100 нулями.)
Методика Сенгера в упрощенном виде выглядит так: молекулу белка расщепляют не полностью, а частично, так чтобы на выходе получались не отдельные аминокислоты, а пептидные цепочки из двух, трех или четырех аминокислот. Порядок аминокислот в этих цепочках уже можно установить, а от них — перейти к порядку аминокислот в более крупных фрагментах, и в итоге — получить порядок аминокислот в самой изначальной цепочке.
Конечно, все это сделать не так просто. В реальности работа оказалась кропотливой, долгой и крайне сложной. Тем не менее к 1953 году (не прошло и десяти лет с момента начала работы) строение инсулина уже было точно установлено. В частности, ученым удалось четко выяснить, чем именно свиной инсулин отличается от бычьего — какая именно аминокислота заменяется на другую.
Затем по этой же методике было установлено строение и других, более сложных белковых молекул. К 1959 году была столь же точно выявлена и структура фермента «рибонуклеаза», в состав которого входит уже 121 аминокислота.
После того как порядок аминокислот в белках был установлен, можно было вплотную приступать к решению загадки столь масштабного уменьшения энтропии, какое имеет место в организме при синтезе строго определенной белковой молекулы. Эта задача оказалась совсем непростой. Процесс построения белка выполняется в несколько шагов, на каждом из которых к строящейся цепочке должна добавляться строго определенная аминокислота, и только она одна. Естественно, в качестве первых целей выбирались самые простые белки. Так, первой искусственно синтезированной молекулой стал окситоцин — гормон гипофиза. Автором этого открытия стали американский биохимик Винсент дю Виньо и его коллеги в 1953 году. Молекула окситоцина миниатюрна по белковым меркам — она состоит всего из восьми аминокислот, так что и белком-то его в принципе можно назвать с натяжкой, однако сам факт был принят научным сообществом с восторгом. Главное — что синтезированный продукт проявил все свойства натурального, и, таким образом, с помощью синтеза на практике было доказано, что молекулярное строение гормона установлено верно.
В 1960 году другой американский биохимик, Клаус Хофман, продвинулся еще дальше, синтезировав цепочку из 23 аминокислот — часть молекулы еще одного продукта гипофиза, адренокортикотрофного гормона.
Вообще, химики с каждым годом добиваются все большего успеха в изучении строения белковых молекул, а если учесть, что реальная работа в этом направлении началась относительно недавно, то в ближайшем будущем можно ожидать в этой области больших достижений.
Но во всем, о чем я до сих пор рассказывал, причина хрупкости белковой молекулы до сих пор не затрагивалась.
Глава 17. СЛАБОЕ ПРИТЯЖЕНИЕ
Можем ли мы быть уверены, что одного лишь большого размера достаточно, чтобы молекула оказывалась столь непрочной? Очевидно, это не так, если взять для примера хоть молекулу целлюлозы — она очень велика, но при этом очень прочна. Да и полипептидная цепочка не обладает повышенной хрупкостью по сравнению с другими длинными молекулярными цепочками, поскольку нам известны белки, состоящие из цепочек аминокислот, связанных пептидными связями, еще менее хрупкие, чем молекулы целлюлозы.
Лучшим примером такого вещества является белок фиброин, имеющий довольно простую для белка структуру. Пять шестых всех составляющих его аминокислот — это глицин, аланин и серии, имеющие самое простое строение. Другие аминокислоты представлены слабо, а пять — отсутствуют вообще. И все же фиброин — это белок, который состоит из аминокислот, скрепленных вместе пептидными связями. Нам это вещество знакомо в первую очередь по волокнам. Оно является главной составляющей шелка. А поскольку шелковая лента прочнее, чем хлопчатобумажная (состоящая по большей части из целлюлозы), то приходится признать, что полипептидная цепочка сама по себе еще не является залогом хрупкости.
И тем не менее факт остается фактом: большинство белковых молекул, в том числе — все ферменты, хоть и состоят из тех же компонентов, что и фиброин, и скреплены воедино теми же связями, все же претерпевают необратимые изменения под воздействием достаточно слабого нагревания. Парадокс: одни и те же составляющие, скрепленные одним и тем же образом, могут оказаться и прочными, как шелк, и хрупкими, как яичный белок.
Более того, получается, что те перемены, благодаря которым сырой яичный белок превращается в твердое белое вещество яичного белка, сваренного вкрутую, не затрагивают ни аминокислот, ни связей между ними — по крайней мере, тех, которые я описал. Тепла, достаточного для того, чтобы сделать яйцо твердым, а фермент — неактивным, оказывается явно мало для того, чтобы разорвать пептидную связь. В денатурированном белке (то есть таком, который не способен более выполнять свои биологические функции) присутствуют все те же пептидные цепочки, состоящие из тех же аминокислот, что и в исходном белке до нагревания.
Разумеется, мы не можем принять представление о том, что тут имеет место что-то мистическое, лежащее вне рациональных законов природы. Если свойства денатурированного яичного белка отличаются от свойств исходного яичного белка, то, значит, между этими двумя веществами есть какая-то разница. Раз молекула белка денатурируется и при этом не разрывается ни одна связь между ее атомами, значит, существуют какие-то более слабые связи, при этом жизненно важные для сохранения особых свойств молекулы, которые разрушаются под воздействием слабых изменений окружающей среды, приводя тем самым к денатурации.
Такое предположение подтверждается и тем фактом, что иногда в денатурированных белках обнаруживаются сочетания белков, не встречающиеся в исходных белках. Чаще всего в этих сочетаниях встречается так называемая «меркаптановая группа», состоящая из атома серы и атома водорода (-S-H) (рис. 25). Она содержится в присутствующей практически во всех белках аминокислоте — цистеине.
Некоторые химические вещества могут вступать в соединение с меркаптановой группой, образуя вещество, выпадающее в виде осадка или растворяющееся, но обладающее при этом характерным цветом. (Химические вещества, используемые для обнаружения определенных атомов или сочетаний атомов с помощью облегчения их визуализации, называются «тестовыми реагентами».) Даже если сам цистеин связан в пептидной цепи, его радикал с меркаптановой группой остается свободным, и те же самые тестовые реагенты, которые вступают в реакцию с чистым цистеином, будут реагировать и с пептидной цепочкой, содержащей цистеин.
Однако многие белки, в состав которых цистеин явно входит (поскольку обнаруживается среди смеси аминокислот, на которые белок распадается под воздействием кислоты), сами по себе в реакцию с тестовыми реагентами не вступают. А вот после денатурации — запросто.
Проще всего предположить, что в природном белке пептидная цепочка имеет такую форму, при которой радикалы части составляющих ее аминокислот направлены не «наружу», а в некую «внутреннюю полость» молекулы. Если эти аминокислоты — цистеин, а следовательно, эти «изолированные» от внешней среды радикалы — меркаптан, то тестовые реагенты просто не могут дотянуться до него, чтобы вступить в реакцию. А после денатурации пептидная цепочка раскрывается, и тестовые реагенты получают доступ к меркаптановой группе.
В процессе денатурации разрушается упорядоченность трехмерной формы пептидной цепочки. Ее звенья принимают произвольное положение в пространстве. Такому увеличению беспорядка соответствует значительное увеличение энтропии. А вот для проведения обратного процесса — формирования искусно сложенного естественного белка из денатурированного — требуется уже уменьшать энтропию, а значит, подобная «ренатурация» практически невозможно (разве что на самой первой стадии процесса). Чтобы можно было представить это положение наглядно — ренатурацией был бы процесс «разваривания» яйца, сваренного вкрутую, обратно в живое яйцо.
Рис. 25. Денатурация пептидной цепочки
Значит, изначальная пептидная цепочка поддерживается в «нужной» форме с помощью неких химических связей, и эти связи настолько слабы, что даже незначительное изменение условий способно их разрушить и тем самым денатурировать белок.
Перед тем как перейти к обсуждению природы этих слабых связей, на которые мы и возложим ответственность как за хрупкость белков, так и за особые свойства ферментов, мне придется сделать небольшое отступление и поговорить о природе химических связей как таковых. Мне придется повторить часть уже сказанного в главе 10, но сейчас подробностей будет гораздо больше.
С самого момента зарождения теории атомов стало ясно, что должна существовать какая-то сила, которая удерживает разные атомы в составе одной молекулы. Более того, тот образ, которым эта сила себя проявляет, оказался индивидуальной характеристикой каждого элемента. К примеру, выяснилось, что один атом водорода никогда не может присоединять к себе более одного чужого атома, один атом кислорода — больше двух других атомов, один атом углерода — больше четырех и так далее.
В 1852 году английский химик Эдуард Франкленд предложил назвать эту способность атомов словом «валентность» (от латинского слова, означающего «способность»). То есть валентность водорода — 1, как и фтора, хлора, брома, йода, натрия и калия. Валентность кислорода — 2, и такой же валентностью обладают сера, магний и кальций. Валентность азота — 3, и в эту же группу входят фосфор, мышьяк и алюминий. Валентность углерода и кремния — 4.
Валентность одного и того же элемента не обязательно всегда одна и та же. К примеру, валентность углерода — в принципе 4, но иногда он имеет валентность 2. Валентность азота — вообще 3, но бывает, что и 5. Валентность железа — 2 или 3; золота — 1 или 3; меди и ртути — 1 или 2 и так далее.
В отношении достаточно простых неорганических веществ вопрос о валентностях не влияет на вид уже устоявшихся формул. Так, железо может соединяться с хлором двумя различными способами. Один атом железа может вступать в соединение как с двумя (дихлорид железа, FeCl2) атомами хлора, так и с тремя (трихлорид железа, FeCl3). В обоих случаях из формулы понятно, с каким именно соединением мы имеем дело, и видно, что в первом случае валентность железа — 2, а во втором — 3.
Однако при переходе к значительно более сложным органическим соединениям введение понятия валентности произвело жизненно необходимую революцию в деле написания формул. Уже в начале XIX века стало ясно, что традиционная схема для органической химии не годится, потому что выяснилось, что совершенно различные вещества могут иметь один и тот же атомный состав.
Первым это обнаружил, к собственному изумлению, немецкий химик по имени Юстус фон Либиг, выделивший в 1823 году вещество, названное им «гремучим серебром». Фон Либиг установил, что молекула этого вещества состоит из четырех атомов — по одному атому серебра, углерода, азота и кислорода. И оказался в недоумении — дело в том, что вещество точно с таким же атомным составом было на тот момент хорошо известно, носило название «изоцианат серебра» и имело абсолютно другие свойства.
Об этом рассказали Берцелиусу, но он отказывался верить услышанному до тех пор, пока сам не открыл два вещества с одинаковым атомным составом, но разными свойствами. Берцелиус назвал такие «родственные» вещества «изомерами», но природа изомерии, как явления, так и осталась на тот момент загадкой.
Ключом к решению стало введенное Франклендом понятие валентности. В 1859 году немецкий химик Фридрих Август Кекуле первым использовал графическое выражение записи формул с учетом валентности каждого элемента. Вот так выглядели в новой записи формулы таких хорошо известных веществ, как вода (H2O), метан (СН4), углекислота (CO2), аммиак (NH3) и хлороводород (HCl):
В составе всех этих веществ атомы водорода (Н) и хлора (Cl) всегда имеют только одну связь, атом кислорода (О) — две, азота (N) — три, углерода (С) — четыре. Эта же система доказала свою работоспособность и в применении к более сложным органическим веществам, таким как сахароза или триптофан. Такая запись получила название «структурная формула», а для записей старого типа, вроде СН4, был принят термин «эмпирическая формула».
Практически сразу стало ясно, что одни и те же атомы вполне можно соединить по-разному, не нарушая законов валентности. Рассмотрим пример первой открытой пары изомеров. Вот как выглядит структурная формула гремучего серебра:
Ag—N=C=O.
(Ag — это обозначение серебра, от латинского «argentum».) А структурная формула изоцианата серебра выглядит так:
Как видно, в обоих случаях валентность атома серебра остается равной 1, кислорода — 2, азота — 3, а углерода — 4.
В более сложных органических соединениях количество вариантов соединения молекул без нарушения принципа валентностей увеличивается многократно и доходит до фантастических величин. К примеру, подсчитано, что с использованием 40 атомов углерода и 82 атомов водорода можно составить более шестидесяти триллионов разных вариантов молекулы.
Вот уже более ста лет химики руководствуются системой Кекуле при составлении возможных вариантов строения новой молекулы и числа ее возможных изомеров. С тех пор, конечно, система во многом была доработана и стала более гибкой, но в основном она все та же и, похоже, останется такой и в обозримом будущем.
Главным недостатком системы валентностей в глазах химиков середины XIX века была ее условность. С чего бы это у кислорода валентность 2, у углерода — 4, а у водорода — только 1? А вот у водорода, натрия и хлора — валентность одинаковая, а все остальные свойства — совершенно разные?
На поверку система валентностей оказалась не такой уж и условной, и доказал это русский химик Дмитрий Иванович Менделеев. В 1869 году он выписал все известные элементы в порядке возрастания атомного веса и наглядно показал, что изменение их свойств в таком расположении подчиняется определенным законам. Расписав все элементы в двухмерной матрице, где элементы со схожими свойствами оказались сгруппированными в столбцы, он получил то, что всем нам сейчас известно как «таблица Менделеева»[5]. В частности, оказалось, что внутри каждого столбца все элементы имеют одинаковую валентность (рис. 26).
К примеру, одновалентные фтор, йод, хлор и бром оказались в одном столбце таблицы; двухвалентные магний, кальций, стронций и барий тоже оказались собранными в одном столбце. Точно так же в одном столбце очутились демонстрирующие валентность 3 или 5 азот, фосфор, мышьяк и сурьма и так далее.
Если же проследить не столбцы, а строки таблицы, то оказывается, что внутри всех строк валентность изменяется одинаковым образом. Взять, к примеру, вторую строку (первую из полных строк таблицы): в порядке возрастания атомного веса в ней перечислены литий, бериллий, бор, углерод, азот, кислород и фтор. Соответственно, валентности этих элементов — 1, 2, 3, 4, 3 (или 5), 2 и 1.
Изобретение периодической таблицы Менделеева стало одной из величайших побед химической теории, заставив ученый мир признать валентность логически неотъемлемым свойством элементов, хотя механизм химических связей все еще продолжал оставаться загадкой.
Затем, примерно в конце века, было обнаружено, что и атом имеет собственное внутреннее строение. Стало известно, что в нем содержатся электроны. Выяснилось, что в середине атома находится крошечное ядро, имеющее положительный заряд, а все остальное пространство атома заполнено облаком отрицательно заряженных электронов, вращающихся вокруг ядра. Ядро атомов каждого элемента характеризуется свойственной только ему величиной заряда. Ядро атома водорода несет минимально возможный заряд, произвольно принятый за 1. Заряд ядра атома углерода в шесть раз больше, поэтому его значение оценивается как 6. Таким же образом значение заряда ядра атома азота принимается за 7, а ядра атома кислорода — за 8. Для всех возможных значений от 1 до 103[6] можно найти свой элемент.
Рис. 26. Таблица Менделеева
В идеале свободный атом имеет ровно столько электронов (заряд каждого из которых равен -1), чтобы уравновешивать положительный заряд ядра. Так, в атоме водорода — 1 электрон, в атоме углерода — 6, в атоме азота — 7, в атоме кислорода — 8 и так далее.
Электроны распределяются по оболочкам, в каждой из которых может содержаться не более определенного их количества. Во внутренней, самой близкой к ядру, оболочке может находиться только 2 электрона, в следующей — уже 8, в следующей — 18 и так далее. Так, если атом углерода имеет 6 электронов, то они должны быть распределены по двум оболочкам — 2 во внутренней и оставшиеся 4 — во внешней. А у атома хлора — 17 электронов, значит, они должны быть распределены уже между тремя оболочками — 2 во внутренней, 8 в средней и оставшиеся 7 — во внешней.
Теперь все закономерности таблицы Менделеева становятся понятны. Взять, к примеру, седьмой столбец: первым в нем идет атом фтора — его 9 электронов поделены между двумя оболочками, внешняя из которых содержит 7 электронов; затем — атом хлора, его 17 электронов поделены уже между тремя оболочками, но внешняя опять же состоит из 7 электронов; 35 электронов брома распределяются уже между четырьмя оболочками, но и тут на внешнюю оболочку приходится только 7 из них. И во внешней (пятой) оболочке йода, имеющего в своем составе 53 электрона, тоже находятся 7 электронов. Свойства этих элементов близки потому, что все они имеют по 7 электронов во внешней оболочке.
Чем глубже химики XX века проникали в предмет, тем обыденнее в химических записях становилось обозначение, при котором элемент маркируется не только обычным символом, но и количеством электронов в его внешней оболочке. К примеру, водород, обладающий всего одним электроном, обозначается как H•.
Углерод, всего имеющий шесть электронов, но во внешней оболочке — только четыре, обозначается как
В таблице 7 приведены «электронные» записи некоторых особо важных для живой материи элементов.
Что касается легких элементов, вроде перечисленных в таблице 7, самым стабильным является случай, когда во внешней оболочке находится восемь электронов. Важным исключением является гелий, имеющий всего одну оболочку с максимальным числом возможного вмещения электронов — 2. Конечно, для него самым стабильным вариантом является случай с двумя электронами во внешней оболочке.
Теперь давайте рассмотрим натрий. Его 11 электронов распределены следующим образом: 2 — во внутренней оболочке, 8 — в средней и 1 — во внешней. Если атом натрия потеряет 1 электрон, то его внешней оболочкой станет средняя, в которой как раз 8 электронов, то есть будет достигнуто стабильное положение. Поэтому атом натрия весьма склонен терять «лишний» электрон.
Таблица 7.
ЭЛЕКТРОННЫЕ ОБОЗНАЧЕНИЯ
Противоположную картину представляет собой атом хлора — его 17 электронов распределены между оболочками следующим образом: 2, 8 и 7. При таком распределении для того, чтобы внешняя оболочка имела 8 электронов, нужно, наоборот, где-то «добыть» недостающий, восьмой.
Понятно, что с такими потребностями атом натрия и атом хлора имеют прямо противоположные, дополняющие друг друга стремления. Если они случайно столкнутся, атом первого легко отдаст электрон атому последнего, и в результате оба обретут более стабильное состояние. Потеряв электрон, атом натрия потеряет и электрический баланс, ведь теперь отрицательный заряд его электронов окажется недостаточным, чтобы уравновешивать положительный заряд ядра, равный по-прежнему 11, тогда как суммарный заряд электронов атома теперь равняется всего лишь -10. Соответственно, весь атом натрия теперь является носителем общего заряда в +1, превратившись, таким образом, в положительно заряженный ион натрия, Na+.
С другой стороны, атом хлора, получив дополнительный электрон, теперь имеет 18 отрицательно заряженных электронов с суммарным зарядом, соответственно, -18, и ядро с положительным зарядом всего 17. Так что общий заряд атома хлора теперь -1, и он превратился в отрицательно заряженный ион хлора Сl-. Так в XX веке, на основании новых представлений о строении атома, был окончательно постигнут механизм формирования ионов, выдвинутый еще в XIX веке как теория, объясняющая функционирование электрической батареи (см. главу 10).
Положительно заряженный ион натрия и отрицательно заряженный ион хлора удерживаются вместе силой электростатического притяжения, существующего между разнонаправленно заряженными частицами, и в результате получается соединение NaCl. Связь, образованная таким образом, называется «ионная связь».
Понятно теперь, почему валентность натрия — 1, ведь у него есть только один электрон, избавившись от которого атом достигнет стабильности в их распределении. И понятно, почему валентность у хлора 1, поскольку для той же самой стабильности ему достаточно получить 1 атом. Вот кальцию и магнию надо будет для того же самого избавиться уже от двух электронов, поэтому и валентность каждого из них равна 2. У кислорода же во внешней оболочке 6 электронов, и для обретения стабильности ему надо присоединить 2, так что его валентность — тоже 2. Если атом кальция отдаст свои два электрона атому кислорода, то и получившийся ион кальция, Са2+, и получившийся ион кислорода, О2-, обретут стабильное состояние в составе образовавшегося вещества с сильной внутренней ионной связью, СаО (оксид кальция — негашеная известь).
Однако для образования межатомной связи совсем не обязательно, чтобы один атом отдавал свой электрон другому. Вот, например, два атома хлора — что удерживает их вместе? Каждому из них не хватает одного электрона, оба в равной степени склонны к приобретению электронов, и ни один не собирается свой электрон отдавать. В общем, невероятно, чтобы в молекуле, состоящей из двух атомов хлора, один из них вдруг поступился собственным электроном в пользу второго.
Этого и не происходит — вместо этого атомы «по-братски» формируют общий для них обоих пул электронов. Чтобы показать наглядно, как это происходит, давайте обозначим электроны одного из них как точки, а второго — как крестики. Еще раз повторюсь — это делается исключительно для удобства восприятия и ни в коем случае не должно восприниматься как свидетельство каких-либо качественных различий между электронами первого и второго атома. Насколько известно, все электроны всех атомов одинаковы. Итак, соединение двух атомов хлора в молекулу хлора можно обозначить так:
В составе молекулы хлора 2 атома хлора обладают все теми же 14 электронами внешних оболочек в сумме; никаких новых электронов в систему не добавлено. Однако 2 электрона, представленные на схеме, как находящиеся посередине между атомами (один — точкой, а второй — крестиком), одновременно принадлежат внешней оболочке и того и другого атома. Соответственно, во внешней оболочке каждого из атомов находится по 8 электронов, и состояние двухатомной молекулы гораздо стабильнее, чем состояние двух отдельных атомов. И поскольку находиться в двух внешних оболочках одновременно электроны могут только в том случае, когда атомы прижаты друг к другу, то для того, чтобы растащить атомы в стороны, то есть перевести их от более стабильного состояния к менее стабильному, требуется затратить энергию.
Другими словами, формирование молекулярного хлора из атомов хлора сопровождается снижением уровня свободной энергии и является, таким образом, спонтанной реакцией. А разложение молекулы хлора требует увеличения свободной энергии, а значит, спонтанно протекать не может.
Роль связки между атомами выполняет в данном случае пара «общих» электронов. Такая связь называется «ковалентной», и именно такую природу имеет большинство связей в органических соединениях.
Метан (СН4) с электронной точки зрения можно рассматривать как сочетание атома углерода, с его четырьмя электронами во внешней оболочке, с четырьмя атомами водорода, каждый из которых имеет единственный электрон.
Атом углерода каждый из своих электронов передает в общее пользование с одним из атомов водорода, а каждый из атомов водорода, в свою очередь, тоже предоставляет собственный электрон в общее пользование. В результате каждый атом водорода имеет по два электрона в своей единственной оболочке (которая обретает, таким образом, стабильное состояние), а внешняя оболочка атома углерода тоже получает стабильное число 8.
Правильное «обобществление» внешних электронов позволяет объяснить все факты, ранее объяснявшиеся через систему прямолинейных связей Кекуле, и, более того, через электроны оказалось возможным объяснить некоторые факты, перед которыми изначальная система формул Кекуле оставалась бессильной.
Вот, к примеру, два атома хлора, составляющие молекулу хлора, одинаковые и электроны держат одинаково крепко. Поэтому и «общие» электроны они распределяют между собой поровну. Атомы водорода и углерода тоже удерживают свои атомы с примерно равной силой, так что и в метане «общие» атомы распределены примерно поровну.
А вот в случае ковалентных связей между водородом и кислородом все несколько по-другому. Атом кислорода с атомом водорода тоже формируют «общую» пару электронов, но при этом атом кислорода, крепче удерживающий свои электроны, будет сильнее перетягивать их в свою собственную внешнюю оболочку, так что оболочке атома водорода электроны будут принадлежать в несколько меньшей степени.
Рис. 27. Поляризованная молекула воды
А раз атом кислорода перетягивает на себя больше половины «общих» электронов, то и отрицательный заряд их большей частью придется на атом кислорода. Соответственно, атом кислорода в целом будет иметь отрицательный электрический заряд дробного значения, а «обделенный» электронами атом водорода — положительный заряд ровно такого же значения.
Соответственно, молекула воды будет обладать небольшим перекосом положительного заряда в сторону водорода и отрицательного — в сторону кислорода, как это показано на рис. 27. Молекулы, в которых наблюдается подобное, называют «полярными», поскольку полюса электрического заряда — водород и кислород — можно рассматривать в них как полюса магнита. А молекулы вроде хлора или метана, где четкой концентрации заряда на конкретных участках не наблюдается, являются «неполярными».
Электрические заряды противоположной направленности двух различных поляризованных молекул будут притягивать друг друга, так же как и противоположно заряженные ионы. Другими словами, молекулы воды в жидком состоянии этого вещества (а во льду — тем более) склонны принимать такое положение, чтобы отрицательно заряженная кислородная часть одной молекулы прилегала к положительно заряженной водородной части молекулы соседней.
Значения зарядов полярных молекул, в которых заряд одного и того же электрона просто оказывается неравномерно распределенным, — гораздо меньше, чем в тех случаях, когда речь идет о полноценной передаче электрона от одного атома к другому. Поэтому и притяжение между полярными молекулами гораздо слабее, чем ионная связь. Эти межмолекулярные притяжения на самом деле в двадцать раз слабее ковалентных связей.
Однако этого оказывается достаточно, чтобы, например, молекулы воды «липли» друг к другу и, соответственно, требовалось гораздо больше энергии на разрыв этих межмолекулярных связей (имеется в виду растапливание льда или выпаривание воды), чем для произведения тех же самых действий в отношении, например, метана.
Поэтому, хотя молекулы метана и воды имеют приблизительно одинаковые размер и сложность строения, температура плавления метана -184 °С, а воды — 0°С; а температура кипения этих веществ -161°С и +100°С соответственно.
Сильнее всего межмолекулярные силы притяжения проявляются тогда, когда в состав молекулы входит положительно заряженный атом водорода, поскольку его размеры настолько малы (водород — самый маленький атом), что он может ближе всего подойти к атомам с сильным отрицательным зарядом (например, кислороду, азоту или фтору). Поскольку известно, что электростатическое притяжение изменяется обратно пропорционально квадрату расстояния между центрами атомов, то понятно, что чем меньше расстояние, тем больше сила притяжения.
Рис. 28. Водородная связь
Рис. 29. Соединение аминокислот
Соответственно, достаточно сильными, чтобы вообще оказаться замеченными, силы межмолекулярного притяжения являются только в тех случаях, когда между двумя отрицательно заряженными атомами оказывается атом водорода. Поэтому такая связь получила название «водородная связь» (рис. 28).
Сразу же становится понятно, какое отношение все вышеизложенное имеет к строению белка. Для начала давайте рассмотрим строение аминокислоты в отображении по системе Кекуле:
Соединение NH2, изображенное слева, — это аминогруппа; соединение СООН справа — это карбоксильная группа. R, прикрепленное к центральному атому углерода, — это радикал, для каждой конкретной аминокислоты — свой.
Когда соединяются две аминокислоты, то карбоксильная группа одной теряет ОН, а аминогруппа другой — Н. Высвободившиеся части тут же объединяются в молекулу воды. А лишившиеся части атомов аминокислоты тоже объединяются с использованием тех связей, которые освобождаются от ОН и Н соответственно. Этот процесс хорошо показан на рис. 29.
Пептидная связь, соединяющая аминокислоты, имеет, как видите, вот такое строение:
Если представить, что цепочка аминокислот в каком-то трехмерном пространстве наложится сама на себя, то вполне может возникнуть ситуация, когда водород, крепящийся к азоту одной пептидной связи, окажется по соседству с кислородом, крепящимся к углероду другой пептидной связи. А если атом водорода находится между атомами азота и кислорода — то мы имеем идеальные условия для возникновения водородной связи. Один из вариантов такой ситуации изображен на рис. 30, и, как видите, при нем вполне воспроизводится ситуация, продемонстрированная на рис. 25. Водородная связь и есть та «слабая связь», о которой я упоминал.
Рис. 30. Водородная связь и пептидная цепочка
В 1936 году американские биохимики Лайнус Полинг и А.Е. Мирски предположили, что именно присутствие в молекуле белка водородных связей делает ее столь хрупкой. Получается, что за особые свойства белка отвечает не только схема аминокислотной цепочки (какие именно аминокислоты и в каком порядке представлены), но и ее трехмерная структура, определяемая водородными связями.
На прочные ковалентные связи, которыми скреплена пептидная цепочка, легкое нагревание действия не окажет, но вот водородные связи, которые в двадцать раз слабее, вполне может разорвать. Из «правильно сложенной» аминокислотная цепочка превращается в таком случае в «свободно болтающуюся», и в результате мы имеем денатурированный белок, утративший свойства белка природного.
Но для того, чтобы понять, как именно должна быть «сложена» аминокислотная цепочка, надо сперва уяснить геометрию молекулы вообще. Насколько удалены друг от друга атомы в молекуле? Какие положения относительно друг друга они занимают? Иными словами — насколько длинными являются межатомные связи и под какими углами друг к другу они расходятся? Можно написать на бумаге двухмерную структурную формулу, но ведь на самом деле структура молекул трехмерна!
Ответ на эти вопросы пришел только с использованием рентгеновских лучей. Если направить пучок рентгеновских лучей на кристалл какого-либо вещества, то упорядоченные слои атомов, составляющие кристалл, частично отразят их. По результатам анализа этого отражения и можно подсчитать расстояние между похожими атомами в структуре кристалла. А там недалеко уже до того, чтобы вывести и саму структуру кристалла.
Этот метод основан на том факте, что облучаемый рентгеновскими лучами объект состоит из упорядочение расположенных атомов. В начале 20-х годов XX века было проведено исследование волокон шелка с помощью рентгеновских лучей. Шелк, разумеется, не кристалл, но и строение его аминокислотных цепочек оказалось в достаточной степени упорядоченным, чтобы произвести соответствующее отражение лучей. Полученные данные позволили показать, к примеру, что длина одной аминокислотной составляющей пептидной цепочки — 0,35 миллимикрона. Отсюда стало возможно высчитать и длину отдельных связей и углы между ними. Затем в 30-х годах XX века с помощью той же технологии были исследованы и другие белки, например содержащийся в волосах кератин.
Рис. 31. Спиралевидная молекула
В начале 50-х годов Полинг с коллегами показали на основании полученных данных, что пептидные цепочки могут сворачиваться в спираль (похожую на спираль винтовой лестницы), не теряя при этом ни одной из своих естественных связей. Спиралевидная форма предоставляет прекрасные возможности для образования водородных связей. Более того, несколько таких спиралей могут и сами сворачиваться в спираль (так же, как канат может состоять из нескольких волокон, скрученных таким же образом, как и он сам, из других, более тонких, волокон), и в этом случае опять же вся структура удерживается в нужной форме с помощью водородных связей (рис. 31).
Эта гипотеза нашла экспериментальное подтверждение, и сейчас представление о спиралевидном строении белковых молекул является общепринятым.
Глава 18. КАК РАБОТАЮТ ФЕРМЕНТЫ
Тот факт, что белковые молекулы имеют спиралевидную форму, удерживаемую водородными связями, объясняет не только хрупкость молекулы фермента и легкость, с которой она теряет свои свойства, но и огромную вариативность этих самых свойств.
Давайте сравним платиновый порошок и молекулу фермента. Как я уже объяснял в главе 12, каталитические способности платины, возможно, объясняются тем, что она имеет свободные валентные связи, с помощью которых притягивает к себе молекулы тех веществ, реакцию которых катализирует. Такое связывание происходит несколько активнее, если поверхность платинового катализатора имеет неправильную форму, — поскольку молекулы реагирующих веществ также имеют неправильную форму, то им может оказаться естественнее плотно прилечь там, где форма поверхности платины соответствует их собственной.
На поверхности платины возможны любые неправильности, поэтому для любой молекулы там окажется соответствующая форма. В результате множество различных молекул могут оказаться временно привязанными к поверхности платины, где они, соответственно, с готовностью вступают в реакцию с другими молекулами. Поэтому платина, как и все прочие катализаторы такого рода, способна охватывать своим действием сравнительно большое число веществ. Но у катализаторов такого рода есть и недостаток — поскольку в каждом отдельно взятом веществе они действуют далеко не на всю площадь (а только на ту ее часть, неправильность формы которой соответствует неправильности формы реагирующих молекул), то и коэффициент полезного действия таких молекул невелик. Для каждого отдельно взятого вещества большая часть поверхности катализатора оказывается неиспользуемой.
С ферментами все обстоит по-другому. Их поверхность имеет не случайную форму, а, напротив, строго упорядоченную с помощью биохимических процессов, происходящих в организме. Чередующиеся радикалы разных аминокислот, составляющих пептидную цепочку, представляют неправильности всех типов и размеров. Некоторые из радикалов, например аспарагиновая кислота или глютаминовая кислота, обладают отрицательными зарядами и будут притягивать любой положительный заряд, как только в пределах досягаемости окажется несущая такой заряд молекула. Другие же, например лизин, аргинин или гистидин, обладают положительным зарядом и будут притягивать молекулы с отрицательными. Третьи, например серии, треонин или тирозин, электрически нейтральны, зато имеют в своем составе группы, способные к образованию водородных связей.
Что же касается радикалов, не образующих связей, например валина, аланина, лейцина, изолейцина, фенилаланина и еще нескольких, то их роль в данном случае защитная; они служат барьерами для того, чтобы только молекулы строго определенной формы могли проникнуть в зону досягаемости тех радикалов, которые смогут их ухватить.
Все радикалы находятся друг к другу в строго определенном отношении, зафиксированном водородными связями, удерживающими молекулу в жесткой форме. В результате к определенному ферменту может присоединиться молекула только строго определенного вида, и только такая молекула в дальнейшем вступит в катализируемую ферментом реакцию. Молекула, подвергающаяся реакции, катализируемой ферментом, именуется субстратом этого фермента. Разумеется, любое воздействие на фермент, приводящее к разрыву водородных связей и установленных для него отношений между радикалами, приведет к потере ферментом его уникальных каталитических свойств.
У такой строгой специфичности молекулы фермента есть одно интересное следствие. Стоит лишь задуматься о химических механизмах жизни как таковой, как становится ясно, что функционирование организма зависит от бесперебойной работы тысяч различных химических реакций с участием множества веществ. Если ферменты настолько специфичны, то означает ли это, что каждый организм — да что там организм, что каждая клетка в организме! — должен быть полон различных ферментов, каждый из которых необходим для одной-единственной реакции?
Да. Так оно и есть. Хоть клетка и имеет крайне малый объем, около 0,03 мм в диаметре, она все же гораздо больше, чем молекула белка. В клетке достаточно места для тысяч различных ферментов. Более того, места хватит для тысяч молекул каждого из них.
На первый взгляд это совершенно неразумная избыточность. Но на самом деле — ровно наоборот, экономичность и эффективность такой системы выше всяких похвал.
Каждый фермент, имеющий строго определенную задачу, обладает гораздо большей полезной площадью поверхности, чем случайным образом оформленная платиновая частица. Он гораздо эффективнее.
Скорость катализируемой реакции измеряется «оборотным числом». Оборотное число — это количество молекул субстрата, ежеминутно подвергающихся реакции при заданной температуре под действием одной молекулы фермента. Фермент каталаза, катализирующий распад перекиси водорода на воду и кислород, имеет оборотное число 2 500 000 при 0 °С. Оборотные числа большинства ферментов ниже, чем каталазы, но все равно многократно выше, чем у катализаторов неферментного происхождения.
Предположим, что различные ферменты в некотором порядке распределены по клетке (а так оно и есть, как мы увидим позже), и тогда движущиеся по клетке субстраты каждую секунду систематически улавливаются и подвергаются преобразованиям.
Кроме того, наличие множества специализированных катализаторов, а не нескольких общих, предоставляет организму возможность тончайшего управления клеточной химией. Уменьшая или увеличивая число молекул того или иного фермента в клетке, можно ускорять или замедлять ход той или иной реакции — одной из тысяч, и только ее.
Если в живом организме ежесекундно проходят тысячи различных реакций взаимодействия, независимо контролируемые тысячами различных ферментов, то выходит, что даже самые примитивные формы жизни устроены сложнее, чем самые сложные рукотворные механизмы.
Факт в том, что живая клетка состоит из гораздо большего количества движущихся деталей, так сказать, чем любое творение рук человеческих, и лишь микроскопически малый размер этих деталей позволяет нам свысока утверждать, что клетка — это «всего лишь» микроскопическая капелька. А если мы говорим о целых организмах, состоящих из триллионов клеток, то тут сложность всей конструкции возрастает до неописуемых величин. Нелепы были бы попытки сравнить ящерицу с камнем (разве что по параметру физического размера). Поэтому я даже не буду задерживаться на сравнивании человека со звездой — понятно, что сравнение будет не в пользу звезды.
Разумеется, в основе вышеприведенного анализа каталитической деятельности ферментов лежит представление о том, что субстрат вступает с ферментом в физический контакт и образует некий промежуточный комплекс «субстрат-фермент». Сложно избежать этого допущения, потому что иначе пришлось бы предположить, что фермент оказывает на молекулу некое бесконтактное воздействие — а ученые не любят бездоказательной мистики.
К тому же имеются убедительные, хоть и косвенные, свидетельства в пользу такого предположения. К примеру, предположим, что в раствор фермента добавили немного субстрата. Реакция начинается сразу же, и химики могут определить скорость, с которой исчезает субстрат или появляется итоговое вещество реакции, — так они получают скорость реакции. Если в тот же раствор фермента добавить больше субстрата — скорость реакции будет выше. Можно воспользоваться такой аналогией: если в супермаркет запустить больше покупателей, то они начнут выносить больше товаров. Если одномоментно удвоить количество покупателей в супермаркете, то логично ожидать, что и товары с полок будут исчезать в два раза быстрее. Вот по тому же принципу удваивается и скорость реакции, если удвоить концентрацию субстрата.
Однако все это верно лишь до определенного момента. По достижении некоторой концентрации субстрата скорость реакции достигает максимума и выше уже не поднимается, сколько субстрата ни добавляй (рис. 32). Аналогия с супермаркетом здесь не теряется — потому что скорость раскупания товара тоже не может возрастать вечно. Как только забиваются кассы, дальнейшее увеличение количества покупателей приводит только к удлинению очередей.
Рис. 32. Зависимость скорости реакции от концентрации субстрата
Точно так же, когда концентрация субстрата достигает такого значения, что каждая молекула фермента работает на полную мощность, дальнейшее добавление субстрата приводит только к увеличению, так сказать, очередей его молекул, стоящих в очереди на обслуживание ферментом. Наблюдаемое явление проще всего объяснить именно через формирование субстратом и ферментом некоего промежуточного комплекса, что и сделал в 1902 году французский химик В. Анри.
В 1913 году двое немецких биохимиков, Леонор Михаэлис и М.Л. Ментен, приняли это предположение и подвергли его математическому анализу наподобие того, что используется химиками при расчете скоростей обычных реакций. В итоге у них получилось уравнение, описывающее изменение скорости реакции в зависимости от концентрации субстрата, — и математическая модель в точности совпадала с экспериментальными данными. В ходе наблюдений за конкретными реакциями ученые сумели с помощью своих уравнений рассчитать силу, привязывающую определенный субстрат к соответствующему ферменту. С тех пор для подобных целей всегда используются уравнения Михаэлиса— Ментена.
Тот факт, что на основе некоторого допущения можно разработать математическую модель, результаты которой в точности соответствуют экспериментальным данным, конечно, не является однозначным доказательством истинности этих допущений. Но некоторое свидетельство в их пользу все же представляет.
Еще одно подтверждение пришло совсем с другой стороны. Предположим, что строение некоего субстрата очень похоже на строение другого вещества. Что произойдет, если это вещество добавить в раствор фермента вместо нужного субстрата? Так сделал в 1930 году биохимик Дж.Г. Кастел, работая с ферментом, субстратом для которого является янтарная кислота (рис. 33).
По структурной формуле янтарная кислота очень близка к другому веществу, малоновой кислоте (рис. 33). Если в раствор фермента добавить вместо янтарной малоновую кислоту, реакции не происходит. У малоновой кислоты отсутствует одна группа СН2, и этого достаточно, чтобы фермент безошибочно различал их.
Но нельзя сказать, что на добавление малоновой кислоты фермент не реагирует вообще никак. Если сначала добавить в него малоновую кислоту, а потом уже в смесь малоновой кислоты и фермента добавить янтарную кислоту, то реакции опять-таки не будет. Малоновая кислота «отравляет» фермент, или, если выражаться рациональнее, подавляет его действие.
Напрашивается вывод, что молекула малоновой кислоты достаточно похожа на молекулу янтарной, чтобы занять ее место на активной поверхности фермента, но недостаточно похожа, чтобы реакция стала осуществляться дальше. Связь малоновой кислоты с ферментом оказывается достаточно сильной, чтобы не распадаться. Это как если в замочную скважину вставить несоответствующий ключ и сломать его внутри. Теперь дверь нельзя открыть ни этим ключом, ни соответствующим. На самом деле механизм улавливания ферментом конкретного субстрата так и именуется — «замочный механизм».
Рис. 33. Молекулы-конкуренты
Малоновая кислота — ингибитор, угнетающее вещество, — конкурирует с «законной» янтарной кислотой за место на рабочей поверхности фермента, поэтому весь процесс носит название «конкурентное ингибирование». С 1930 года изучено уже множество случаев конкурентного ингибирования. Были внесены изменения даже в уравнение Михаэлиса—Ментена для расчета формирования соединений фермента с ингибитором, а не только с субстратом, и снова математические расчеты совпали с экспериментальными данными.
Конкурентное ингибирование может быть методом управления скоростью реакций, катализируемых ферментами в тех случаях, когда по какой-либо причине невозможно физически удалить сам фермент или, наоборот, интенсифицировать его производство. Существует ряд групп важных для организма веществ, сходных по своему строению. Аминокислоты валин, лейцин и изолейцин — похожи. Сахара глюкоза и галактоза — похожи; и так далее. Отношения конкурентного ингибирования между ними практически неизбежны. Похоже, что присутствие в клетке этих веществ в различных соотношениях постоянно производит конкурентное ингибирование тех или иных ферментов в зависимости от их относительной концентрации, таким образом оказывая тонкое влияние на биохимию клетки, изменяя ее в нужную сторону или, наоборот, поддерживая ее в правильном состоянии. Получается своего рода автопилот на молекулярном уровне.
Гораздо более впечатляющих результатов можно добиться с помощью намеренного добавления в организм некоторых веществ. Такие вещества могут иметь лабораторное происхождение и быть полностью чужеродными живой ткани. Такого рода намеренное конкурентное ингибирование позволяет провести различие между организмами даже в том случае, если они тесно переплетены между собой, как, например, паразитирующая бактерия и зараженный организм носителя.
Действие многих ядов обусловливается именно их активным вмешательством в деятельность множества ферментов. Например, такой яд, как дихлорид ртути (сулема), может убить вообще все живое — и микробы, и больного.
А вот если использовать конкурентное ингибирование, то можно вывести из строя один, и только один фермент из всех присутствующих в клетке. При правильно подобранной дозировке можно добиться, чтобы фермент бактерии прекратил свою деятельность, а ферменты человека практически не пострадали — частично из-за повышенной чувствительности фермента бактерии, частично благодаря тому, что ингибитор легче проникнет сквозь клеточную мембрану бактерии, чем человека. А может оказаться и так, что один и тот же фермент нужен больше бактерии, чем человеку, по причине разницы в механизмах обмена веществ.
Первым важным примером такого рода стал сульфаниламид (рис. 34), вещество, впервые синтезированное в 1908 году. В 1932 году один немецкий биохимик занимался исследованием различных красителей на предмет того, могут ли они убивать бактерии, не нанося при этом существенного вреда высшим организмам. Одно из исследуемых веществ, под названием «пронтосил», оказалось очень эффективным средством против некоторых видов стрептококков, о чем и было заявлено на весь мир в 1934 году.
Будучи введенным зараженной лабораторной мыши, пронтосил оказывал свое действие, но вот в пробирке бороться с бактериями отказывался. Соответственно, возникло предположение, что реальную пользу оказывает не сам пронтосил, а некое вещество, формируемое организмом на его основе. Французские биохимики разложили молекулу пронтосила и получили, в частности, составляющую, оказавшуюся сульфаниламидом. Вот она-то и оказалась эффективным средством борьбы с бактериями как в живом организме, так и в лабораторной пробирке.
Так было получено первое из целого ряда «чудо-лекарств», которые в течение одного поколения позволили человеку покончить с инфекционными заболеваниями, довлевшими над ним на протяжении всей истории.
Рис. 34. Молекулы-конкуренты
Как выяснилось, сульфаниламид по структуре своей похож на вещество под названием «парааминобензойная кислота» (рис. 34), которое является важной составляющей всех клеток. Он конкурентно подавляет фермент бактерии, работающий с этим веществом, и, таким образом, убивает бактерию.
С тех пор было разработано много других антибиотиков (пенициллин, стрептомицин и т. п.), каждый из которых работает, очевидно, посредством того или иного конкурентного подавления, хотя какие именно ферменты подавляются в том или ином случае, биохимики пока сказать не могут.
«Замочный механизм», позволяющий ферменту отличать одно вещество от другого, выглядит особенно примечательно в свете «оптически активных соединений». Последний термин необходимо пояснить, чем я сейчас и займусь, — а начну со света.
С давних пор было известно, что луч света, переходя из воздуха в другую прозрачную среду, например воду, — преломляется. Однако в 1670 году датский физик Эразм Бартолин обнаружил, что кристалл исландского шпата (разновидность карбоната кальция, СаСО3) преломляет луч света двумя разными способами одновременно, формируя таким образом два луча из одного. Это явление получило название «двойная рефракция».
Явление двойной рефракции не могла объяснить ни одна теория на протяжении более ста лет. Однако в начале XIX века было установлено, что свет ведет себя так, как если бы он состоял из крошечных волн, и с такой точки зрения вопрос о двойной рефракции достаточно быстро оказался решенным.
В обычном луче света, например исходящем от солнца или любого другого нагретого предмета, световые волны колеблются во всех возможных направлениях. Одни колеблются вверх-вниз, другие — влево-вправо, третьи — где-то между первыми и вторыми… Но упорядоченная атомная структура исландского шпата (напомню — теория атомного строения тоже утвердилась в начале XIX века) оставила световым волнам возможность колебаться только в двух направлениях, под прямым углом друг к другу.
Соответственно, при попадании в кристалл формируются два вида световых лучей — в одном из них волны колеблются только вверх-вниз (к примеру), а в другом — только влево-вправо. У этих двух лучей разные свойства, и они преломляются с разным углом, поэтому попадающий в кристалл луч разделяется надвое.
Луч света, волны которого колеблются только в одной плоскости, называется «поляризованным». Этот довольно неудачный термин ввел французский инженер Этьен Луи Малюс, открывший в 1810 году, что волна света, отраженного от стекла под определенным углом, тоже начинает колебаться только в одной плоскости.
Рис. 35. Призма Николя
Были разработаны методы определения того, в какой именно плоскости колеблется свет конкретного луча; автор метода, лучшего из всех, изобретенного в 1828 году, — британский физик Уильям Николь. Он составил вместе две призмы исландского шпата и склеил их канадским бальзамом таким образом, чтобы один из поляризованных лучей проходил насквозь, а второй — отражался по линии соединения. Получался только один, поляризованный, луч (рис. 35).
Исходящий луч может пройти еще через одну призму Николя, если она ориентирована точно параллельно первой. Если вторую призму Николя начать медленно вращать, то будет видно, что сквозь нее проходит все меньше и меньше поляризованного света, до тех пор, пока вторая призма Николя не окажется под прямым углом по отношению к первой — тогда свет не сможет проходить вообще. Устройство с двумя такими призмами называется «поляриметр». Сейчас вместо дорогих и громоздких призм Николя используются пластиковые листы, внутри которых находятся правильным образом ориентированные органические кристаллы. Их называют «поляризационными светофильтрами».
Рис. 36. Оптическая активность
Если луч поляризованного света проходит по пути из одной призмы Николя в другую через воздух или воду, с плоскостью его колебания ничего не происходит. Сквозь вторую, параллельно ориентированную, призму свет проходит без каких-либо существенных изменений.
Однако в 1815 году французский физик Жан Батист Био обнаружил, что если поляризованный свет проходит сквозь кристалл кварца, то плоскость его колебаний при этом изменяется. После того как поляриметр был доработан, оказалось, что свет, пропущенный через кристалл кварца, становится заметно тусклее, проходя через вторую призму Николя, — ее опять приходилось вращать до тех пор, пока она не оказывалась ориентированной параллельно новой плоскости колебаний световой волны, измененной под влиянием кварца. Угол этого изменения можно измерить с достаточной точностью по изменению угла ориентации второй призмы Николя, необходимого для того, чтобы свету вернулась прежняя яркость (рис. 36).
Кроме того, Био показал, что и при прохождении поляризованного света сквозь растворы некоторых органических веществ, например скипидара или камфоры, плоскость его колебаний тоже может изменяться. Именно это свойство вещества и именуется «оптической активностью». Био считал, что причиной ее должна служить какая-то асимметрия в структуре оптически активных веществ, приводящая к искривлению луча света всегда в одном и том же направлении. По его мнению, в «симметричных» веществах плоскость колебаний света тоже искривляется, но одинаково во всех направлениях, так что внешне никаких изменений незаметно.
В 1848 году молодой французский химик Луи Пастер (тогда ему было только двадцать шесть лет, и ему еще предстояло сделать одну из самых блестящих карьер в научном мире) ошеломил ученую общественность тем, что доказал, что так оно и есть — но крайней мере, в отношении кристаллов (рис. 37). На примере кристаллов виннокислого аммония он обнаружил, что кристалл выделяется в двух видах, оба из которых асимметричны и являются точным зеркальным отражением друг друга, так же как руки и ноги человека.
Рис. 37. Двусторонняя асимметрия
Пастер очень осторожно, с помощью микропинцета и увеличительного стекла, разделил кристаллы на две кучки — левосторонние в одну, правосторонние в другую, — и оказалось, что раствор каждой из этих кучек проявляет свойство оптической активности! Если же оба раствора смешать, то в получившейся смеси оптической активности не наблюдается.
Разделение равномерной смеси кристаллов обоих видов надвое по разделительному признаку — это увеличение упорядоченности, а значит — уменьшение энтропии. В нашем примере с игральными картами это равносильно тому, чтобы взять перетасованную колоду и рассортировать на две половины, красные отдельно, черные отдельно. Перед нами, кстати, замечательный пример того, как локальное уменьшение энтропии происходит за счет ее глобального увеличения. Пастеру приходилось напряженно вглядываться в увеличительное стекло и аккуратно брать кристаллики микропинцетом. Понятно, что увеличение его энтропии имело гораздо большее значение, чем произведенное им уменьшение энтропии среди кристаллов.
Так или иначе, Пастер сумел доказать наличие асимметрии только для кристаллов. А в растворах оптически активные вещества представлены в виде молекул. Так где же там может скрываться асимметрия? В самих молекулах, что ли?
Правильный ответ — да! Он был получен в 1874 году, когда двое молодых химиков, голландец Якоб Хендрик Вант-Гофф (двадцать два года) и француз Жозеф Ашиль ле Бель (двадцать семь лет) независимо друг от друга выдвинули новую теорию атома углерода, с помощью которой удалось усовершенствовать систему записи формул Кекуле с учетом некоторых новых фактов.
При изображении структурных формул по методике Кекуле четыре связи, которыми обладает углерод, принято рисовать торчащими во все четыре стороны, что естественно для двухмерного изображения. Однако такой вид не отражает реальности, поскольку если бы все было так, то, например, существовало бы две разновидности метиленхлорида (СН2Cl2), соответствующие двум формулам:
где в одном случае атомы хлора находятся по соседству, а во втором — нет. Однако на практике до сих пор обнаружен пока только один метиленхлорид.
Теория Вант-Гоффа—Беля гласит, что четыре связи углерода направлены в двух перпендикулярных друг другу плоскостях (рис. 38). Изобразить это в двух измерениях сложно, проще всего представить себе равностороннюю пирамиду, вершина которой смотрит в небо. Направления четырех связей — из центра к углам пирамиды, соответственно, угол между всеми связями — один и тот же, около 109°. Атом углерода можно переворачивать как угодно любой из связей вверх — общая картина от этого не изменится.
Рис. 38. Атом углерода — тетраэдр
Каждая из этих связей находится на равном расстоянии от остальных, так что если метиленхлорид составлен именно таким образом, то совершенно не имеет значения, на каких именно связях закреплены два атома хлора. Все связи одинаковы. Вы можете сами проверить это на модели: воткните в пластилиновый или восковой шарик четыре палочки в виде описанного мной треножника. Пусть две палочки будут белыми (допустим, это связи с водородом), а две — зелеными (связи с хлором). Попробуйте поменять их между собой, и вы убедитесь, что аналогичного эффекта можно добиться и простым переворачиванием треножника. Соответственно, согласно теории Вант-Гоффа—Беля, метиленхлорид имеет только одно возможное представление — и это согласуется с практическими данными.
Однако, если к каждой из четырех связей углерода прикрепить по разной группе, результат будет уже другим. В этом вы тоже можете убедиться, поэкспериментировав с пластилиновым шариком и четырьмя палочками. Получится, что в таком случае существуют две возможные комбинации, каждая из которых является зеркальным отражением второй. Вы увидите, что, сколько ни крути модель, перевести одно из них в другое не получится. По системе Кекуле эти зеркальные варианты можно отобразить, как показано на рис. 39, и перевести одну формулу в другую невозможно.
Рис. 39. Левосторонние и правосторонние вещества
Вскоре было установлено, что в каждом случае, когда органическое вещество выказывало оптическую активность, в молекуле обнаруживалась асимметрия, обусловленная наличием как минимум одного «несимметричного углерода» (такого, к которому присоединяется четыре различные группы). При прохождении через вещества одной категории угол плоскости света смещался по часовой стрелке, другой — против часовой. Так при какой же куда?
Казалось, что ответить на этот вопрос невозможно, поэтому в 1891 году немецкий химик Эмиль Фишер вынес по этому поводу произвольное решение. Он выписал на бумаге два варианта строения вещества под названием глицеральдегид (который можно рассматривать как крайне простую молекулу сахара), и пометил один из них как D-глицеральдегид («правосторонний»), а второй — как L-глицеральдегид («левосторонний»). Все остальные оптически активные вещества теперь осталось рассмотреть по аналогии с этими двумя и отнести либо к «левосторонней», либо к «правосторонней» группам. Совсем недавно оказалось, что Фишер действительно был прав. Распределенные им по группам вещества действительно имеют именно то строение, которое он предполагал.
Когда в лабораторных условиях создается какое-либо из веществ, имеющих асимметричную структуру, оба зеркальных варианта формируются в равных количествах, поскольку такова ситуация максимального беспорядка, а следовательно, максимальной энтропии. Для того чтобы вещества одной категории получалось больше, чем другой, необходимо идти на специальные ухищрения, например использовать в качестве сырья другое оптически активное вещество.
Такие вещества добываются из животных и растительных источников. На самом деле все присутствующие в живой ткани вещества, имеющие в своем составе асимметричный атом углерода, представляют собой либо одну, либо вторую оптически активную форму. В этом отношении живая ткань являет собой поразительный пример механизма уменьшения энтропии — как и в отношении создания специфических белков. Естественно, все это делается за счет глобального ее увеличения.
Выяснилось, что все природные сахара — «правосторонние», а все природные аминокислоты (в том числе приведенный для иллюстрации на рис. 39 серии) — «левосторонние». То есть в общем случае организм не может использовать ни левосторонние сахара, ни правосторонние аминокислоты, поэтому их также называют «неестественными» сахарами и аминокислотами. Однако в небольшом количестве в природе они все же встречаются. В состав стрептомицина входит левосторонний сахар, а в состав некоторых антибиотиков — правосторонние аминокислоты. Жизненно необходимое человеку вещество «аскорбиновая кислота» имеет отношение к «неестественным» левосторонним сахарам.
Тот факт, что все природные аминокислоты — левосторонние, крайне важен для пептидной структуры. Если задаться целью создать модель пептидной цепочки с использованием тетраэдрального представления углеродных связей, то окажется, что радикалы звеньев-аминокислот в цепочку направлены по очереди в разные стороны. Тогда вдоль цепочки получается достаточно места для всех групп атомов. Если бы все аминокислоты были правосторонними, ситуация была бы той же.
Однако, если бы часть аминокислот были левосторонними, а часть — правосторонними, то неизбежными стали бы случаи соседства в цепочке левосторонней и правосторонней аминокислот. Их радикалы оказались бы на одной стороне цепочки, и места для обоих просто не хватило бы. Именно поэтому все аминокислоты в белке должны быть либо левосторонними, либо правосторонними. Тот факт, что они оказались левосторонними, видимо, является результатом случая, произошедшего давным-давно в доисторические времена, когда появилась на свет первая белковая молекула.
Молекулы ферментов (тоже сами по себе оптически активные и асимметричные, благодаря наличию в их составе аминокислот), разумеется, отличают оптически активный субстрат от его зеркального отображения, так же как мы не надеваем на правую ногу левый ботинок. Реагируя с одним вариантом зеркального отображения и не реагируя с другим, ферменты поддерживают асимметрию в организме.
Для того чтобы ферменты могли проводить подобное различие между зеркальными вариантами вещества, субстрат должен крепиться к молекуле фермента как минимум в трех точках, и это — еще одно косвенное свидетельство в пользу образования промежуточного комплекса «субстрат-фермент».
Кстати, в 1949 году гипотеза о промежуточном образовании получила окончательное подтверждение — британский биохимик Бриттон Ченс смог непосредственно обнаружить наличие этого комплекса с помощью очень тонкого теста на светопоглощение.
До сих пор я рассуждал так, как будто в состав белков не входит ничего, кроме аминокислот. Да, в отношении большей части белков это так и есть. Однако при распаде многих белков, помимо аминокислот, обнаруживались и отличные от них вещества. Такие белки называют «составными», и самым известным из них является гемоглобин, придающий крови характерный красный цвет.
В 60-х годах XIX века немецкий биохимик Феликс Хоппесейлер сумел показать, что частью структуры гемоглобина является вещество «гем», являющееся не аминокислотой, а сложной группой атомов, содержащей один атом железа. Позже были открыты и ферменты, важную составную часть которых тоже представляет собой гем.
Гем называют «простетической группой» (от греческого слова, означающего «добавление», от которого происходит и слово «протез»), и он необходим для функционирования тех белков, частью которых является. Гем в составе гемоглобина и различных гемсодержащих ферментов — это одно и то же вещество, но у каждого белка имеется своя отдельная функция, определяемая аминокислотной составляющей. Тут можно провести аналогию с режущей кромкой инструментов — топора, серпа, стамески… Режущая кромка одинакова, но предназначение инструмента зависит от его формы в целом.
Гем прочно прикреплен к остальной части белковой молекулы, и удалить его можно, только разложив саму молекулу. Во всех прочих случаях первыми отваливаются аминокислоты. К примеру, некоторые ферменты в процессе очистки диализом теряют каталитические свойства. Причина этого кроется не в денатурации, поскольку, если ту же самую воду, которой промывали мембранный мешочек, потом долить в раствор фермента, он снова обретает свои каталитические свойства. Явно какая-то важная часть фермента в этом случае утрачивается, а потом, вместе с водой, возвращается обратно.
Впервые это продемонстрировали в 1904 году английские химики Артур Харден и У.Дж. Янг, проведя диализ фермента зимазы, полученного из дрожжей. Ту часть его, которая была удалена в процессе диализа, ученые назвали «козимазои». Если она так легко удаляется и так же легко возвращается на место, решили химики, значит, удерживающие ее в составе молекулы связи должны быть очень уж слабыми. Кроме того, молекула козимазы должна иметь достаточно малый размер, чтобы проникнуть сквозь мембрану. И еще — выяснилось, что кипячение не разрушает структуру козимазы, следовательно, это не белок.
Потом и у других белков обнаружилось свойство терять небольшие частицы и утрачивать при этом свои характерные способности; тогда эти «небольшие частицы» получили общее имя — «коферменты».
Работа по установлению химической природы коферментов ведется с 20-х годов XX века по сей день. В составе большей части из них был обнаружен атом фосфора, а многие содержали такие сочетания атомов, каких в организме не обнаруживалось более нигде. Например, в составе козимазы было найдено кольцо из пяти атомов углерода и одного атома азота, как в соединении, имеющем название «пиридин». Сам по себе пиридин в живых тканях не встречается, как и пиридиновое атомное кольцо, за исключением нескольких коферментов. То же самое можно сказать еще о ряде групп атомов, имеющихся в других коферментах.
Ферменты присутствуют в организме лишь в небольших, достаточных для осуществления катализа количествах, так что и коферменты, особенно содержащие такие редкие соединения атомов, присутствуют в крайне малом количестве.
Этот факт имеет значение в свете другой линии исследования, которая проходила независимо от той, о которой я только что рассказывал. На протяжении всей своей истории человек периодически отмечал существование определенной связи между питанием и некоторыми заболеваниями. К примеру, в 1753 году шотландский врач по имени Джеймс Линд предположил, что наличие в рационе цитрусовых и свежих овощей позволяет предотвратить цингу. Эта болезнь, выражавшаяся в кровоточении десен и общем ослаблении организма, была настоящим бичом моряков, которым приходилось иногда по нескольку месяцев сидеть на диете из солонины и сухарей. Несколько десятков лет спустя командование британского флота решило прислушаться к совету врача и включить в диету моряков лимоны — цинга просто испарилась с британских кораблей.
В 1896 году голландский врач Кристиан Эйкман, работая в Восточной Индии, сумел воспроизвести у домашней птицы симптомы распространенного среди местного населения заболевания берибери только за счет кормления их шлифованным рисом. Вылечить болезнь удалось так же просто — добавив в пищу птицы рис нешлифованный.
Очевидно, в рисовой шелухе, которая при шлифовке удаляется, содержится небольшое количество некоторого вещества, необходимого для здоровой жизни. В течение всего следующего десятилетия биохимики обнаруживали подобные вещества и в других пищевых продуктах. Выяснилось, что в состав вещества, содержащегося в рисовой шелухе, входит аминогруппа, и Казимеж Функ, биохимик польского происхождения, исходя из предположения, что и в других подобных веществах есть аминогруппа, назвал их все скопом «витаминами» («жизнь + амины»). Потом оказалось, что аминогруппа — совсем не обязательный элемент витаминов, но название к тому времени уже прижилось.
В течение 30-х годов XX века, да и позже, ученые выделяли все новые витамины и выясняли их строение. И чем дальше, тем больше становилось очевидным, что в витаминах содержатся те же самые редкие группы атомов, что и в коферментах. Выводы, мне кажется, напрашиваются сами.
Организм живого существа, например человека, не может самостоятельно производить некоторые «необычные» сочетания атомов, потому что для этого у него отсутствует соответствующий химический механизм. А вот растения способны такие вещества вырабатывать, и травоядные животные получают их вместе с пищей. Так эти вещества, в небольшом количестве, попадают и в организм человека, но, как я уже говорил, небольшого количества оказывается вполне достаточно, так как и коферментов в организме очень мало.
При нормальном питании в организм человека поступают все необходимые вещества. Однако если диету искусственно ограничить, например питаться лишь тем, что может пролежать без холодильника весь долгий путь морского путешествия, или переусердствовать при очистке зерна, то при этом из пищи пропадает необходимая доза витаминов. А без них организм не может формировать соответствующие коферменты. Когда доходит до этой стадии, ферменты, в состав которых эти коферменты должны были бы входить, становятся недееспособными, внутриклеточные химические механизмы начинают буксовать, и человек заболевает, ему становится все хуже, и если положение не исправить, то в конце концов он умрет.
Эти неаминокислотные составляющие белков не являются по природе своей чисто органическими веществами. Я уже сказал, что для жизнедеятельности человека необходимо железо, поскольку оно входит в состав гемоглобина и гемсодержащих ферментов. Более того, оно необходимо в приличных количествах, поскольку гемоглобин составляет значительную часть крови.
Однако некоторые ферменты присутствуют в организме в гораздо меньшем количестве, нежели гемоглобин, и содержат уникальные, присущие в организме только им элементы — соответственно, в целом содержание этих элементов в организме не то что просто мало, а ничтожно мало. Например, фермент карбонангидраза содержит в своем составе цинк. В состав других ферментов входят магний, медь, кобальт или молибден. Для того чтобы обеспечивать потребности человека в этих веществах, они должны присутствовать в рационе в минимальном объеме, но полное их отсутствие приведет к нарушению работоспособности важнейших ферментов и, соответственно, к болезни и смерти.
Глава 19. ДЛЯ ЧЕГО ЖЕ ОНИ НУЖНЫ?
Теперь, после того, как мы подробно выяснили, почему присутствие ферментов в ящерице и их отсутствие в камне так важно, разумно поинтересоваться: какие же именно химические реакции катализируют ферменты, если уж эти реакции являются отличительным признаком живой материи?
На самом деле еще задолго до того, как было достигнуто сколь бы то ни было серьезное понимание природы ферментов и подробностей их функционирования, химики уже проявляли интерес к химическим реакциям жизни. В конце концов, суть происходящей реакции можно уловить и не зная подробностей ее осуществления, подставив вместо них уклончивое «ну, как-то чем-то катализируется, наверное».
Как уже говорилось в главе 14, все химические реакции, происходящие в процессе жизнедеятельности, именуются одним емким словом «метаболизм», или «обмен веществ».
Обратите внимание, что я определил метаболизм как химические изменения, происходящие «в процессе жизнедеятельности», а не «внутри живой ткани»! Это очень важно, потому что существует ряд химических реакций, происходящих вне живой ткани, и тем не менее крайне важных для нее.
Я имею в виду пищеварение. Когда вы глотаете пищу, она движется вниз по пищеводу, попадая оттуда в желудок, а затем — в кишечник. В ходе этого процесса она претерпевает существенные изменения, и то, что в итоге выбрасывается через анус, принципиально отличается от того, что было поглощено через рот. Во время нахождения в пищеварительном канале (общее название для всей системы труб от рта до ануса; см. рис. 40) пища не находится внутри организма в строгом смысле. Она продолжает оставаться частичкой внешнего мира, зажатой между ртом и анусом. Различные железы, от крупных вроде печени и поджелудочной до многочисленных мелких, выделяют в пищеварительный канал свои соки. Соки эти перемешиваются с перемолотой пищей, и содержащиеся в них ферменты катализируют все те реакции обмена веществ, которые мы называем общим словом «пищеварение».
Именно благодаря тому, что реакции пищеварения происходят вне самого организма, они первыми и попали в поле зрения ученых (как об этом говорилось в главе 15). Пищеварительные соки можно извлечь из канала с помощью трубок, не нанося обследуемому никакого вреда, кроме легкого неудобства, а затем тщательно изучить их действие на пищу в лабораторных условиях. Нет причин полагать, что в пробирке и в пищеварительном канале одна и та же реакция будет проходить по-разному, ведь и в том и в другом случае она проходит вне самого организма.
Счастливый случай для великого дела изучения процессов пищеварения произошел в 1822 году, когда американскому хирургу по имени Уильям Бомон попался уникальный больной — Алекс Сен-Мартин, канадский путешественник, получивший в результате огнестрельного ранения необычную травму — не-зарастающее отверстие в животе (фистулу), ведущее прямо в желудок. Бомон получил, таким образом, возможность в течение десяти лет непосредственно наблюдать, как желудок вырабатывает свои пищеварительные соки и какое воздействие они оказывают на различную пищу при тех или иных обстоятельствах. В 1833 году Бомон опубликовал результаты своих наблюдений, и физиологи пришли в полный ажиотаж.
Рис. 40. Пищеварительный канал
Такие больные, как Сен-Мартин, встречаются крайне редко, и сотворить такое с человеком специально — дело немыслимое. Поэтому физиологам 40-х годов XIX века по всей Европе пришлось выбрать максимально приближенный к этому вариант — они стали создавать искусственные фистулы у собак, и изучение процессов пищеварения приобрело массовый характер.
С помощью таких методов исследования в XIX веке был собран достаточно полный свод представлений о биохимии пищеварения, и хотя это было знание только о «внешних рубежах» метаболизма, для начала получилось очень неплохо.
В целом была собрана следующая информация: по мере продвижения пищи по пищеварительному каналу она подвергается воздействию одного за другим различных соков, каждый из которых содержит свойственный только ему набор ферментов — по конвейерному принципу. Давайте рассмотрим этот процесс на примере углеводов.
Основные углеводы, содержащиеся в нашей пище, — это целлюлоза, крахмал, сахароза и лактоза. Целлюлозу организм человека расщеплять не умеет, и она выходит с фекалиями практически в нетронутом виде. А вот крахмал начинает распадаться на более мелкие части, именуемые декстринами, уже под воздействием фермента, присутствующего в слюне, птиалина.
Но птиалин не может обрабатывать пищу долго — еда проглатывается и опускается в желудок, кислотное содержимое которого быстро разрушает птиалин. Однако как только пища из желудка попадает в тонкий кишечник, там она снова подвергается действию уже другой амилазы (так называются все ферменты, катализирующие процесс распада крахмала, в том числе и птиалин), слегка щелочной, производимой поджелудочной железой. Здесь процесс распада крахмала продолжается — медленно, но непрерывно. Крахмал продолжает распадаться на декстрины, а декстрины — на более мелкие, пока не получатся фрагменты, состоящие всего из двух молекул глюкозы. Они называются мальтозой.
Дальше в пищеварительном тракте пища подвергается обработке другими пищеварительными соками, содержащими, в частности, фермент «мальтазу», катализирующую распад мальтозы на отдельные молекулы глюкозы.
Есть в пищеварительных соках и такие ферменты, как «сахараза» и «лактаза», катализирующие расщепление, соответственно, сахарозы на глюкозу и фруктозу и лактозы на глюкозу и галактозу. Таким образом, посредством скоординированной деятельности ферментов расщепляемые углеводы из исходной пищи превращаются в простые вещества с шестью атомами углерода — глюкозу (в основном), фруктозу и галактозу.
Жиры попадают в ежовую рукавицу жирорасщепляющих ферментов («липаз»), одной из которых является желудочный сок, ферментативная деятельность которого, впрочем, не очень активна ввиду его высокой кислотности, и сок поджелудочной железы, который как раз очень активен в этом отношении. Сок печени (желчь) не содержит ферментов, зато содержит определенные вещества (соли желчных кислот), которые облегчают перемешивание жиров с водянистыми пищеварительными соками, а значит, и сам процесс их переваривания. К тому времени, когда жиры достигают нижней части тонкого кишечника, они уже разложены на глицерин (трехуглеродный спирт) и жирные кислоты (длинные углеводные цепочки с карбоксильной группой на конце).
Белкам, как и следовало ожидать, предстоит самая сложная обработка. Пепсин, содержащийся в желудочном соке, чувствует себя в кислотной среде как дома — это редкий случай среди ферментов, его активность вне кислотной среды невозможна. Он катализирует процесс распада определенных пептидных связей, а соляная кислота желудочного сока катализирует распад всех пептидных связей без исключения. Трипсин и химотрипсин сока поджелудочной железы тоже являются расщепляющими белок ферментами («протеазами»), и их черед наступает, когда пища покидает желудок и переходит в тонкий кишечник. Они катализируют распад пептидных связей, с которыми не справились ни пепсин, ни соляная кислота. В результате в основную часть тонкого кишечника белки попадают в виде множества мелких пептидов, состоящих из двух-трех-четырех аминокислот. А соки кишечника содержат множество «пептидаз», которые и завершают работу по катализированию распада различных пептидов на одиночные аминокислоты.
У всех этих пищеварительных изменений есть общие детали. Прежде всего, все они заключаются в превращении больших молекул в маленькие. Такие метаболические превращения сравнительно больших и сложных молекул в маленькие и простые именуются словом «катаболизм». Следовательно, можно сказать, что пищеварение — это ряд катаболических изменений.
Далее, различные катаболические преобразования, происходящие при пищеварении, всегда подразумевают расщепление некоторых химических связей и присоединение в месте расщепления молекулы воды. Такой способ разрывать связь с помощью добавления воды — вполне естественное изобретение, если принять во внимание, что живая ткань большей частью из воды и состоит — на 60 процентов, если мерить по весу, и на 98 процентов, если считать по количеству отдельных молекул (это то, что касается именно человека). Такой процесс получил название «гидролиз» (от греческих слов, означающих «терять с водой»), а подробности гидролитических изменений, происходящих при переваривании пищевых веществ каждого из трех классов, приведены на рис. 41.
Итоговые продукты пищеварения — единицы строения, полученные путем катализируемого ферментами гидролиза из сложных веществ, изначально присутствующих в пище, — могут проходить сквозь мембрану кишечника («абсорбироваться», или «впитываться») и попадать таким образом уже непосредственно внутрь организма. Более сложные молекулы этого сделать, как правило, не могут.
Таково значение пищеварения: оно превращает невпитываемые питательные вещества во впитываемые единицы, из которых они состоят. Более того, для организма крайне важно, чтобы исходные питательные вещества во всей своей сложности не впитывались. Набор углеводов и жиров, естественный для каждого организма, в мелочах отличается от набора углеводов и жиров, естественных для других организмов. А уж про белки и говорить нечего. Организму нечего и пытаться внедрить в свою структуру чужие молекулы, все сразу и в неизмененном виде. На самом деле, даже когда такое происходит, и чужие белки или сложные углеводы по какой-то причине в нетронутом виде попадают в организм, он тут же начинает вырабатывать особые белковые молекулы (антитела), которые связывают посторонние молекулы и быстро выводят их из строя.
В дальнейшем антитела не исчезают из организма, что обеспечивает человеку иммунитет против болезни в будущем, если белок, на который они выработаны, является частью вредоносного микроорганизма или производимым таким микроорганизмом токсином. Однако антитела могут сослужить и плохую службу, сделав человека «гиперчувствительным» к присутствию чужеродных белков вполне безобидной природы — в виде наступления аллергических реакций, вроде сенной лихорадки, астмы или пищевой аллергии.
Если же организм имеет дело не со сложными веществами, а всего лишь с их структурными единицами, то таких проблем не возникает. Не важно, сколь различны между собой белки коровы, утки или пшеницы и насколько все они вместе отличаются от человеческих белков, — все они состоят из одних и тех же аминокислот. Будучи разложенными в организме, они предоставляют для впитывания организмом именно аминокислоты — прекрасный строительный материал для человеческих белков. Точно так же и чужеродные углеводы разлагаются на глюкозу, из которой строятся уже человеческие углеводы, а чужеродные жиры — на глицерин и жирные кислоты, из которых создаются человеческие жиры.
Рис. 41. Гидролиз в процессе пищеварения
Пройдя сквозь кишечную мембрану и будучи впитанными, структурные единицы попадают уже непосредственно в организм. Таким образом, из вида биохимиков и физиологов XIX века они после этого пропадали. О процессе метаболических изменений, происходящих в самом организме (промежуточном метаболизме), можно было судить лишь по косвенным признакам.
Точнее говоря, природа конкретных изменений в целом была уже понятна. Ясно, что глюкозе и жирным кислотам предстояло подвергнуться, хотя бы частично, дальнейшему разложению на еще более мелкие молекулы углекислоты и воды. Аминокислоты тоже должны превратиться, хотя бы частично, в углекислоту, воду и азотсодержащую мочевину. Эти процессы должны происходить хотя бы потому, что в моче имеется мочевина, а в выдыхаемом воздухе — газообразная углекислота, а вода вообще выделяется организмом всеми возможными способами — и с мочой, и с дыханием, и через кожу с потом (рис. 42).
Рис. 42. Общая схема метаболизма
Кроме того, различные структурные единицы должны, хотя бы частично, подвергнуться изменениям, которые вновь построят из них сложные молекулы. В отношении аминокислот и жирных кислот это казалось однозначным, поскольку в человеческом организме содержатся строго специфические, человеческие белки и жиры, которые можно сформировать только из структурных единиц.
Присутствие в организме специфических человеческих углеводов — менее очевидно. Точнее, в 1844 году немецкий биохимик К. Шмидт обнаружил, что в крови содержится в небольшом количестве глюкоза, но речь шла именно о самой глюкозе как о структурной единице. Однако в 1856 году французский физиолог Клод Бернар увенчал свои многолетние исследования открытием того факта, что в печени содержится склад крахмалоподобных углеводов, имеющих некоторые отличия от самого крахмала. Бернар назвал этот углевод «гликогеном», от греческого «производить сахар», поскольку в процессе гидролиза именно это с углеводом и произошло бы.
Происходящие в организме метаболические реакции, в ходе которых производятся большие и сложные молекулы из маленьких и простых — белки из аминокислот, жиры из жирных кислот, гликоген из глюкозы, — являются примерами анаболизма.
Понятно, что как анаболитические, так и катаболитические реакции, включенные в процесс промежуточного метаболизма, неизбежно имеют место именно таким образом, как описано выше. Поняв это, можно приступать к их изучению, даже не зная химических подробностей.
К примеру, концентрация глюкозы в крови всегда постоянна. Каждый кубический сантиметр крови содержит, грубо округляя, один миллиграмм глюкозы, служащей промежуточным запасом пищи для омываемых кровью клеток. Когда происходит расщепление большого объема пищи и в организм одновременно поступает много глюкозы, ее уровень в крови не испытывает скачкообразного возрастания. И точно так же он не падает, когда в результате долгого голодания организм расходует глюкозу, не получая компенсирующего притока ее извне.
Такая гармония является возможной благодаря уравновешенности анаболитических и катаболитических процессов. Глюкоза, получаемая в ходе расщепления пищи (катаболизм), проходит сквозь стенки кишечника в кровеносные сосуды, сходящиеся в так называемую «воротную вену». Воротная вена доставляет глюкозу в печень, где распадается на сеть «синусоид», омывающих клетки печени. Глюкоза переходит из крови в клетки печени, и там из нее формируется гликоген (анаболизм), в виде которого она и хранится для последующего использования.
После того как кровь покидает печень, концентрация глюкозы в ней уже соответствует норме. По печеночной вене кровь попадает из печени в сердце, откуда разносится по всему организму. Содержащаяся в ней глюкоза впитывается различными клетками организма и в них уже разлагается на углекислоту и воду (катаболизм).
Общего уменьшения уровня глюкозы в крови из-за впитывания клетками не происходит, потому печень постоянно обеспечивает свежий ее приток.
Однако по окончании переваривания пищи глюкоза перестает поступать в организм через стенки кишечника, и, если голодание затянется, нового поступления ее не будет в течение нескольких часов, а то и дней. И что тогда? Что ж, в такой ситуации, когда воротная вена вынуждена гнать в синусоиды кровь, лишенную глюкозы, срабатывают обратные механизмы. В гликоген превращать больше нечего, но сам-то гликоген в печени еще хранится! И вот теперь организм начинает его потихоньку расщеплять (катаболизм), ровно с такой скоростью, чтобы обеспечить кровь в печеночной вене строго рассчитанным количеством глюкозы.
Балансируя, таким образом, между катаболизмом и анаболизмом, печень превращает масштабные колебания уровня глюкозы в крови в ровную линию. Можно сказать, что она оказывает то же действие на уровень глюкозы, что банковский счет — на уровень финансов преуспевающего семейства, где в успешные периоды деньги оседают и откуда в неудачные периоды они берутся, так чтобы уровень жизни при всех этих колебаниях особенно не менялся.
Поддержание баланса глюкозы в организме — на самом деле процесс очень тонкий. Он осуществляется с помощью двух гормонов — инсулина и глюкагона, каждый из которых производится определенными клетками поджелудочной железы и выделяется напрямую в кровь. (Таким образом, поджелудочную железу можно рассматривать как железу двойного назначения — она является и пищеварительной, выделяя соки в тонкий кишечник через проток, и эндокринной, выделяя гормоны непосредственно в кровь.)
Наличие в крови инсулина стимулирует реакцию анаболизма, то есть превращение глюкозы в гликоген, что приводит к снижению уровня глюкозы в крови. Глюкагон же, наоборот, стимулирует реакцию катаболизма, то есть превращение гликогена в глюкозу, и повышает уровень последней в крови.
Если, по какой-либо причине, баланс реакций в организме смещается в сторону катаболизма так, что печень выпускает в кровь слишком много глюкозы, то, попадая в клетки поджелудочной железы, кровь с высоким содержанием глюкозы начинает стимулировать производство инсулина, что, в свою очередь, приводит к моментальному снижению уровня глюкозы. Если снижение заходит слишком далеко, то кровь с низким содержанием глюкозы стимулирует производство уже глюкагона, что приводит к повышению ее уровня. Таким образом, постоянный уровень глюкозы обеспечивается благодаря тому, что сейчас принято называть «механизмом обратной связи».
Случается так, что поджелудочная железа человека оказывается не в состоянии производить инсулин. В результате мы имеем дело с заболеванием под названием «сахарный диабет». Если действие глюкагона не сдерживается антагонистом, то уровень глюкозы в крови начинает повышаться сверх нормы и достигает опасных значений. Организм начинает пытаться избавиться от лишней глюкозы через почки—и появление глюкозы в моче свидетельствует уже о достаточно далеко зашедшем диабете.
До начала XX века лечить это заболевание не умели. Да, врачи и биологи XIX века сумели с помощью вакцин и антитоксинов победить множество инфекционных заболеваний, но перед диабетом они оставались бессильными. Его ведь вызывает не микроб и не яд — он является следствием сбоев в работе внутренней химии организма, расстройства обмена веществ.
Доказательство тому было получено в 1889 году, когда двое немецких физиологов, Й. фон Меринг и О. Минковски, обнаружили, что для того, чтобы вызвать у собаки диабет, достаточно просто удалить у нее поджелудочную железу. Ученые пустились в поиски содержащегося в поджелудочной железе вещества, которое могло бы произвести противоположное действие, будучи введенным в кровоток, но первые двадцать лет исследований ни у кого ничего не получалось.
В 1921 году канадский врач Фредерик Грант Бентинг предположил, что причина неудач может крыться в белковой природе искомого вещества, благодаря чему после извлечения поджелудочной железы из организма оно могло очень быстро разлагаться под воздействием протеаз поджелудочной. С помощью молодого студента по имени Чарльз Герберт Бест Бентинг попробовал извлечь поджелудочную железу для исследования по-новому — перевязав предварительно проток. Это помогло исключить из общей картины действие пищеварительных соков железы — производящие их части железы атрофировались. После этого уже была извлечена оставшаяся часть железы, и из нее было извлечено вещество, впоследствии названное инсулином.
С помощью инсулина, изготавливаемого из поджелудочной железы забитого скота — коров и свиней, можно сдерживать проявления диабета (но, увы, добиться полного излечения, то есть научить организм снова вырабатывать инсулин, — нельзя), и сейчас диабетики могут вести полноценную жизнь.
Вернемся к балансу глюкозы. Печень может содержать лишь ограниченный объем гликогена. Когда количество гликогена доходит до 10—15 процентов от ее общего веса, то больше она принять на хранение уже не может. Кроме того, гликоген может храниться и в мышцах — до количества не более 1 процента. Мышц в организме гораздо больше, чем печени, так что общее количество гликогена, содержащегося в мышцах, гораздо больше, чем содержащегося в печени, несмотря на более низкую концентрацию. В целом печень может хранить около 250 граммов гликогена, а мышцы — около 350. То есть всего в организме может храниться около 600 граммов гликогена.
Теперь давайте вспомним содержание главы 14, где я писал, что энергетическая ценность углеводов при превращении их в углекислоту и воду составляет около 4 килокалорий на грамм. Таким образом, если все 600 граммов гликогена израсходовать, организм получит 2400 килокалории. В принципе этого может хватить на день обычного энергорасхода, но ведь известно, что человек может не есть несколько недель и не только не умирает при этом, но и уровень глюкозы в его крови остается на допустимом уровне.
Возникает и еще один вопрос, близкий по сути к предыдущему: известно, что можно постоянно съедать больше крахмала, чем его расходуется на энергетические цели. Куда же девается при этом вся глюкоза, на которую этот крахмал распадается, если организм может хранить ее лишь в таких скромных объемах?
Ответ на эти вопросы кроется в веществах другого класса — в жирах. Всем нам известно, что от картошки, да и вообще от любой насыщенной крахмалом пищи толстеют, а что это может означать, кроме того, что организм умеет превращать углеводы в жиры? Очевидно, глюкоза тоже расщепляется на какие-то более мелкие единицы, которые превращаются организмом в жирные кислоты, из которых в дальнейшем строятся жиры. Это вполне экономичный подход с точки зрения организма, поскольку один грамм жиров содержит 9 килокалорий, а не 4, как углеводы. Соответственно, при одном и том же весе жир является в два с четвертью раза более вместительным хранилищем энергии, чем углевод. Переедающие и располневшие люди выглядели бы куда более страшно, если бы хранили весь своей энергетический запас не в жировом, а в углеводном виде, например в виде крахмала, как это делают картошка или рис.
Более того, этот процесс обратим. Известно, что при длительном голодании вес теряется. Поскольку жировой запас, в отличие от углеводного, не ограничен в объеме, то и голодать человек может неделями.
Если же ситуация совсем критическая и даже жировые запасы исчерпаны, то в энергетическую топку идут уже белки. От аминокислот отрезается азотная часть, а все остальное превращается организмом в глюкозу. В результате при затянувшейся голодовке ткани начинают пожирать сами себя.
Все это наталкивает на мысли о том, что на каком-то уровне катаболизма все виды питательных веществ приходят к одним и тем же структурным единицам. У глюкозы и жирных кислот должны быть какие-то общие «кирпичики», более простые, чем оба этих вещества. И аминокислоты, избавленные от азотной части, тоже должны в процессе катаболизма распадаться на те же «кирпичики», чем бы они ни оказались (рис. 43).
То есть создается впечатление полной универсальности биохимии в организме. Кажется, что из одних и тех же «кирпичиков» он может анаболичес-ки создавать все, что угодно.
Но надо иметь в виду и ограничения. Организм не может подменять один химический элемент другим, значит, эти «кирпичики» могут состоять только из углерода, водорода и кислорода, поскольку при их формировании из белков удаляется азот.
Рис. 43. Общий строительный «кирпичик»
А если азота в этом веществе не содержится, значит, и аминокислоты из него создавать уже не получится без привлечения дополнительного источника азота, каковым в общем случае может служить только белковая пища.
Отсюда вывод: можно прожить на диете с низким содержанием углеводов и жиров, поскольку при достаточном поступлении белков некоторые аминокислоты будут анаболизированы в белки организма, а остальные — очищены от азота, низведены до состояния общего «кирпичика», а затем анаболизированы в необходимые организму жиры и углеводы.
А вот без белков прожить не получится. Диета с низким белковым содержанием приведет к тому, что организм начнет расщеплять собственные ткани, и в конце концов человек умрет, сколько бы ни было в его пище жиров и углеводов. В отсутствие источника азота собрать из общих «кирпичиков» полноценный белок невозможно.
Но ограничения на гибкость биохимии организма не исчерпываются необходимостью источника азота. Как я уже говорил в предыдущей главе, организм не способен самостоятельно вырабатывать некоторые витамины. Да, они не требуются в больших количествах, и организму можно было бы простить подобную ограниченность, просто не обращая на нее внимания, но в более крупном масштабе она сказывается и на самих белках.
В начале XIX века во Франции было предпринято много попыток добиться получения дешевой пищи путем варки костей и соединительной ткани (неперевариваемой в общем случае) для получения желатина, который вполне хорошо усваивается организмом. Единственная проблема заключалась в том, что желатин, будучи единственным присутствующим в пище белком, не может поддерживать жизнедеятельность.
В течение XIX века химики выяснили, что белки состоят из множества различных аминокислот, и в 1872 году немецкий биохимик О. Нассе сумел продемонстрировать, что одна из них, тирозин, в желатине отсутствует. Позже обнаружилось, что в нем отсутствуют и другие аминокислоты — цистин, триптофан и метионин. Но ведь белок в пищеварительном тракте распадается на аминокислоты, и именно они впитываются организмом! Следовательно, оставалось предположить, что оценивать надо не питательные свойства белка, а питательные свойства аминокислот, а белок рассматривать уже с точки зрения того, какие именно аминокислоты в нем присутствуют.
Эксперименты диетологов, при которых источником азота служили не белки, а смеси аминокислот, ясно показали, что жизнедеятельность и рост тканей могут продолжаться и без белков, если в пище присутствуют все аминокислоты. Когда американский биохимик Уильям Роуз зафиксировал некоторые проблемы у испытуемых при проведении подобного эксперимента, он предположил, что причина проблем в том, что в его смесь не попала некая неизвестная доселе аминокислота. Он стал искать ее и в 1935 году открыл треонин — последнюю по времени обнаружения значимую аминокислоту. С добавлением треонина в питательную смесь все пошло на лад (что является дополнительным косвенным свидетельством в пользу того факта, что других аминокислот в составе белков не встречается).
Роуз проводил свои эксперименты на взрослых людях — аспирантах, для которых не самая увлекательная диета из крахмала, кукурузного масла, смеси аминокислот и витаминноминерального комплекса воспринималась как возможность послужить науке, ну и, несомненно, завершить собственное образование. В качестве критерия оценки достаточности диеты Роуз использовал нечто, что он сам называл «азотным балансом».
Содержание азота в пище может уравновешиваться содержанием азота в фекалиях (та часть азота из пищи, которая не впиталась) и в моче (так часть, которая впиталась, но впоследствии была отсечена по той или иной причине от белков организма и отправлена в отбросы). В обычных условиях у взрослого человека количество азота, содержащегося в пище, равно количеству азота, выделяемого с мочой и фекалиями. Содержание азота в организме при этом остается неизменным — соблюдается кислотный баланс.
Однако азот всегда в какой-то степени теряется. Даже если организм получает достаточно калорий, так что необходимости в расщеплении белков для получения энергии нет, все равно белки с некоторой скоростью избавляются от азотного содержимого (иногда этот процесс называют «износом»). Если не возмещать эти потери, то количество выделяемого организмом азота превысит количество азота поглощаемого и содержание азота в организме будет снижаться. Это называется «отрицательным азотным балансом».
Может случиться и так, что приток азота будет превышать его исход, так что содержание азота в организме будет возрастать — это называется «положительным азотным балансом». Для растущих детей положительный азотный баланс — норма, так же как и для выздоравливающих больных или оправляющихся после голодовки людей. В их организмах идет активный процесс строительства тканей после длительного периода отрицательного азотного баланса.
Для того чтобы в организме поддерживался азотный баланс, анаболизм и катаболизм белков должны протекать скоординированно. Скорость синтеза белков из аминокислот должна соответствовать скорости износа белков. Но для синтеза необходимо, чтобы в организме в достаточных количествах присутствовали все аминокислоты, входящие в состав требуемого белка (как правило, это все 19 аминокислот). Диетологические эксперименты показали, что недостаток даже одной аминокислоты приводит к невозможности формирования белка — организм не умеет собирать белки с гнездом для недостающей аминокислоты «на потом».
Если одна из аминокислот отсутствует, изнашивающиеся и уничтожаемые организмом белки не заменяются и все остальные аминокислоты, присутствующие в достаточном количестве, могут сгодиться только на производство энергии. Организм очищает, их от азота и катаболизирует. В результате мы имеем отрицательный азотный баланс.
Таким образом, понятно, что в организме должны присутствовать все аминокислоты — но значит ли это, что все они должны присутствовать именно в диете? Нет. Роуз установил, что некоторые аминокислоты вполне можно исключать из диеты аспирантов, не вызывая у них при этом отрицательного азотного баланса. Например, совершенно безо всяких последствий можно удалить из смеси аланин. Но ведь аланин является необходимым элементом строения белка, и он просто обязан присутствовать в организме! Вывод ясен: значит, организм каким-то образом сам синтезирует аланин, используя для этого азот из других аминокислот.
Таблица 8
НЕОБХОДИМЫЕ АМИНОКИСЛОТЫ
Аминокислота … Ежедневная норма (г)
Фенилаланин … 1,1
Метионин … 1,1
Лейцин … 1д
Лизин … 0,8
Валин … 0,8
Изолейцин … 0,7
Треонин … 0,5
Триптофан … 0,25
Таким образом, часть аминокислот можно исключить из пищи и организм сам будет синтезировать их в достаточном количестве.
С другой стороны, если исключался из диеты, например, лизин, то у обследуемого тут же фиксировался отрицательный азотный баланс. Лизин необходимо получать с пищей; организм явно не умеет производить его самостоятельно, независимо от наличия в нем других аминокислот. Поэтому лизин входит в число «необходимых» аминокислот.
Роуз установил, что «необходимых» аминокислот, то есть таких, которые организм должен получать с пищей, — всего восемь, и подсчитал минимальную ежедневную норму потребления каждой из них, при которой в организме не наблюдается отрицательного азотного баланса и расщепления собственных тканей. Аминокислоты и их ежедневная норма потребления приведены в таблице 8.
Таков еще один пример ограничений, налагаемых природой на гибкость химических процессов живого организма, помимо невозможности производить витамины. Витаминов достаточно потреблять в день по нескольку миллиграммов, а вот аминокислоты необходимо получать в количествах, превышающих аналогичные цифры для витаминов в сотни и даже тысячи раз.
Глава 20. ЖИЗНЬ БЕЗ ВОЗДУХА
Как видите, многое о процессах, происходящих в живой ткани, можно сказать на одной лишь основе рассмотрения веществ, которые мы имеем на входе в организм и на выходе из него. Мы решили, что должен существовать некий общий строительный «кирпичик», из которого создаются и белки, и жиры, и углеводы. Мы пришли к выводу, что все структурные единицы пищи — глюкоза, жирные кислоты, аминокислоты и прочие — либо катаболизируются на углекислый газ и воду, либо анаболизируются в крахмал, белки или жиры. Мы даже установили, что одни вещества, такие как аланин, вырабатываются организмом самостоятельно, а другие, такие как лизин, — нет.
Это все, до чего мы могли додуматься, или есть еще резервы?
Ну, например, мы можем воспроизвести такое умозаключение: фермент может катализировать реакцию только в точке равновесия, причем не важно, с какой стороны идет реакция (см. главу 12). Следовательно, когда сложные вещества, поступающие с пищей, подвергаются гидролизу с помощью пищеварительных ферментов, то это тоже происходит в точке равновесия реакции. И известно, что гидролиз проходит полностью, поскольку практически все содержащиеся в пище сложные вещества в итоге оказываются гидролизованными и впитываются организмом.
Впитываются! По мере впитывания организмом аминокислоты жирные кислоты и простые сахара исчезают со сцены. Остаются только сложные вещества. Они тоже распадаются и так далее. Иными словами, соблюдается закон действия масс (см. главу 9) — путем удаления конечных продуктов точка равновесия сдвигается все дальше в сторону гидролиза.
Позволяют ли нам эти данные выдвинуть какие-то предположения о происходящем в клетках? Внутри тканей присутствуют только продукты гидролиза, так что можно представить те же самые ферменты катализирующими обратную реакцию в той же самой точке равновесия. Вместо разрыва связей путем добавления воды, от одной из аминокислот, скажем, отнимается атом водорода, а от другой — соединение атома водорода с атомом кислорода, тогда у обеих аминокислот освобождается по одной возможности для образования пептидной связи (см. формулу после рис. 29). Такой «антигидролиз» называют «конденсацией». Если конечные продукты этой реакции (белок и воду в данном случае) удалять из клетки с той же скоростью, с какой они образуются, то реакция конденсации может идти сколько угодно, вплоть до полной обработки всех имеющихся веществ.
Картинка, при которой одни и те же ферменты управляют процессами как анаболизма, так и катаболизма, в зависимости от того, какие именно вещества удаляются с места прохождения реакции, конечно, выглядит красиво. Но насколько она соответствует реальности?
В частности, в пользу этого предположения свидетельствует тот факт, что в лабораторных условиях пищеварительные ферменты можно заставить катализировать анаболитические реакции. К примеру, если аминокислоты подвергнуть при соответствующих условиях воздействию пепсина или химотрипсина, то действительно, происходит некий синтез, и в итоге получается нерастворимое белкообразное вещество пластеин. Пластеин — это смесь пептидов с малой молекулярной массой, цепочки которых состоят не более чем из десяти—двенадцати аминокислот; но вполне вероятно, что внутри живых тканей условия для формирования белков более благоприятны, чем в лабораторной пробирке, и там могут создаваться более крупные и сложные белки.
Но, увы, в целом теория имеет и ряд серьезных недостатков. Во-первых, пищеварительные ферменты в живых тканях никогда не встречаются. Какая разница, может пепсин или химотрипсин способствовать формированию белка или нет, если и тот и другой все равно отсутствуют в клетках, где это формирование происходит?
И опять же, нельзя забывать о свободной энергии. В целом реакции катаболизма сопровождаются снижением ее уровня. В случае гидролиза это снижение невелико по сравнению с другими видами реакций катаболизма, о которых чуть позже, но все же достаточно велико в целом. При гидролизе пептидной связи свободная энергия уменьшается на величину от 0,5 до 4 килокалорий на моль вещества, в зависимости от того, какие именно аминокислоты были задействованы в разорванной связи.
Это означает, что гидролиз белка — реакция, направленная «вниз с холма», и точка равновесия при ней сильно смещена в сторону полного гидролиза. Уровень свободной энергии снижается достаточно сильно, чтобы обратимость реакции не оказывалась ярко выраженной. На самом деле в точке равновесия подвергнувшимися гидролизу оказывается около 99 процентов белков.
Это не означает, что реакцию совсем нельзя обратить — надо просто создать для этого правильные условия. В лабораторной пробирке обеспечивается удаление воды сразу же по мере ее формирования (вода является одним из продуктов реакции конденсации). Соответственно, реакция сдвигается в сторону белка и идет производство пластеина. Однако в живой клетке образующаяся в большом количестве вода не может удаляться с нужной скоростью, и удалять с такой скоростью образующийся белок тоже сложно. Так что, если описанный путь — единственно возможный, значит, надо искать, как организм решает задачу быстрого удаления из клетки образующихся веществ. Вообще-то живая ткань преподносит много сюрпризов, и вполне возможно, что данная задача тоже нашла у природы какое-то оригинальное решение. Но все же, может быть, в живой ткани происходит не простое «обращение реакции», а какой-то иной процесс?
Что ж, если при реакции катаболизма уровень свободной энергии, как правило, снижается, то при имеющей обратную направленность реакции анаболизма он должен повышаться. Вместо того чтобы с безумной скоростью удалять продукты и клетки для того, чтобы сдвинуть точку равновесия ради протекания реакции в обратном направлении, не проще ли напрямую затратить на осуществление реакции немного энергии? В этом случае реакция пойдет куда надо, в зависимости не от состава веществ в клетке, а от приложения энергии. Не поступает энергия — идет реакция катаболизма; подали энергию — идет реакция анаболизма.
Откуда же возьмется в таком случае энергия? Самый простой ответ — из дальнейшего катаболизма структурных единиц. Из превращения глюкозы в углекислоту и воду можно получить на единицу веса в сотни раз больше энергии, чем из гидролиза гликогена на глюкозу (и, соответственно, чем требуется для конденсации глюкозы в гликоген). Следовательно, пожертвовав на катаболизм одной молекулой глюкозы, можно добиться соединения сотни других молекул глюкозы в гликоген.
Хорошо, но каков же тогда конкретный механизм, перевода энергии катаболизма на полезные цели — на проведение энергоемких реакций анаболизма? Чтобы ответить на этот вопрос, надо сначала подробно рассмотреть катаболизм. Никуда теперь от этого не деться. Необходимо понять, что происходит с питательными веществами после того, как их структурные единицы впитываются клетками. Пора проникнуть в тайны промежуточного метаболизма.
Одним из видов катаболизма, интересовавшим ученых с давних пор и послужившим исходной точкой для исследования промежуточного метаболизма, является факт ферментации глюкозы дрожжами. Во-первых, ферментация дрожжами Сахаров всегда, начиная с доисторических времен, имела для человечества большое практическое значение, так что мотивация для изучения этого явления была вполне достаточной. А во-вторых, дрожжевая ферментация — все же достаточно простое явление, которое можно изучать, не сталкиваясь с теми осложнениями, которые возникают при рассмотрении тканей животных. Ферментирующее действие дрожжей приводит к распаду глюкозы на этиловый спирт с высвобождением углекислого газа, так что выражение для этого процесса можно записать так:
С6Н12O6 → 2С2H6O + 2CO2.
Обратите внимание — это выражение уравновешено! Каждая молекула глюкозы в процессе катаболизма распадается на две молекулы этилового спирта и две молекулы углекислого газа. Больше ничего.
Это кажется удивительным. После того как Лавуазье продемонстрировал, что животные не могут существовать без кислорода, казалось естественным, что при всех важных реакциях катаболизма должен быть как-то задействован и кислород. Однако здесь его нет.
А в других реакциях, происходящих с участием дрожжей? И на этот вопрос был дан отрицательный ответ. Такой приговор вынес Луи Пастер в 1861 году — он показал, что все без исключения процессы жизнедеятельности дрожжей проходят при полном отсутствии кислорода. Он назвал это «la vie sans air» — «жизнь без воздуха».
Превращение глюкозы в этиловый спирт и углекислый газ — пример «гликолиза» (что по-гречески значит «расщепление сахара»), а для подчеркивания того факта, что этот процесс проходит «без воздуха», его часто называют еще «анаэробным гликолизом», где «анаэробный» по-гречески и означает «без воздуха».
Начиная с наблюдений за горящим топливом весь опыт человечества говорит о том, что получение энергии связано с соединением углесодержащих веществ с кислородом, но не будем же слишком строги в этом отношении. Энергию можно производить и другими способами.
При расщеплении одного моля глюкозы на этиловый спирт и углекислый газ высвобождается около 36 килокалорий свободной энергии. Это, конечно, гораздо меньше, чем можно было бы получить путем полного превращения этого же количества глюкозы в воду и углекислый газ; в последнем случае изменение уровня свободной энергии составило бы 686 килокалорий, так что при гликолизе производство энергии составляет лишь двадцатую часть от возможного. Однако для жизнедеятельности дрожжей этого оказывается достаточно.
Более того, вполне вероятно, что когда-то давным-давно никакого кислорода в атмосфере Земли не было, так что единственными способами выработки энергии для тогдашних живых существ были методы, родственные гликолизу. Даже сегодня сложные организмы, обычно получающие энергию за счет катаболизма глюкозы до уровня воды и углекислого газа с потреблением кислорода, при особых обстоятельствах могут временно переключиться и на гликолиз.
В качестве примера можно назвать мышечную ткань. В начале XX века было обнаружено, что мышцы содержат в небольшом количестве молочную кислоту, трехуглеродное соединение с эмпирической формулой С3H6O3. (Раньше это вещество обнаруживали только в прокисшем молоке, отсюда и название.) Выяснилось также, что в процессе работы мышц содержание молочной кислоты в них повышается.
В 1918 году немецкий биохимик Отто Майерхоф показал, что повышение содержания в мышцах молочной кислоты сопровождается снижением содержания в них гликогена. Казалось очевидным, что мышечная деятельность подразумевает расщепление гликогена на глюкозу и превращение последней в молочную кислоту. Реакцию перевода глюкозы в молочную кислоту можно записать так:
С6Н12О6 → 2С3H6O3.
И снова перед нами уравновешенное выражение. Одна молекула глюкозы расщепляется на две молекулы молочной кислоты без какого-либо участия кислорода. Наверное, именно эта или очень похожая реакция происходит и при прокисании молока, когда попавшие в него бактерии превращают молочный сахар в лактозу. Результат, получаемый в мышцах или в прокисшем молоке, отличается от результата, получаемого в дрожжах, поскольку в последнем случае молочная кислота продолжает расщепляться дальше:
С3Н6О3 → С2Н6О + СО2,
то есть на этиловый спирт и углекислый газ. Однако с точки зрения энергетики это маловажная деталь, поскольку на этом дополнительном шаге не вырабатывается какого-либо существенного объема энергии.
Хорошо, что этого не происходит в мышцах. Спирт — гораздо более ядовитое вещество, чем молочная кислота, и его присутствие в клетке было бы гораздо опаснее. Дрожжи могут себе позволить вырабатывать спирт, ведь они выбрасывают его в окружающую среду; но даже при этом они умирают, когда концентрация спирта в окружающей среде достигает около 18 процентов. А мышцам пришлось бы выбрасывать спирт в кровь, так что организм очень быстро опьянел бы и умер. В принципе, наверное, и приспособиться к высокой концентрации спирта в крови организм мог бы, но этого не произошло. Очевидно, более выгодным в процессе эволюции многоклеточных оказалось избавиться от завершающего этапа гликолиза, чем вводить механизмы ликвидации его последствий.
Майерхоф не просто показал, что сложные организмы способны проводить анаэробный гликолиз, несмотря на то что, как правило, они пользуются более эффективными реакциями с задействованием кислорода. Он обнаружил также, что и дрожжи, и мышцы пользуются при этом одними и теми же коферментами. Стало ясно, что и глюкоза в клетках обоих видов расщепляется с помощью сходных реакций. Так постепенно становилось ясно, что метаболические механизмы всех живых существ в принципе сходны и различия между ними не так уж существенны. Все проводимые со времен Майерхофа исследования только подтверждают эту точку зрения.
Легко понять, зачем мышцам нужна способность к гликолизу. Конечно, мышцы могут получить из глюкозы гораздо больше энергии путем полного расщепления ее на воду и углекислый газ — так они и делают в условиях отсутствия особой нагрузки. Однако для этого им, естественно, необходим кислород. Он попадает в мышцы с потоками крови, и если бы вся требуемая мышцам энергия могла вырабатываться только путем «правильного» полного расщепления, то их работоспособность была бы ограничена скоростью поступления кислорода.
Когда мышцы начинают расходовать больше энергии (например, при занятиях спортом), организм начинает ускорять кровоток. Человек принимается глубже и чаще дышать, сердце бьется чаще и сильнее. Естественно, скорость поступления в мышцы кислорода тоже повышается, и в них начинает вырабатываться больше энергии. Однако скорость дыхания и сердцебиения не может возрастать безгранично. А вдруг мышцам требуется еще больше энергии, чем они могут произвести с использованием всего поступающего объема кислорода, пусть и увеличенного?
«Ничего не получится» — теоретически вполне допустимый с научной точки зрения ответ, но на самом деле это не так. Эволюция всегда приводит к распространению механизмов, позволяющих их носителям хоть чуть-чуть, да опередить конкурентов. Так что с точки зрения выживаемости мышцам оказалось «выгодно» сохранить устаревшую способность к анаэробному гликолизу, ведь она позволяет вырабатывать «еще чуть-чуть» энергии дополнительно к получаемой с помощью кислородозависимых реакций.
Конечно, это неэффективный способ. Для того чтобы добиться того же эффекта, что при расщеплении одной молекулы глюкозы на воду и углекислоту, путем расщепления той же глюкозы на молочную кислоту, нужно потратить девятнадцать молекул против одной. Но в случае необходимости лучше неэффективно растратить запас глюкозы, чем оказаться в ситуации, когда какого-то мизерного количества энергии не хватает, чтобы спасти, скажем, собственную жизнь.
Этот процесс тоже имеет свои ограничения. Молочная кислота накапливается в мышцах по мере их работы, и, хотя она и не столь токсична, как спирт, все же и ее присутствие можно терпеть лишь до определенной концентрации. В мышцах, находящихся в состоянии покоя, концентрация молочной кислоты — 0,02 процента. В процессе работы она может доходить до 0,25 процента, но не более. Мы ощущаем возрастание молочной кислоты как один из признаков усталости, и в итоге любая мышца, как ее ни стимулируй, должна прекратить свою деятельность. Она не выдержит большего количества молочной кислоты.
Что же далее происходит с молочной кислотой? Ведь в процессе отдыха мышца должна, очевидно, восстановиться? Британский физиолог Арчибалд Вивиен Хилл показал, что после насыщения молочной кислотой мышца начинает больше обычного потреблять кислород. Такое ощущение, что кислород, которого так не хватало для сжигания глюкозы во время работы, теперь стремится наверстать упущенное. Получается нечто вроде возмещения «кислородного долга», и именно благодаря этому мы еще долго продолжаем тяжело дышать, а наше сердце — усиленно биться уже после того, как работа завершена. Теперь кислород необходим нашим тканям уже не для совершения работы, а в качестве «возмещения долга».
Химически это «возмещение долга» выражается в расщеплении молочной кислоты на воду и углекислоту. При этом вырабатываются те самые оставшиеся восемнадцать девятнадцатых энергии, потенциально скрытые в расщеплении глюкозы:
2С3H6O3 + 6O2 → 6СO2 + 6H2O
ΔF = -650 ккал.
При этом вырабатывается гораздо больше энергии, чем, требуется для того, чтобы снова собрать из двух (Молекул молочной кислоты молекулу глюкозы:
2C3H6O3 → C6H12O6
ΔF = +36 ккал.
Если предположить, что вырабатываемую при катаболизме молочной кислоты энергию можно пустить на формирование глюкозы из других молекул молочной кислоты, то понятно, что катаболизма одной молекулы молочной кислоты хватит для анаболизма множества других молекул. Даже если эффективность передачи энергии при этом будет составлять процентов 50, все равно достаточно расщепить на воду и углекислоту одну молекулу молочной кислоты, чтобы десять других объединить в молекулы глюкозы.
В итоге, когда «кислородная задолженность» ликвидирована, большинство молекул молочной кислоты снова оказываются в составе гликогена, наготове для следующего этапа работы, а потери гликогеновых запасов компенсируются бесконечным притоком глюкозы из печени.
Катаболизм молочной кислоты, благодаря которому становится возможным анаболизм других ее же молекул, является примером «парной реакции» (рис. 44). В целом реакция сопровождается снижением уровня свободной энергии. То есть, несмотря на то что при формировании глюкозы из молочной кислоты уровень свободной энергии повышается, это происходит не иначе как в ответ на распад молочной кислоты на углекислоту и воду, а при этом процессе уровень свободной энергии снижается, причем общая величина снижения за счет реакций второго типа — больше, чем общая величина повышения за счет реакций первого типа, так что в целом мы наблюдаем снижение, как и всегда при любых других проявлениях жизнедеятельности.
Рис. 44. Молочная кислота в мышцах
Легко говорить о парности реакций катаболизма и анаболизма молочной кислоты, но как именно такая парность обеспечивается? Каким образом энергия, вырабатываемая при одной реакции, передается другой?
Первая подсказка была получена в 1905 году. Английские химики Харден и Янг (те самые первооткрыватели зимазы) обнаружили, что если скорость производства дрожжами углекислого газа падает, то ее можно вернуть на прежний уровень, если добавить в дрожжи неорганический фосфат (примером такого вещества может служить фосфат калиевой кислоты, КН2РO4). Более того, по мере выработки углекислого газа количество фосфата в растворе уменьшалось!
Харден и Янг решили, что единственное, куда мог деваться фосфат, — это соединяться с каким-то органическим веществом. В этом случае он действительно перестал бы встречаться в виде простого иона и, соответственно, реагировать с тестовым реагентом. Ученые принялись анализировать смесь на предмет наличия в небольших количествах какого-нибудь органического вещества с содержанием фосфатной группы — и нашли такое вещество! Фосфатная группа оказалась связанной с молекулой сахара с помощью некоей связи, характерной для подобных соединений, именуемых «эфирами». Соответственно, данное вещество получило название «эфир Хардена—Янга». Со временем было установлено и точное строение этого вещества; оказалось, что это простой сахар, фруктоза, к которому крепятся две фосфатные группы. Теперь его так и называют — фруктозодифосфат.
Фруктозодифосфат является примером «метаболического посредника», вещества, встречающегося в схеме обмена веществ где-то посередине между известным исходным веществом (в данном случае это глюкоза) и легко определяемым итоговым веществом (в данном случае это этиловый спирт и углекислота). Определение и установление метаболических посредников крайне важно для правильного понимания процессов обмена веществ, происходящих в живой ткани, так что можно сказать, что с 1905 года начался отсчет систематического изучения метаболических посредников.
Вскоре были обнаружены и другие органические фосфаты, и, ко всеобщему изумлению, стало ясно, что именно фосфатные группы имеют непосредственное отношение практически к каждому шагу метаболизма. Ранее считалось, что фосфатные группы в живых организмах встречаются только в костях как часть неорганического скелета, а об их присутствии в большом количестве в мягких тканях по большей части не подозревали, а если ученые их там и обнаруживали, то не придавали этому факту особого значения. Теперь же фосфаты вдруг оказались в центре всеобщего внимания, поэтому и нам не грех будет посвятить им целую главу.
Глава 21. ЗНАЧЕНИЕ ФОСФАТОВ
Перед тем как обсуждать связь между фосфатными группами и метаболизмом, надо сначала немного поговорить о самом фосфоре.
В таблице Менделеева фосфор находится сразу же под азотом, что свидетельствует о сходстве атомного строения этих двух элементов. У атома азота две электронные оболочки, во внешней из них находится пять электронов, а у атома фосфора — три оболочки, во внешней из которых тоже находится пять электронов. Соответственно, в электронном изображении фосфор можно представить как
то есть точно так же, как и азот.
Атом фосфора может принимать в совместное пользование три электрона других атомов, предоставляя при этом в совместное пользование и три своих, так чтобы в целом достигать стабильного числа восемь. Так, например, с водородом фосфор образует соединение (фосфин, РН3) таким образом:
Точно так же образуется и аммиак (см. главу 17).
Кроме трех электронов, которые фосфор может предоставлять в совместное пользование, у него есть еще два, которые он никуда предоставлять не собирается (к примеру, в фосфине они остаются в полном распоряжении фосфора). Однако эти два электрона вполне могут быть предоставлены в пользование атому, которому только их и не хватает для обретения заветных восьми электронов во внешней оболочке. Естественно, первым из такого рода атомов нам приходит в голову кислород, во внешней оболочке которого всего шесть атомов.
Если сосредоточиться только на фосфоре и кислороде, то можно представить «разделяемые» его атомы как «просто связи» и рассматривать только «неразделяемые», таким вот образом:
Как видите, теперь потребность атома кислорода в восьми электронах удовлетворена без каких-либо потерь для фосфора, который также сохраняет эти электроны в своей внешней оболочке.
Связь, образуемая подобным образом — когда оба электрона предоставляются одним и тем же атомом, — так же сильна, как и образуемая обычным способом, когда каждый атом предоставляет по одному электрону для образования пары. В химии она именуется «координационной связью», и ее часто изображают на схемах в виде маленькой стрелочки, указывающей от того атома, который предоставляет электроны, на тот, который их принимает. Таким образом, фосфор имеет три ковалентных и одну координационную связь, что можно изобразить так:
Зачастую, как в случае с фосфином, задействованными оказываются только три ковалентные связи. Однако, особенно в тех случаях, когда речь заходит об атомах кислорода, для координационной связи тоже находится работа[7]. Кстати, все вышесказанное в равной степени относится и к атомам азота.
Самым важным фосфорсодержащим соединением является ортофосфорная кислота, которую часто называют просто «фосфорной кислотой» (Н3РO4), в которой всеми четырьмя связями фосфор соединен с атомами кислорода. Ее можно представить таким образом:
Где бы в живой ткани ни появлялся атом фосфора, он всегда оказывается входящим в состав соединения, родственного фосфорной кислоте. К примеру, фосфорная кислота может ионизироваться, сначала за счет ионизации одного атома водорода (Н+), в результате чего получается «первичный фосфат-ион» Н2РО4-, с отрицательным зарядом -1, а затем — второго и третьего атомов водорода с образованием вторичного и третичного фосфат-ионов: НРО42- и РО43-. Первые два из этих ионов обнаруживаются и в крови, и в тканях.
Кроме того, фосфорная кислота или получаемые из нее ионы могут вступать в соединение с другими веществами. В таких соединениях участвуют (иногда и более одной) гидроксильные (содержащие и водород, и кислород) группы, присутствующие в молекуле. Мы сосредоточимся именно на этой части молекулы фосфорной кислоты и, краткости и удобства ради, обозначим оставшуюся часть как (P). В таком виде краткая запись молекулы фосфорной кислоты будет выглядеть как Н — О — (P). В тех случаях, когда речь будет идти более чем об одной гидроксильной группе, к центральной (P) будут обозначены присоединенными вторая и третья гидроксильные группы.
При вступлении в соединение фосфорная кислота или ее ионы обычно непосредственно соединяются с гидроксильной группой другого вещества, что можно изобразить так: R — О — Н, где R — любая углеродосодержащая группа. Таким образом, запись R — О — Н может обозначать и спирт, и сахар или другие соединения, о которых мы не упоминали, — в общем, любое вещество, в состав которого входит гидроксильная группа.
Таким образом, реакцию фосфорной кислоты, скажем, с сахаром можно представить на рис. 45. В процессе присоединения отщепляется молекула воды, то есть мы имеем дело с реакцией конденсации, значит, реакцию обратную данной следует признать реакцией гидролиза.
Обычно уменьшение свободной энергии связано именно с гидролизом, так что точка равновесия данной реакции смещена далеко в сторону смеси сахара и фосфорной кислоты. При гидролизе сахарофосфата (примером такого вещества является упомянутый в предыдущей главе эфир Хардена—Янга) высвобождается от 2 до 4 килокалорий на моль вещества, в зависимости от конкретного вещества. То есть при гидролизе эфирной связи сахарофосфата высвобождается примерно столько же свободной энергии, сколько и при гидролизе пептидной связи белковой молекулы.
Естественно, для того, чтобы сформировать эфир путем конденсации сахара и фосфорной кислоты, необходимо затратить те же 2—4 килокалории на моль. Значит, чтобы создать такого рода эфирную связь, надо потратить столько же энергии, сколько на создание пептидной связи.
Рис. 45. Фосфорная кислота и сахар
Поскольку фосфорная кислота обладает гидроксильной группой, то одна молекула фосфорной кислоты вполне может конденсироваться и с другой такой же молекулой. В результате получается сочетание атомов типа — О — (|3), «пирофосфатная связь».
Конденсированные кислоты, приведенные на рис. 46, оставались бы вне поля зрения органической химии, если бы не тот факт, что в 1929 году немецкий биохимик К. Лохманн сумел выделить из мышц вещество, оказавшееся продуктом конденсации трифосфорной кислоты с органическим веществом аденозином, встречающимся в составе нуклеиновых кислот[8]. Соответственно, продукт конденсации получил название «аденозинтрифосфат».
Постепенно обнаруживалось участие аденозинтрифосфатов (теперь их принято обозначать общеизвестным уже сокращением АТФ) в различных реакциях, протекающих в организме. Они участвуют в процессе сокращения мышц; в передаче нервных сигналов; практически во всех стадиях обмена веществ.
Почему? Ну, начать хотя бы с того, что две фосфатные группы на удаленном от аденозина конце молекулы легче подвергаются гидролизу, чем фосфатные связи в целом. Это свидетельствует о том, что при гидролизе пирофосфатной связи уровень свободной энергии уменьшается сильнее, чем при гидролизе обычной фосфатной связи. Исследования подтвердили это предположение. Фриц Липман, американский физик немецкого происхождения, предположил по результатам своих исследований начала 40-х годов XX века, что существуют два типа фосфатных связей — обычные фосфатные связи, как в сахарофосфате, «низкоэнергетические», и «высокоэнергетические», примером которых является пирофосфатная связь.
Рис. 46. Пирофосфатная связь
Сперва выяснилось, что при гидролизе высокоэнергетической фосфатной связи высвобождается от 11 до 16 килокалорий энергии на моль вещества, просто колоссальная цифра по сравнению с двумя—четырьмя килокалориями на моль, высвобождаемыми при гидролизе обычной фосфатной связи. Однако дальнейшие исследования показали, что эта цифра завышена. В 50-х годах XX века уточненные исследования показали, что в среднем при гидролизе высокоэнергетических фосфатных связей высвобождается от 5 до 10 килокалорий, в среднем — 8. А при гидролизе некоторых фосфатных связей, которые принято было считать низкоэнергетическими, могло высвобождаться и до 6 килокалорий на моль. Получается, никакого строгого разрыва между этими двумя группами нет вообще.
Но все же остается признать, что существует один тип фосфатных связей, при гидролизе которых выделяется в среднем 8 килокалорий на моль вещества, и другой, при гидролизе связей которого выделяется в среднем 4 килокалории на моль. Хотя различие между ними не так велико, как показалось сначала, и некоторые биохимики уже начинают колебаться, есть ли оно вообще, я все же считаю оправданным разделение фосфатных связей на высоко- и низкоэнергетические.
Многие биохимики по привычке разделяют высоко- и низкоэнергетические фосфатные связи графическим обозначением валентной связи в формуле. Низкоэнергетическая связь обозначается обычным образом R — О — (P), а высокоэнергетическая фосфатная связь — волнистой линией. Так, обозначив АТФ за А, можно представить формулу таким образом:
Последние две связи, как видите, — пирофосфатные и высокоэнергетические. Если одну из них разорвать посредством гидролиза, то останется «аденозиндифосфат», или АДФ, формула которого выглядит как А — О — (P) — О — (P). Если разорвать еще одну, то останется «аденозинмонофосфат», или АМФ (он же «адениловая кислота»), формула которого А — О — (P). Теперь осталась только низкоэнергетическая фосфатная связь. Ее тоже можно разорвать с помощью гидролиза, так чтобы остался только аденозин, но энергии при этом третьем по счету гидролизе выделится немного — в два раза меньше, чем в любом из предыдущих случаев.
Помимо иирофосфатной, существуют и другие высокоэнергетические фосфатные связи. Возьмем органическую кислоту в общем случае (общую формулу можно записать так:
где R — любое из бесчисленного множества углеродсодержащих соединений, а СООН — «карбоксильная группа»), с которой мы уже не раз встречались.
Если фосфорная кислота конденсируется с гидроксильной частью карбоксильной группы (как на прилагаемой диаграмме), то в результате получается «ацилфосфат», изображаемый с волнистой связью, чтобы подчеркнуть ее высокую энергию (рис. 47).
Теперь давайте посмотрим, как высокоэнергетическая связь вступает в игру. Для этого вернемся к гликогену. Гликоген, содержащийся в печени и мышцах животных, в подробностях строения не совсем похож на крахмал, хранящийся в «запасниках» растений, но и гликоген, и крахмал формируются из молекул глюкозы, которые конденсируются с выделением при этом воды. Когда крахмал расщепляется в пищеварительном канале, амилазы катализируют процесс гидролиза единиц глюкозы на отдельные молекулы, добавляя воду обратно и разбивают крахмал на все более короткие цепочки, пока не получаются снова отдельные молекулы глюкозы.
И печень, и мышцы тоже должны уметь расщеплять гликоген на отдельные молекулы глюкозы, чтобы поддерживать должный ее уровень в крови. Так что логично предположить, что в тканях тоже работает некий фермент, подобный амилазам, который выполняет сходную работу — катализирует гидролиз.
Для проверки этого предположения необходимо было придумать такой эксперимент, который позволил бы понять, какие именно реакции происходят в живых тканях. Проще всего было бы сделать это, выбрав в качестве живой пробирки какое-нибудь подходящее животное вроде мыши. К сожалению, даже мышь — слишком сложное для такой задачи существо, в ее организме одномоментно проходят тысячи реакций.
Поэтому для упрощения задачи мышь придется убить и взять для исследования крошечные кусочки ее печени и мышц. Если правильно извлечь эти ткани и быстро подвергнуть обследованию, можно застать в образцах ферменты в работоспособном состоянии. Такие образцы помещали в растворы различных химических веществ. Действие ферментов настолько специфично, что если та или иная ткань катализирует определенную реакцию в лабораторных условиях, то вполне вероятно, что и в живом организме она катализирует ту же реакцию.
Рис. 47. Ацилфосфат
Если необходимо ускорить дело, то образец можно растолочь до полужидкой гомогенной кашицы («гомогената»), которую и поместить в субстрат. Тогда не придется ждать, пока субстрат проникнет в клетки—в процессе размешивания все ферменты лишились защиты клеточных мембран, и ничто не мешает им теперь проявлять каталитические свойства.
В гомогенате тоже содержится очень много ферментов, и обычно требуется сократить их число во избежание побочных реакций, которые могут помешать, и для того, чтобы концентрация необходимого фермента оказалась более высокой, чем в живом организме.
Это достигается путем подвергания гомогената условиям, о которых известно, что в них один фермент отделяется от другого. При помещении материала в некоторые растворы одни белки втягиваются в раствор, другие остаются в гомогенате. Отфильтровав после этого смесь, мы получим раствор, в котором содержатся только растворимые белки, «экстракт ткани», или «вытяжка из ткани». Получившуюся вытяжку можно дальше подвергнуть воздействию определенных кислот, ионов или некоторых органических растворов при низких температурах. При каждом из этих действий одни ферменты будут осаждаться, а другие останутся в растворе. Если повезет — можно дойти и до такого этапа, когда в растворе останется вообще только один, нужный, фермент.
Именно в результате длительной работы с вытяжками из ткани чета американских биохимиков чешского происхождения, Карл Кори и Герти Кори, сумели показать, что расщепление гликогена в тканях не имеет ничего общего с гидролизом и не катализируется амилазами.
В 1935 году К. и Г. Кори обнаружили, что если поместить вытяжку из мышц в гликоген, то никакого расщепления происходить не будет, пока в раствор не будет добавлен фосфат-ион. Естественно, первым делом исследователи предположили, что продукт распада должен будет вступить в соединение с фосфат-ионом, стали искать и в конце концов нашли в смеси сахарофосфат (не глюкозу!). В 1937 году они установили, что этот сахарофосфат, получивший к тому времени название «эфир Кори», является «глюкозо-1-фосфатом». (Шесть атомов углерода, входящих в состав глюкозы, имеют, согласно международной договоренности, номера от 1 до 6, и глюкозо-1-фосфат — это молекула, в которой фосфатная группа крепится к атому углерода № 1.)
Так оказалось, что гликоген в организме подвергается не гидролизу, а распаду с использованием фосфорной кислоты. Я поясню, что я имею в виду, на примере прилагаемой диаграммы. Пусть G — глюкоза, тогда гликоген — это цепочка G3, соединенная кислородными связями.
Рис. 48. Фосфоролиз гликогена
Длинная глюкозная цепочка гликогена расщепляется на одиночные молекулы сахара путем добавления наперерез связям элементов фосфорной кислоты. Если бы добавляемые элементы были молекулами воды, то речь шла бы о гидролизе. Раз вместо воды используется фосфорная кислота, то и реакцию эту естественно назвать «фосфоролизом» (рис. 48). Таким образом, гликоген в живых тканях расщепляется на глюкозо-1-фосфаты с помощью фосфоролиза.
Разница между этими двумя типами реакций имеет отношение к свободной энергии. Гидролиз гликогена на глюкозу подразумевает значительное уменьшение уровня свободной энергии, а для того, чтобы подобным же образом снова создать гликоген из глюкозы, потребуется такое же количество энергии приложить на каждое заново формируемое звено связи.
Фосфоролиз же гликогена на глюкозо-1-фосфат подразумевает крайне малое снижение уровня свободной энергии. Гликоген и глюкозо-1-фосфат находится почти на одинаковом энергетическом уровне. Соответственно, реакция фосфоролиза легко обратима, так что при равных концентрациях организм может легко переключаться между расщеплением и построением гликогена, в зависимости от потребностей, поддерживая таким образом необходимую для здоровья гармонию, что уже упоминалось в главе 19.
Однако производство глюкозо-1-фосфата всей полноты проблемы не снимает. Прежде всего, сахарофосфаты по какой-то причине не могут проникать через клеточную мембрану, так что любое соединение, содержащее глюкозо-1-фосфат, будучи созданным в клетке печени, обречено в ней и оставаться, пока не утратит фосфат. Поэтому при пищеварении образуется именно глюкоза, поскольку только она способна преодолеть кишечные мембраны и попасть в клетки тканей — глюкозо-1-фосфат не смог бы. И только глюкоза может присутствовать в крови, поскольку только она, а не глюкозо-1-фосфат, может проникать из крови в клетки и питать их. Поэтому именно глюкозу, а не глюкозо-1-фосфат, клетки печени должны выбрасывать в кровь.
Так и происходит. В клетках печени был обнаружен фермент, катализирующий превращение глюкозо-1-фосфата в глюкозо-6-фосфат (фосфатная группа при этом смещается от углерода-1 к углеро-ду-6, что не требует каких-либо заслуживающих упоминания перемен в энергии), а затем был обнаружен и второй фермент, действие которого заключается в отсечении фосфатной группы посредством гидролиза. Этот шаг высвобождает глюкозу, которая просачивается сквозь клеточную мембрану и попадает в кровоток.
Но обойти требования, касающиеся свободной энергии, невозможно. При переходе от глюкозо-6-фосфата к непосредственно глюкозе происходит ее высвобождение. То же самое произошло бы и при расщеплении гликогена на глюкозу напрямую; так не все равно — расщеплять гликоген напрямую или через посредническую цепочку из двух сахарофосфатов? Чем это лучше? Тогда перед тем, как образовывать гликоген из глюкозофосфатов, для образования глюкозофосфатов из глюкозы организму все равно придется где-то брать энергию — так не проще ли сразу образовывать его из глюкозы, минуя промежуточные стадии?
Нет. При формировании гликогена перед организмом встают две основные проблемы: надо создать большую и сложную молекулу из простых и маленьких и надо найти энергию для соединения каждой из связей в цепочке, каковых в каждой молекуле гликогена по тысяче. Если организм будет поставлен перед задачей создать гликоген сразу из глюкозы, ему придется решать обе эти проблемы одновременно, и очевидно, что организм с ними не справляется.
Если же сначала глюкоза преобразуется в глюкозо-6-фосфат, то энергию искать все равно приходится, но первая проблема при этом снимается — простое вещество переходит в другое, почти столь же простое. Затем, когда глюкозофосфат уже сформирован, организму остается только объединить единицы глюкозы в огромную молекулу, но энергии для этого уже почти не требуется. Таким образом, одна сложная задача для организма разбивается на две простые, и с ними поодиночке организм вполне справляется.
Описываемый баланс гликогена и глюкозы проиллюстрирован на рис. 49.
Рис. 49. Связь гликогена и глюкозы
Следующий вопрос таков: так или иначе, при переходе от глюкозы к гликогену организму все же необходимо найти-то источник энергии. Где же он ее берет? Иными словами, глядя на рис. 49, мы можем спросить: за счет чего организм переводит глюкозу в глюкозо-6-фосфат?
Вот здесь и проявляется роль высокоэнергетической фосфатной связи. Для перехода от глюкозы к глюкозо-6-фосфату требуются две вещи — фосфатная группа и энергия. АТФ обладает и тем и другим.
Реакцию глюкозы с АТФ можно выразить следующим образом:
Представим себе, что это выражение представляет собой комбинацию двух реакций. Первая — это перевод глюкозы в глюкозо-6-фосфат. При этом формируется низкоэнергетическая фосфатная связь, для чего требуется затратить около 4 килокалорий на моль вещества. Вторая — перевод АТФ в АДФ путем гидролиза высокоэнергетической фосфатной связи, в процессе чего высвобождается около 8 килокалорий на моль вещества. Получается, что гидролиза АТФ более чем достаточно для того, чтобы глюкоза могла превратиться в глюкозо-6-фосфат.
Это пример специфической парной реакции, при одной части которой высвобождается больше энергии, чем при второй — тратится, так что в итоге энергия все равно высвобождается (второй закон термодинамики не обойдешь).
До последнего времени существовало мнение, что АТФ — это и есть энергетический концентрат организма, и везде, где требуется проведение энергоемкой реакции, подключается АТФ. Однако с помощью современных методик анализа ткани было установлено, что существуют и другие трифосфаты, и теперь считается, что для различных реакций существуют и различные источники энергии. Тем не менее все они действуют по тому же принципу, и то, что я рассказал об АТФ, в равной степени относится и к близким к нему веществам.
Фруктоза и галактоза, два других простых сахара, впитываемые организмом, тоже образуют соединения при энергетической помощи АТФ (и особых ферментов, разумеется, не тех, которые действуют в отношении глюкозы). Фруктозо-1-фосфат и галактозо-1-фосфат превращаются в тот же глюкозо-1-фосфат с помощью реакций, не требующих заслуживающей упоминания энергии, а дальше фруктоза и галактоза обычным путем превращаются в гликоген.
Формирование гликогена из простых Сахаров, таким образом, «называется «гликогенезом», а расщепление гликогена на простые сахара — «гликогенолизом». Схема с участием АТФ и всех трех Сахаров представлена на рис. 50.
Рис. 50. АТФ и гликоген
Но что-то слишком гладко все получается. И правда, не можем же мы утверждать, что энергетический запас АТФ и подобных ему молекул — ответ на все задачи жизни? Что же происходит, когда он исчерпывается?
Естественно, он не исчерпывается, потому что если бы он исчерпался, то анаболизм прекратился бы, а вместе с ним — и жизнь. Поскольку жизнь не прекращается, значит, запас энергии каким-то образом возобновляется так же быстро, как и тратится.
Это означает, что организм каким-то образом строит АТФ из АДФ с той же скоростью, с какой АТФ расщепляется до АДФ в ходе множества парных реакций. Кажется, мы совсем запутались. Решив проблему энергоемких (4 килокалории на моль) процессов соединения глюкозы за счет гидролиза АТФ до АДФ, теперь мы должны решить проблему еще более энергоемких (8 килокалорий на моль) процессов создания АДФ из АТФ?
Что ж, они происходят в ходе анаэробного гликолиза, который я описывал в предыдущей главе.
На протяжении 30-х годов XX века биохимики выделяли промежуточные вещества реакций гликолизации дрожжей или живых тканей и искали ферменты, катализирующие реакции с участием этих промежуточных веществ. Выделение промежуточных веществ и изучение реакций позволило им шаг за шагом собрать, как мозаику, всю цепь катаболизма от глюкозы до молочной кислоты.
Сначала к глюкозе присоединяется фосфатная группа, затем, после перехода во фруктозу, — вторая. (Образованный таким образом фруктозодифосфат — это и есть тот самый «эфир Хардена—Янга», который я упоминал в прошлой главе.) Прикрепление каждого фосфата требует участия АТФ, так что может показаться, что цепочка гликолиза лишь усугубляет проблему, используя АТФ для своих целей, вместо того чтобы его создавать. Но мы ведь еще не закончили.
Фруктозодифосфат со своими шестью атомами углерода расщепляется на две половинки по три атома углерода в каждой (глицеральдегид-3-фосфата), в каждой из которых оказывается по одному фосфату. Что происходит с этим веществом дальше, показано на рис. 51.
Как видите, к нему добавляется вторая фосфатная группа, но не методом обычной конденсации. То есть в ходе этой реакции не образуется вода (Н — О — Н). Вместо этого выделяются два атома водорода — и все. Такой процесс называется дегидрогенизацией. При этом два выделяющихся атома водорода не образуют молекулы газообразного водорода, хотя я и записал их в выражении как просто 2Н. Их дальнейшая судьба немного сложнее, и мы вернемся к ним позже.
В результате дегидрогенизации образуется ацилфосфат, который, как я уже упоминал, является высокоэнергетическим соединением. Откуда же берется энергия для его образования? Из потери двух атомов водорода. Дегидрогенизация подразумевает снижение уровня свободной энергии на 35—70 килокалорий на моль вещества, и этого более чем достаточно, чтобы получить необходимые 8 килокалорий для формирования высокоэнергетической связи. (В строго анаэробных условиях такого масштабного пустого расходования энергии, что нам приходит в голову при виде приведенных цифр, не получается, потому что оба атома водорода в итоге потом возвращаются — вместе со своей энергией.)
Далее в цепочке формируется вторая высокоэнергетическая связь в ходе реакции, менее энергичной, чем дегидрогенизация, но тем не менее достаточной для превращения уже существующей низкоэнергетической связи в высокоэнергетическую.
Любое вещество, в состав которого входит высокоэнергетическая фосфатная связь (например, 1,3-дифосфоглицериновая кислота), может вступать в реакцию с АДФ для передачи ему этой фосфатной связи, образуя АТФ. На такой перенос связи никаких заслуживающих упоминания энергозатрат не требуется. Таким образом, формирование любой высокоэнергетической фосфатной связи равносильно формированию молекулы АТФ.
Рис. 51. Дегидрогенация
Рис. 52. Схема гликолиза
Итак, подытожим. При анаэробном гликолизе каждая молекула глюкозы начинает свое превращение в молочную кислоту с помощью двух молекул АТФ. Однако в конечном итоге глюкоза распадается на соединения с тремя атомами углерода, каждый из которых к моменту окончательного превращения в молочную кислоту доставляет в организм две молекулы АТФ.
Следовательно, шесть атомов углерода, содержащихся в глюкозе, используя две молекулы АТФ, создают их четыре, таким образом принося организму доход в две молекулы АТФ (рис. 52), которые потом можно использовать в парных реакциях для осуществления процессов анаболизма.
Но, как я уже говорил, гликолиз — неэффективный способ производства энергии. Если бы организм жил на одном гликолизе, он вел бы такое же тупое существование, как и дрожжи. Нас интересует большее, поэтому мы сейчас обратимся к кислороду.
Глава 22. ПЕРЕДАЧА ЭЛЕКТРОНОВ
Львиная доля производимой в процессе обмена веществ энергии выделяется в ходе реакций, в которых участвует атмосферный кислород. Перед тем как мы сможем свободно рассуждать об этих реакциях, надо сначала обговорить основные вещи.
Общепринятый термин для описания всех реакций, при которых в наличии имеется пламя, — «горение». Однако, после того, как Лавуазье показал, что при сгорании древесины происходит массированное соединение содержащихся в ней веществ с кислородом, распространение получило и более осмысленный термин «окисление».
Этот термин оказался не только более осмысленным, но и более общим. Процесс медленного соединения металлов с кислородом, в результате которого образуется окалина (сейчас мы называем ее оксидом), как показал Лавуазье, тоже является окислением, хотя горением его не назовешь. Иными словами, окисление — это любая реакция соединения вещества с атмосферным кислородом, независимо от того, вспыхивает ли при этой реакции пламя. Атмосферный кислород является в данном случае примером «агента окисления» (это может показаться тавтологией, но вскоре я покажу, что атмосферный кислород — не единственный распространенный в природе агент окисления).
С другой стороны, долгое время было принято говорить о процессе «восстановления» (англ. «reduction», от латинского «вести обратно») руды в состояние металла. Люди много веков наблюдали, как железо превращается в ржавчину, а большая часть металлических руд тоже похожа на ржавчину.
Обращаться с оксидами металлов, как с рудой, приходится довольно часто. Чтобы снова сделать из них металл, требуется удалить из состава оксидов атом кислорода. Так, если нагревать железную руду вместе с коксом, то атомы углерода, содержащиеся в коксе, соединятся с атомами кислорода, содержащимися в руде, оставляя металл свободным:
2Fe2O3 + ЗС → 3CO2 + 4Fe.
Поскольку восстановление спровоцировал углерод, то он являет собой пример «агента восстановления».
Таким образом, окисление — это процесс добавления кислорода к веществу, а восстановление — процесс удаления кислорода из вещества. Природа этих двух процессов прямо противоположна.
Есть еще один распространенный способ устранения кислорода из соединения с металлом — обработка водородом. В этом случае водород, как и углерод, служит агентом восстановления. Он вступает в соединение с кислородом и восстанавливает, в частности, медь, после того как она окислится дочерна.
Реакции с использованием водорода вызывают особый интерес у органических химиков. Они обнаружили, что определенные химические вещества, богатые кислородом и способные окислять металлы путем формирования оксидов, имеют также и свойство «выдирать» водород из молекул органических соединений. Соответственно, эти богатые кислородом вещества, среди которых — перманганат калия (КMnO4) и хромовокислый калий (К2CrO4), тоже являются агентами окисления. У ученых создалось стойкое представление, что все они отдают часть своего кислорода на окисление металлов или используют его для соединения с водородом, выцепляя его из органических молекул с последующим образованием воды. Соответственно, потеря водорода (дегидрогенизация) тоже стала рассматриваться учеными как форма окисления, даже если ни один атом кислорода к органической молекуле напрямую и не присоединялся.
Однако, если окисленную таким образом органическую молекулу обработать газообразным водородом (как правило, в присутствии какого-нибудь катализатора), реакцию окисления можно обратить вспять. Добавление водорода (гидрогенизацию) можно, таким образом, рассматривать как реакцию восстановительную, даже если опять же никакой кислород ниоткуда не извлекался.
Короче говоря, органические химики решили рассматривать окисление как добавление кислорода или удаление водорода, а восстановление — как удаление кислорода или добавление водорода.
Но и это еще не все обобщение. Металлы покрываются ржавчиной и патиной и под воздействием фтора, хлора, брома и серы, хотя ни кислород, ни водород тут вообще ни при чем. Точно таким же образом в качестве восстановительных агентов могут выступать металлический натрий, калий, магний и кальций, хотя в происходящих с их участием реакциях не затрагивается ни кислород, ни водород. Распространять термины «окисление» и «восстановление» на бесконечное множество реакций добавления и извлечения того или иного вещества казалось уже неразумным, и надо было ввести какое-то более глобальное обобщение. Оно было сделано только после открытия электронов.
В XX веке обнаружилось, что, подвергаясь окислению, вещество теряет электроны, а подвергаясь восстановлению — получает. Возникло естественное предложение вообще перестать использовать термины «окисление» и «восстановление» в связи с приобретением или потерей веществом какого-либо элемента, а пользоваться ими для обозначения процессов потери или приобретения электронов.
К примеру, когда металлический натрий вступает в реакцию с газообразным хлором для образования хлорида натрия, атом натрия теряет электрон и становится ионом натрия. Соответственно, можно сказать, что хлор окислил натрий, и рассматривать хлор как агент окисления. Однако в ходе той же самой реакции атом хлора приобретает электрон и становится ионом хлора. Значит, натрий восстанавливает хлор и является в таком случае агентом восстановления (рис. 53).
Рис. 53. Окислительно-восстановительная реакция
Опять же, при горении углерода в кислороде образуется углекислый газ, в котором каждый атом углерода связан ковалентными связями с двумя атомами кислорода. Передачи электрона, как таковой, в данном случае не происходит, ни один атом не теряет полностью электрона и не приобретает его. Но атом кислорода держит электроны крепче, чем атом углерода. Так что можно сказать, что атом углерода теряет часть своего электрона и все же является окисленным, а кислород выступает в качестве агента окисления. С другой стороны, атом кислорода приобретает часть электрона, а значит — восстанавливается, а восстановительным агентом является углерод.
Как видите, не бывает ни окисления самого по себе, ни восстановления самого по себе. В обычных химических реакциях электроны не могут существовать сами по себе, они могут лишь переходить от одного атома к другому, целиком либо частично. Атом, теряющий электрон, — окисляется, приобретающий — восстанавливается. Значит, окисляемое вещество всегда является агентом восстановления для второго участвующего в реакции вещества, а то, в свою очередь, — агентом восстановления для первого. Разумеется, это касается не всех реакций — если атомы распределяются поровну, как в случае образования молекулярного хлора из атомного, то в этом процессе нет ни восстановления, ни окисления.
Принимая во внимание неразрывную связь между окислением и восстановлением, химики дали такого рода реакциям двойное название «окислительно-восстановительных».
Так как же проходят с точки зрения перераспределения электронов реакции гидрогенизации и дегидрогенизации?
Эффект от потери водорода необходимо рассматривать по-разному, в зависимости от того, имела ли место также потеря электронов, поскольку для данного процесса это вопрос первостепенной важности. Иногда вещество высвобождает атом водорода вообще без «положенного» ему электрона. Водород, лишенный электрона, является положительно заряженным ионом водорода Н+. А остаток вещества становится, таким образом, отрицательно заряженным ионом, и весь процесс в целом получает название ионизации. Получило ли вещество в этом случае электрон и можно ли считать его подвергшимся «восстановлению»?
Правильный ответ — нет. Ион водорода высвобождается только в том случае, если его связь с неким совместно используемым электроном (общим, чаще всего, с кислородом) уже является столь слабой, что он просто «отпадает» от соединения. Он не теряет электрона в процессе ионизации, а остальная часть соединения — не приобретает его. Скорее следует признать факт свершившейся ионизации признаком того, что электрон уже перешел от водорода к остальной части вещества в результате каких-то предыдущих событий. Сама по себе ионизация не является ни окислением, ни восстановлением.
Рис. 54. Дегидрогенизация — электронная запись
Но, предположим, что атом водорода удален из соединения вместе со своим электроном. Такая ситуация представлена на рис. 54. (Вопрос о том, что происходит при этом с самим атомом водорода, отложим на потом. Сейчас рассмотрим только освободившуюся связь.)
Теперь можно сказать, что у органического вещества остался один электрон в полном распоряжении — а раньше было два, но в частичном. Поскольку атом углерода держит электроны чуть крепче, чем атом водорода, то когда у углерода и водорода было два совместно используемых электрона, на долю углерода приходилась чуть большая часть. Теперь же «чуть большая часть от двух», то есть «чуть более одного электрона», заменено на просто «один электрон». Значит, часть электрона соединение потеряло, и его можно счесть окисленным. Таким образом, дегидрогенизация остается окислительной реакцией и в новом, электронном понимании.
Следуя такой же логике, можно доказать и что потеря атома кислорода (хоть в одиночку, хоть в составе гидроксильной группы) вместе со всеми электронами предоставляет оставшейся части молекулы полный контроль над одним электроном вместо слабых попыток совместного с кислородом контроля над двумя электронами. Оставшаяся часть молекулы приобретает таким образом долю электрона, так что удаление из нее кислорода означает восстановление.
Но вернемся к дегидрогенизации, схема которой приведена на рис. 54. Обратите внимание, что после удаления атома водорода у углевода остается один непарный электрон. Группа атомов, обладающая непарным электроном, называется «свободным радикалом».
Свободные радикалы в таком виде пребывают недолго, поскольку оставшийся без пары электрон — очень нестабильное образование. Он вынужден искать себе пару, и вскоре обязательно с его участием происходит какая-нибудь химическая реакция.
Конечно, если удалить два атома водорода (каждый вместе со своим электроном), так что одновременно в одной молекуле образуются два непарных электрона, то они вполне могут найти себе пару в лице друг друга, образовав «двойную связь», как на рис. 55.
В большинстве случаев окисления органических веществ происходит действительно именно такая «двойная» дегидрогенизация — потеря двух атомов водорода. При такого рода дегидрогенизации происходит значительное снижение уровня свободной энергии — настолько значительное, что такие реакции, происходящие в процессе катаболизма, и представляют собой источник энергии для образования высокоэнергетических фосфатных связей.
Тем не менее при обычных условиях такого, как правило, не случается. Органическое вещество может существовать годами, и никакой дегидрогенизации с ним не происходит, пока оно не окажется в центре значительного изменения уровня свободной энергии.
Рис. 55. Образование двойных связей
Понятно, что потребуется еще и значительное количество энергии активации. В 1935 году Михаэлис (тот самый, один из авторов формулы Михаэлиса— Ментена) указал, что крайне маловероятно, чтобы органическое соединение потеряло два атома водорода одновременно. Гораздо вероятнее, что сначала оно потеряет один атом, а потом — второй. То есть должна существовать некая промежуточная форма, когда один электрон уже утрачен, а второй — еще нет, и в этот момент вещество будет представлять собой свободный радикал.
Свободный радикал — нестабилен, а для его создания требуется приложить много свободной энергии. С потерей второго электрона энергозатраты более чем восполнятся; однако сначала все же надо оторвать первый электрон, а для этого надо найти энергию активации, и именно эта сложность и не дает всем органическим соединениям (включая те, из которых состоим мы сами) немедленно разложиться на воду и углекислоту.
Однако в тканях имеются ферменты, катализирующие дегидрогенизацию при комнатной температуре. Это делается за счет снижения энергетического содержания свободного радикала — его стабилизации, иными словами. Таким образом, энергия активации уменьшается до той точки, при которой кинетической энергии молекул при комнатной температуре оказывается достаточно, чтобы приводить к образованию свободных радикалов. Когда это происходит, то, разумеется, тут же теряется и второй атом водорода и образуется двойная связь.
Но каким же образом стабилизируется свободный радикал?
На протяжении всего XIX века химики пытались создать вещества, которые мы сейчас называем свободными радикалами и которые существовали бы хоть сколько-нибудь долго, но ничего у них не выходило. Получилось это, наконец, у американского биохимика Мозеса Гомберга только в 1900 году. Гомберг показал, что некоторые сложные свободные радикалы можно заставить существовать неопределенно долго, и об их существовании свидетельствует цвет раствора.
Первый созданный таким образом свободный радикал, трифенилметил, состоит из атома углерода, соединенного с тремя бензольными кольцами. (Сам бензол состоит из шести атомов углерода и шести атомов водорода, объединенных в симметричное замкнутое кольцо.) Все три бензольных кольца, как нам известно, находятся в одной плоскости и расположены симметрично относительно центрального атома углерода, как изображено на рис. 56.
Рис. 56. Свободный радикал трифенилметил и его отношение к бензольному кольцу
Но с чего вдруг этот конкретный свободный радикал оказался таким стабильным? Впервые разумно объяснить это смог американских химик Лайнус Полинг только в начале 30-х годов XX века. Полинг взял на вооружение теории 20-х годов о том, что электрон — это не крошечный шарик, лишенный собственных свойств, а совокупность волн, способных размываться по большему или меньшему пространству, в зависимости от обстоятельств.
Основываясь на представлении о волновой природе электронов, Полинг разработал математическую теорию, которую назвал «теорией резонансов». Помимо прочего, с помощью этой теории он смог показать, что чем в большей степени непарный электрон способен размываться, тем более он стабилен.
Вероятность размывания электрона больше в тех случаях, когда молекула, в состав которой он включен, расположена в одной плоскости и симметрична. Трифенилметил Гомберга идеально удовлетворяет этим требованиям. На рис. 56 я изобразил непарный электрон в виде точки, но это уже не соответствует реальным представлениям химиков о природе электрона. Правильнее было бы изобразить его в виде-туманности, обволакивающей молекулу, с симметричными областями высокой концентрации на некоторых участках.
Михаэлис, услышав про теорию резонанса, указал, что соединение фермента с субстратом — гораздо более симметрично, чем молекула субстрата сама по себе. В таком случае свободный радикал субстрата, объединенного с ферментом, будет гораздо более устойчивым соединением, чем просто свободный радикал субстрата, и для образования свободного радикала из комплекса «субстрат-фермент» потребуется гораздо меньше энергии, чем для образования свободного радикала из просто субстрата, — именно за счет этого фермент столь успешно катализирует реакцию.
Вернемся же к судьбе тех двух атомов водорода, которые были удалены из органического вещества путем дегидрогенизации. Один из возможных вариантов — что они объединятся в молекулу газообразного водорода и улетят. Однако при дегидрогенизации органических веществ в живой ткани этого, как правило, не происходит, за исключением тканей нескольких видов бактерий.
Альтернативный вариант — атомы перейдут к некоей «принимающей» молекуле, которая, приобретя атомы водорода, таким образом «восстанавливается». В качестве варианта такой молекулы напрашивается кислород, значит, пора нам присмотреться к электронному строению этого элемента.
В атоме кислорода восемь электронов, два во внутренней оболочке и шесть — во внешней. В электронной записи этот атом можно отобразить так:
В обычных условиях этот атом в свободном виде не встречается, а существует по парам, составляющим молекулу кислорода. Логично предположить, что при этом у двух атомов формируется общее множество из двух пар электронов, так что в оболочке каждого из них оказывается вожделенная восьмерка:
Проблема в том, что кислород обладает, ко всему прочему, еще и сильным магнетическим действием, и химики уверены, что причиной тому — наличие непарных электронов. Так что более вероятной кажется вот такая картина:
Это уже два свободных радикала, которые тем не менее являются стабильными. Достаточно интересное исключение для тех, кто занимается теоретической химией, но мы сейчас в это углубляться не будем.
Такая молекула кислорода легко может принять два атома водорода следующим образом (привожу как «электронную», так и обычную запись):
H2O2 — это перекись водорода, достаточно нестабильное соединение, имеющее тенденцию к расщеплению на воду и кислород:
2H2O2 → 2H2O + O2.
Распад перекиси водорода — спонтанная реакция, представляющая уменьшение свободной энергии (рис. 57). Своей медленной скоростью (а хранить раствор перекиси водорода при низких температурах можно достаточно долго без значительных потерь) она обязана тому факту, что для распада необходимо разорвать связь О—О, а для этого нужна достаточно большая энергия активации.
Для получения этой энергии активации, а значит, и ускорения распада перекиси водорода достаточно даже слабого нагревания. Ряд химических веществ способны этот распад катализировать, например железные опилки или широко распространенный фермент каталаза.
Поскольку при переходе от перекиси водорода к воде уровень свободной энергии значительно снижается, то можно сказать, что при переходе от кислорода к воде уровень свободной энергии снижается сильнее, чем при переходе от кислорода к перекиси водорода. Следует ли в таком случае ожидать, что кислород, принимая водород, каждый раз будет образовывать воду?
Застревание происходит на этапе разрыва связи О—О. Если кислород соединяется с водородом при высоких температурах (к примеру, при сжигании смеси кислорода с водородом или сжигании же какого-нибудь органического соединения) связь кислорода с кислородом рвется без проблем и образуется вода.
Рис. 57. Перекись водорода и вода
Если же кислород соединяется с водородом при комнатной температуре, как это случается при некоторых реакциях, катализируемых ферментами, на разрыв связи «кислород-кислород» энергии может и не хватить и вместо воды образуется перекись водорода.
Однако в живых тканях перекись водорода в каких-либо значительных концентрациях не встречается — и хорошо, потому что она очень ядовита. Одним из возможных тому объяснений служит присутствие каталазы. Ее действие может заключаться в том, что любая образующаяся молекула перекиси водорода тут же расщепляется с образованием воды. Однако, как мы вскоре увидим, вполне вероятно, что крупномасштабного образования перекиси водорода в организме вообще не происходит, а каталаза служит лишь для подстраховки и потребность в ней возникает нечасто.
Кислород, конечно, наиболее вероятный захватчик свободного атома водорода, но не единственно возможный. Атом водорода, который одно органическое вещество отпускает, может быть принят целым рядом других органических веществ.
Чтобы лучше понять этот факт, представим, что множество органических веществ могут существовать в двух формах — в восстановленной и окисленной, причем разница между ними будет заключаться в присутствии или отсутствии двух атомов водорода. Это можно выразить следующим образом:
АН2 ↔ А + 2Н.
ВН2 ↔ В + 2Н и так далее.
восстановленная форма ↔ окисленная форма
Окислительно-восстановительные реакции будут, естественно, разными для разных веществ. К примеру, у первой из вышеприведенных реакций точка равновесия может быть смещена вправо, так что АН2 будет иметь ярко выраженную склонность к потере двух атомов водорода. С другой стороны, у второй реакции точка равновесия может быть смещена влево, так что В будет иметь склонность к присоединению атомов водорода.
В таком случае, если смешать АН2 и В, то получим следующую реакцию:
АН2 + В → ВН2 + А.
АН2, теряя атомы водорода, окисляется агентом окисления В. Само же В, приобретая водород, восстанавливается агентом восстановления АН2.
Теперь нам остается только разработать какой-то способ измерить склонность водорода перетекать от одного вещества к другому, и это даст нам возможность предсказать, какое из них будет окисляться, а какое — восстанавливаться.
Для этого необходимо вспомнить, что и потеря, и принятие атомов водорода на самом деле лишь один из аспектов потери и принятия электронов. Любое вещество, имеющее склонность раздавать электроны, оказывает «давление», посылающее их по электрической цепи. Такое давление является электрическим потенциалом. Можно установить электрические батареи типа I, о которых я говорил в главе 10, и измерить в вольтах электрический потенциал той или иной окислительной реакции. Привести их к определенным стандартным условиям — и мы получаем «окислительный потенциал».
Окислительный потенциал реакции, при которой атом водорода отдает один электрон и превращается в ион водорода, произвольно принят за ноль. Окислительный потенциал любого атома или молекулы, проявляющих меньшую склонность к тому, чтобы отдавать электрон, считается положительным, проявляющих большую склонность отдать электрон — отрицательным.
Любое вещество всегда будет принимать электроны (иногда вместе с атомами водорода в качестве бесплатного приложения) от другого вещества, имеющего меньший положительный (или вообще отрицательный) окислительный потенциал. И точно так же любое вещество будет отдавать электроны (иногда вместе с атомами водорода) другому веществу, имеющему больший положительный (или меньший отрицательный) окислительный потенциал.
Можно даже представить серию окислительно-восстановительных реакций с участием одних и тех же электронов или одних и тех же атомов водорода, переходящих от одного вещества к другому по цепочке последовательного уменьшения отрицательных и увеличения положительных окислительных потенциалов.
Именно так на самом деле и происходит в живой ткани — давайте же вернемся к ней.
Глава 23. ЖИЗНЬ С ВОЗДУХОМ
При рассмотрении реакций, проходящих с участием атмосферного кислорода, естественно возникает желание разобраться в самом процессе впитывания кислорода живой тканью (ну, наполняет он легкие, и что дальше?).
Из таких разных существ, как картошка и мышь, добывались образцы тканей, системы ферментов в которых оставались в достаточной степени нетронутыми, чтобы продолжать катализировать положенные им реакции с использованием кислорода даже в отрыве от самого организма. Для некоторых целей нет необходимости сохранять клетки нетронутыми, поскольку реакции, потребляющие кислород, могут происходить и в достаточно чистых растворах ферментов.
Такие реакции обычно проводят в маленьком закрытом контейнере, так чтобы изменения давления в нем оказывались ощутимыми. Такой контейнер состоит из двух частей, в одной из которых находится раствор субстрата, а в другой — раствор фермента или образцы тканей. Стоит чуть-чуть покачать контейнер — и начнется реакция.
В обычных условиях начал бы потребляться кислород и выделяться углекислый газ. В результате потребления кислорода в контейнере мог бы образоваться частичный вакуум, но благодаря производству углекислого газа (что всегда происходит, когда речь идет о живых клетках) потеря возмещается и нормальное давление газа сохраняется. Однако, если внутри контейнера есть еще и небольшая ниша, в которой находится некий раствор, быстро поглощающий углекислый газ, то возмещения общего объема газа в контейнере происходить не будет. Общее снижение давления будет свидетельствовать о потреблении кислорода.
Контейнер герметично соединен с U-образной трубкой, открытой в атмосферу, нижняя часть которой заполнена цветной жидкостью. С одной стороны трубки на жидкость давит воздух, содержащийся в контейнере, с другой — обычное атмосферное давление. По мере протекания в контейнере катализируемой ферментом реакции и потребления кислорода давление в нем падает, и баланс между внутренним и внешним давлением нарушается. Жидкость в трубке со стороны атмосферы ползет вниз, а со стороны, присоединенной к контейнеру, — вверх.
Естественно, в таких случаях принимаются все меры к тому, чтобы движение жидкости осуществлялось только под воздействием возрастающей разреженности воздуха в контейнере. Контейнер помещен в теплую ванночку и содержится при постоянной температуре во избежание изменения объема воздуха в связи с изменениями температуры. Рядом находится такой же контейнер, но лишенный фермента, — контрольный, чтобы экспериментаторы видели, насколько на колебания жидкости в трубке влияют посторонние факторы, например небольшие колебания атмосферного давления.
В конечном итоге точно фиксируется сдвиг уровня жидкости в трубке и по нему определяется количество потребленного в результате катализируемой ферментом реакции кислорода. Только что описанное устройство в самом распространенном виде изобрел в 1923 году немецкий биохимик Отто Варбург, поэтому его иногда называют «респирометром Варбурга». Слово «респирометр» происходит от слов «дыхание» и «мерить».
Если в респирометр Варбурга поместить растолченную мышцу, то по мере того, как содержащиеся в ней ферменты будут катализировать реакции, кислород будет потребляться. Однако через некоторое время потребление кислорода начинает снижаться до весьма низких значений. Казалось, что ферменты денатурировались и утратили активность. Впрочем, потеря активности наблюдалась и в том случае, когда ферментам создавались все условия для того, чтобы они не денатурировались. Тогда возникло предположение, что замедление реакции связано с полной выработкой субстрата.
В последнем случае потребление кислорода снова возросло бы с добавлением субстрата, — оставалось только решить, что же именно является необходимым субстратом. Видимо, субстрат для некоторых ферментов находился не в растворе, помещенном в контейнер, а в самой мышце, так что в контейнер стали по очереди добавлять обнаруживаемые в ней вещества.
В 1935 году венгерский биохимик Альберт Сент-Дьёрдьи установил, что потребление кислорода возобновляется в том случае, если к толченой мышце добавить одно любое из четырех веществ — янтарную кислоту, фумаровую кислоту, яблочную кислоту или щавелево-уксусную кислоту. Молекулярное строение этих веществ сходно, как видно из рис. 58. Все они являются «двухосновными кислотами», поскольку молекула каждой содержит по две карбоксильных группы.
Очевидно, каждое из этих веществ каким-то образом задействуется в реакциях с потреблением кислорода. Однако они не могут использоваться просто как строительный материал, поскольку объем кислорода, который начинает потребляться после добавления любого из этих веществ, значительно превышает необходимый для связывания всего вновь добавленного количества. Видимо, начинает происходить не одна реакция, а ряд реакций, при которых используемое вещество (к примеру, янтарная кислота) возобновляется с той же скоростью, что и расходуется, так что ее участие скорее следует счесть каталитическим. По мере продолжения серии реакций становится понятно, что запас янтарной кислоты возобновляется не полностью, так что идет ее медленное растрачивание, и, в конце концов, для продолжения реакций оказывается необходимым добавление новой порции янтарной кислоты извне.
Рис. 58. Двухосновные кислоты
Дальше мы увидим, что четыре перечисленных вещества принимают участие не в четырех различных реакциях, а в одной и той же. Доказательство этого факта было получено благодаря малоновой кислоте.
Если в толченую ткань добавить янтарной кислоты для того, чтобы возобновить потребление кислорода, то стоит только после этого добавить малоновой кислоты, как потребление кислорода тут же снова прекращается. Это вполне ожидаемый эффект, поскольку малоновая кислота является конкурентным угнетателем янтарной (см. главу 18). Однако после добавления малоновой кислоты останавливалось потребление кислорода и возобновившееся после добавления любого из трех остальных веществ. А ведь напрямую подавлять реакции, проходящие с участием яблочной или щавелево-уксусной кислоты, малоновая кислота не может. Значит, будучи добавленной в растолченную ткань, она останавливает общий ход реакции за счет того, что где-то в нем используется часть именно янтарной кислоты. После того как было проведено много исследований в этом направлении, немецкий биохимик Ханс Адольф Кребс сумел продемонстрировать, что добавление и других веществ, в частности — лимонной кислоты (в которой содержится шесть атомов углерода и три карбоксильные группы, а не четыре атома углерода и две карбоксильные группы, как в четырех установленных Сент-Дьёрдьи кислотах), тоже приводит к возобновлению реакций с потреблением кислорода. В 1940 году Кребс разработал схему, в которой все необходимые вещества заняли свое логическое положение, и с тех пор эта схема претерпевала лишь самые незначительные изменения.
По понятным причинам эта серия химических реакций получила название «цикл Кребса», но есть названия и более описательные — «цикл трикарбоновых кислот», или «лимоннокислый цикл», поскольку лимонная кислота обладает тремя карбоксильными группами.
Давайте посмотрим, стараясь обойтись как можно меньшим числом формул и подробностей, как же работает цикл Кребса.
При анаэробном гликолизе, как я объяснял в главе 20, молекула глюкозы превращается в две молекулы молочной кислоты, производя при этом две высокоэнергетические фосфатные связи, принимающие в итоге вид АТФ. Далее предстоит катаболизм молочной кислоты с образованием дополнительных высокоэнергетических связей.
Этот процесс начинается с устранения из молочной кислоты двух атомов водорода (дегидрогенизации) с образованием пировиноградной кислоты, как показано на рис. 59.
Сочетание С=О называется «кетоновой группой», или, короче, «кетогруппой», а сочетание СООН, вам, я надеюсь, уже знакомое, — «карбоновокислой группой». Любое химическое соединение, где, как, например, в пировиноградной кислоте, содержатся обе эти группы, называется «кетокислотой».
В организме кетокислоты практически неизбежно подвергаются химической реакции, в ходе которой теряют один атом углерода. Опустив подробности, скажем лишь, что в результате пировиноградная кислота (с тремя атомами углерода) превращается в уксусную (с двумя атомами углерода), как показано на рис. 59.
Рис. 59. Дегидрогенизация и окислительная декарбоксилизация
Такая реакция является примером «окислительной декарбоксилизации». Окислительной — потому что при ней удаляется два атома водорода, а декарбоксилизации — потому что углекислота при этом тоже удаляется. Конкретно эта реакция окислительной декарбоксилизации катализируется ферментом, в котором используется кофермент, содержащий группу атомов, представляющую собой довольно сложную молекулу «тиамин». Это и есть тот самый витамин В1? отсутствие которого вызывает у человека болезнь берибери. Именно дефицит этого витамина Эйкман изучал в 90-х годах XIX века (см. главу 18), и именно связанные с ним исследования положили начало изучению витаминов в целом. И вот пример того, для чего нужен витамин, — без него реакция превращения пировиноградной кислоты в уксусную не состоится и вся метаболическая цепочка реакций начнет пробуксовывать.
При переводе органических веществ в воду и углекислый газ вода образуется в ходе реакций дегидрогенизации, поскольку атомы водорода, теряемые такими веществами, как молочная кислота, в итоге объединяются с кислородом. Углекислый газ формируется по большей части в ходе реакций окислительной декарбоксилизации кетокислот.
Именно на этапе дегидрогенизации и производится используемая организмом энергия. Само по себе устранение из вещества углекислоты не позволяет получить достаточно энергии для формирования высокоэнергетических фосфатных связей. Значит, можно сделать вывод, что организм получает энергию за счет сжигания водорода, а сжигание углерода — в общем-то случайное побочное явление. Это неудивительно, поскольку, как я уже писал (см. главу 8), при сжигании водорода высвобождается гораздо больше тепла, чем при сжигании углерода.
Следующим этапом уксусная кислота добавляется в щавелево-уксусную и попадает в цикл Кребса (как вы помните, щавелево-уксусная кислота оказалась одним из первых веществ, участие которого в цикле стало известно).
В начале 40-х годов XX века подробности процесса добавления были еще неизвестны. Однако уже в 1947 году Липман (первооткрыватель высокоэнергетических фосфатных связей) сумел выделить вещество, служащее коферментом для данной реакции, и назвал его «кофермент А».
Рис. 60. Кофермент А
Молекула кофермента А достаточно сложна, и я не буду вас мучить. Большая часть ее — это пантотеновая кислота, витамин В3, который организм сам производить не умеет, а значит — должен получать с пищей.
Та часть кофермента А, которая участвует в реакции, — это тиоловая группа (— S — Н). Поэтому молекулу кофермента А часто обозначают так:
CoA — S — Н.
Кофермент А конденсируется с уксусной кислотой, как показано на рис. 60, образуя ацетилкофермент А. На самом деле он участвует в реакции окислительной декарбоксилизации пировиноградной кислоты, так что сама уксусная кислота здесь образоваться не может. Сразу получается ацетилкофермент А.
Ту часть молекулы уксусной кислоты, которая присоединена к коферменту А, иногда называют «двухуглеродным фрагментом». Это дань традиции, происходящей из тех времен, когда точное строение этой части еще было неизвестно.
В организме происходит много реакций, при которых двухуглеродный фрагмент переходит от одного вещества к другому, и в каждом случае именно кофермент А является той рабочей лошадкой, которая выполняет эту задачу. Позже было установлено, что кофермент А участвует и в реакции с альфа-кетоглютаровой кислотой, тоже задействованной в цикле Кребса, и там выполняет задачу переноса уже четырехуглеродного фрагмента. Не стоит считать, что кофермент А может иметь дело только с двухуглеродными фрагментами, и мы еще вернемся к этой теме, когда речь зайдет о других его задачах по переносу.
Добавление к щавелево-уксусной кислоте ацетилкофермента А показано и на рис. 60. Эта сложная реакция (но при тщательном рассмотрении вы сами убедитесь, что каждому атому слева соответствует атом справа), в результате которой образуется лимонная кислота со своими шестью атомами углерода, а кофермент А формируется заново и отправляется за следующей молекулой уксусной кислоты.
После образования лимонной кислоты она проходит через ряд реакций и в итоге избавляется-таки от добавленного к ней двухуглеродного фрагмента. Таким образом, лимонная кислота превращается обратно в щавелево-уксусную. Теперь щавелево-уксусная кислота снова может приобрести двухуглеродный фрагмент, который снова будет утерян при следующей итерации цикла Кребса, и так далее.
Формулы, которые я приводил в данной главе, иллюстрируют основные этапы процесса: окислительную декарбоксилизацию, дегидрогенизацию, катализируемый перенос коферментами и так далее. Так что теперь мы можем перейти, уже без формул, к схеме-иллюстрации процесса катаболизма молочной кислоты. Эта схема приведена на рис. 61, и, уверяю вас, там показаны только самые основные моменты.
Рис. 61. Катаболизм молочной кислоты
Как видите, молочная кислота сначала подвергается одной дегидрогенизации, превращаясь таким образом в пировиноградную, затем — второй в процессе образования ацетилкофермента А, а затем — еще четырем в процесс цикла Кребса. Всего получается шесть дегидрогенизаций, в ходе которых теряется двенадцать атомов водорода.
Но ведь в молекуле молочной кислоты всего шесть атомов водорода, как вы сами можете убедиться, взглянув на формулу, изображенную на рис. 59. Как же она ухитряется потерять двенадцать?
Как показывает общая схема цикла Кребса, на входе в него на трех разных участках поступают три молекулы воды. Они-то и предоставляют те самые недостающие шесть атомов водорода.
Кроме того, серия изменений, которым подвергается молочная кислота и вещества, в которые она последовательно превращается, включает в себя де-карбоксилизацию в процессе образования ацетил-кофермента А и еще две декарбоксилизации в ходе цикла Кребса для образования всего трех молекул углекислоты.
Соответственно, общее выражение будет выглядеть так:
С3H6O3 + 3H2O → 3CO2 + 12H.
молочная кислота
Возникает несколько вопросов. Во-первых, давайте вернемся к судьбе наших атомов водорода. Понятно, что должен использоваться кислород, поскольку, в конце концов, и сам цикл Кребса был открыт только благодаря исследованиям процессов потребления кислорода. Однако кислород ведь не принимает атомы водорода напрямую, поскольку эксперименты показывают, что перекись водорода не образуется в тканях, даже если ткани бедны каталазой.
Значит, кислород принимает атомы водорода через какое-то посредничество, так чтобы в итоге получалась не перекись водорода, а вода. Остается предположить, что атомы водорода сначала принимает какая-то другая молекула, не кислород, а затем — передает кислороду. Так же как кофермент А переносит двухуглеродные фрагменты, какой-то другой кофермент должен переносить и атомы водорода.
На самом деле такие «переносчики водорода» были открыты еще за поколение до того, как был обнаружен кофермент А. Первым из переносчиков водорода был вообще самый первый из открытых коферментов — козимаза, обнаруженная Харденом и Янгом (см. главу 18). В начале 30-х годов XX века была установлена и молекулярная структура козимазы. Я не буду сейчас углубляться в подробности, как и в отношении кофермента А, но основные моменты перечислю.
Прежде всего, в состав козимазы входит молекула сахара из пяти атомов углерода, две фосфатные группы и азотсодержащее атомное кольцо. Все это позволяет отнести молекулу к классу нуклеотидов. Азотсодержащее кольцо имеет пиридиновую форму, как я уже упоминал в главе 18, так что вся молекула получила научное название «дифосфопиридиннуклеотид», или, в сокращенной записи, ДПН. В 1934 году Варбург, изобретатель респирометра, выделил очень похожий кофермент, который отличался от козимазы только тем, что в его состав входят три, а не две фосфатные группы. Соответственно, это вещество получило название «трифосфопиридиннуклеотид», в сокращении ТПН.
И в ДПН, и в ТПН входит особый вариант пиридинового кольца, известный как никотинамид, который организм может образовывать только на основе похожего вещества — никотиновой кислоты. Значит, либо никотинамид, либо никотиновая кислота тоже должны присутствовать в пище — это тоже витамины группы В.
На протяжении 30-х и 40-х годов XX века ученые выделяли все больше и больше ферментов, катализирующих дегидрогенизацию различных веществ, и все открытые ферменты получили общее название «дегидрогеназы». В состав большой части дегидрогеназ входят в качестве необходимого кофермента либо ДПН, либо ТПН. Поэтому дегидрогеназы получили еще одно название, свидетельствующее о важности для их строения пиридинового кольца: «пиридин-ферменты».
Активной группой, «режущей кромкой», так сказать, каждого пиридин-фермента является именно ДПН или ТПН. Однако специфику фермента определяет все же аминокислотная составляющая (апофермент). Именно она представляет собой решающий фактор, благодаря которому вступить в контакт с коферментом, а значит — послужить субстратом, могут только особые вещества. То есть десяток разных пиридин-ферментов, в состав которых входят десять различающихся между собой аминокислот, будут катализировать дегидрогенизацию десяти разных веществ, и ни один из ферментов не сможет повлиять на девять «соседских» субстратов.
Вообще говоря, из шести процессов дегидрогенизации, включенных в катаболизм молочной кислоты, пять проходят с помощью пиридин-ферментов, причем каждый раз разных. Шестая же дегидрогенизация проходит с участием янтарной кислоты, и об этом чуть позже.
Функция ДПН и ТПН — принимать атом водорода, отдаваемый субстратом. Субстрат отдает атом водорода и окисляется, а ДПН или ТПН — принимает и восстанавливается. Восстановленный ДПН или ТПН можно обозначить, не вдаваясь в тонкости строения, просто как ДПН- 2Н или ТПН- 2Н. Таким образом, дегидрогенизацию молочной кислоты в пировиноградную, катализируемую пиридин-ферментом «дегидрогеназой молочной кислоты», можно представить, не вдаваясь в подробности (поскольку структурные формулы молочной и пировиноградной кислот вы можете посмотреть на рис. 59), так:
С3Н6О3 + ДПН → С3Н4О3 + ДПН ∙ 2Н
молочная кислота пировиноградная кислота
ДПН∙2Н далее передаст оба атома водорода другому веществу и будет снова окислен до состояния обычного ДПН. Теперь он готов снова принять два атома водорода, чтобы опять передать их дальше, и так далее.
Так что же это за «другое вещество», которому ДПН отдаст водород? Кислород?
Давайте посмотрим. Если пиридин-фермент принимается за работу по дегидрогенизации субстрата, например, молочной кислоты, при отсутствии других ферментов и субстратов и в азотистой атмосфере, то реакции не произойдет. Да, атомы водорода ДПН примет, но передать их будет нечему. А общее количество присутствующих в системе молекул ДПН настолько мало по сравнению с количеством молекул молочной кислоты, что даже полное восстановление всего запаса ДПН не отразится сколь-нибудь заметным окислением молочной кислоты. Пока ДПН не сможет отдавать получаемые атомы водорода, реакция не запустится.
Исправить положение удается, если добавить в систему кислород, из чего становится ясно, что кислород принимает водород в реакциях с участием пиридин-фермента.
Однако, если добавить в систему другие вещества, например метиленовую синь, то реакция состоится и в отсутствие кислорода. Метиленовая синь будет принимать атомы водорода у ДПН ∙ 2Н. Это вещество, как понятно из названия, имеет синий цвет, но восстановленная метиленовая синь — бесцветна. Так что за ходом реакции можно следить по постепенному обесцвечиванию метиленовой сини.
Это, конечно, интересно, но практического решения проблемы нам не дает, поскольку в живой ткани метиленовая синь не встречается. Эти экспериментальные данные свидетельствуют лишь о том, что ДПН и ТПН могут при определенных обстоятельствах отдавать атомы водорода другим веществам, но каким же именно веществам они отдают атомы в живой ткани?
Отвлечемся ненадолго, а потом продолжим.
В 30-х годах XX века (а то и раньше) ученые нередко выделяли из тканей желтое вещество, получившее название «флавин», от латинского «желтый». К концу десятилетия было установлено строение этих веществ — обнаружилось, что они содержат систему из трех колец, которую организм сам создать не в силах и, опять же, должен получать с пищей в виде «рибофлавина» — одной из разновидностей витамина В.
Варбург показал, что флавины связаны с системами ферментов, которым и передают свой желтый цвет, и первый обнаруженный фермент такого рода получил название «старый желтый фермент Варбурга». В составе флавинов были в конечном итоге найдены два важных кофермента — «флавинмононуклеотид» (ФМН) и «флавинадениндинуклеотид» (ФАД).
Ферменты, в состав которых входят ФМН или ФАД, называются «флавоферментами», и, как оказалось, они, как и ферменты, включающие в себя ДПН или ТПН, катализируют дегидрогенизацию. К примеру, дегидрогенизация янтарной кислоты (единственная, как я уже говорил, во всем цикле катаболизма молочной кислоты, обходящаяся без пидидин-фермента) происходит именно под каталитическим действием «дегидрогеназы янтарной кислоты», коферментом которой является ФАД.
В этом случае, как и в предыдущем, предназначение коферментов — также принимать из субстрата атомы водорода, становясь при этом ФМН- 2Н или ФАД- 2Н, а затем отдавать этот водород чему-то еще.
Но есть и разница. Коферменты флавинов могут отдавать атомы водорода кислороду с образованием перекиси водорода. Вследствие этого дегидрогеназы флавоферментов называют еще «аэробными дегидрогеназами», поскольку они могут осуществлять каталитическую деятельность в присутствии кислорода, как единственного принимающего водород вещества. А дегидрогеназы пиридин-ферментного класса называют «анаэробными дегидрогеназами», потому что они не умеют этого делать.
Таким образом, если в систему, содержащую пиридин-ферменты, добавить флавофермент и субстрат (которые сами по себе в реакцию не вступают), то флавофермент примет атом водорода у пиридин-фермента и передаст его кислороду. Сам по себе флавофермент в прямой контакт с субстратом не вступает, а пиридин-фермент — не вступает в контакт с кислородом. Однако вместе они успешно катализируют дегидрогенизацию субстрата и восстановление кислорода в перекись водорода, как схематически изображено на рис. 62.
Перенос проходит, как видите, в три этапа, на каждом из которых происходит своя окислительно-восстановительная реакция. Как я уже объяснял в конце предыдущей главы, атомы водорода постепенно движутся по пути увеличения окислительного потенциала.
Почему же атомы водорода не могут сразу от ДПН∙2Н переходить к кислороду? Такой процесс тоже подразумевал бы увеличение окислительного потенциала. Зачем же нужен промежуточный процесс? Тут можно воспользоваться следующей аллегорией: если сила тяжести тянет человека вниз, он может, подчиняясь ей, сделать два шага по ведущим вниз ступенькам, а может и один — через ступеньку. Как правило, необходимость в промежуточном восстановленные формы окисленные формы
этапе обусловливается понижением энергии активации. Видимо, организм не может предоставить сразу достаточное количество энергии для того, чтобы преодолеть порог, необходимый для прямой передачи атомов водорода от органического вещества к кислороду. Так что приходится пользоваться промежуточным этапом в виде неорганического посредника.
Рис. 62. Этапы дегидрогенизации
В 50-х годах XX века было обнаружено, что в флавоферментах содержатся атомы металла, а в пиридин-ферментах — нет. То есть, например, дегидрогеназа янтарной кислоты имеет в своем составе атомы железа, другие флавоферменты — атомы меди или молибдена. Железо может принимать форму как двух-, так и трехвалентного иона (Fe2+ и Fe3+). Приняв один электрон, трехвалентный ион железа превращается в двухвалентный, а тот, потеряв электрон, — обратно в трехвалентный. Так, переключаясь из одной формы в другую, атом железа может выступать переносчиком электронов. Такую же работу может выполнять и медь, переключаясь из состояния одновалентного иона меди (Cu+) в состояние двухвалентного (Cu2+) и обратно. Молибден тоже обладает подобным свойством.
Такой перенос электронов могут осуществлять только металлосодержащие флавоферменты, а чисто органические пиридин-ферменты — не могут. И видимо, перенос электронов — необходимая часть процедуры снижения энергии активации переноса водорода к молекуле кислорода. Ничего точнее сказать, увы, по сей день невозможно.
Можно подумать, что теперь ситуация с атомами водорода, полученными в ходе катаболизма, благополучно прояснена, но это, конечно, не так. Когда кислород принимает атомы водорода из флавоферментов, образуется перекись водорода. Однако в целом нам известно, что перекись водорода в организме не образуется, так что приведенная схема явно не завершена. Должно быть что-то еще.
В 1925 году британский биохимик Д. Кейлин занимался изучением того, как размешанные в растворе взвеси истолченных тканей различных видов — от бактериальных до нервных тканей высших животных — поглощают свет. Он обнаружил около полудюжины разных полос поглощения и приписал их наличие предположительному существованию вещества, которое назвал «цитохром» (от греческих слов, означающих «клетка» и «цвет»). Дальнейшие исследования показали, что полосы поглощения существуют попарно, и каждая пара полос поглощения привязана к своему веществу. Естественно, они получили названия «цитохром a», «цитохром b» и «цитохром с». Со временем выяснилось, что даже такое деление не совсем точно, было вещество близкое к цитохрому a, но все же не полностью с ним идентичное, и оно получило название «цитохром a3».
Единственным цитохромом, который удалось достаточно легко выделить из взвеси тканей, оказался цитохром с. Обнаружилось, что это сравнительно простой белок, молекулярный вес его — около 13 000, и каждая молекула этого вещества содержит один атом железа. Этот атом является частью гема, такого же гема, какой входит и в состав гемоглобина (см. главу 18). Дальнейшие исследования показали, что и в других цитохромах тоже содержится железо — и в каждом случае оно входило в состав либо гема, либо очень похожей на гем группы атомов.
Соответственно, цитохромы получили видовое название «гемоферменты». Каталаза, как я уже упоминал в предыдущей главе, тоже является примером гемофермента, но она не выполняет функций цитохромов. Гемоглобин — это гемосодержащий белок, но не гемофермент. Не все ферменты, в составе которых имеется железо, — гемоферменты. К примеру, в состав дегидрогеназы янтарной кислоты тоже входит атом железа, но не как часть гемовой группы.
Когда была установлена схема передачи водорода («дыхательная цепочка»), вскоре стало ясно, что цитохромы должны быть в нее где-то включены. Они присутствуют практически во всех клетках, за исключением разве что клеток некоторых «обязательно анаэробных» бактерий — то есть таких, которые могут жить только при отсутствии кислорода. Факт того, что в их клетках цитохромы отсутствуют в сочетании с тем, что эти бактерии не могут использовать кислород, сам по себе уже свидетельствует в пользу важности роли цитохромов в дыхательных цепочках.
И опять же, любое вещество, препятствующее деятельности цитохромов — а особенно колебаниям атома железа между двух- и трехвалентным состоянием, что прекращает передачу электрона, — препятствует и поглощению кислорода. Воздействие цианидных групп (—С=N) таких веществ, как синильная кислота (HCN) или цианистый калий (KCN), приводит к прочному застыванию атома железа в одном из состояний, в результате чего дыхание быстро и навсегда прекращается (именно поэтому цианиды так ядовиты).
О положении цитохромов в цепочке можно судить по окислительным потенциалам, приведенным в таблице 9. Очевидно, цитохромы стоят где-то после флавинов, принимают электроны от атомов водорода и передают их по одному путем колебания железа между двух- и трехвалентным ионным состоянием, от «b» к «c», от «c» к «a», от «a» к «a3».
Возможно, при этом передаются и сами атомы водорода, хотя в этом отношении точных данных нет.
Однако где-то ведь цепочка должна закончиться! На каком-то этапе водород должен быть передан кислороду — и это этап цитохрома a3. Окислительный потенциал системы «кислород/вода» равен +0,80, и он в конце концов берет свое. Поскольку цитохром a3 может использовать кислород в качестве получателя водорода, в результате чего образуется вода, а не перекись водорода (получается, вот он, фермент, катализирующий разрыв связи О—О!), то его можно назвать «оксидазой». На самом деле именно под этим названием цитохром a3 и известен по большей части — «цитохромоксидаза».
Все, получили воду, можно теперь расслабиться. Теперь дыхательная цепочка собрана до конца.
Опять возникает вопрос: почему же она оказывается такой длинной? Почему же требуется так много коферментов и простетических групп, чтобы перенести атомы водорода от субстрата к ферменту?
Таблица 9
ОКИСЛИТЕЛЬНЫЕ ПОТЕНЦИАЛЫ
Окислительно-восстановительная система … Окислительный потенциал
ДПН/ДПН∙2Н … - 0,32
ФАД/ФАД- 2Н … - 0,22
b(Fe3+)/b(Fe2+)* … - 0,05
c(Fe3+)/c(Fe2+)* … + 0,25
a(Fe3+)/aFe2+)* … + 0,29
a3(Fe3+)/a3(Fe2+* … + 0,30
* цитохромы
Как я уже говорил, при дегидрогенизации вещества уровень свободной энергии снижается на 35—70 килокалорий на моль вещества, но организм не может использовать высвобождающуюся энергию, если только не запасет ее в виде высокоэнергетических фосфатных связей. Насколько известно, в ходе одной реакции может образоваться только одна высокоэнергетическая связь. Поскольку запасти таким образом можно только 8 килокалорий на моль вещества, то перевод одной реакции дегидрогенизации в одну реакцию образования высокоэнергетической фосфатной связи означал бы потерю семи восьмых энергии.
Наличие длинной дыхательной цепочки позволяет живой ткани разбить процесс уменьшения свободной энергии на фрагменты, на каждом из которых можно создавать по одной высокоэнергетической фосфатной связи. В начале 50-х годов XX века достаточно убедительно было показано, что таким образом в среднем на основе одной реакции дегидрогенизации удается создать по три высокоэнергетических фосфатных связи. Таким образом, эффективность использования энергии достигает хотя бы 35 процентов.
Рис. 63. Окислительное фосфорилирование
Естественно, возникает вопрос, а где же именно, на каком участке дыхательной цепочки формируются высокоэнергетические фосфатные связи. Для ответа на этот вопрос попытаемся действовать методом исключения.
Система с участием дегидрогеназы молочной кислоты производит три высокоэнергетические фосфатные связи на каждую потребляемую молекулу молочной кислоты. Однако система с участием дегидрогеназы янтарной кислоты произведет лишь две высокоэнергетические фосфатные связи на каждую потребляемую молекулу янтарной кислоты. Дегид-рогеназа янтарной кислоты — флавофермент, так что при дегидрогенизации янтарной кислоты из процесса выпадает этап пиридин-фермента. Поскольку этому выпадению соответствует потеря одной реакции образования высокоэнергетической фосфатной связи, то остается сделать вывод, что одна такая связь образуется именно при переходе от ДПН к ФАД.
Путем добавления в дыхательную систему различных химических веществ можно исключать из цепочки те или иные звенья и отмечать, сократится ли при этом количество образуемых высокоэнергетических фосфатных связей. Итоговые предположения об участках образования этих связей приведены на рис. 63.
Каковы же механизмы реакций «окислительного фосфорилирования» (то есть производства высокоэнергетических фосфатных связей путем окисления, представленного в виде переноса атомов водорода)? Это до сих пор неизвестно. Если излагаемая в данной книге информация производит впечатление, что наука сумела решить все проблемы, то заверяю вас — это впечатление ошибочно.
Рис. 64. АТФ и цикл Кребса
Без знания точных подробностей производства высокоэнергетических связей тем не менее возможно подсчитать количество производимого на каждой стадии катаболизма молочной кислоты — результаты приведены на рис. 64.
Как видите, результатом катаболизма молочной кислоты на углекислоту и воду, в отношении которого калориметр показывает цифру в 325 калорий на моль вещества[9], являются 18 молекул АТФ. Если считать, что при формировании каждой высокоэнергетической фосфатной связи уровень свободной энергии возрастает на 8 килокалорий на моль вещества, то в целом в результате катаболизма каждого моля молочной кислоты организм переводит в высокоэнергетические фосфатные связи и запасает 144 килокалории химической энергии. 144 из 325 — это около 45 процентов, в общем, неплохая эффективность.
В какой же части клетки проходят процессы окислительного фосфорилирования? В данной книге я еще ни разу не предпринимал попыток описать устройство клетки. А клетка устроена очень сложно, она обладает множеством специализированных частей (органелл) со специализированными свойствами, и чем более тонкие инструменты оказываются в руках цитологов, тем более тонкие свойства органелл удается обнаружить.
Начнем с того, что каждая неповрежденная клетка имеет внутреннюю часть небольшого объема, которая носит название «клеточное ядро», тонкой мембраной отделенное от остальной части клетки (цитоплазмы). Главная задача ядра — обеспечение размножения клеток и точный перенос генов, управляющих химическими свойствами, от материнской клетки к дочерней. Однако к процессу производства энергии ядро никакого отношения не имеет и ни флавоферментов, ни цитохром не содержит. Для дегидрогенизации как таковой не требуется ничего, кроме пиридин-ферментов, которые сами по себе кислород не используют. Иными словами, ядро — система анаэробная, так что искать место проведения энергопроизводящих реакций с потреблением кислорода следует в цитоплазме.
Различные органеллы цитоплазмы (да и ядра) реагируют на разные красители по-разному — одни поглощают, другие нет, так что их можно «помечать» с помощью соответствующих красителей, специфичных для каждой из органелл. Тогда клеточные частицы, обычно неразличимые глазом, начинают сверкать всеми цветами радуги.
В 1898 году немецкий цитолог С. Бенда с помощью комплекса красителей сумел обнаружить, что небольшие гранулы в цитоплазме огромного множества клеток окрашиваются подозрительно контрастно. Он назвал эти гранулы «митохондриями» (от греческого «хрящевые нити»). Название было неудачным, поскольку к хрящам эти нити никакого отношения не имеют. Тем не менее название это прижилось, как и многие другие ошибочные имена, и мы пользуемся им по сей день.
На протяжении примерно одного поколения функции митохондрий оставались неизученными, и они были для всех просто «еще одним видом клеточных частиц». Однако в 30-х годах XX века с развитием ультрацентрифуг (см. главу 16) стало возможным разложение клетки на составляющие путем ее разрушения и осаждения по очереди различных содержащихся в ней веществ. Таким образом были получены и суспензии, состоящие из одних митохондрий.
А в 40-х годах XX века появились и новые микроскопы с небывалой увеличительной мощностью. Теперь вместо лучей света, фокусируемых с помощью оптических линз, стали использоваться пучки электронов, фокусируемые с помощью магнитных полей. С помощью таких электронных микроскопов наконец-то стало возможным как следует рассмотреть митохондрии, диаметр которых составляет всего один-три микрона, то есть в тысячу раз меньше самой клетки.
Использование электронного микроскопа позволило установить, что митохондрия окружена двойной мембраной, рассекающей тело органеллы, разделяющей ее на части и многократно увеличивающей, таким образом, площадь поверхности митохондрии.
В ходе экспериментов выяснилось, что суспензия митохондрии катализирует все без исключения реакции, входящие в цикл Кребса. Так стало ясно, что «электростанцией» клетки служит именно митохондрия, мембраны которой представляют собой скопление ферментов и коферментов, необходимых для катаболизма пищевых веществ и производства высокоэнергетических фосфатных связей. Было подсчитано, что в среднем отдельная митохондрия представляет собой около 10 000 «сборочных пунктов», на каждом из которых может происходить полный цикл катаболизма, отщепляться атом водорода и создаваться высокоэнергетическая фосфатная связь.
Более подробная информация о молекулярном устройстве митохондрии наверняка еще появится по мере разработки более мощных научных инструментов.
Глава 24. ГДЕ СХОДЯТСЯ ВСЕ ПУТИ
Последние четыре главы были посвящены, тем или иным образом, процессам, связанным с катаболизмом глюкозы — сначала до молочной кислоты путем анаэробного гликолиза, потом — до углекислоты и воды путем цикла Кребса. Однако нельзя сказать, чтобы это были единственные способы, которыми организм может создавать высокоэнергетические связи для хранения химической энергии.
К примеру, еще в начале 50-х годов XX века британский биохимик Ф. Диккенс с коллегами смогли показать, что во многих тканях растений и микроорганизмов, а иногда — и животных, глюкоза расщепляется на трехуглеродные соединения не путем анаэробного гликолиза, а каким-то другим путем. Этот другой путь сходится с обычным гликолизом где-то на полдороге. Он проходит через этапы пяти- и четырехуглеродных Сахаров и не является анаэробным. При нем используется и дыхательная цепочка, и атмосферный кислород.
Наличие такого запасного пути важно в двух отношениях. Во-первых, если деятельность основного механизма окажется временно нарушенной, то организм не останется совсем без ресурсов — он сможет просуществовать за счет запасного механизма.
Во-вторых, при любом катаболическом механизме производится не только энергия, но и ряд промежуточных веществ. Эти промежуточные вещества организм может впоследствии использовать как строительные материалы для процессов анаболизма. К примеру, различные промежуточные вещества, участвующие в цикле Кребса, могут служить основой для формирования некоторых аминокислот. Достаточно прибавить к щавелево-уксусной кислоте аминогруппу, и она станет аспарагиновой кислотой; прибавить аминогруппу к альфа-кетоглутаровой кислоте — она станет глютаминовой кислотой (именно поэтому наличие этих двух кислот в пище не является обязательным).
Так что разумная избыточность механизмов обмена веществ имеет свои преимущества, поскольку предоставляет организму большее количество строительных материалов. Упомянутый выше «обходной путь» приводит к созданию нескольких пятиуглеродных Сахаров и родственных им веществ. Их можно использовать для образования необходимых огромных молекул нуклеиновых кислот, чьей важной составляющей являются именно пятиуглеродные сахара.
Анаэробный гликолиз и реакции цикла Кребса тем не менее являются главными путями катаболизма глюкозы, и рассматривать альтернативные варианты более подробно сейчас не имеет смысла.
Однако приведенное в предыдущих главах описание катаболизма все же неполно. До сих пор я рассуждал только о катаболизме глюкозы. Но в главе 19 я указал, что жиры и белки, особенно последние, тоже являются важными источниками энергии. Что же происходит с ними? Явно ведь не то же самое, что с углеводами?
Давайте посмотрим.
В течение первого десятилетия XX века, когда Харден и Янг только начинали изучать промежуточный катаболизм глюкозы, немецкий биохимик Франц Кнооп взялся за решение той же задачи в отношении жиров.
Кнооп использовал технологию кормления собак строго определенной пищей с последующим изучением мочи. Однако ученый сумел серьезно улучшить эту методику. Если бы он просто кормил собак жирами и получал на выходе воду и углекислоту, то было бы совершенно непонятно, из жиров ли создана полученная молекула воды или углекислоты или из чего-то еще. Молекулы жира надо было как-то пометить, чтобы ее составные части можно было потом опознать, после того как они пройдут всю цепочку обмена веществ организма животного. Кнооп решил кормить собак фенилдеривативами различных жирных кислот.
Рис. 65. Фенилдериватив жирной кислоты
Разрешите пояснить. Во-первых, жирные кислоты — это основной продукт расщепления жиров. Их молекулы состоят из длинных углеводных цепочек, обычно по шестнадцать—восемнадцать атомов углерода длиной, где один атом углерода на одном из концов цепочки входит в карбоксильную группу. В качестве примера распространенной восемнадцатиуглеродной кислоты можно назвать стеариновую кислоту. Если такое вещество подвергнуть обработке таким образом, чтобы к противоположному от карбоксильной группы концу присоединилось бензольное кольцо, то в результате получится именно фенилдериватив, изображенный на рис. 65.
Фенилдериватив жирной кислоты — это вещество, которое организм обработать не способен. Ни у собаки, ни у человека не существует ферментов, с помощью которых можно было бы разорвать само бензольное кольцо или отщепить его от углеродной цепи. Ткани организма собаки могут катаболизировать всю остальную часть жирной кислоты, но от бензольного кольца и того фрагмента жирной кислоты, к которому бензольное кольцо прикреплено, избавиться можно только выбросив его из организма с мочой. Соответственно, Кнооп мудро рассудил, что если в моче обнаружатся соединения, содержащие бензольные кольца, то это и будут остатки использованной организмом собаки жирной кислоты.
Таким образом, пометив жирные кислоты, Кнооп создал первый в мире «маркер» вещества (то есть пометку на веществе, с помощью которого можно проследить его дальнейшую судьбу). Перед тем как приступить к описанию полученных Кноопом результатов, я вкратце обрисую дальнейшую историю маркеров, поскольку эта технология оказалась крайне важной для развития биохимии в целом.
Напрашивается возражение, гласящее, что Кнооп, дескать, пичкает организм подопытного животного неестественными для того пищевыми веществами, «нефизиологичными». Пусть они нетоксичны и на здоровье организма их прием никак не отражается, но откуда у исследователя может быть уверенность, что само присутствие маркера никак не повлияло на способ обработки молекулы организмом? А вдруг бензольное кольцо подавило действие какого-нибудь важного фермента? Короче говоря, откуда мы знаем, что эти вещества следуют теми же метаболическими путями, что и нормальная, естественная пища?
Идеально было бы придумать такой маркер, чтобы организм не мог отличить помеченное вещество от непомеченного, а экспериментатор — мог. Казалось бы, нельзя требовать от мироздания слишком многого, но лет через десять после экспериментов Кноопа произошел один из самых счастливых случаев в истории науки — были открыты изотопы.
В 1913 году британский физик Фредерик Содди показал, что атомы одного элемента могут быть не абсолютно похожи. Да, все они имеют одинаковое количество протонов ядра, и такое же количество электронов на орбите, и одинаковые химические свойства (см. главу 17). Однако число нейтронов в ядрах разных атомов одного и того же вещества может различаться, а значит — и их атомный вес. Такие атомы называют «изотопами» одного и того же элемента.
Так, например, одни атомы углерода имеют ядро, содержащее шесть протонов и шесть нейтронов. Атомный вес такого атома — 12. Ядро других содержит шесть протонов и семь нейтронов и имеет атомный вес 13. На бумаге обозначение этих изотопов будет выглядеть как C12 и С13. Каждый из них будет иметь те же шесть электронов — два во внутренней оболочке и четыре во внешней; каждый будет участвовать в одних и тех же реакциях в организме. Организм не различает изотопов.
Затем в 1919 году британский физик Фрэнсис Уильям Астон изобрел масс-спектрограф — устройство, искажающее траекторию полета ионов в магнитном поле. Чем тяжелее ион, тем меньше искажается его траектория. Таким образом, стало возможно отделить C12 от С13 в случае, когда они присутствуют в одном и том же наборе. Поскольку траектория их полета искажается в разной степени, то и конечная точка попадания на фотопластину у этих двух изотопов оказывается разной, и по окончании сортировки можно подсчитать сравнительную частоту их наличия по степени потемнения пластины. Так было установлено, что в природном угле соотношение C12 к С13 составляет 989 к 11.
Теперь предположим, что пища для лабораторных животных изготавливается только с использованием С13, без единого атома C12. Для организма разницы нет. Поэтому он подвергнет вещество, содержащее С13, той же обработке, какой подверг бы и вещество, содержащее C12. Это вещество будет превращено организмом в другое, тоже с аномально высоким содержанием С13; в итоге понятно, что любое вещество с аномально высоким содержанием С13 всегда окажется происходящим от исходного питательного продукта, помеченного изотопом. Наличие аномального количества изотопа определяется экспериментатором путем сжигания вещества, получения углекислого газа и прогона этого газа через масс-спектрограф. По результатам спектрографии ученые уже могут строить предположения о метаболических механизмах, действующих в тканях живых существ.
Легко сказать, да трудно сделать. Для этого сначала надо набрать изотопов (которые встречаются в природе, как уже говорилось, очень редко), создать питательные вещества с их участием, потом выделить из организма другие вещества в чистом виде и в конце концов провести очень непростую процедуру масс-спектрографий. Из-за всех этих трудностей масс-спектрография так и не получила широкого распространения до 1932 года, когда американский химик Гарольд Юри открыл дейтерий, или тяжелый водород.
Ядро обычного водорода состоит только из протона, так что его атомный вес — 1, а ядро дейтерия — из протона и нейтрона, поэтому его атомный вес — 2. Эти изотопы обозначаются, соответственно, как Н1 и Н2. И если между C12 и С13 разница масс составляет 8 процентов, то между Н1 и Н2 — 100 процентов.
Из такой колоссальной разницы масс между водородом и дейтерием можно извлечь определенные преимущества. Более тяжелые изотопы участвуют в тех же реакциях, что и более легкие, но с меньшей скоростью. Для всех остальных элементов, кроме водорода, разницей в скорости вполне можно пренебречь; однако в случае с водородом уже заметно, что реакции с участием дейтерия протекают медленнее. Перегонка и электролиз воды, в состав которой входит не водород, а дейтерий, происходят заметно медленнее. Если подвергать перегонке или электролизу большое количество воды, то ближе к концу процедуры оставшаяся часть воды будет представлять собой высокую концентрацию воды тяжелой. Из такой тяжелой воды можно изготавливать дейтерийсодержащие продукты. Ну и отделять дейтерий от водорода в спектрографе тоже сравнительно несложно.
В 1935 году американский физик немецкого происхождения Рудольф Шёнхеймер пометил жирные кислоты дейтерием, так же как Кнооп за поколение до того — бензольным кольцом. Позже, по мере развития технологий, Шёнхеймер использовал для пометки аминокислот тяжелый азот, N15 (обычный азот — N14). В результате своих экспериментов он сумел доказать, что организм ведет чрезвычайно активную химическую деятельность. Даже в тех ситуациях, когда никаких видимых следов активности незаметно, постоянно идут перемещения, переносы, соединения и распады, постоянно перемешиваются атомы.
Но технология маркирования изотопами по-прежнему оставалась неуклюжей и неудобной. Попав в организм, вещество, содержащее изотоп, растворялось по всему организму, и найти его потом оказывалось очень непросто.
Но выход был найден. Атомы некоторых изотопов содержат неустойчивое соединение протона с нейтроном. Из таких атомов с известными скоростями и в известном количестве испускаются различные субатомные частицы. К примеру, С14, ядро которого состоит из шести протонов и восьми нейтронов, испускает энергетические частицы такими темпами, что половина С14 превращается в N14 (самый распространенный вариант азота) за пять тысяч лет.
Такое явление называется радиоактивностью. Если в пищевые вещества включить радиоактивный атом С14, то с точки зрения обмена веществ он будет проявлять все те же свойства, что и обычные стабильные изотопы C12 или С13, но по маркеру из энергетических частиц экспериментатор всегда сможет его найти. С14 можно отловить даже в том случае, если его концентрация крайне мала.
Оставалось только придумать способ производства самих радиоактивных изотопов в достаточном количестве. До Второй мировой войны приходилось полагаться только на естественно встречающиеся в природе радиоактивные изотопы — а это были по большей части изотопы атомов, не участвующих в пищевой цепочке животных. Но после окончания войны практически ни одно исследование метаболизма уже не велось без использования веществ, помеченных радиоактивными изотопами С14, Н3, Na24 и так далее. Теперь работу биохимика невозможно представить без них.
Но вернемся же к Кноопу и его первым в мире опытам с молекулярными маркерами…
Предоставляя собакам с пищей маркированные жирные кислоты с четным количеством атомов углерода, ученый выделял из мочи животных бензольное кольцо в сочетании с группой, включающей в себя два атома углерода, — такое вещество называется фенилуксусной кислотой. Кислота эта, в свою очередь, крепилась к молекуле глицина. Если же на входе подавались кислоты с нечетным числом атомов углерода, то на выходе получалось бензольное кольцо, к которому крепился только один атом углерода («бензойная кислота»), и она тоже крепилась к молекуле глицина (рис. 66). Организм часто добавляет глицин к молекуле, которую надо вывести из организма, чтобы она легче выводилась через почки, так что Кнооп не стал обращать на глицин внимания, а сосредоточился на фенилуксусной и бензойной кислотах.
Рис. 66. Катаболизм жирных кислот
Кнооп объяснил полученные результаты тем, что длинная цепочка жирной кислоты разрезается на блоки по два атома углерода, начиная с карбоксильной группы. Оторвать углерод от бензольного кольца организм не может, поэтому если общее количество звеньев цепочки оказывается четным, то прикрепленными к бензольному кольцу остаются два звена, если нечетным — то одно.
Такое предположение казалось тем более логичным, что известно, что все жирные кислоты всех жиров живых тканей состоят из четного числа атомов углерода — значит, двухуглеродные блоки по какой-то причине естественны для организма, и именно их он использует при строительстве собственных жирных кислот. В природе очень часто встречаются восемнадцати- и шестнадцатиуглеродные жирные кислота, а семнадцатиуглеродных не встречал пока еще никто (те жирные кислоты с нечетным числом атомов углерода, которые Кнооп скармливал собакам, не в счет, они были искусственно синтезированы в лаборатории).
Два года спустя немецкий биохимик Густав Эмбден внес в систему еще одно усовершенствование. Он обнаружил, что при обработке жирной кислотой тканей печени в растворе появляется цепочка из четырех атомов углерода — ацетоуксусная кислота:
Это вещество вместе с рядом других входит в группу «кетонных тел», названных так из-за присутствия кетогруппы С=О. Ацетоуксусная кислота — пример жирной кислоты, от которой начал отщепляться двухуглеродный отрезок, как я сейчас объясню, и это утвердило Кноопа в его предположении о «нарезании» организмом двухуглеродных отрезков.
Кетонные тела не встречаются в каких-либо значительных количествах ни в крови, ни в моче здоровых животных, несмотря на то что печень производит их, будучи изолированной. А вот в крови и моче диабетиков — встречается! Поскольку диабет — это расстройство в первую очередь углеводного метаболизма, то его связь с производством кетонных тел — продуктов метаболизма жиров — демонстрирует связь между этими двумя метаболическими механизмами.
Несмотря на столь давний интерес ученых к проблеме, подробности метаболизма жиров оставались неизвестными до тех пор, пока не была разработана вышеописанная технология изотопного маркирования. Лишь в 1951 году биохимики получили возможность писать формулы жирового метаболизма хоть с какой-то степенью уверенности.
Рис. 67. Цикл окисления жирной кислоты
В свете сегодняшнего знания мы можем сказать, что Кнооп был прав: действительно, углеродная цепочка жирных кислот «нарезается» организмом на фрагменты по два атома углерода, начиная с карбоксильного конца. Только надо внести два уточнения. Во-первых, для того, чтобы подвергнуться катаболизму, жирная кислота должна конденсироваться с коферментом А. Во-вторых, сам процесс отрезания двух атомов углерода происходит в четыре этапа (рис. 67).
Первый этап — дегидрогенизация. От каждого из двух атомов углерода, соседствующих с карбоксильной группой, отщепляется по атому водорода. Второй этап — гидратация. К веществу добавляется вода таким образом, что гидроксильная группа присоединяется ко второму атому углерода карбоксильной группы (этот атом называется «бета-углерод», соответственно, вся реакция имеет название «бета-оксидация»). На третьем этапе удаляются еще два атома водорода, так что бета-углерод становится частью кетогруппы. Если посмотреть сейчас на формулу ацетоуксусной кислоты, то станет ясно, что она — продукт именно этого, третьего, этапа. На четвертом этапе два атома углерода отщепляются одновременно в составе ацетилкофермента А, и от цепочки остается новая, укороченная на два атома углерода жирная кислота, которая конденсируется с коферментом А и отправляется на следующую итерацию цикла.
Полное название этого цикла — «цикл окисления жирной кислоты». На самом деле это скорее спиралеобразный, чем циклический, процесс, поскольку нельзя сказать, что в конце мы приходим к тому же, что имели в начале, поскольку с каждой итерацией жирная кислота становится короче на два атома углерода. Таким образом, восемнадцатиуглеродная жирная кислота, например стеариновая, в конце концов превращается в девять молекул ацетилкофермента А.
После формирования ацетилкофермента А он вступает в соединение с щавелево-уксусной кислотой для образования лимонной кислоты и входит, таким образом, в цикл Кребса, описанный в предыдущей главе. Не важно, сформирован ли ацетилкофермент А из жирной кислоты или путем катаболизма глюкозы; организм не может определить происхождение вещества (рис. 68).
Ацетилкофермент А тоже можно рекомбинировать с получением в итоге жирной кислоты. Для этого надо обратить цикл окисления жирных кислот. То есть две молекулы ацетилкофермента А объединяются для получения ацетоацетилкофермента А, затем добавляются два атома водорода, удаляется вода, добавляются еще два атома водорода — и вот мы получили четырехуглеродную жирную кислоту, конденсированную с коферментом А. Эту цепочку можно продолжать сколько угодно, добавляя каждый раз по ацетилкоферменту А.
Рис. 68. Соединение путей катаболизма углевода и жира
Получается, что ацетилкофермент А и есть тот самый общий строительный «кирпичик», наличие которого я логически обосновал в главе 19, рассуждая о том, как крахмалистая пища переводится в жир, а нормальный уровень глюкозы в крови поддерживается за счет расщепления жира.
Конечно, и в метаболизме жирных кислот, как и в метаболизме глюкозы, важное место занимает дыхательная цепь. При каждой итерации цикла окисления жирных кислот происходит две дегидрогенизации. Первая катализируется флавоферментом, а вторая — пиридин-ферментом. Можно считать, что в первом случае производится две молекулы АТФ, а во втором — три, так что при каждой итерации цикла производится в целом пять молекул АТФ путем окислительного фосфорилирования.
В случае, скажем, стеариновой кислоты, в состав которой входят восемнадцать атомов углерода, происходит восемь итераций цикла (понятно, почему не девять? Попробуйте разрезать полоску бумаги на 9 частей, и увидите, что потребуется совершить всего 8 разрезов), и при этом производится девять молекул ацетилкофермента А.
То есть при переводе молекулы стеариновой кислоты в девять молекул ацетилкофермента А получается 8 умножить на 5, то есть 40 молекул АТФ. Если посмотреть на схему цикла Кребса, приведенную на рис. 64, то видно, что в этом цикле из ацетилкофермента А производится 12 молекул АТФ. Соответственно, если 9 молекул ацетилкофермента А умножить на 12, получим 108 молекул АТФ.
Таким образом, в процессе перехода от стеариновой кислоты к углекислоте и воде образуется не менее 40+108, то есть 148 молекул АТФ. Но это еще не все. Типичная молекула жира, например стеарин, состоит из трехуглеродного спирта, глицерина, в соединении с тремя молекулами стеариновой кислоты. Каждая из трех молекул стеариновой кислоты послужит формированию 148 молекул АТФ, то есть всего образуется 3 x148 = 444 молекулы АТФ. Глицерин же будет превращен в пировиноградную кислоту, что само по себе даст еще 15 молекул АТФ — итого организм получит 459 молекул АТФ в результате катаболизма каждой молекулы стеарина.
Идем дальше. При переходе одного грамма жира в углекислоту и воду высвобождается 9 килокалорий тепла (см. главу 14). Один моль стеарина весит 891 грамм, соответственно, при переходе одного моля стеарина в углекислоту и воду высвобождается 891 х 9 = 8019 килокалорий. Путем образования 459 молекул АТФ запасается 459 х 8 = 3672 килокалории химической энергии. Значит, эффективность процесса — 3672: 8019 = чуть более 45 процентов. Это превосходный результат.
Но если посмотреть на рис. 64, видно, что ацетилкофермент А попадает в цикл Кребса путем соединения с щавелево-уксусной кислотой. А щавелево-уксусная кислота производится в достаточном количестве только путем углеводного метаболизма (до какой-то степени — белкового метаболизма), но никак не метаболизма жиров.
Если в пище много жиров, но мало углеводов, ацетилкофермента А производится много, но щавелево-уксусной кислоты — мало. Ацетилкофермент А начинает накапливаться, конденсироваться сам с собой, образовывая ацетоуксусную кислоту, и в организме образуется повышенная концентрация кетонных тел, находящая выражение в состоянии, известном как «кетоз».
Такая диета, богатая жирами, но бедная углеводами, называется «кетогенной», потому что способствует повышению концентрации кетонных тел. Голодание — тоже кетогенный процесс, потому что все углеводородные запасы организм исчерпывает за день, а дальше начинаются процессы извлечения энергии из жиров. Если печень обрабатывать жирной кислотой, не добавляя при этом углеводов, то, по наблюдениям Эмбдена, тоже начинается кетоз.
Ни голодание, ни кетогенные диеты обычно не приносят большого вреда, поскольку человеку свойственно избегать и первого, и второго. Но даже если обстоятельства вынуждают человека к таким условиям, то даже небольшое количество переваренных углеводов произведет корректирующий антикетогенный эффект.
Вот при диабете кетоз становится действительно опасным. Если болезнь не лечить, то развивается хроническое расстройство углеводного метаболизма, приводящее ко все более жесткой нехватке щавелево-уксусной кислоты и, соответственно, прогрессирующему кетозу. Именно токсическое действие кетоновых тел обычно и приводит к коме и смерти диабетика.
Строго говоря, не все жиры имеют своим основным предназначением производство энергии. Те жиры, что я обсуждал в этой главе, относятся к «простым» жирам, состоящим из глицерина и жирных кислот. Существуют также «сложные» жиры, в состав которых входят еще и фосфатная группа и одна из нескольких азотсодержащих групп. А еще есть такие вещества, как холестерин, обладающие свойствами жиров, но имеющие совершенно другое молекулярное строение.
У этих последних в организме есть особые функции. Из фосфатсодержащих жиров состоит мембрана митохондрий, служащая, как я уже писал, полем деятельности для различных ферментов, катализирующих реакции цикла Кребса и дыхательной цепочки. Что же касается холестерина, то из него состоит большая часть жировой оболочки нервов.
Сложные жиры и холестерин содержат не меньше энергии, чем простые жиры, но их роль в клеточном механизме настолько велика, что их энергозапасы не расходуются даже при крайних стадиях истощения. Я не привожу здесь подробного рассмотрения этих крайне важных веществ только потому, что они не задействованы в процессах энергообмена.
Теперь давайте вернемся к белкам, попадающим после процесса переваривания в организм в виде аминокислот. Перед тем как использовать их для производства полезной энергии, надо сначала убрать из них азот.
В 1773 году французский химик Руэль (учитель Лавуазье) обнаружил в моче азотистое соединение и назвал его, естественно, мочевиной. Когда в начале XIX века химики стали изучать строение белков, мочевина была сразу признана «тем самым» веществом, посредством которого организм избавляется от азотистой составляющей белков.
Формула мочевины —
Ее короткая запись — NH2CONH2. Получилось так, что именно с мочевиной оказались связаны два самых замечательных открытия в биохимии. Она стала первым органическим веществом, которое удалось синтезировать из неорганического материала (см. главу 13), и катализирующий ее распад фермент был кристаллизован первым (см. главу 15).
В XIX веке способ образования мочевины в организме оставался неизвестен. Однако уже в первое десятилетие XX века, когда Харден и Янг, с одной стороны, и Кнооп — с другой, начали продвижение в тайны промежуточных этапов метаболизма, немецкий биохимик Альбрехт Коссель вместе с английским коллегой Генри Дэкином пошли в такое же наступление на секреты промежуточных этапов белкового метаболизма.
Они обнаружили фермент, названный ими «аргиназа», действие которого заключалось в катализировании гидролиза аминокислоты аргинина. При этом с помощью реакции, изображенной на рис. 69, образовывалась и мочевина. Кусок молекулы аргинина, остающийся по завершении процесса, — это аминокислота орнитин, которая встречается только как промежуточный продукт образования мочевины, и частью белковых молекул не является.
Значение аргиназы подчеркивают несколько фактов. Мочевина производится в печени (если удалить у животного печень, производство мочевины прекращается), и наивысшая концентрация аргиназы наблюдается тоже в печени. Аргиназа встречается в тканях всех животных, в чьем организме производится мочевина, например амфибий или млекопитающих. А вот в тканях животных, в чьем организме производятся другие азотсодержащие продукты — птиц, например, или рептилий, — она не встречается. Понятно, что аргинин и аргиназа участвуют в каком-то механизме, с помощью которого живые ткани синтезируют мочевину.
Организм человека производит в день от десяти до тридцати пяти граммов мочевины, не истощая при этом запасов аргинина. Значит, они возобновляются путем синтеза аргинина из орнитина.
Это стало окончательно ясно в 1932 году благодаря работам Кребса (того самого, впоследствии — первооткрывателя цикла Кребса) и его коллеги К. Хенселейта с образцами печеночной ткани. Они обнаружили, как и ожидалось, что добавление аргинина стимулирует производство мочевины. Такой же эффект оказывало и добавление орнитина, и этот факт утвердил ученых в мысли, что печень производит из орнитина аргинин. В конце концов они обнаружили, что еще одно вещество, сходное по строению с аргинином — цитруллин, — тоже стимулирует производство мочевины.
Рис. 69. Гидролиз аргинина
Рис. 70. Цикл образования мочевины
В качестве объяснения Кребс и Хенселейт составили схему, которую принято сейчас называть «циклом образования мочевины» — она приведена на рис. 70. Эта схема показывает, что орнитин, цитруллин и аргинин постоянно синтезируются заново. Смотрите, при превращении орнитина в цитруллин организм добавляет одну молекулу аммиака и одну молекулу углекислоты, а при превращении цитруллина в аргинин — еще одну модекулу аммиака. Что же касается воды, то одна ее молекула добавляется организмом на этапе гидролиза аргинина, но на каждом из двух этапов одна молекула воды из системы извлекается, так что в целом можно говорить об извлечении одной молекулы воды. И в конце концов при гидролизе аргинина извлекается одна молекула мочевины. Вот как выглядит запись всей реакции в целом:
2NH3 + СO2 → NH2CONH2 + H2O.
Конечно, приведенная схема цикла образования мочевины сильно упрощена. Никто из выдвинувших ее на самом деле, конечно, не считал, что на входе подается молекула аммиака как таковая. Аммиак — очень ядовитое вещество, и в организме в чистом виде встречаться не может. Однако только в 50-х годах XX века, когда начали проводить эксперименты с изотопным маркированием, стали известны подробности этих реакций.
Выяснилось, что азотсодержащие группы добавляются в виде аминогрупп, получаемых из аминокислот. При переходе от орнитина к цитруллину глютаминовая кислота (одна из наиболее распространенных аминокислот) отдает и аминогруппу, и эквивалент углекислоты. В этом случае она должна использовать высокоэнергетическую фосфатную связь, поручаемую из АТФ. При переходе от цитруллина к аргинину аминогруппу отдает другая аминокислота, аспарагиновая, и снова за счет АТФ.
То есть производство мочевины — это энергоемкая реакция. На каждой итерации цикла потребляется по две молекулы АТФ.
Не стоит считать, что единственными аминокислотами, способными отдавать аминогруппу на производство мочевины, являются глютаминовая и аспарагиновая кислоты. В 30-х годах XX века, работая с изотопом N15, о чем я рассказывал в этой же главе, Шёнхеймер установил, что если дать на входе один вид аминокислоты, помеченный изотопом, то вскоре изотопы окажутся в составе аминокислот всех видов, за исключением лизина. Естественно, напрашивается вывод, что аминогруппа легко передается от одного вещества к другому. Были обнаружены и ферменты, катализирующие подобные реакции (трансаминазы), и установлены подробности переносов, получивших название «трансаминирование» (от «транс» — перенос и «амино»). После трансаминирования аминогруппу NH2 заменяет связанный двойной связью кислород (рис. 71).
Трансаминазы представляют собой пример ферментов, использующих в качестве кофермента пиридоксальфосфат, в котором содержится группа атомов, организмом не синтезируемая в принципе. Так был обнаружен еще один витамин группы В, пиридоксин.
Итак, движение аминогрупп осуществляется от аминокислот в целом к глютаминовой кислоте и аспарагиновой кислоте, а от них уже в цикл производства мочевины. Те аминокислоты, в состав которых входит лишний атом азота или атом серы, избавляются от них с помощью механизмов, которые я здесь не буду описывать. Достаточно будет сказать, что, так или иначе, все атомы азота и серы устраняются и остается только «углеродный скелет».
Этот углеродный скелет может представлять собой одно из тех веществ, с которыми мы уже сталкивались при описании катаболизма углеводов или белков. К примеру, когда аланин подвергается трансаминации, он теряет аминогруппу и приобретает связанный двойной связью кислород, вследствие чего образуется пировиноградная кислота.
С помощью кофермента А пировиноградная кислота избавляется от гидроксильной группы обычным способом, и образуется ацетилкофермент А, который уже может вступить в цикл Кребса. Для организма нет разницы, образована ли пировиноградная кислота из глюкозы или из аланина. И в том и в другом случае это одна и та же пировиноградная кислота, с одним и тем же энергетическим содержанием. Другие аминокислоты, например валин, серии, треонин и цистеин, тоже преобразуются, несколько более длинным путем, в пировиноградную кислоту.
Рис. 71. Трансаминация
Несколько аминокислот, например лизин, подвергаются изменениям, в ходе которых превращаются в ацетоуксусную кислоту и далее — в ацетил-кофермент А, после чего входят в цикл Кребса по пути катаболизма жиров.
А некоторые аминокислоты входят в цикл Кребса и сами по себе. К примеру, аспарагиновая кислота сразу после деаминации становится щавелево-уксусной кислотой, а глютаминовая кислота — альфа-кетоглутаровой кислотой. Оба этих вещества являются промежуточными продуктами цикла Кребса и могут сразу быть приняты в него на соответствующих этапах.
На рис. 72 подведены итоги катаболических взаимосвязей белков, жиров и углеводов.
Рис. 72. Присоединение белка
Конечно, обратив различные реакции катаболизма, можно получить аминокислоты из соответствующих углеродных скелетов. К примеру, если организм пресыщен глютаминовои кислотой и в то же время наблюдается нехватка аланина, в некоторых случаях запускается процесс передачи аминогруппы от глютаминовои кислоты к пировиноградной кислоте и формирования из последней аланина. В случае обратной ситуации организм точно так же может инициировать процесс передачи аминогруппы от аланина к альфа-кетоглутаровой кислоте, а из последней — образовывать глютаминовую. Присутствие в пище аминокислот, которые могут быть синтезированы подобным образом, не обязательно.
С другой стороны, некоторые аминокислоты проходят во время реакций получения углеродных скелетов хотя бы один необратимый этап. Такие аминокислоты уже нельзя вернуть в исходное состояние с помощью каких бы то ни было промежуточных веществ. Их присутствие в пище необходимо, я приводил список этих аминокислот в главе 19.
Глава 25. ОСНОВНОЙ И ГЛАВНЫЙ ИСТОЧНИК
В двух предыдущих главах я указывал на то, что энергия, производимая с помощью катаболизма углеводов и жиров, переводится на хранение в виде высокоэнергетических фосфатных связей с эффективностью 45 процентов. Хоть это и высокий показатель эффективности, гораздо более высокий, чем у многих полезных изобретений человека, все равно очевидно, что больше половины энергии, получаемой при расщеплении пищевых продуктов, теряется. (Ну, не то чтобы она совсем уж прямо терялась, даже в тепловой форме она помогает человеку, как теплокровному созданию, поддерживать температуру тела на должном уровне.)
Более того, энергия теряется и при использовании ее из АТФ. Так, если АТФ используется для образования сахарофосфата или пептидной связи, то тратятся все 8 килокалорий, тогда как для реакции необходимо только 4, то есть эффективность снижается еще в два раза.
В целом получается, что лишь процентов 10 от энергетического содержания пищи уходит действительно на уменьшение энтропии. А пустая трата оставшихся 90 процентов — это вклад живого существа в общее увеличение энтропии, неизбежно следующее из второго закона термодинамики.
Из этого можно сделать вывод, что из десяти килограммов переваренной пищи получится один килограмм живой ткани. Теперь предположим, что один вид живых существ («потребитель») получает пищу путем поедания другого живого существа («производителя»). Если потребителю необходимо лишь поддерживать свою клеточную массу на протяжении жизни, то получается, что производитель должен поддерживать свою клеточную массу на уровне в десять раз большем.
Если же и потребитель, в свою очередь, служит пищей для третьего типа организмов (назовем его потребитель-2), то выходит, что клеточная масса потребителя тоже должна десятикратно превышать клеточную массу потребителя-2. Можно ввести еще потребителя-3, -4 и так далее.
Поясню на примере: допустим, львы живут за счет поедания зебр. Если популяции обоих видов стабильны, то на каждый килограмм массы львов должно приходиться по десять килограммов массы зебр. А поскольку зебры живут за счет поедания травы, то на каждый килограмм массы зебр должно приходиться по десять килограммов массы травы.
Это пример простейшей пищевой цепочки — и каждая пищевая цепочка непременно имеет пирамидальную форму. Много звеньев в ней быть не может, поскольку с каждым шагом вверх приходится делить на 10, и в итоге мы очень быстро доходим до крайне малых значений, даже начиная с вполне внушительных. Те немногие виды живых существ, что венчают пирамиду, — это должны быть сильные и крупные существа, способные поедать других хищников и не поедаемые сами, в свою очередь, уже никем, — находятся действительно в завидном положении, но их не может быть много. Белый медведь, живущий за счет поедания морских котиков, или кашалот, питающийся гигантскими кальмарами, или косатка, охотящаяся на других дельфинов, — все это, так сказать, «дорогие» и «энергоемкие» формы жизни. Земля таких много не вынесет.
Улучшить свое положение в этом отношении представители «высшего» вида могут, сократив число звеньев в цепочке. Если бы лев мог научиться есть сразу траву, а не зебр, то тем самым он увеличил бы свой пищевой запас вдесятеро. Количество львов в мире могло бы удесятериться без ухудшения качества жизни каждого из них — или при сохранении сегодняшнего количества каждый лев мог бы стать вдесятеро крупнее.
Для львов это, конечно, нереально, но не случайно крупнейшие на Земле животные — слоны, бегемоты и носороги — травоядны.
По правде говоря, на Земле существовали когда-то и хищники размером куда больше слона. Масса тираннозавра, крупнейшего из когда-либо существовавших наземных хищников, была как минимум вдвое больше, чем у современного слона. Но и травоядные животные того периода, составлявшие рацион тираннозавра, были куда крупнее современных. И самые крупные из древних гигантских рептилий мезозойской эпохи — брахиозавры и бронтозавры — были все же травоядными.
Океан, куда более богатый жизнью, чем суша, дает возможность существовать самым крупным хищникам. Кашалот по размерам и массе не уступает самым крупным из динозавров — а ведь он хищник, употребляющий в пищу других хищников (гигантских кальмаров), размером не слишком уступающих ему самому. Однако самый крупный из китов, голубой кит, масса которого может достигать 150 тонн, самое крупное животное изо всех, когда-либо существовавших на Земле, тоже устранил из пищевой цепочки несколько звеньев и питается крошечными креветкообразными рачками и прочим планктоном, процеживая ради этой пищи тонны воды через китовый ус.
То же самое можно сказать и про человека. Никакой человеческий гений не в силах преодолеть законы термодинамики. Да, человек может повысить запасы продовольствия за счет включения тех видов живых существ, которых он ранее не ел. Он может вырубить леса и засеять высвобождающиеся площади съедобными злаками, уничтожив при этом все растения, пытающиеся конкурировать со злаками, и всех насекомых, пытающихся конкурировать с самим человеком в деле поедания этих злаков (ну, насколько получится, конечно). Он может выращивать животных специально на пищу, вытесняя дикие виды животных и истребляя хищников. Тем не менее никуда не деться от того факта, что запасы продовольствия человечества должны десятикратно превышать по массе массу самого человечества.
Обстоятельства могут вынудить человека и к сокращению пищевой цепочки. Если он питается травоядными животными, то на каждый килограмм массы человека должно приходиться сто килограммов массы растений. Если же человек питается непосредственно растительной пищей, то на каждый килограмм его массы достаточно будет и десяти килограммов массы растений. По мере роста плотности населения, как показывает диета азиатов уже сейчас, человеку, независимо от собственного желания, придется перейти на растительную пищу.
Если бы звенья пищевой цепочки были ограничены только живыми существами, то жизнь на Земле продлилась бы недолго. Невозможно было бы долго поддерживать огромный процент теряемой при каждом приеме пищи энергии. Тот факт, что жизнь никак не прекращается вот уже самое меньшее миллиард лет, свидетельствует только о том, что на каком-то этапе в пищевую цепочку должна поступать энергия извне, из источника, не имеющего отношения к живым организмам, причем в количестве достаточном для возмещения потерь.
Возможными источниками поступления большого количества энергии из неодушевленного пространства являются: 1) солнечное излучение; 2) ветер; 3) течение воды; 4) приливы; 5) внутреннее тепло Земли и 6) ядерная реакция.
Энергия приливов доступна лишь на небольшой территории, как, впрочем, и энергия течения воды. Энергия ветра, хоть и не ограничена пространственными рамками, зато крайне ненадежна. Внутреннее тепло Земли то не чувствуется почти совсем, то вдруг прорывается в виде бедствий — землетрясений и извержений вулканов. Что же касается ядерной энергии (в виде естественной радиоактивности, космического излучения и так далее), то она слишком тонко распределена. Ни один из этих источников нельзя рассматривать как достаточно (но не катастрофически) мощный, достаточно распространенный и достаточно надежный для того, чтобы положиться на него как на энергетическую основу всего живого.
Остается только солнечное излучение.
К этому выводу можно прийти не только методом исключения. Даже самый поверхностный взгляд на мир приводит нас к убеждению, что именно солнечное излучение является первичным источником энергии жизни. Пищевая цепочка, так или иначе, заканчивается зелеными растениями. Они являются «первичным производителем». И на суше, и в море, если проследить пищевую цепочку донизу, она закончится тем, что животные поедают растения. В море растения — это в первую очередь одноклеточные водоросли, общий вес которых, несмотря на то что каждая из них крошечна, во много раз больше, чем общий вес всех многоклеточных на планете.
Существуют растения, не являющиеся зелеными. Это грибы[10]. Они могут расти только на органических материалах и с точки зрения энергии относятся скорее к животным, чем к растениям. Так что и они получают энергию из когда-то живого источника, а не из неживой материи.
Очень достойно со стороны растений никого не есть в том смысле, в каком это делают животные и грибы. Растения могут жить и развиваться при полном отсутствии органических веществ. Однако между собой они конкурируют за свет точно так же, как животные — за пищу. Некоторые растения могут жить в тени, но ни одно не может существовать в полной темноте дольше, чем животное обходиться без пищи.
Каждый, кто видел, как растения в тропических дождевых лесах тянутся к солнцу, вытягивая во все стороны широкие листья навстречу свету, наблюдал борьбу за выживание, не менее жестокую и бескомпромиссную, чем у животных. Не важно, что здесь все происходит медленно и молча, не важно, что бой идет за невесомые солнечные лучи, а не за живые организмы.
Да и не обязательно ехать в тропики, чтобы стать свидетелем такой борьбы. Ее можно наблюдать и на лужайке в деревне, где широкие листья одуванчика ловят солнечные лучи, безжалостно перехватывая их и обрекая хилую травку на смерть в тени.
Но солнечный свет — нематериален, пусть даже он и несет какую-то энергию, а растение ведь состоит из материи и должно хранить энергию в виде материальных химических веществ. Откуда же берется материя?
Все растения растут на какой-то почве, так что логичнее всего предположить, что материал для построения растения именно из нее и берется. В 60-х годах XVII века фламандский химик по имени Ян Баптист ван Гельмонт решил проверить это предположение. Он посадил иву и выращивал ее в горшке на протяжении пяти лет. Дерево росло и набрало 150 фунтов веса, а вес почвы, в которой оно росло, уменьшился при этом разве что на пару унций. Тогда ван Гельмонт решил, что растение строится не за счет почвы, а за счет воды, которой его поливают и без которой любое растение, сколь плодородной ни была бы почва, неизбежно погибает.
С современной точки зрения ван Гельмонт был прав. Почва состоит по большей части из глинозема и прочих веществ, не играющих большой роли в обмене веществ. По большей части почва выполняет чисто механическую функцию — служит твердым, но проницаемым основанием, на котором растение может располагаться и в котором удерживается необходимая растению вода.
Вода необходима растению, и не только потому, что она составляет большую часть самого растения (как и представителей прочих форм жизни), но и потому, что в ней растворяются небольшие количества неорганических веществ, необходимых растению, которые оно не может впитать иначе, кроме как в виде раствора. Удобрения используются как раз для того, чтобы восполнить запас этих необходимых растению веществ, истощенный предыдущими поколениями растений.
В принципе возможно выращивать растения и при отсутствии почвы, в одном лишь растворе необходимых неорганических веществ. Это называется «гидропоникой», и реальность гидропоники доказывает правоту ван Гельмонта в его утверждении о том, что вода нужнее, чем почва. Вот в чем ван Гельмонт был не прав — так это в том, что вода — это все, что нужно растению, поскольку одной лишь воды, и даже воды с добавлением неорганических веществ недостаточно, чтобы поддерживать жизнь. Химикам XVIII века, взявшимся за тщательное изучение органических веществ, это было уже ясно.
Органической характеристикой живой ткани является углерод. Углерода, присутствующего в растворимой форме в плодородной почве, недостаточно, чтобы обеспечить потребность постоянно увеличивающего свои размеры растения в углероде. При гидропонике питательная смесь может быть вообще полностью лишенной углерода, а растение все равно будет откуда-то брать этот элемент. Откуда? Раз ни в почве, ни в воде его нет, то остается только воздух.
Именно ван Гельмонту принадлежит честь открытия существования различных газов, и именно он впервые описал свойства того газа, который мы сейчас называем углекислым. На протяжении следующего за его открытиями столетия исследования различных газов проводились все активнее, и в 1727 году английский физиолог Стивен Гейлс, проявлявший большой интерес к газам, обнаружил, что ответ на вопрос, мучивший ван Гельмонта, кроется в открытом самим же ван Гельмонтом углекислом газе.
Но ведь углекислый газ составляет лишь 0,03 процента в атмосфере, так что остается только удивляться, как вещество, присутствующее в столь малой концентрации, может служить источником углерода для множества окружающих нас организмов. Что ж, все равно углекислого газа оказывается достаточно, если учесть, что атмосфера огромна и общая масса ее невероятно велика, как ни тяжело это представить людям, мыслящим аллегориями типа «легкий как воздух». Общий вес углекислого газа, содержащегося в атмосфере, составляет, хотите верьте, хотите нет, 4 х 1014 килограммов. В океане его растворено еще в пятьдесят раз больше, либо в виде углекислоты, либо в виде иона бикарбоната, так что общая масса углерода, доступного для потребления живыми формами на суше и в море, составляет 2 x 1016 килограммов.
Подсчитано, что общая масса углерода, связанного в составе живых существ, — около 2,5 x 1014 килограммов; так что суммарный запас углерода, содержащегося в море и в воздухе, примерно в восемьдесят раз превышает количество углерода, заключенного в живых тканях. Как я уже сказал в начале главы, масса доступной пищи должна быть вдесятеро больше массы ее потребителя, и если считать углекислоту основной пищей для всего живого на Земле, то ее хватит на все живое на нашей планете.
В 70-х годах XVIII века английский унитарианский священник Джозеф Пристли продвинулся еще на шаг дальше. Он посадил растение под герметичным куполом, оно какое-то время росло, пока не исчерпало весь углекислый газ, содержащийся в замкнутом объеме, а затем прекратило рост, несмотря на обилие воды и солнечного света. Помещенная под такой же герметичный купол мышь быстро расходовала весь содержащийся в замкнутом объеме кислород и умирала. А вот мышь вместе с растением под одним куполом могли прожить гораздо дольше, чем каждое из этих существ по отдельности. Из этих наблюдений Пристли сделал вывод, что растение наверняка не только потребляет углекислый газ (это если оперировать сегодняшними терминами — Пристли выражался несколько по-другому), но и выделяет кислород, а животные, наоборот, потребляют кислород и выделяют углекислый газ. Таким образом каждое существо из такой пары помогает удовлетворить потребности другого.
Теперь оставалось только отметить подобную же связь и на уровне всей планеты — что и сделал голландский физик Ян Ингенхауз. В своей вышедшей в 1779 году книге он отметил, что животный и растительный мир на Земле находится в равновесии. Растения поглощают воду и углекислый газ и с помощью света (Ингенхауз оказался также и первым, кто недвусмысленно подчеркнул необходимость света) производят из них свои собственные ткани и выделяют кислород. Поскольку свет является важнейшим условием процесса формирования тканей из углекислоты и воды, то этот процесс был назван фотосинтезом, что по-гречески означает «сборка с помощью света».
С другой стороны, продолжал Ингенхауз, животные, поедая растения и вдыхая кислород, снова превращают их в углекислый газ и воду.
По мере развития химии питательных процессов становилось ясно, что принятым среди растений способом хранения энергии является крахмал. Представим эмпирическую формулу крахмала как СбН10О6. Тогда представления Ингенхауза можно выразить так:
6СO2 + 5H2O ↔ С6Н10О5 + 6O2.
При таком раскладе цикл может продолжаться вечно. Углерод, водород и кислород будут постоянно перемещаться от растений к животным и обратно, с суши в море и обратно — такое циклическое перемещение было названо «углеродный цикл». Другие элементы тоже используются циклическим образом. Растения извлекают из земли азот, серу, фосфор и другие неорганические элементы и встраивают их в состав своих тканей. Животные съедают растения и переводят эти элементы в собственные ткани, а извергая всю жизнь отходы и в конце концов умирая с последующим разложением тел, — возвращают их в почву.
И на всех этапах цикла используется безвозвратно только одно — энергия солнечного излучения. И его потребляется гораздо больше, чем хватило бы для запуска процесса уменьшения энтропии, так что в целом энтропия опять увеличивается, как это происходит всегда и как требует второй закон термодинамики.
В 1819 году двое французских химиков, Пьер Жозеф Пеллетье и Жозеф Бьенемэ Каванту, выделили из растений вещество зеленого цвета. Они назвали выделенный продукт «хлорофиллом», от греческого «зеленый лист» — понятней некуда.
Однако прошло еще сто лет, прежде чем было установлено строение хлорофилла. Начиная с 1910 года немецкие химики Рихард Вильштеттер и Ганс Фишер провели ряд экспериментов по расщеплению молекулы хлорофилла на фрагменты и изучению их свойств, в результате чего было составлено представление и о самой молекуле хлорофилла. Оказалось, что по основе строения хлорофилл очень похож на гем, являющийся частью гемоглобина, каталазы и цитохромов. Основные отличия хлорофилла от гема заключаются, во-первых, в том, что посреди молекулы, там, где у гема — железо, у хлорофилла — магний, а во-вторых, в том, что к хлорофиллу крепится еще и длинная углеводная молекула, принадлежащая к классу каротеноидов.
Своим цветом молекула хлорофилла обязана тому факту, что она поглощает свет некоторых волн видимой части спектра, в частности длинные волны красного и оранжевого участков спектра, а большую часть остальных — отражает. Если из солнечного света вычесть красный и оранжевый цвета, то получится зеленый — что мы и наблюдаем.
Поглощая свет, хлорофилл повышает свое энергетическое содержание. В главе 11 я уже описывал механизм, с помощью которого молекула хлора расщепляется светом на более энергетически насыщенные атомы хлора. Конечно, процессы, в которых участвует хлорофилл, не так просты, но принцип тот же — хлорофилл получает дополнительную энергию за счет поглощения света.
Получив энергию, хлорофилл теперь может ее потратить и вернуться в «естественное состояние», произведя при этом некую энергоемкую реакцию, определяющую весь процесс фотосинтеза.
Так что же это за «определяющая реакция»? Ответ на этот вопрос тоже стал возможен только с появлением технологий изотопного маркирования.
Как видно из формулы, приведенной в этой главе, в реакцию фотосинтеза должно входить соединение воды и углекислоты. В состав обеих этих молекул входит кислород, так что логично предположить, что производимый растениями молекулярный кислород должен включать в себя атомы из обоих этих веществ. В конце концов, фотосинтез ведь должен представлять собой реакцию, обратную дыханию. Если при дыхании кислород объединяется с органическими веществами для образования и углекислоты, и воды, то при фотосинтезе углекислый газ и вода должны расщепляться для образования кислорода, верно ведь?
Но голые рассуждения, не подтвержденные экспериментальными свидетельствами, могут оказаться очень обманчивыми. И вот американские биохимики Сэмюэл Рубен и Мартин Кеймен решили получить такие свидетельства, устроив эксперимент с использованием тяжелого, но нерадиоактивного изотопа кислорода О18. Большая часть всех атомов кислорода, 99,76 процента, принадлежит к самому распространенному изотопу, О16, так что вещество с необычно большим содержанием О18 всегда заметно отличимо в масс-спектрографе.
В 1938 году Рубен и Кеймен изготовили некоторое количество воды с содержанием О18 и стали поливать этой водой растения. В производимом растениями кислороде О18 оказалось столько же, сколько и в употребленной ими воде. С другой стороны, если же растениям подавался углекислый газ с содержанием О18, то лишь крайне малый процент этого О18 попадал в состав производимого растениями кислорода. Вывод ясен — вода, и только она, в процессе фотосинтеза расщепляется, и только из расщепленной молекулы воды образуется кислород. А молекула углекислого газа остается нерасщепленной и интегрируется в таком виде в состав формируемых в процессе фотосинтеза органических тканей.
Таким образом были установлены общие очертания реакции фотосинтеза. Хлорофилл поглощает солнечный свет и использует полученную таким образом энергию для энергоемкой реакции расщепления воды на водород и кислород (рис. 73). Эта реакция называется «фотолиз», или «фотохимическая диссоциация» воды.
Получаемый таким образом водород может использоваться двумя различными способами. Половина атомов водорода направляется в дыхательную цепочку, как и водород, получаемый в результате обычной дегидрогенизации. В принципе фотолиз воды можно рассматривать и как катализируемую хлорофиллом дегидрогенизацию воды. После этого водород снова объединяется с кислородом на заключительном этапе цитохромоксидазы и опять образуется молекула воды. По ходу этих реакций формируется три молекулы АТФ; таким образом энергия солнечного излучения преобразуется в химическую энергию АТФ, а поскольку кислород, полученный одновременно с пущенным в дыхательную цепочку водородом, при образовании воды снова потребляется, то в этой цепочке реакций выделения кислорода не происходит.
Оставшаяся половина атомов водорода вступает в соединение с углекислотой с образованием углеводов (вот здесь-то и высвобождается кислород, который больше растению ни для чего в дальнейшем не пригодится и потому выпускается в атмосферу). Это энергоемкая реакция, и она проходит за счет АТФ, образованных в процессе фотолиза и реакции формирования воды.
Так энергия солнечного излучения, будучи переведенной в химическую энергию АТФ, используется для образования углеводов (а в конечном итоге—и жиров и прочих составляющих тканей), за счет чего существуют все формы жизни на Земле — и растительные, и животные.
Рис. 73. Фотосинтез
Теперь осталось только установить, как именно водород соединяется с углекислотой. Это оказалось непростой задачей. Исследователи пытались использовать углекислый газ, содержащий необычный изотоп, но через короткий промежуток времени этот изотоп обнаруживался уже во всех составляющих тканей. Тогда ученые решили выделить хлоропласта (клетки растения, содержащие хлорофилл) отдельно и проверить на них, но изолированный хлорофилл вообще отказывался проявлять какие бы то ни было фотосинтетические свойства, так что и эксперименты с упрощенной системой, оказавшие такую неоценимую помощь при работе с реакциями, катализируемыми ферментами, в данном случае ни к чему не привели.
Надеяться оставалось только на радиоактивные изотопы. К сожалению, единственным известным в 30-х годах XX века радиоактивным изотопом углерода был С11, столь нестабильный, что за полчаса почти весь уже переставал существовать, и при этом очень дорогой.
Но вот в 1940 году Рубен и Кеймен открыли С14, радиоактивный изотоп углерода, оказавшийся, ко всеобщему изумлению, сравнительно стабильным, а потому — удобным для практического применения. Вообще, можно сказать, что С14 — это самый полезный изо всех изотопов.
После Второй мировой войны американские биохимики А. Бенсон и Мельвин Кальвин попытались исследовать фотосинтез с помощью С14. Они взяли взвесь одноклеточных водорослей и обработали ее углекислотой с содержанием С14. Через небольшой промежуток времени они убили клетки в надежде на то, что С14 успел использоваться лишь на ранних этапах внутриклеточных реакций. Затем содержимое убитых клеток было сегментировано с помощью технологии бумажной хроматографии (см. главу 16). Осталось только посмотреть, какие участки бумаги проявляют радиоактивность, и определить, какое вещество на них отложилось.
Всего полторы минуты спустя различных радиоактивных веществ оказалось уже не менее пятнадцати, тогда Бенсон и Кальвин еще больше сократили временной промежуток. Через пять секунд после обработки радиоактивной углекислотой радиоактивных веществ на бумаге оказалось пять, впрочем, наибольшую радиоактивность проявляли два из них. Оба оказались разновидностями фосфоглицериновой кислоты, в состав которой входят три атома углерода.
Проведя множество подобных экспериментов, Бенсон и Кальвин разработали логическую схему происходящего. Углекислота, попадая в клетку, соединяется с рибулозо-1,5-дифосфатом. (Этот сахар, содержащий пять атомов углерода и две фосфатные группы, называют еще «углекислотной ловушкой».)
Получив углекислый газ, рибулозо-1,5-дифосфат превращается в соединение из шести атомов углерода и вскоре распадается на две молекулы по три атома углерода в каждой — это и есть обнаруживаемые при бумажной хроматографии фосфоглицериновые кислоты. Это энергоемкий шаг, и именно при нем используются АТФ, образованные путем фотолиза и реакции формирования воды. Затем эти трехуглеродные сахара преобразуются в крахмал посредством ряда реакций, которые уже хорошо изучены и не требуют дальнейшего приложения энергии.
Наверное, самым примечательным свойством фотосинтеза является тот факт, что в качестве источника энергии при нем применяются красный и оранжевый цвета. Фотохимические реакции, производимые человеком в лаборатории, обычно задействуют гораздо более энергетически насыщенное излучение синей, фиолетовой и ультрафиолетовой части спектра. Способность хлорофилла использовать длинноволновое излучение очень важна, так как его в солнечном свете содержится гораздо больше, чем ультрафиолета. Кроме того, более длинные волны света лучше проникают сквозь атмосферную пыль, чем коротковолновое излучение, так что длинноволновой свет можно назвать более надежным источником энергии.
Фотосинтез имеет необычно высокую эффективность для фотохимической реакции. Отто Варбург и Дин Берк в 1950 году выдвинули предположение, что на участие в фотосинтезе одной молекулы углекислоты требуется затратить всего четыре кванта красного света. Для перевода одного моля углекислоты в углевод требуется 115 килокалорий, а если Варбург и Берк правы, то для аналогичной реакции, используя красный свет, потребуется всего 175 килокалорий. Таким образом, получили феноменальную эффективность фотосинтеза, равную 115/175, то есть около 65 процентов.
Итак, как и предположил сто лет назад Майер (см. главу 4), вся жизнь играет в потоках солнечной энергии. Сама солнечная энергия выделяется в процессе превращения водорода в гелий в условиях невообразимо высоких температуры и давления солнечного ядра. Процесс образования энергии сопровождается соответствующей потерей массы.
Атом водорода при превращении в гелий теряет менее 1 процента собственной массы, но размеры Солнца огромны, и количество атомов, подвергающихся подобной метаморфозе, столь велико, что Солнце теряет по 4 200 000 тонн массы каждую секунду. Высвобождаемая в результате этого энергия имеет объем около 8 х 1021 (восемь секситиллионов) килокалорий в секунду.
Высвобождение энергии за счет потери массы в условиях солнечного ядра является спонтанной реакцией и сопровождается масштабным увеличением энтропии. Во всех остальных звездах происходит то же самое — на одних медленнее, чем в Солнце, на других гораздо быстрее.
Получается, что во вселенских масштабах главным процессом является возрастание энтропии путем звездного излучения. Каким образом Вселенная набрала столько энергии, чтобы терпеть подобное возрастание энтропии на протяжении миллиардов лет своего существования и чем все это закончится (в конце главы 5 я упоминал, например, теорию «тепловой смерти Вселенной») — пусть решают астрономы. Биологи же и биохимики вполне могут принять исходящий от Солнца поток энергии за постоянную величину — по крайней мере, на протяжении существования жизни на Земле (вероятно, пару миллиардов лет) и еще на несколько миллиардов лет вперед.
И лишь с помощью столь глобального увеличения вселенской энтропии, выражаемого в выработке солнечной энергии, жизни на Земле удается немного понижать энтропию в пределах своей компетенции.
Стоит упомянуть о том, что подавляющая часть солнечной энергии теряется в космосе и бесконечно летит по межзвездному пространству в неизвестном направлении. Земле достается лишь мизерная часть. Хотя «мизерной» ее можно назвать лишь по сравнению с общим количеством солнечного излучения, абсолютные же цифры остаются поражающими воображение — 2 x 1013 (двадцать триллионов) килокалорий в секунду.
Но и это — лишь потенциально доступная в идеальном случае величина. Около половины этой энергии сразу же отражается облаками, океанами и полярными льдами. Из того, что остается, часть рассеивается атмосферой, а часть — бесполезно тратится на нагревание океанской воды или песков в пустынях.
На поверхность растений попадает лишь 3 процента от общего количества солнечной энергии, направленной на Землю. И из этого объема две трети поглощается, не доходя до хлорофилла. Наконец, две трети энергии, достигающей хлорофилла, преобразуется в высокоэнергетические фосфатные связи.
Получается, что путем фотосинтеза на Земле ежесекундно производится 3 х 1011 килокалорий высокоэнергетических фосфатных связей.
Принимая энергопотери едока при поедании пищи за 90 процентов, мы видим, что 3 x 1011 килокалорий, производимых растениями, могут служить источником энергии для животного мира, использующего 3 х 1010 килокалорий в секунду. Подсчитано, что на суше обитает около одной восьмой всех животных на Земле, потребляя при этом 4 x 109 килокалорий в секунду.
Население Земли составляет сейчас около 2,3 x 109 человек[11], и если взять среднедневную норму потребления энергии человеком за 2000 килокалорий, то получится, что на все человечество тратится 53 000 000 килокалорий в секунду. Пока что человек составляет, таким образом, уже более 1 процента от всего животного мира Земли.
Если количество людей возрастет в восемьдесят раз, то это будет предел, больше которого растительный мир не сможет прокормить. И то только при условии, что все остальные животные на Земле, конкуренты человека за пищу, будут уничтожены и все растения будут служить пищей одному лишь человеку. Человечество может избежать этой ловушки, начав использовать и морские растения, — тогда оно может расти до уровня в 650 раз больше сегодняшнего, но это опять же идеальный случай — если все морские животные тоже будут уничтожены и человек научится питаться непосредственно планктоном.
Получается, что максимальное количество людей, которое может прокормить Земля, — 1,5 x 1012, то есть полтора триллиона.
На каждого человека в таких условиях будет приходиться лишь по сотне квадратных метров территории. На каждом гектаре будет находиться по сто человек — везде, даже в Гренландии, Антарктиде и пустыне Сахара. Для сравнения, сейчас даже на Род-Айленде, являющемся самым густонаселенным штатом США, плотность населения — три человека на гектар.
Звучит ужасно. Однако еще ужаснее, что если темпы роста человечества сохранятся (удваивание каждые шестьдесят лет), то максимально возможный уровень будет достигнут уже через 550 лет, в 2500 году.
С другой стороны, одни виды животных, таких как коровы, свиньи, куры или рыба, вряд ли захотим полностью уничтожить, так как наличие их мяса в рационе крайне желательно, а другие виды, такие как крысы или насекомые, вряд ли сможем, так что придется сойтись на той цифре, что максимальная масса людей на планете может составлять не более одной десятой от общей массы живых существ. В таком свете ситуация выглядит еще хуже.
Да, тогда максимальное количество людей на планете не сможет превысить 150 000 000 000, и плотность населения не превысит показателя в 10 человек на гектар. Пространства будет чуть больше, а еда — чуть разнообразнее. Однако времени до такого положения нам осталось еще меньше — всего 350 лет, до 2300 года.
Данные расчеты приведены, конечно, без поправок на то, что при достижении некоего угрожающего положения дел будут приняты меры по ограничению рождаемости в глобальном масштабе или, может быть, разразится мировая ядерная война. (Я бы предпочел первое, но иногда вероятность второго кажется слишком большой.)
И все же не стоит унывать. Будущее человечества можно представить не только в темных тонах. С точки зрения некоего внеземного наблюдателя локальное уменьшение уровня энтропии на Земле, на фоне глобального ее увеличения в процессе солнечного излучения окажется незамеченным, как если бы капля воды поднималась вверх по Ниагарскому водопаду.
Но масштабы — это еще не все. Жизнь достигла таких высот сложности, каких с помощью грубой солнечной энергии достигнуть было крайне маловероятно. И вершина жизни — человеческий разум — получил возможность, равной которой никогда еще не предоставлялось и значение которой не поддается какой бы то ни было строгой оценке.
Человек обязан подчиняться законам термодинамики и всегда будет обязан им подчиняться, но это не значит, что он полностью беззащитен перед ними. Раз уж в законах нельзя найти лазейку, то можно попытаться использовать их себе на пользу!
Получив власть над энергией атома, человек совершил достижение, сравнимое с овладением огнем (с описания которого я и начал эту книгу). Овладение огнем избавило человека от непосредственной зависимости от солнечного света и тепла, а овладение атомной энергией сделало его независимым и от самого Солнца.
Точнее, даже несмотря на наличие водородных реакторов, человек все еще сохраняет некоторую зависимость от Солнца в плане получения биологической энергии — создания питательных веществ в процессе фотосинтеза. Но недалек тот день, когда человек окончательно изучит фотосинтез, и тогда, используя энергию водородных реакторов, вещество Вселенной в качестве сырья, искусственно созданный фермент — вместо хлорофилла, человек научится сам производить пищу в любых количествах, независимо как от Солнца, так и от растений.
Тогда весь мир, все планеты всех звезд станут ему домом.
По крайней мере, те, которые останутся к тому времени свободными.
* * *
Примечания
1
Количественное выражение усилия, задействованного в толкающем или тянущем движении, можно использовать в качестве грубого определения термина «сила». Вообще же «сила» имеет строгое научное определение, до которого мы доберемся позже, а пока нам хватит и интуитивного понимания этого слова.
(обратно)2
На самом деле, конечно, горячая камера не остывает, а холодная — не нагревается, потому что горячую постоянно подогревает огонь, а холодная так же постоянно охлаждается, будучи омываемой холодной водой. Тем не менее часть тепловой энергии пара не переводится в работу, поскольку тратится на поддержание температуры пара, а часть теплового дефицита конденсатора таким же образом уходит на поддержание его в холодном состоянии. Таким образом, мы видим, что машина не производит всего того количества работы, которое от нее можно было бы ожидать, исходя из разности температур по формуле Карно.
(обратно)3
В 1961 году этот порядок был несколько изменен: атомный вес углерода был принят за 12,00000, а атомный вес остальных атомов — пересчитан с учетом нововведения. Поэтому атомный вес кислорода сейчас составляет 15,9994.
(обратно)4
Что, собственно, представляет собой сам «заряд», до сих пор неизвестно, но оставим этот вопрос философам. Чем бы заряд ни являлся по сути, мы точно знаем, что он имеет измеряемые свойства отталкивания и притяжения и четко определимые свойства. Физикам этого достаточно.
(обратно)5
В англоязычной, соответственно — международной, терминологии имя русского ученого Менделеева опускается. Так что западному читателю таблица Менделеева известна просто как безымянная периодическая таблица элементов. (Примеч. пер.)
(обратно)6
Имеется в виду — на год написания книги. Сейчас уже можно смело заменить цифру 103 на 109. (Примеч. пер.)
(обратно)7
Поскольку валентность кислорода — 2, то и координационная связь до обретения четкого представления об электронном строении атомов рассматривалась как двойная:
Именно благодаря этому представлению считалось, что валентность фосфора (как и азота) равна пяти.
(обратно)8
Нуклеиновые кислоты не играют большой роли в вопросах энергообмена и поэтому не являются предметом рассмотрения данной книги. Однако в принципе нуклеиновые кислоты — важнейшее вещество для жизни как таковой, и даже можно сказать, что именно нуклеиновые кислоты и представляют собой жизнь. В частности, они управляют снижающим энтропию процессом синтеза особых белков; подробнее я рассматриваю их, например, в последней трети моей книги «Источники жизни».
(обратно)9
В главе 20 я называл цифру 650 килокалорий — но пусть это вас не смущает, так как там речь шла о реакциях с использованием двух молекул молочной кислоты. Прочие подробности описаны мной в уже упоминавшейся книге «Источники жизни».
(обратно)10
Ввиду вышеописанных соображений современная биология не считает грибы растениями, выделяя их в отдельное царство, наряду с растениями и животными. (Примеч. пер.)
(обратно)11
Это данные на год написания книги, сейчас уже около 6 х 109 г (Примеч. пер.)
(обратно)



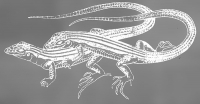







Комментарии к книге «Энергия жизни. От искры до фотосинтеза», Айзек Азимов
Всего 0 комментариев