Что, если Ламарк прав? Иммуногенетика и эволюция
Глава 1 ИДЕИ ЛАМАРКА И ДАРВИНА - ДВЕ СТОРОНЫ ОДНОЙ МЕДАЛИ
За последние 45 лет мы стали свидетелями бурного роста новой области науки — молекулярной генетики. Она преобразует наши представления о механизмах наследственности и эволюции жизни на Земле. Пора проанализировать уроки этого периода и изложить их в доступной для широкого круга читателей форме. Революционные представления Чарлза Дарвина о естественном отборе как главной движущей силе эволюции сейчас превратились в догму. Обновление наших взглядов на эволюцию требует учета данных, полученных молекулярной генетикой, особенно — молекулярной генетикой иммунной системы. К концу двадцатого столетия в этой области молекулярной биологии выходит на сцену и становится рядом с Чарлзом Дарвином другой «дедушка» эволюционной теории, французский биолог Жан Батист де Ламарк. Поэтому сейчас следует рассмотреть идеи и проблемы, еще недавно казавшиеся еретическими: Работает ли принцип Ламарка в Природе? Насколько проницаем барьер Вейсмана? (теоретический барьер между клетками тела и половыми клетками — сперматозоидами и яйцеклетками). Могут ли наследоваться приобретенные признаки ? Если да, можем ли мы описать процесс такого наследования молекулярными терминами ?
Тридцать лет назад эти вопросы поставил в серии ярких, умных книг крупный ученый и философ Артур Кестлер (Koestler). Мысли и слова, высказанные им, не были гласом вопиющего в интеллектуальной пустыне; более того, некоторые из его научных догадок вызвали живой интерес среди ученых.
В научной картине «внутреннего мира» клеток и молекул иммунной системы неоламаркистские представления об обратной связи генов сомы и зародышевой линии давно занимают видное и законное место. В этой книге мы покажем, как можно языком молекулярной генетики описать явление соматического гипермутирования генов антител и предполагаемый процесс переноса информации от сомы к половым клеткам.
Мы также исследуем применимость наших толкований к органам и тканям вне иммунной системы. Пока еще рано делать окончательные заключения, однако, можно сформулировать четкие вопросы и некоторые выводы, важные для будущих научных исследований.
Сам Чарлз Дарвин 130 лет назад создал модель наследования приобретенных признаков. Свои представления о наследовании он назвал теорией пангенезиса, которая имела заметные ламаркистские черты. Мы подробно опишем и этот малоизвестный исторический факт, и бурную историю развития идей Ламарка, и отношение к ним на протяжении девятнадцатого и двадцатого столетий. По нашему мнению, острые споры о механизме эволюции гораздо более плодотворны для развития эволюционной теории, нежели рабская привязанность к неодарвинизму, превратившая в заклинание бесконечное повторение одного и того же тезиса: «Эволюция идет только путем естественного отбора случайных мутаций». (Мы имеем в виду труды Ричарда Докинза (Dawkins) и Дэниеля Деннета (Dennet).
Мы постараемся, не злоупотребляя научными терминами, объяснить читателям основные положения молекулярной генетики, быстро изменяющей наш взгляд на мир. Важные определения и биохимические термины приводятся в сопровождающих текст таблицах и рисунках. Если вы столкнетесь с незнакомыми терминами, советуем обращаться к словарю в конце книги.
Мы обсудим следующее важнейшее утверждение: измененные гены соматических клеток (клеток тела) могут встраиваться в геном половых клеток (яйцеклеток и сперматозоидов) и наследоваться потомками в соответствии с генетическими законами. По существу, это молекулярная версия идеи о наследовании приобретенных признаков, четко сформулированной Ламарком и позже принятой Дарвином в его теории пангенезиса.
В центре внимания этой книги будут научные исследования, которые, по нашему мнению, заставляют пересмотреть общепринятую точку зрения на поведение генов. Генетика все глубже проникает в сложные молекулярные процессы, находящиеся в самом сердце механизма наследственности. Однако мы сразу хотим подчеркнуть, что пока все наши выводы основываются на анализе работы иммунной системой позвоночных (тип Vertebrata).
Традиционное, и в целом правильное, представление о генетических механизмах эволюции основано на главном предположении Чарлза Дарвина. Он считал, что изменчивость между видами и в пределах вида определяется наследственными особенностями составляющих их особей. «Орудующая» в природе «смерть-старуха» забирает слабых и оставляет наиболее приспособленных. Именно этот процесс называется естественным отбором. В колоссальной предсуществующей изменчивости, часто едва заметной, можно обнаружить, например, различия между особями по размерам тела, пищевым потребностям или по способности избегать хищников. Наиболее приспособленные выживут и передадут свои признаки потомкам. Таким образом, естественный отбор действует на имеющуюся в популяции организмов наследственную изменчивость. В современной трактовке единственный тип генетических изменений, допускаемый в данной схеме, — это случайные мутации генов в половых клетках (яйцеклетках и сперматозоидах). Именно это составляет суть оставленного Чарлзом Дарвином наследия, изложенного в его книге Происхождение видов, опубликованной в 1859 г. Это — его вклад в современные представления о механизмах эволюции, приведшей к появлению высокоорганизованных растений и животных. Основы современной неодарвинистской теории суммированы в табл. 1.1.
Теория естественного отбора доминировала в нашем мышлении и направляла развитие генетики и теории эволюции в течение большей части двадцатого столетия. Однако логически последовательный механистический принцип эволюционных изменений бьш впервые сформулирован французским биологом Жаном Батистом Ламарком в 1809 г., за пятьдесят лет до опубликования Происхождения видов Дарвина. Именно Ламарка можно считать отцом идеи превращения видов. Он не представлял себе механизма, основанного на естественном отборе, но очень четко сформулировал мысль о том, что приобретенные признаки могут быть переданы следующим поколениям — идею, которую потом долго разделяли многие биологи и философы. Попросту говоря, это означает, что изменившиеся у какого-нибудь животного размер или форма тела, например, в результате изменения питания или пищевых привычек, могут быть переданы его потомкам.
Основные положения традиционной неодарвинистской теории эволюции
• Наследственность
Генетический материал (ДНК) может передаваться неизменным от поколения к поколению.
• Мутации
Изредка в ДНК возникают стойкие изменения - мутации. Чарлз Дарвин называл такие изменения наследственной информации спортами. Например, замена А основания на G приводит к появлению новой последовательности нуклеотидов в данном участке хромосомы, и, соответственно, в информационной РНК. Это приводит к изменению последовательности аминокислот в белке и, следовательно, к изменению его структуры и/или функции. Мутации служат постоянным источником новой генетической информации, на которую может действовать отбор. Полагают, что подобные изменения последовательностей нуклеотидов редки.
• Случайная передача отцовских и материнских хромосом потомку
Оплодотворенная яйцеклетка, из которой развивается человеческий эмбрион, имеет 46 хромосом. В репродуктивных органах (семенниках и яичниках) половозрелых людей происходит особое деление клеток (мейоз), в результате которого число хромосом уменьшается вдвое (гаплоидное число 23). Гаплоидный набор хромосом упаковывается в сперматозоиды у мужчин и в яйцеклетки у женщин. При оплодотворении число хромосом восстанавливается до 46 (диплоидное число). Потомок получает от каждого из родителей 23 случайно выбранные хромосомы, которые родители в свою очередь унаследовали от своих родителей. Все яйцеклетки содержат половую хромосому одного типа, а именно Х-хромосому. В сперматозоидах содержатся либо Х-, либо Y- хромосома. Набор половых хромосом XX определяет женский пол плода, XY - мужской. Все остальные признаки детерминируются случайным сочетанием хромосом. Таким образом, наши обычные житейские наблюдения над детьми справедливы, и если нам кажется, что у «Тома мамино лицо, но папины руки!», значит так оно и есть.
• Рекомбинация
У видов, размножающихся половым путем, физический обмен (кроссинговер, или рекомбинация) между отцовскими и материнскими хромосомами, который происходит во время образования гамет (сперматозоидов и яйцеклеток), вызывает перетасовку существующих последовательностей ДНК. Этот процесс приводит к появлению новых комбинаций наследственных признаков у потомков.
• Естественный отбор и эволюция
Не все генетически разные организмы размножаются одинаково, т.е. с одинаковой скоростью. Условия среды отбирают более приспособленные организмы и дают им селективные преимущества. Если бы не было отбора, не было бы и общих генетических изменений. Эволюция, следовательно, является результатом взаимодействия генетического материала с внутренними (клеточными, внутри организма) и с внешними условиями развития организма и может быть представлена как отбор комбинаций генов, имеющих наибольшую приспособленность.
• Изоляция
В больших популяциях свободное скрещивание между разными генотипами, расширяющее пул генов, в котором действует естественный отбор, невозможно из-за внутренних и внешних изолирующих факторов. Самым простым является географическое отделение потомков от общего предка. Например, некогда единая популяция вьюрков на островах Галапагосского архипелага со временем разделилась на изолированные, небольшие, инбредные популяции. Дарвин заметил, что именно это оказалось важнейшим условием появления новых видов.
• Дрейф
Последовательности ДНК, различаются ли они по большому участку или по одному нуклеотиду, могут быть потеряны по случайным причинам. Генетический дрейф является частью случайного фонового шума, изменяющего сложившийся состав последовательностей ДНК в популяции.
• Барьер Вейсмана
Приобретенные соматические модификации у многоклеточных организмов не могут наследоваться.
Итак, мы представили вам две, отнюдь не несовместимые, концепции. Первая — традиционная неодарвинистская теория о том, что важная для эволюции генетическая изменчивость существует до того, как подействует селективная сила (естественный отбор). И вторая — традиционно отвергаемая ламарков-ская теория о том, что генетическая изменчивость возникает одновременно с отбором. Последняя концепция особенно важна для процессов, протекающих в иммунной системе, для которых селективная сила, или стимул внешней среды (инфекционное заболевание), действует одновременно с появлением новых генетических вариантов.
Таким образом, исторически всегда существовал альтернативный (ламаркисткий) взгляд на механизм эволюционных изменений. Этот механизм легко объясняет, почему некоторые виды смогли очень быстро генетически измениться при внезапных изменениях среды, во время катастроф; также легко объяснить быстрое создание разных пород домашних животных. В этой книге мы рассмотрим, насколько реальны такие изменения с позиций молекулярной генетики. Мы ни в коем случае не утверждаем, что идея Дарвина о естественном отборе случайной предсуществующей изменчивости неверна. Наоборот, мы стремимся доказать, что дарвиновская идея чрезвычайно важна для ламаркистской концепции обратной связи генов сомы и зародышевой линии. По-видимому, правы и Дарвин, и Ламарк. Их взгляды дополняют друг друга. Именно это мы попытаемся продемонстрировать с помощью создаваемой нами теории эво-люционно-генетических изменений иммунной системы.
Это же исторический факт, что сам Чарлз Дарвин, а до него его дед, были ламаркистами. Дарвин разделял идею Ламарка о наследования приобретенных признаков. Ламаркистские доводы об упражнении и неупражнении органов появляются во многих местах его Происхождения видов (1859). Через десять лет после выхода этой книги он публикует теорию пангенезиса [З]. Этот его вклад в науку часто вычеркивается из научной литературы неодарвинистами, которых, по-видимому, сильно задевает тот факт, что основатель теории естественного отбора нашел необходимым воспользоваться ламаркистской «ересью» для объяснения причин генетической изменчивости. Основой для этой теории послужили прекрасные наблюдения Дарвина над изменчивостью и приспособленностью растений и особенно животных в ходе одомашнивания: «Измененные условия вызывают последствия, передающиеся по наследству, например, изменение периода цветения растений, перенесенных из одного климата в другой. У животных усиленная работа или неиспользование каких-то органов оказывают существенное влияние; так, я заметил, что у домашней утки кости крыла весят меньше, а кости ног больше по отношению ко всему скелету, чем те же кости у дикой утки, и это отличие можно с уверенностью приписать тому, что домашняя утка гораздо меньше летает и больше ходит, чем ее дикие предки... .Значительное наследуемое развитие вымени у коров и коз в тех странах, где этих животных обычно доят, по сравнению с животными в других странах, представляет, вероятно, другой пример последствий активной работы, органа»
Рис. 1.1. Теория пангенезиса Чарльза Дарвина, 1868. Теория пангенезиса предложена Чарльзом Дарвином для объяснения причин биологической изменчивости, на которую действует естественный отбор. Основная идея его теории «упражнения и неупражнения» заключается в повышении активности органа-мишени, вызванной стимулами внешней среды (например, токсинами в изменившейся пище). Измененная метаболическая активность ткани-мишени (в данном случае, печени) приводит к приспособлению, далее, согласно теории, из этого органа выделяются «геммулы», или «пангены», которые попадают в кровеносную систему и из нее в половые клетки. Таким образом, измененная функция органа фиксируется в половых клетках и наследуется потомками. Следовательно, Дарвин предположил ламаркистский механизм генетической передачи приобретенных признаков.
В 1868 г. Дарвин пришел к заключению, что соматические изменения, появляющиеся в результате специфического приспособления, стимулируют клетки органа-мишени к выделению некоего наследственного материала в форме, которую он назвал геммулами (или пангенами). Геммулы — это представители каждой нормальной или измененной части тела. Онивыделяются активным органом в кровоток, и, циркулируя по телу, могут попадать в половые клетки и передаваться следующему поколению. Рис. 1.1 иллюстрирует теорию пангенезиса Дарвина. Как мы покажем в следующих главах, Дарвин предвидел не только естественный отбор случайных изменений, но и роль выделяемых телом геммул, записывающих наследуемый эффект, как мы говорим сейчас, на ДНК зародышевой линии.
В 1977 г. Тед Стил предложил гипотезу соматического отбора, которая представляет собой современную молекулярную точку зрения на идею пангенезиса (Steele, 1977). Согласно этой гипотезе, эволюция генов вариабельных участков антител происходит через преодоление вейсмановского барьера, т. е. в результате обратной связи генов сомы (тела) и зародышевой линии. Этот механизм допускает появление новых генетических вариантов в ответ на внедрение микробов из внешней среды. Таким образом, гипотеза соматического отбора представляет собой версию ламарковского наследования, основанную на современных молекулярных данных. Вначале эта идея многими была признана как «еретическая». Однако появившиеся за последние двадцать лет данные изменили отношение к ней. Сейчас нет сомнений в том, что в результате активации антигенами вторгнувшегося инфекционного агента гены, кодирующие белки (антитела), необходимые для распознавания чужеродного агента, подвергаются в соматических клетках быстрому мутиро-ванию (гипермутированию). Самые последние исследования подтверждают то, что мутантные гены антител попадают в ДНК зародышевой линии в результате процесса обратной транскрипции. На рис. 1.2 показано, как соматические изменения могут включаться в ДНК половых клеток.
Рис. 1.2. Предполагаемый механизм соматического отбора в иммунной системе.
1. Множество разнообразных В-лимфоцитов существует до того, как чужеродный антиген попадает в организм. Каждая клетка экспесси-рует на своей поверхностной мембране антитела одной специфичности. Гены вариабельной V-области кодируют те участки антитела, которые образуют антигенсвязывающий центр (как показано на рисунке). Чужеродный антиген связывается с В-клетками, имеющими комплементарное антитело — таким образом, эти клетки «отбираются» в дарвиновском смысле («клональная селекция»).
2. После связывания антигена В-клетка активируется и делится, давая потомков, которые в свою очередь тоже делятся. В результате образуется множество идентичных дочерних клеток — клон. Все клетки клона экспрессируют одинаковые антитела («клональная экспансия»). В отдельных клетках этого клона гены вариабельной области могут мутировать (соматические мутации). Эти клетки в свою очередь могут быть отобраны антигеном для образования нового клона.
3. Внутри клеток клона создаются РНК-копии генов вариабельной V-области. Зрелые молекулы информационной РНК переходят в цитоплазму, где они транслируются в последовательности аминокислот, составляющие белковые цепи антитела
4. Молекулы РНК V-генов (ядерные или цитоплазматические) могут «захватываться» безвредными эндогенными РНК-ретровирусами (продуцируемыми клеткой). Вирусный фермент обратная транс-криптаза может синтезировать ДНК-копию этой РНК (эта копия ДНК называется ретротранскриптом, или кДНК).
5. Копии V-генов антител с помощью вирусов переносятся в сперматозоиды или яйцеклетки, встраиваются в ДНК половых клеток (зародышевой линии) и передаются потомкам, (см. гл. 6)
Открытие в конце 1950-х г. Говардом Теминым (Temin) феномена обратной транскрипции поначалу вызвало сомнение. Однако после присуждения в 1975 г. Темину и Балтимору (Baltimore) Нобелевской премии этот процесс признан всеми как важный элемент репликации ретровирусов (таких, как ВИЧ) и некоторых других событий в клетке. (Свое название ре-тровирусы получили вследствие того, что у них поток генетической информации направлен от РНК к ДНК, т. е. в направлении, обратном существующему во всех живых клетках — от ДНК к РНК.) Главная цель этой книги — показать, как новые данные молекулярной генетики разрушают построения неодарвинистов, рассматривающих отбор случайных генетических вариантов в качестве единственного фактора эволюционных изменений. Мы хотим доказать актуальность новой теории эволюции иммунной системы, основанной на объединении концепций Дарвина и Ламарка.
Почему же точка зрения Ламарка вызвала столько споров? В наши планы не входит полный анализ этого вопроса, однако некоторые исторические моменты борьбы дарвинизма и ламаркизма все же следует отметить. Во-первых, в 1885 г., через три года после смерти Дарвина, немецкий биолог Август Вейсман (Weismann), отвечая на вызов, брошенный теорией пангенезиса, провозгласил существование барьера между соматическими и половыми клетками (рис. 1.3), защищающего половые клетки от любого изменения тела. Вейсман пытался проверить, могут ли наследоваться приобретенные родителями увечья. Например, он вырезал аппендикс или другую ткань и показывал, что потомство не наследует этих нарушений. Но любой мыслящий человек и без этого знает, что иудейская традиция обрезания ни разу не привела к рождению мальчика без крайней плоти. Вейсман провел и другие эксперименты, в частности, с гидрой (Hydra). Однако наиболее известна его работа по отрубанию хвостов у только что родившихся крысят. В длившихся много поколений экспериментах Вейсман показал, что отрубание хвостов никогда не приводило к появлению бесхвостого потомства. Ученые, критиковавшие этот эксперимент, указывали, что такими опытами нельзя проверить идею Ламарка. Короткий обрубленный хвост — это модификация, индуцированная не крысой. А по Ламарку наследоваться могут только модификации, индуцированные ответом организма на условия среды. Если бы Вейсман изучал поведение потомков от крыс, лишенных хвостов, он вполне мог бы наблюдать мелкие наследственные модификации поведения (например, при кормлении, чистке, передвижении).
Рис. 1.3. Барьер Вейсмана. В 1885 г Август Вейсман провозгласил существование тканевого барьера, защищающего половые клетки от любого влияния сомы. На языке современных терминов это можно сформулировать так: мутации в соматических клетках (клетках тела) никогда не передаются в клетки зародышевой линии (репродуктивные клетки).
Существование вейсмановского барьера было якобы неопровержимо доказано в 1911 г. работой Кастла и Филлипса (Castle, Phillips) из Гарвардского университета. Они удалили яичники у белой морской свинки (альбиноса) и пересадили ей яичники черной морской свинки [4]. Белая мать-реципиент при скрещивании с нормальным белым самцом дала несколько черных потомков в течение шести-двенадцати месяцев после операции. Точно такой же результат наблюдался бы при скрещивании белого самца с черной самкой. Таким образом, новая «белая» сома не оказала никакого влияния на половые клетки в пересаженных «черных» яичниках. Однако подобные «острые» эксперименты можно критиковать по тем же причинам, что и отрубание хвостов. Нет никаких причин предполагать, что адаптивный ответ самок с пересаженными яичниками должен быть связан с генетическим контролем окраски шерсти.
Гипотезу Ламарка пытался доказать австрийский биолог Пауль Каммерер (Kammerer). Эта работа имела трагические последствия. Каммерер сообщил, что изменение полового поведения и некоторых других инстинктов у морских животных и земноводных может приводить к появлению потомства, имеющего те же поведенческие или морфологические черты, которые приобрели их родители в течение жизни. Его наиболее известные эксперименты проведены на жабах-повитухах Alytes obstetricians. Большинство видов жаб и лягушек спариваются в воде. Самцы этих видов крепко захватывают самку и долго (дни и недели) удерживают ее до тех пор, пока она не отложит икру.
Для того чтобы удерживать скользкую самку, у самцов на ладонях и пальцах имеются мозолистые и ороговевшие брачные бугорки. Alytes спариваются на суше, у них нет таких бугорков, так как кожа самок сухая и грубая. Пауль Каммерер обнаружил, что, если Alytes заставить спариваться в воде, как это делают другие жабы, то через несколько поколений у них появляются брачные бугорки. Это и есть приобретенный наследственный признак.
В начале двадцатого века эти эксперименты вызвали острую полемику, которая, в конце концов, завершилась тем, что профессор Кембриджского университета Вильям Бэтсон (Bateson) обвинил Каммерера в фальсификации. Артур Кестлер в своей книге Case of Midwife Toad («Дело жабы-повитухи») приводит документы по этому трагическому делу и утверждает, что обвинения не были в достаточной мере доказаны. Но удар был нанесен, и не выдержав оскорбления, в 1926 г. Каммерер покончил жизнь самоубийством. Недавно Марк Гиллман (Gillman) проанализировал этот исторический эпизод в книге Envy as a Retarding Force in Science, 1996 («Зависть как тормоз в науке»).
Еще одной исторической причиной, по которой ламаркистское мышление стало «закрытой зоной» в науке, можно считать разгром советской генетики в 40-е гг. Иосиф Сталин поручил селекционеру Т. Д. Лысенко улучшить сельское хозяйство в СССР. К сожалению, пытаясь продемонстрировать увеличение урожая зерновых с помощью приема, названного яровизацией, Лысенко применил неапробированную процедуру. Этот прием заключался в различных способах обработки семян, например, изменении температуры и питания во время прорастания. Он использовался для получения более продуктивных растений, из семян которых, по утверждению Лысенко, вырастают растения лучшего качества. Но лысенковский подход к возрождению идей Ламарка заставил отвернуться от него западньк ученых и генетиков, работающих в Советском Союзе. Проблема противостояния была решена печально известными жестокими преследованиями научных оппонентов Лысенко [5].
Мы считаем, что все эти обстоятельства истории науки и общества надолго затормозили рациональное развитие идей Ламарка, которые сейчас выливаются в представления об обратной связи генов.
Важно упомянуть еще два момента, оказавших влияние на развитие биологической науки. Первое — это, не побоимся сказать, обожествление Дарвина, особенно в Британии. Дарвина превратили в икону, однако мы полагаем, что на определенном этапе это было действительно необходимо для того, чтобы внедрить в умы человечества ключевую идею о естественном отборе случайных изменений. Без этой концепции было бы трудно объяснить многие биологические явления, будь то Ц структура популяции, изменчивость генов или работа иммунной системы. Это было необходимо для противостояния наивному креационизму, утверждавшему, что все виды возникли одновременно и относительно недавно.
Согласно дарвиновской теории эволюции, для появления новых форм и видов необходимо длительное время. Этот факт согласуется с данными современных палеонтологических и геологических исследований. Действительно, между всеми существующими в настоящее время живыми организмами установлено молекулярно-эволюционное родство. Получение данных, позволивших сделать столь важные заключения, стало возможным благодаря появлению в конце 80-х гг. приборов для автоматического определения последовательности нуклеотидов в ДНК (ДНК-секвенаторы). Новая технология дала возможность генетикам и молекулярным биологам получать точную информацию о большом числе генов (о последовательности нуклеотидов в ДНК). Большая часть этих данных собрана в обширных общедоступных базах данных в Интернете, например в Genbank.
Присуждение в 1993 г. Нобелевской премии по химии Кэри Маллису (Mullis) за открытие и разработку метода полимеразной цепной реакции (ПЦР) подчеркивает важность новых технологий в получении научного знания. Метод ПЦР используется с конца 1980-х годов. Он дает возможность увеличивать число копий отдельного участка ДНК в миллионы раз. После этого с помощью секвенатора можно легко определить порядок нуклеотидов A, G, С и Т в этом фрагменте (определения терминов даны в табл. 1.2). Метод ПЦР стал для генетиков новым мощным «телескопическим» средством, позволяющим увидеть молекулярное строение и информационное содержание различных последовательностей нуклеотидов. Именно метод ПЦР, который можно назвать «генетическим копированием», побудил к созданию книги и фильма «Парк юрского периода», показав возможность (пока нереальную) того, что сохранившиеся древние ископаемые останки ДНК можно размножить, а затем с помощью клонирования «воскресить» вымерших животных.
Основные генетические термины
• ДНК
Дезоксирибонуклеиновая кислота. Очень длинная полимерная молекула, состоящая из четырех типов нуклеотидов, содержащих информационные «основания» А (аденин), G (гуанин), С (цитозин) и Т (тимин). Хромосомы представляют собой длинные последовательности ДНК, включающие миллионы оснований (в клетках эукариот хромосомная ДНК соединена с белком). Молекула ДНК в хромосоме находится в форме двухцепочечной спирали (см. гл. 2). Символически последовательность нуклеотидов в ДНК можно записать так:
5'-AGCTTATTGCATAAGCGCGAT-3'
• 5'и3'
Это - обозначения соответственно левого и правого концов последовательности оснований ДНК или РНК.
• Генетический код
Участок ДНК, который кодирует информацию, определяющую последовательность аминокислот (белок), считывается триплетами оснований, или кодонами. Например, вышеприведенная последовательность триплетов, прочтенная слева направо, должна кодировать следующую последовательность аминокислот:
Ser-Leu-Leu-His-Arg-Asp
• РНК
Рибонуклеиновая кислота. Очень длинная полимерная молекула, похожая на ДНК; в ее состав входят четыре типа оснований А (аденин), G (гуанин), С (цитозин) и U (урацил), Информационная РНК, которая кодирует аминокислотную (белковую) последовательность, скопирована с гена. РНК обычно одноцепочечная. Например, символическую последовательность оснований информационной РНК можно записать так:
5'-AGCUUAUUGCAUAAGCGCGAU-3'
Обратите внимание: это та же последовательность, что и приведенная выше последовательность ДНК, только вместо Т стоит U. Т в ДНК функционально то же самое, что U в РНК.
• Нуклеиновые кислоты
Химический термин для обозначения ДНК и РНК.
• Белки (протеины)
Белки - это длинные полимеры, состоящие из аминокислот. Вместе с сахарами и жирами белки являются строительными блоками нормальной соматической клетки. Химическое строение аминокислоты совершенно иное, чем нуклеиновой кислоты.
• Аминокислоты - это основной составляющий элемент полимерной аминокислотной цепочки, называемой белком. Основания - «буквы» - нуклеиновых кислот читаются по три сразу как набор триплетных кодонов, причем каждая аминокислота кодируется одним или несколькими триплетами. Белки всех живых систем состоят из 20 обычных аминокислот: Gly (глицин), А1а (аланин), Val (валин), Leu (лейцин), Ile (изолейцин), Pro (пролин), Рпе (фенилаланин), Туг (тирозин), Тгр (триптофан), Ser (серин), Thr (треонин), Cys (цистеин), Met (метионин), Asn (аспарагин), Gln (глутамин), Lys (лизин), Arg (аргинин), His (гистидин), Asp (аспарагиновая кислота) и Glu (глутаминовая кислота). Белковую последовательность (как показано выше) можно записать так: Ser-Leu-Leu-His-Lys-Arg-Asp
• Соматические клетки
Клетки тела многоклеточного организма.
• Половые клетки
Сперматозоид и яйцеклетка, при слиянии которых образуется зигота и формируется новый организм.
• Антитело
Белок, продуцируемый белыми кровяными клетками (В-лимфоцитами), который помогает избавить организм от инфекционного чужеродного агента.
За последние 25 лет создано много новых молекулярно-биологических методов манипулирования с ДНК, например, удаление оснований, вставки, сшивание и амплификация (размножение) клонированных фрагментов. Эти методы значительно повысили уровень знаний о процессах, создающих естественную генетическую изменчивость. Действительно, молекулярные биологи работают с нуклеотидньши последовательностями почти так же, как с текстами, предложениями и буквами на экране компьютера. Объединение молекулярных методов с компьютерными технологиями дает возможность искать ответы на новые и важные вопросы о происхождении человека, природе заболеваний (например, СПИДа), причинах мутаций. В ходе этой работы появляется много информации, проливающей свет на эволюционный процесс.
Последовательности ДНК многих сходных по функции (гомологичных) генов и последовательности аминокислот белковых продуктов этих генов похожи у разных организмов — от бактерий до высших растений и животных. Например, известен белок цитохром С, выполняющий важную роль в производстве внутриклеточной энергии (энергетическая молекула называется АТФ) в результате «сжигания» пищевых молекул, поглощенных живой клеткой. Сравнение последовательностей нуклеотидов в ДНК (или последовательностей аминокислот) генов цитохрома С разных видов показало, что этот ген (за исключением редких мутаций) практически одинаков у всех видов, использующих АТФ. Он обнаруживается и у грибов, и у насекомых, и у высших растений, и у животных. И это несмотря на то, что миллион миллионов лет, а может быть и больше, отделяет эти виды от их общего предка (рис. 1.4). Такая картина молекулярной эволюции, свидетельствующая о гомологии ДНК-последовательностей в разное время и у разных видов, повторяется для сотен хорошо изученных генов и является убедительным доказательством факта эволюции. Жаркие споры идут не о самом факте эволюции, но о механизмах эволюции на молекулярном, клеточном, организменном и популяционном уровнях.
Еще одно обстоятельство, оказавшее влияние на отношение к основной идее Ламарка, связано с созданием стройной системы взглядов, необходимой для развития современной генетики. Большая часть ранних работ по генетике была бы невозможной без концепции относительно стабильного гена. Начало этой концепции положено работой августинского монаха Грегора Менделя (1859 г.), законы которого были переоткрыты Гуго де Фризом и другими в начале XX века. Со временем представление о генах как о стабильных менделевских единицах наследственности, нанизанных на хромосому «как бусины на нитку», стало широко принятым. Считалось, что гены, экспрессирую-щиеся в разных органах взрослых растений и животных, защищены в половых клетках барьером Вейсмана и передаются потомкам практически неизменными. Происходит только перемешивание и перетасовка генов в результате генетической рекомбинации отцовских и материнских хромосом во время формирования половых клеток в ходе особого клеточного деления, называемого мейозом (см. таблицу 1.1).
Концепция стабильного гена способствовала развитию современной генетики в контексте идей Дарвина. Выявление и определение генетических связей между родителями и их потомками были бы совершенно бессмысленными в мире, где любое соматическое изменение могло бы быстро включаться в половые клетки. Например, в менделевских экспериментах по скрещиванию разных форм гороха нельзя было бы сформулировать идею о рецессивных и доминантных генах для разных признаков, если бы гены могли изменяться в каждом поколении под влиянием среды.
Рис. 1.4. Увеличение разнообразия форм жизни на Земле в ходе эволюции. Новейшие филогенетические древа, включающие основные клеточные формы жизни — экстремофилы, или археи, истинные бактерии (прока-риоты) и высшие клетки с окруженным мембраной ядром (эукариоты) — можно найти в книгах Вез (Woese, 1994) и Мадигана и Марса (Madigan, Marrs, 1997). По современным оценкам самая ранняя клеточная форма возникла примерно 3,9 млрд. лет назад (Holland, 1997). Фред Хойли и Чандра Викрамасинх (Hoyle, Wickramasinghe. «Our Place in the Cosmos») приводят убедительные свидетельства того, что многие тела Солнечной системы, особенно кометы, а также планеты с органической атмосферой (аммиак, метан) изобилуют клеточными формами жизни. Таким образом, ранняя химическая эволюция могла происходить не на Земле. Более того, свидетельства, представленные Хойли и Викрамасинхом, наводят на мысль, что за последние 4 млрд. лет Земля много раз заражалась клеточными или вирусными генетическими системами, возможно, во время прохода нашей Солнечной системы через плотные молекулярные облака Млечного Пути.
Именно на этом историческом фоне мы хотим обосновать необходимость использования идей Ламарка о вызванных средой быстрых генетических изменениях и обратной связи между сомой и зародышевой плазмой для объяснения процессов, происходящих в иммунной системе позвоночных. Современные данные, по нашему мнению, вполне согласуются с ламаркистскими представлениями о наследовании приобретенных признаков.
В 1979 г. Тед Стил высказал эту идею в книге Somatic Selection and Adaptive Evolution (Соматический отбор и эволюция). Книга вызвала бурную дискуссию. Одни называли такие взгляды хулиганством и еретичеством, другие полагали, что они знаменуют начало новой главы биологии. Боб Бландэн (Blanden) был среди тех, кто с энтузиазмом воспринял идею о том, что ламар-ковские механизмы работают — по крайней мере в иммунной системе. Тесное плодотворное сотрудничество Теда Стила и Боба Бландэна не только помогло им выдержать бурные научные споры конца 1970-х—начала 1980-х годов, оно внесло большой вклад в развитие аргументов, поддерживающих гипотезу о ламаркистском наследовании в иммунной системе. Наш взгляд на эту проблему можно сформулировать так: «если наследование приобретенных признаков в иммунной системе не является истинным фактом, то единственная альтернатива этому — существование разумного манипулятора генами, т. е. признание «божественного вмешательства».
Теперь оставим историю и займемся анализом существующих молекулярных и генетических данных, которые привели нас к гипотезе о том, что в иммунной системе позвоночных действуют ламарковские механизмы.
Гл. 2 мы начинаем с элементарного описания генов и основного закона молекулярной и клеточной биологии о движении генетической информации в живых системах, т. е. с центральной догмы молекулярной биологии. Некоторые основные понятия (ДНК, РНК, основания A, G, С и T/U, белки) уже даны в табл. 1.2. В гл. 2 мы вкратце изложим современную точку зрения на ранние этапы эволюции. По-видимому, первой информационной молекулой, способной к дарвиновской эволюции, была РНК. Но, как ни парадоксально, первичный генетический материал во всех клетках и у многих вирусов — это ДНК. Почему?
В гл. 3, 4 и 5 мы обсудим дарвиновский процесс «выживания наиболее приспособленных», который идет в популяциях белых кровяных клеток (лимфоцитах), когда иммунная система борется с инфекционным агентом. (В нашу эпоху СПИДа тысячи биологов занимаются исследованием молекул и клеток иммунной системы млекопитающих.) В гл. 5 мы изложим современную точку зрения на молекулярные процессы, протекающие в иммунной системе, и подчеркнем, что идеи Дарвина и Ламарка взаимно дополняют друг друга.
Гл. 6 ключевая в нашей книге. Именно в ней мы пытаемся обосновать нашу гипотезу о проницаемости барьера Вейсмана за эволюционное время, по крайней мере для V-генов иммунной системы. Центральная информационная молекула в этой «драме» уже не стабильная двухцепочечная ДНК (в которой последовательностями нуклеотидов А, G, С и Т записана генетическая информация), а сравнительно нестабильная молекула-посредник РНК.
В гл. 7 мы исследуем интересные факты наследования некоторых анатомических структур человека и животных. Приводятся данные о том, что самцы грызунов с индуцированными диабетом и другими эндокринными нарушениями часто передают i свои измененные свойства потомкам. В этой главе мы также рассмотрим свидетельства за и против существования обратной связи сомы и зародышевой линии для других органов и тканей. Это то же самое, что обсуждать, имеет ли дарвиновская теория пангенезиса всеобщее значение. Мы выдвигаем на первый план проблемы, решение которых чрезвычайно важно для современной молекулярной генетики.
Наконец, в эпилоге мы подробно, хотя и умозрительно, обсудим некоторые более широкие приложения идей Ламарка. Например, мы рассмотрим их значение для генетической инженерии, включающей соматическую генотерапию, и концепцию «генетической ответственности». Мы также воспользуемся возможностью ответить на критику нашей теории.
Глава 2 В НАЧАЛЕ БЫЛА РНК
Цель данной главы — рассказать об основных открытиях и идеях молекулярной генетики, на наших глазах превративших эту область биологии в самостоятельную научную дисциплину. В отличие от многих других явлений окружающего нас мира, описанных палеонтологами, антропологами и натуралистами, объекты современной молекулярной и клеточной биологии невидимы. Их приходится упорно «вычесывать» из микроскопической среды замысловатыми экспериментами, используя методы биохимии и молекулярной биологии. От этого задача «пересказа истории исследований» для широкого круга читателей представляется устрашающе сложной. Для ее решения мы используем большое количество рисунков и схем. Их в нашей книге больше, чем в других популярных изданиях.
Большая часть наших знаний в области молекулярной генетики получена за последние 45 лет. Хронология наиболее важных достижений и открытий этого времени приведена в табл. 2.1.
Мы должны предупредить, что будем говорить об очень сложных процессах обмена информацией в живых клетках, протекающих в пространстве, измеряемом микронами (микрон — одна миллионная метра). Сами клетки можно увидеть в обычном световом микроскопе (увеличение примерно от 100 до 600). Если всю ДНК, содержащуюся в 46 хромосомах человека, сложить конец к концу, получится нить длиной несколько метров. В этой длинной нити ДНК содержится огромное количество генетической информации, и, несмотря на это, она сложена и умещена в крошечном пространстве клеточного ядра диаметром всего в несколько микрон. Мы не будем останавливаться подробно на сложных правилах, по которым клетка работает с такими гигантскими полимерами (т. е. хромосомами) и копирует (реплицирует) их. Достаточно только сказать, что процесс репликации хромосом и деления клетки — митоз — протекает за 5—20 ч. в зависимости от типа клеток. (В результате митоза образуются две дочерние клетки, являющиеся точными копиями родительской.)
Важнейшие открытия и достижения молекулярной генетики
• 1952г. Показано, что материалом наследственности у бактериофагов является ДНК, а не белок (А. Херши и М. Чейз).
• 1953г. Открыта структура (двойная спираль) ДНК (Дж. Уотсон и Ф. Крик). П. Медавар с коллегами выявили факт приобретенной иммунологической толерантности у новорожденных мышей
• 1957-59гг. Сформулирована клонально-селекционная теория приобретенного иммунитета, предсказывающая «дарвиновский» отбор антигенами клеток, продуцирующих специфические антитела. (М. Бернет, Д. Талмейдж, Н. Ерне)
• 1957-59 гг. Доказан предсказанный Уотсоном и Криком механизм репликации двойной спирали ДНК и обнаружен фермент ДНК-полимераза (ДНК -> ДНК копирование; М. Мезельсон, Ф. Сталь, А. Корнберг)
• 1959г. Предсказано существование обратной транскриптазы (РНК -> ДНК копирование) (Г. Темин)
• 1961 г. Обнаружена информационная РНК. Это молекула-посредник между геном и белком. Установлен факт копирования ДНК -> РНК с помощью фермента РНК-полимеразы. (С. Бреннер, Ф. Жакоб, М. Мезельсон, Б. Ход, С. Спигельман)
• 1961-66 гг. Расшифрован генетический код. При синтезе последовательности аминокислот, или белка, последовательность оснований информационной РНК считывается по три (ко-дон) (М. Ниренберг, Г. Г. Корана, Ф. Крик, С. Бреннер)
• 1965г. Предложена модель генов антител, предсказывающая V —> С-перестройку (В. Дрейер, Дж. Беннет)
• 1970г. Предложена двусигнальная модель индукции иммунного ответа, усовершенствовавшая представления о различении своего и не-своего (П. Бречер, М. Кон)
• 1970г. Обнаружена обратная транскриптаза опухолевых РНК-вирусов (ретровирусов), т. е. копирование РНК->ДНК (Г.Темин, Д. Балтимор)
• 1968-74 гг. Предложено рациональное объяснение соматических мутаций генов антител. Установлена «зависимость Ву-Кэбота» для V-областей антител (Т. By, Е. Кэбот). Предсказано существование определяемого антигеном соматического гипермугирования вариабельных генов антител (А. Каннингам).
• 1974-77 гг. Установлена уникальная организация генов антител и доказана V -> С-модель Дрейе-ра-Беннета. Опубликованы первые данные по последовательностям ДНК, подтверждающие, что вариабельные гены антител подвергаются соматическому мутированию В. Тонегава)
• 1977гг. Открыты интроны, или некодирующие встроенные последовательности, в генах эука-риот (Р. Роберте, П. Шарп)
• 1979г. Сформулирована теория соматического отбора, предсказывающая движение наследственной информации от сомы к зародышевой линии для вариабельных генов антител в иммунной системе (Э. Стил)
• 1981 г. Широко признаны доказательства того, что определяемое антигеном соматическое гипермутирование генов антител в иммунной системе действительно происходит.
• 1982г. Широко признаны доказательства существования не-вирусной «общей» обратной транскрипции (РНК -» ДНК)
• 1982-83гг. Открыты рибозимы, или ферменты, основанные на РНК (Т. Кеч, С. Альтман)
• 1985г. Предложен метод ПЦР (К. Маллис)
• 1987г. Предложена модель обратной транскрипции для объяснения определяемого антигеном соматического гипермутирования вариабельных генов антител (Э. Стил, Дж. Поллард)
• 1987г. Предложены общая теория эволюции иммунной системы, «концепция протектона» (Р. Лангман,. М. Кон)
• 1992г. Опубликованы данные, согласующиеся с моделью соматического гипермутирования, основанной на обратной транскрипции. Накапливаются сведения, подтверждающие теорию соматического отбора (Г. Ротенфлу, Р. Бландэн, Э. Стил)
• 1996г. Обнаружений рекомбинационный след в V-генах зародышевой линии, что подтверждает схему интеграции, предсказанную теорией соматического отбора (Г. Вейлер, Р. Бландэн, Г. Ротенфлу, П. Зилстра, Э. Стил).
Таким образом, «генетический чертеж», определяющий большое разнообразие живых форм, обусловлен сложной живой информационной системой клетки. Эта система аналогична компьютерным кодам, хранящимся в маленьких полупроводниковых микросхемах, из которых состоит часть центрального обрабатывающего блока компьютера; Законы генетического кода и его перевода в биологические продукты живого организма открывались учеными параллельно с развитием компьютерных технологий. Однако природа создала удивительно совершенные системы хранения и поиска информации задолго до того, как люди придумали силиконовые компьютерные микросхемы. Силиконовые микросхемы для массового производства только лишь сейчас достигли размеров в 1 микрон. Всем известно, что новые поколения компьютеров и компьютерных программ появляются примерно каждые пять лет. Подобные перемены системы понятий и взглядов происходят и в современной молекулярной и клеточной биологии. Благодаря им мы перешли на новый уровень знаний генетических функций, которые рассматриваются в этой главе.
Живые системы функционируют в окруженной мембраной контролируемой микросреде
Началом молекулярной генетики можно считать открытие строения и роли отдельной клетки. Несколько миллиардов лет назад на Земле начала распространяться клеточная форма жизни. Неотъемлемой чертой живых клеток является репли-кация и передача от материнских клеток к дочерним информационных молекул, сначала РНК, а затем ДНК.
Избирательно проницаемая мембрана, окружающая клетку, обеспечивает контролируемую внутреннюю среду (раствор солей и других молекул в воде), внутри которой реплицируется геном, синтезируются и работают все ферменты и мультимолекулярные машины (органеллы). В результате сложного транспортного процесса молекулы (например, белки, углеводы и жиры) постоянно проникают в клетку и пополняют запас молекулярных строительных блоков. Липидная (жировая) водонерастворимая мембрана предотвращает растворение клеточного содержимого в окружающей среде. На мембране располагается множество специализированных молекул, осуществляющих взаимодействие клетки с внешней средой. Некоторые клетки имеют десятки, если не сотни, различных специфических поверхностных рецепторов, которые позволяют им распознавать внешние стимулы и отвечать на них. Некоторые из этих рецепторов действуют и как транспортные каналы, обеспечивающие движение определенных молекул через клеточную мембрану. В клетке непрерывно протекает несметное число химических реакций, которые координируются и совмещаются во времени и пространстве подобно сложным компьютерным программам. Каждая реакция достигает своей определенной цели, важной для роста и выживания клетки.
Рис. 2.1. Высшие и бактериальные клетки, вирусы. Высшие (эукариотические) клетки в 10-100 раз крупнее, чем бактериальные (прокариотические). Избирательно проницаемая мембрана (состоящая из множества липидных молекул), регулирует перемещение различных веществ, включая воду, в клетку и из клетки. Мембрану бактериальной клетки окружает довольно жесткая клеточная стенка. Растительные клетки также имеют внешнюю грубую клеточную стенку (на рисунке не показана). В состав высших клеток входит окруженное мембраной ядро, содержащее несколько хромосом (длинных линейных молекул ДНК). Бактериальные клетки имеют только одну кольцевую хромосому. В высших клетках РНК-копии генов производятся в ядре (процесс транскрипции) и перемещаются в цитоплазму после преобразования (процессинга). (См. рис. 4.4 и 4.5). Затем в цитоплазме эти молекулы информационной мРНК транслируются в белок с помощью специальной молекулярной машины, или органеллы, которая называется рибосомой. В бактериальной клетке РНК и белки производятся в цитоплазме, так как у бактерий нет мембраны, окружающей единственную хромосому. Вирусы — паразиты, которые внедряются в клетку и используют ее молекулярный аппарат для собственного размножения. Они очень мелкие, приблизительно в 10-15 раз меньше, чем клетки, и состоят только из белковой оболочки и генома, представленного ДНК- или РНК-молекулой. Вирусы имеют разные формы и размеры, а молекулы нуклеиновых кислот в их геноме могут быть и двухцепочечными, и одноцепочечными, и линейными, и кольцевыми. Вирусам, которые размножаются в бактериальных клетках, дано специальное название — бактериофаги. Некоторые вирусы безвредны, например, эндогенные РНК-ретровирусы, которые закодированы в геноме нормальных клеток (в виде ДНК) и продуцируются (в виде РНК-транскриптов) нормальной клеткой, например, стимулированным антигеном В-лимфоцитом (см. рис. 1.2).
Что происходит, когда мы съедаем кусочек шоколада и усваиваем сахар? Биохимики установили, что типичная клетка для выделения энергии из молекулы глюкозы использует 30 или более специфических ферментативных реакций. Каждый шаг в этой цепи реакций нужен для отрыва от молекулы глюкозы энергии, заключенной в химических связях, удерживающих атомы в молекулах. Эти химические реакции являются частью процесса «молекулярного питания» клетки, который создавался в ходе эволюции для извлечения максимального количества полезной энергии.
Бактериальные клетки по своим основным функциям несколько отличаются от более специализированных (дифференцированных) клеток многоклеточного организма. Они меньше, их геном состоит из небольшого числа генов. Поскольку требуется координация меньшего числа реакций, бактериальные клетки способны расти и делиться очень быстро. В благоприятных условиях среды на это уходит от 20 до 30 минут. Эта способность к быстрому делению делает бактерии при попадании в организм многоклеточного хозяина опасными болезнетворными агентами. Это же свойство делает бактерии и мельчайшие вирусы, которые в них размножаются (фаги), чрезвычайно полезным инструментом современных исследований в молекулярной генетике.
На рис. 2.1 показаны вирусы в сравнении с бактериальной клеткой и клеткой высших организмов. Вирус представляет собой цепочку генов (вирусный геном может состоять и из ДНК, и из РНК в зависимости от типа вируса), упакованную в белковый чехол или мембранную оболочку. Вирусы сами по себе не растут и не делятся. Все вирусы — паразиты; для того, чтобы приобрести способность размножаться, они должны проникнуть внутрь клетки-хозяина. Это позволило Херши (Hershey) и Чейзу (Chase) в 1952 г. доказать, что генетическим материалом вирусов является нуклеиновая кислота, а не белок (табл. 2.1). Одни вирусы заражают бактериальные клетки, другие — клетки высших многоклеточных организмов, растений и животных. Некоторые вирусы, например, вирусы гриппа и иммунодефицита человека (ВИЧ), вызывающий СПИД, способны быстро изменяться. И это позволяет им ускользать от иммунной системы.
Проникнув в клетку, вирус освобождает свой геном от оболочки и приступает к захвату клеточных метаболических путей для своих собственных целей. (Компьютерный вирус, внедряясь в определенную часть компьютера- «хозяина» достигает подобных же целей.) Внутри клетки ДНК- и РНК-содержащие вирусы размножаются и производят свои белки. Затем происходит сборка зрелых вирусных частиц, которые покидают приютившую их клетку и начинают заражать другие клетки. Одни вирусы убивают клетку при размножении. К ним относится, например, вирус гриппа. Другие мирно сосуществуют с живой клеткой, которую они инфицировали, а вирусное потомство постоянно выходит через клеточную мембрану. Третьи, например, вирус герпеса, могут до начала репликации много лет находиться внутри живой клетки в скрытом (латентном) состоянии. Однако самая крайняя степень паразитизма проявляется у ретровирусов. Некоторые из них, например, ВИЧ, создают ДНК-копию своего РНК-генома, встраивают ее в хромосому(ы) клеточного ядра и реплицируются вместе с хромосомами в ходе нормальных клеточных делений.
Молекулярно-генетические процессы основываются на трех основных принципах
• каждую отдельную химическую реакцию осуществляет специфический катализатор;
• ДНК состоит из двух цепочек нуклеотидов, основания которых связаны парами;
• генетическая информация передается от генов к белкам.
Эти принципы лежат в основе механизма наследственности.
Каждую отдельную химическую реакцию осуществляет специфический катализатор
Открытие этого важнейшего правила молекулярной генетики заняло много лет. Сейчас это аксиома: для протекания каждой отдельной химической реакции в живой клетке необходим специфический белковый фермент (или молекула РНК с ферментными функциями). Ферменты — это биологические катализаторы, они изменяют субстрат, сами оставаясь неизменными. Это очень важная концепция. Из нее следует, что ни один многоступенчатый биологический процесс не может происходить случайно. Все они регулируются рядом координированных взаимодействий между молекулами, которые по форме подходят друг к другу как два кусочка трехмерной мозаики.
Под действием катализатора химическая реакция идет быстрее и эффективнее. Так, в отсутствие фермента молекула А не могла бы немедленно вступить в реакцию с молекулой В и образовать продукт АВ (рис. 2.2). Это могло бы произойти случайно, но ждать этого пришлось бы миллионы лет, если бы вообще удалось дождаться. Специфический фермент, который имеет места «стыковки» для А и В, связывается с ними и держит обе молекулы так тесно, что у них нет другого выбора, как только образовать химические связи друг с другом. Ферменты, таким образом, можно назвать генетически закодированными инструментами, созданными природой для осуществления химических реакций, отобранных входе эволюции. Для проведения сложного набора реакций работа нескольких ферментов синхронизируется и координируется. Таким образом, ферменты способны к коллективному выполнению сложных задач, например таких, как выделение энергии из съеденного кусочка шоколада. Другими словами, каждый фермент можно сравнить с отдельной инструкцией, которая является частью большой компьютерной программы. Однако есть одно фундаментальное отличие. Компьютерный набор инструкций создается человеком для достижения поставленной им цели. Специфическое Действие ферментов регулировалось миллионами (а может быть и миллиардами) лет эволюции путем естественного отбора. Компьютерная программа — результат работы человеческого мозга, а молекулярные процессы, направляющие биологическую эволюцию, происходят через взаимодействие молекул.
Рис. 2.2. ферменты (белки или РНК) - «молекулярные машины», или катализаторы. Изображен белковый фермент, осуществляющий химическую связь между двумя разными молекулами, А и В, с образованием сложной молекулы АВ. Некоторые ферменты состоят из РНК, их называют рибозимами. 1. фермент имеет два связывающих центра, с которыми стыкуются соответствующие им субстраты А и В. 2. Фермент изменяет форму и создает соответствующие молекулярные взаимодействия и силы, облегчая образование химической связи между А и В. 3. Продукт АВ высвобождается. 4. Свободный фермент может использоваться снова.
В клетке работают тысячи ферментов. Одни из них создают строительные блоки для генов; другие распознают пищевые молекулы и обеспечивают их попадание из окружающей среды; наконец, третьи перестраивают различные молекулы внутри клеток. Большинство биологических катализаторов, так же как и многие структурные компоненты клетки, — белки, но есть и катализаторы, представленные РНК.
В конце 1950-х годов Г. Темин предсказал существование обратной транскрипции. Он обнаружил, что опухолевые РНК-содержащие вирусы исчезают при добавлении их к клеткам в культуре ткани. Для объяснения этого он предположил, что вирус создает ДНК-копию своего РНК-генома, затем встраивает эту ДНК-копию в хромосомы клетки (причем исходный вирусный РНК-геном, в конце концов, разрушается). Следовательно, он предсказал существование фермента, который, используя в качестве матрицы молекулу РНК, создает молекулу ДНК. После десятилетних поисков, в конце 1960-х годов, сам Говард Темин обнаружил этот фермент. За эту работу он был удостоен Нобелевской премии (в 1975 году), разделив ее с Давидом Балтимором, который подтвердил существование фермента, названного обратной транскриптазой. Это открытие изменило первоначальные представления о переносе генетической информации. В последние годы стало также известно, что молекулы РНК могут играть роль катализаторов. Они могут сами себя разрезать и сшивать («редактировать») и потенциально способны к саморепликации.
Для каждой из известных биологических реакций существует специфический катализатор. Мы уверены, что катализатор (обычно белок, иногда РНК) должен существовать для любой гипотетической реакции. Все известные данные подтверждают это.
В основе механизма наследственности лежит простое правило спаривания оснований
Другой важный принцип, управляющий механизмом наследственности, это правило спаривания оснований (нуклеотидов), входящих в состав ДНК: всегда А соединяется с Т; a G — с С.
Во всех живых клетках генетическая информация зашифрована в последовательности оснований ДНК. Длинная линейная цепь ДНК представляет собой ряд нуклеотидов, различающихся по азотистым основаниям, входящим в их состав. Основания принято обозначать буквами A, G, С и Т (табл. 1.2). Порядок нуклеотидов в гене определяет последовательность аминокислот в белке. Поясним это.
Трехмерная структура ДНК была открыта в 1953 г. Джеймсом Уотсоном (Watson) и Фрэнсисом Криком (Crick). За это открытие, послужившее началом новой эпохи в биологии, в 1962г. ученые получили Нобелевскую премию по физиологии и медицине. Оказалось, что структура ДНК чрезвычайно проста и придает этой молекуле такие свойства, которые делают ее главным кандидатом на роль носителя наследственной информации. ДНК состоит из двух комплементарных цепей, закрученных друг относительно друга так, что образуется знаменитая «двойная спираль» (рис. 2.3). Каждая цепь представлена последовательностью повторяющихся нуклеотидов, включающих азотистые основания А (аденин), G (гуанин), С (цитозин) и Т (тимин).
Две цепочки ДНК идут антипараллельно по отношению друг к другу и спарены основаниями. Спаривание оснований определяет стабильность и высокую точность копирования генома. Двухцепочечная ДНК более стабильна и труднее разрушается, чем одноцепочечные ДНК или РНК. Правило спаривания оснований гласит: если в одной цепочке находится А то, в другой в том же положении будет находиться Т; если в одной цепочке находится G, то в другой будет С. Например, если порядок оснований в одной цепочке 5'—AGCTAT—3', то в другой, комплементарной, порядок будет 3'—TCGATA—5'. To есть, цепочки антипараллельны и комплементарны друг другу. Символы концов цепочек 5' и 3' (произносится «пять штрих» и «три штрих») объяснены в таблице 1.2.
Рис. 2.3. Два способа изображения двухцепочечной ДНК. Слева показана двойная спираль, имеющая две спаренные основаниями комплементарные цепи. Цепи в правозакрученной спирали антипараллельны, т.е. направление одной — от 5' к 3', другой — от 3' к 5'. Обратите внимание, что там, где в одной цепи находится основание аденин (А), в комплементарной цепи в той же позиции находится тимин (Т); там где в одной цепи находится основание гуанин (G), в комплементарной цепи в той же позиции присутствует цитозин (С). Основания являются частью нуклеотида, содержащего углевод рибозу. Нуклеотиды соединены друг с другом фосфодиэфирной связью, образующей остов каждой цепи Для удобства молекулу ДНК (всегда подразумевается, что она двухцепочечная, если не сказано иначе) изображают в упрощенной двумерной форме (справа). При репликации цепи раскручиваются, освобождая матричную последовательность свободных (неспаренных) оснований, по которой ДНК-полимераза строит комплементарную цепь (рис. 2.4, Б).
Именно в этом заключается чрезвычайно простой закон, определяющий структуру ДНК. Открытию правила спаривания оснований способствовали эмпирические данные Эрвина Чаргаффа (Chargaff), полученные в 1940-х годах. Анализируя химический состав ДНК, он показал, что во всех препаратах ДНК, выделенных из разных организмов, число молекул А всегда равно числу молекул Т; и точно также, число молекул С всегда равно числу молекул G. Эта закономерность была названа «правилом Чаргаффа». Чаргаффу, однако, не удалось связать полученные данные со структурой ДНК и механизмом наследственности. В полной мере оценить результаты Чаргаффа стало возможным лишь после открытия двойной спирали. В истории науки немало других примеров, когда важная информация не оказывает никакого влияния и «скрыто» лежит до тех пор, пока где-то вдохновенная созидательная интуиция не откроет ее истинную цену.
Правило спаривания оснований и антипараллельное расположение комплементарных цепочек объясняют, как создается дочерняя молекула с идентичной родительской последовательностью оснований (и, следовательно, содержащейся в ней информацией). Если цепочки разделить, можно предположить, что последовательность 3'—TCGATA—5' может служить матрицей для выстраивания в линию сначала А, затем G, затем С, затем Т и так далее до образования комплементарной последовательности 5'—AGCTAT—3' (рис. 2.3). Обьга-но копирование ДНК происходит с чрезвычайно большой скоростью и точностью. Однако в некоторых случаях имеют место ошибки, изменяющие последовательность оснований. Такие ошибки называются мутациями. Они создают наследственную изменчивость, на которую действует естественный отбор.
Итак, если линейную информационную макромолекулу ДНК сравнить с длинными полосами лент, которые использовали в первых компьютерах, то ДНК хромосом можно представить как последовательность миллионов букв (оснований). В этих последовательностях закодирован весь набор инструкций, представляющих генетический материал всех живых клеток на Земле. Проект «Геном человека» поставил целью определить порядок этих букв во всех 22 парах аутосом и в двух половых хромосомах человека. Этой работой занимается целый ряд специализированных лабораторий мира, владеющих методами клонирования и секвенирования генов. В общедоступных базах j данных и в персональных компьютерах молекулярных биологов хранятся сотни файлов, содержащих информацию о тысячах (может быть, миллионах) последовательностей ДНК. Достижения компьютерных технологий дают возможность биологам манипулировать последовательностями (например, искать определенную последовательность, разрезать ее или вставлять дополнительную информацию). Можно смело утверждать, что для появления ряда новых открытий молекулярной биологии р было необходимо развитие современных компьютерных технологий (табл. 2.1).
Генетическая информация передается от генов (нуклеиновых кислот) к белкам -центральная догма молекулярной биологии
До сих пор мы рассказывали о том, как организован геном человека, тот наследственный чертеж, по которому «строится» наш организм; упомянули мы и о том, что большинство химических реакций происходит с участием специфических белков — ферментов. Возникает вопрос, как информация, записанная в ДНК, превращается в тысячи различных белков, необходимых для функционирования и роста клеток? Как из одной клетки развиваются мириады разных клеток, из которых состоят ткани высокоорганизованных животных?
На эти ключевые вопросы ученые начали искать ответы только после открытия структуры ДНК. В начале 1960-х годов Фрэн-сис Крик, Сидней Бреннер (Brenner) и их коллеги совместно с Гобиндом Кораной (Khorana) и Маршаллом Ниренбергом (Nirenberg) выяснили, как информация, записанная в молекуле ДНК, может быть переведена с языка линейной последовательности оснований (GCTGGACTAATC) на язык соответствующей последовательности аминокислот (Ala, Gly, Leu, lieu). Эта грандиозная задача по дешифровке была решена к 1966 г., когда были окончательно установлены правила генетического кода. Определенный набор из трех оснований, расположенных в определенном порядке, соответствует определенной аминокислоте в белковой цепи. Так, в нашем примере GCT кодирует Ala (ала-нин), GGA кодирует Gly (глицин) и так далее (табл. 1.2 и приложение).
Экспериментально было показано, что существует информационная молекула — посредник между ДНК и белком. Этим посредником оказалась РНК, которая, в отличие от ДНК, состоит только из одной цепи. Однако ее химический состав оказался очень похожим на ДНК. И РНК, и ДНК построены из одинаковых основных строительных блоков. РНК содержит основания А (аденин), G (гуанин), С (цитозин) и U (урацил). Соотношение между двумя нуклеиновыми кислотами следующее. Если порядок оснований в ДНК 3'-TCGAATA-5', то порядок оснований в РНК (копия которой синтезируется по ДНК-матрице) будет 5'—AGCUUAU—3', где вместо Т (тимин) теперь стоит U (урацил). Мы уже упоминали это правило в гл. 1, табл. 1.2.
Рис. 2.4. Поток генетической информации - центральная догма молекулярной биологии.
А. Поток генетической информации направлен от нуклеиновых кислот (ДНК/РНК) к белкам и никогда в обратном направлении.Это означает, что последовательности оснований ДНК и РНК могут служить матрицами для синтеза других ДНК- или РНК-последовательностей, а аминокислотные последовательности в белках никогда не служат матрицей для синтеза РНК (или ДНК) последовательности оснований. Основные процессы копирования нуклеиновых кислот — это ДНК-> ДНК (репликация ДНК), ДНК->РНК (транскрипция), РНК->РНК (репликация РНК) и РНК->ДНК (обратная транскрипция). Аминокислотные последовательности, составляющие белки, определяются последовательностью оснований в. молекуле мРНК. Этот сложный процесс, называемый трансляцией, проходит в рибосомах на цитоплазме.
Б. Первый этап репликации ДНК заключается в локальном раскручивании двойной спирали, в результате которого матричные последовательности становятся доступными для копирования (этот участок называется вилкой репликации). Затем сложный набор белковых ферментов, включая ДНК-полимеразу, копирует каждую цепь, синтезируя комплементарную цепь (скорость копирования примерно 1000 оснований в секунду). Синтез всегда идет в направлении от 5'- к 3'-концу. Когда процесс достигает конца матричной молекулы, каждая из двух дочерних нитей состоит из одной новой цепи и одной родительской.
В. Отдельные участки ДНК-последовательности копируются или в мРНК, которая кодирует специфическую последовательность аминокислот (см. приложение), или в рибосомную РНК (рРНК), или в транспортную РНК (тРНК), которые являются частью молекулярного механизма, необходимого для трансляции мРНК в белок (см. приложение). РНК-по-лимераза копирует матричную цепь ДНК (чтобы это могло произойти, необходимо локальное раскручивание спирали ДНК). Синтез РНК также идет в направлении от 5'- к 3'-концу, так что матричная цепь ДНК имеет антипараллельную ориентацию от 3' к 5'. Последовательность оснований за кодирующим участком гена определяет терминацию (конец) синтеза РНК.
Самое важное — это то, что последовательность оснований ДНК определяет комплементарную последовательность РНК. Процесс синтеза на ДНК-последовательности соответствующей РНК-последовательности называется транскрипцией. На рис. 2.4 обратите внимание, что движение генетической информации происходит в направлениях ДНК -> РНК -> белок.
Также обратите внимание на то, что РНК-последовательность может служить матрицей для синтеза ДНК-последовательности (обратная транскрипция), а последовательность аминокислот в белке никогда не служит матрицей для обратного потока информации от белковой последовательности к РНК.
Все это еще не дает ответа на поставленные в начале вопросы. Как последовательность ДНК, переписанная в последовательность РНК (которая называется информационной РНК, или мРНК), переводится в белок? Большая часть данных, отвечающих на этот вопрос, получена М. Ниренбергом и Г. Кора-ной в начале 1960-х годов. По мере накопления информации становилось ясным, что процесс синтеза аминокислотной последовательности по триплетному коду мРНК чрезвычайно сложен. Этот процесс назвали трансляцией (от англ. translation — перевод). В общем виде он описан в приложении. Информационная РНК выходит из ядра в цитоплазму, где она транслируется в соответствующую последовательность аминокислот (белок). Она напоминает компьютерную ленту, подающуюся через устройство, которое считывает по три основания одновременно. Каждый триплет оснований определяет одну аминокислоту. «Читающее устройство» клетки называется рибосомой — это молекулярная органелла, состоящая из РНК и белков. Рибосома транслирует (переводит) мРНК в белковую последовательность — линейную цепочку аминокислот. Функциональным белком эта цепочка становится только после того, как примет определенную трехмерную устойчивую форму.
Рис. 2.5. ДНК, РНК и белки имеют трехмерную структуру. На уровне генетической (нуклеотидной) и белковой (аминокислотной) информации часто удобно рассматривать линейные последовательности (слева); на уровне функции в клетке все эти молекулы имеют сложную трехмерную структуру.
А. Двухцепочечная ДНК — это правозакрученная спираль. Однако существует и более сложная укладка, особенно в высших клетках, позволяющая компактно упаковывать хромосомы внутри ядра. В зависимости от стадии клеточного цикла, спирали образуют комплексы с разнообразными белками, многие из которых определяют, какие гены будут транскрибироваться в мРНК.
Б. Одноцепочечные молекулы РНК могут складываться в сложные структуры с локальными спариваниями оснований комплементарных последовательностей. Эта вторичная структура особенно важна для функционирования транспортных и рибосомных РНК.
В. Аминокислотные последовательности белка принимают сложную пространственную структуру.
Генетический код, насколько известно до сих пор, универсален для всех живьк организмов на Земле: от мельчайших вирусов и бактерий до растений и животных. В ходе эволюции жизни на Земле около 3—4 млрд. лет назад этот код был отобран как оптимальный механизм переноса информации, приводящий к образованию белка, и с тех пор ни разу не был ни изменен, ни заменен. В противоположность этому современные компьютерные программы постоянно обновляются и заменяются. Очень интересны рассуждения Лесли Оргела (Orgel) и Фрэн-сиса Крика о возникновении генетического кода, опубликованные примерно 25 лет назад. Они полагают, что сложный молекулярный аппарат, требующийся для транслирования РНК в белок, мог быть занесен на Землю живыми организмами (бактериями) откуда-то из Вселенной — или кометами, или космическим кораблем из сверхразумной цивилизации. Варианты этой идеи отстаивают и астрофизики Фред Хойли (Hoyle) и Чандра Викрамасинг (Wickramasihghe) в книгах Life Cloud (Облако жизни) и Our Place in the Cosmos (Наше место во Вселенной) (рис. 1.4).
Рис. 2.6. Наследование изменении в последовательности оснований ДНК. Репликация ДНК — это процесс копирования. Несмотря на высокую точность этого процесса иногда все-таки происходят замены, вставки или потери оснований. Такие ошибки, например замена одного основания, редкие события. Их частота составляет примерно 1 на миллиард реплицированных оснований (см. рис. 5.2). Традиционно последовательность оснований ДНК представляют цепью 5'-3' (она имеет ту же ориентацию, что и мРНК, которая никогда не служит матрицей для синтеза мРНК).
А. В верхнем примере восьмое основание G заменено на А в этом же положении. Если эта замена происходит в участке гена, кодирующем аминокислоты, это может привести к появлению в ходе трансляции другой аминокислоты в белке или к преждевременному окончанию (терминации) синтеза белка (т. е., эта замена может привести к появлению стоп-кодона ТАА, TAG или TGA).
Б. Замена одного основания — простейший тип мутации; более сложные мутации могут приводить к потере или вставке одного или нескольких оснований. Если вставки или потери происходят в нетрэчскри-бируемых или фланкирующих участках, это может не привести к серьезным генетическим последствиям. Однако если они происходят в участке, кодирующем аминокислоты, последствия обычно летальны, так как последовательность аминокислот в белке будет совершенно другой, покольку вставка или потеря оснований изменяют рамку считывания кодонов. Чаще всего, изменение рамки считывания кодонов (этот тип мутаций называется «сдвиг рамки») приводит к появлению стоп-кодона, а именно ТАА, TAG или TGA, которые преждевременно останавливают синтез белка.
Где бы ни возник генетический код, он стал основным кодом жизни на Земле. Он привел к развитию чрезвычайно сложных и разнообразных биологических форм, оставаясь неизменным для всех организмов.
Когда мы клонируем какой-нибудь ген (скажем, ген инсулина человека), мы реплицируем (размножаем) его в бактериальных клетках и, таким образом, производим большое количество инсулин-специфической ДНК. Это говорит о том, что аппарат репликации ДНК бактерий обрабатывает ДНК-последовательность человека так же, как и бактериальную. Если мы хотим получить большое количество белка инсулина для лечения диабета, мы «экспрессируем» клонированный ген человека в бактерии. То есть, мы заставляем бактерию производить человеческий инсулин. И бактерия создает тот же самый инсулин, с той же последовательностью аминокислот, что и клетка человека. Это означает, что генетический код прочитывается одинаково и в бактериальной, и в человеческой клетках, а разошлись они в ходе эволюции, возможно, 3,6 млрд. лет назад.
Итак, гены в хромосомах представлены двухцепочечной ДНК. По мере роста клетка производит копию каждой цепи ДНК, и образуются две двухцепочечные спирали. В каждую из двух новых дочерних клеток, образующихся в результате деления, попадает по одной новой молекуле ДНК. Для роста и выполнения своих функций в дифференцированных тканях многоклеточного организма клетки нуждаются в тысячах различных белков, которые объединяются в структуры, которые мы называем «мультимолекулярными машинами». Такие объединения белков (и РНК) координируют и проводят все химические реакции в клетке, которые необходимы ей для поддержания жизни, роста и развития. Генетическая информация, зашифрованная в линейной последовательности оснований ДНК, определяет (через РНК) весь набор белков, в которых нуждаются различные клетки. Информационные молекулы продуцируют практически бесконечное разнообразие белков — с разными последовательностями аминокислот, структурой и функциями, — которое дало начало удивительному разнообразию и великолепию форм жизни на Земле.
Хотя мы говорим о линейных последовательностях ДНК, РНК и белка, надо помнить, что все эти информационные и функциональные полимеры имеют трехмерную структуру. Так, двухцепочечная ДНК — это правозакрученная спираль (рис. 2.5, А). Одноцепочечная РНК способна формировать сложную структуру за счет спаривания соседних комплементарных последовательностей (рис. 2.5, Б). Цепочка аминокислот в белке также складывается в характерную трехмерную форму (рис 2.5, В). Следовательно, на уровне генетической информации нам достаточно думать в терминах линейных последовательностей, но на функциональном уровне жизнь протекает в трехмерном пространстве.
Таким образом, во многих отношениях клетки и многоклеточные организмы могут рассматриваться как самопрограмми-руюшиеся многоцелевые информационные системы, способные изменяться во времени. Допустим, что в ДНК-последовательности 5'—AGCTAT—3' третье основание С заменено на Т; тогда последовательность станет другой, и все ее потомки также будут другими. Иными словами, мутантная (измененная) последовательность передается по наследству всем дочерним молекулам (рис. 2.6). Поэтому на молекулярном уровне дарвиновский отбор можно представить как отбор наиболее приспособленных последовательностей. Самые убедительные доказательства естественного отбора были получены в молекулярно-генетических исследованиях.
Обратная транскрипция — создание ДНК-копии по матрице РНК
За десять лет после открытия структуры ДНК и расшифровки генетического кода сформулированная Джеймсом Уотсоном в 1952 г. гипотеза об однонаправленном переносе генетической информации (от нуклеиновых кислот к белку и никогда наоборот) превратилась в общепризнанную «центральную догму молекулярной биологии». Эта аксиома, как мы уже сказали, остается в силе для всех биологических систем.
Это правило переноса генетической информации составляет суть молекулярной биологии. Только один раз, в 1970 г., оно было модифицировано, когда признали существование обратной транскрипции. Впервые обратная транскрипция была обнаружена у опухолевых вирусов мышей и кур. Сейчас эти РНК-сод ержашие вирусы называют ретровирусами. Их инфекционный цикл хорошо изучен. Вирус проникает в клетку-мишень, и на основе своей РНК создает копию ДНК, которая встраивается в хромосому хозяина. При делении клетки встроенная копия ДНК вирусного генома удваивается и передается дочерним клеткам. Таким образом, наследственный материал вируса оказывается включенным в геном клетки. Вирусная РНК может образоваться позже путем копирования встроенной ДНК. Это приведет к образованию новых инфекционных вирусов.
Именно таким образом вирус иммунодефицита человека (ВИЧ) встраивается в ядерную ДНК и размножается вместе с клеточным геномом. Вот почему от этого вируса трудно избавиться, ведь каждая встроенная (интегрированная) ДНК-копия вируса может использоваться для образования множества копий РНК в результате нормального процесса транскрипции, а это в свою очередь приводит к появлению новых инфекционных ВИЧ-частиц. Еще один пример ретровирусов — это вирусы, вызывающие рак легких и лейкоз у человека и животных.
В конце 1997 г. в журнале «Nature» была опубликована работа группы Ролфа Цинкернагеля (Zinkemagel) из Цюриха, в которой показано, что в некоторых клетках животных, содержащих обратную транскриптазу ретровирусов, могут образовываться ДНК-копии других РНК-содержащих вирусов. Это захватывающее открытие означает, что обратная транскрипта-за, кодируемая ретровирусами, потенциально способна делать копии ДНК с других молекул РНК, присутствующих в клетке. Значит, возможно образование свободных ДНК-копий (их называют кДНК, или ретротранскрипты) собственных генов по матрице мРНК. Эта идея, допускающая теоретическую возможность передачи генетической информации от сомы к зародышевой плазме (о чем и говорил Тед Стил еще в 1979 г.), приблизила нашу теорию об эволюции иммунной системы позвоночных к реальности. В следующих главах мы детально опишем молекулярные данные, поддерживающие эту теорию.
Мир РНК — передача функции генетического чертежа от РНК к ДНК
Есть еще один вопрос, который биологи продолжают себе задавать, несмотря на то, что мы все больше и больше узнаем о молекулярно-генетических процессах. Что появилось раньше: ДНК, РНК или белок? Этому вопросу посвящено много исследований. Здесь мы остановимся на основных моментах.
В начале 1980-х годов Томас Кеч (Cech), Сидней Алтман (Altman) и их коллеги открыли ферментативные свойства молекул РНК, которые были названы «рибозимами»[6]. С этого времени появилось много концепций, касающихся «мира РНК». Предполагается, что первой живой молекулой был полимер РНК. Белков, какими мы их знаем теперь, и содержащих ДНК хромосом еще не существовало. В мире РНК микроскопические живые формы были самореплицирующимися молекулами РНК разной длины, от сотен до тысяч оснований. Репликация линейной цепочки РНК контролировалась самой молекулой (рибозимом), определенным образом сложенной. Итак, согласно этой гипотезе, первыми молекулами, способными к само-репликации и, следовательно, к дарвиновской эволюции, были не двойные спирали ДНК, как теперь, а РНК. Репликация же ДНК требует сложного набора специфических ферментов, составляющих «машину репликации ДНК».
Открытие ферментативных функций РНК и ее способности к саморепликации завершило 30—40-летний период попыток рационально объяснить первые шаги молекулярной эволюции жизни. Тот факт, что одноцепочечные молекулы РНК способны сами себя реплицировать и изменять, представлялся с функциональной точки зрения существенным. Сейчас известно, что все матричные процессы копирования, затрагивающие РНК (транскрипция, репликация и обратная транскрипция — рис. 2.4 А, В), склонны к ошибкам.
Это важно для нас, потому что все гены клеточных организмов представлены двухцепочечными молекулами ДНК, чрезвычайно точную репликацию которых осуществляет сложный аппарат (включающий от 30 до 40 разных белков). Высокая точность копирования достигается за счет того, что несколько белков, участвующих в репликации ДНК, занимаются исключительно редактированием и исправлением вновь образуемой копии ДНК. Например, если во время репликации вместо С встанет А, фермент- «редактор» заметит это, так как будет нарушен нормальный процесс спаривания оснований, и вставит на нужное место правильное основание. Если химическое повреждение основания происходит после того, как вновь синтезированная цепочка соединяется с родительской (матрицей), образуется «изгиб» двойной спирали, который запускает редакторские функции ферментного комплекса, вырезающего поврежденную последовательность и синтезирующего заново правильную копию (рис. 2.7). Это сродни процессу, который происходит при проверке полноты данных в ходе передачи электронного сообщения. Вот почему генные мутации, возникающие исключительно на уровне ДНК, — чрезвычайно редкие события. Мутации, которые мы видим, это те мутации, которым удалось пройти сквозь все нормальные редакторские и корректорские кордоны репликационной машины. Репликация ДНК — это процесс копирования очень высокой точности. В самом деле, на каждые миллиард реплицированных оснований остается нераспознанной только одна ошибка.
Таким образом, древний мир РНК представляется «эволюционирующим хаосом», в котором выживали наиболее приспособленные самореплицирующие молекулы. Манфред Эйген (Eigen) с коллегами провели поучительное исследование, которое показало, каким образом склонное к ошибкам копирование РНК и отбор могут давать квази-оптимальную популяцию молекул РНК. Эта популяция молекул РНК способна быстро эволюционировать при изменении окружающей среды.
Одноцепочечная РНК химически менее устойчива, нежели двухцепочечная ДНК. Очевидно, что в какой-то момент далекого эволюционного прошлого ранним формам жизни стало выгодно стабилизировать свой наследственный чертеж. Это послужило началом перехода от мира РНК к миру ДНК. Первый необходимый шаг на пути к миру ДНК — это передача информационной функции от РНК-последовательности к ДНК-последовательности, т. е. появление обратной транскрипции.
Рис. 2.7. Репарация ДНК. Ошибки в ДНК-последовательности оснований, которые передаются по наследству, вносят вклад в генетическую изменчивость популяций и, таким образом, в эволюцию путем естественного отбора. Ошибки, или мутации, редки, потому что аппарат репликации ДНК осуществляет несколько последовательных редакций и проверок молекулярной целостности двойной спирали. На рисунке схематично показан один из типов исправления ошибок, включающий удаление химически измененного или неправильного основания, которое не может спариваться с комплементарным основанием в другой цепи. Короткий участок вокруг неспаренного (или поврежденного) основания удаляется специальными разрезающими ферментами (эндонуклеазами). Образовавшийся пробел заполняется в результате репаративного синтеза ДНК в направлении от 5' к 3'. В качестве матрицы для этого синтеза служит другая цепь.
Наиболее вероятно, что древняя обратная транскриптаза была РНК-ферментом (рибозимом). Появление более сложных белковых обратных транскриптаз произошло позже.
Тем не менее для некоторых РНК-содержащих вирусов, таких как вирус гриппа и ретровирусы, высокий уровень ошибок, свойственный процессу образования РНК, в сочетании с некоторыми другими особенностями генома дает селективные преимущества. Высокий уровень мутирования (примерно одно ошибочное основание на каждую тысячу реплицированных оснований) делает их неуязвимыми перед иммунной системой инфицированного хозяина. Это привело к тому, что даже после появления в ходе эволюции белковых ферментов, РНК сохранилась в качестве вирусного генома. Совсем недавно, в конце 1980-х гг., Элизабет Блакберн (Blackburn) показала, что ферменты, которые строят ДНК-последовательности по РНК матрице на концах хромосом позвоночных (теломерах) путем обратной транскрипции, имеют явную эволюционную связь с вирусными ферментами, копирующими вирусные РНК. Это еще один пример эволюционной значимости РНК.
Почему мы придаем такое огромное значение этому шагу молекулярной эволюции? Потому что далее мы покажем насколько важна обратная транскрипция для всех современных ламарковских идей о существовании обратной связи генов, которая делает возможным наследование приобретенных соматических мутаций.
Глава 3 ИММУННАЯ СИСТЕМА
Организм человека постоянно подвергается нападению агрессивных патогенных вирусов и бактерий. Как иммунной системе удается отбивать эти атаки? Как она различает, где «свои» и где «чужие»? Каким образом наш организм быстро создает целые армии новых антител для борьбы с доселе неизвестными патогенами? Каковы механизмы иммунологической памяти, позволяющей клеткам иммунной системы эффективнее бороться с возбудителем при повторной встрече с ним. Если хоть на минуту задуматься над этими вопросами, можно понять, что научное и философское значение ответов на них выходит за узкие рамки иммунной системы. Именно поэтому иммунная система столь интересна для исследования, а за работы, раскрывающие механизмы иммунитета, присуждено так много Нобелевских премий.
В этой и двух следующих главах (гл. 4 и 5) мы расскажем о развитии иммунологии, об эволюции иммунной системы позвоночных и о современных молекулярно-генетических исследованиях в этой области. По мере того как мы находим ответы на поставленные вопросы, нашим глазам открываются все новые научные, практические и этические проблемы. В свете этих новых знаний, многое из того, что раньше нам казалось незыблемым, сейчас представляется спорным. В иммунологии сошлись все современные идеи генетики, теории развития и теории эволюции. Наша задача показать, что недавние научные открытия ставят под вопрос неодарвинистские концепции эволюции. В гл. 6 мы изложим свои представления о том, как сложные молекулярные процессы в иммунной системе могут приводить к переносу генетической информации из соматических клеток в половые. Эта концепция составляет главную тему нашей книги, а именно что признаки, приобретенные в течение жизни, могут передаваться потомкам.
Основные понятия иммунологии
• Антиген
Антигены - чужеродные белки и углеводы, которые стимулируют образование специфических антител, связывающихся с данным антигеном, но не с другими неродственными антигенами. Собственные антигены - белки или углеводы, которые являются составной частью данного организма. В норме иммунного ответа против собственных антигенов нет.
• Антигены гистосовместимости/киллерные Т-клетки
Антигены гистосовместимости называются также антигенами главного комплекса гис-тосовместимости, или ШС-антигенами. Эти антигены проявляются в большинстве клеток тела. Киллерные Т-клетки одного индивида могут распознавать МНС-антигены другого неидентичного индивида и реагировать на них, отторгая пересаженные ткани. МНС-антигены также действуют как антигенпрезентирующие структуры, например, представляя фрагменты вирусных белков (пептиды) киллерным Т-клеткам, активируя их и заставляя атаковать и лизировать зараженные клетки.
• Антитело
Белок, продуцируемый В-лимфоцитом (белая кровяная клетка) в ответ на чужеродный антиген (бактериальные клетки, вирусные частицы и их токсичные продукты). Типичное строение имеет иммуноглобулин G (IgG) - белковый гетеродимер (рис. 3.2). Существует множество разных антител, каждое из которых распознает определенный антиген.
• Вариабельная (V-) область/антигенсвязывающии центр
На концах как Н-, так и 1-цепей находится вариабельная (изменчивая) последовательность аминокислот (рис. 3.2). Эта область называется также антигенсвязываю-щим центром. V-области образуют антигенсвязывающий центр антитела (или Т-кле-точного рецептора).
• В-лимфоциты
Развивающиеся в костном мозге белые кровяные клетки, продуцирующие антитела. В-клетки связываются и отбираются антигеном, что приводит к активации выделения антител или пролиферации клеток.
• Гаптены
Небольшие химические соединения (бензольные кольца и их производные), созданные химиками, которые сами по себе не способны вызвать образование антител. Если гаптены присоединены к крупному «носителю» (чужеродному белку), их можно использовать для индукции анти-гаптеновых антител.
• Гены «домашнего хозяйства»
(от англ. housekeeping - домашнее хозяйство) Все жизненно необходимые гены, белковые или РНК продукты которых существенны для основных функций клетки (например, ферменты энергетических путей, ферменты репликации ДНК и т.д.)
• Иммуноглобулин
Название белка антитела, сокращенно Ig. Существует пять классов иммуноглобули-нов: 1дМ, IgD, IgG, IgA, IgE. Классификация основана на последовательности аминокислот С-областей Н-цепей; каждый класс Ig выполняет свою функцию.
• Клональная селекция/специфичность антител
На поверхности каждой отдельной зрелой В-клетки проявляются антитела одной специфичности, т.е. для синтеза каждой молекулы Ig используется один набор генов вариабельной области антитела. Чужеродный антиген, попадающий в организм, стимулирует только те В-клетки, с которыми он может связываться. Эти клетки активируются и начинают делиться (пролиферируют), образуя клон специфичных В-клеток, причем все потомки имеют идентичную специфичность (рис. 4.1).
• Константная (С) область/классы иммуноглобулинов
Аминокислотная последовательность молекулы антитела, которая не принимает участия в связывании антигена и, следовательно, не меняется от одной молекулы к дру-8 гой. Константные С-области тяжелых цепей определяют функцию антитела, например, способность запустить фагоцитоз. С-области тяжелых цепей подразделяются на пять основных типов последовательностей (и, следовательно, функций), называемых классами иммуноглобулинов (см. выше).
• Протестом
Единица «защиты» определена как минимальная критическая концентрация специфичного антитела в крови, необходимая для защиты против инфекции.
• Т-лимфоциты
Развивающиеся в тимусе белые кровяные клетки, на поверхности которых экспресси-руются сходные с антителами молекулы, называемые Т-клеточными рецепторами (ТкР). Существует два типа Т-клеток: киллерные Т-клетки и хвлперные Т-клетки.
• Фагоциты/фагоцитоз
Фагоциты - белые кровяные клетки, которые захватывают (фагоцитируют) и переваривают бактерии и клеточные обломки.
• Цитокины/интерфероны
Белки, выделяемые активированными хелперными Т-клетками, которые дают сигналы к активации и дифференцировке другом белым кровяным клеткам, включая другие Т- и В-клетки.
Начать это путешествие в знание мы должны с объяснения некоторых понятий. Нам необходимо рассмотреть наиболее важные клетки, молекулы и гены иммунной системы и дать определения основных терминов (табл. 3.1 и 5.1).
Краткая история прививок и вакцинаций
Научные основы вакцинации были заложены в XVIII—XIX столетиях. В Европе прививка в качестве защитной меры от оспы была впервые предложена леди Мэри Уортли Монтагью (Montagu). Эта женщина в 22-летнем возрасте перенесла жестокую оспу, оставившую следы на ее лице. В 1717 г. леди Монтагью вместе со своим мужем, британским послом в Константинополе, путешествовала по Турции. Ее внимание привлек местный обычай, называемый «прививкой». В письме на родину, датированном 1 апреля 1717 г., она писала: «Оспа, такая страшная и беспощадная у нас, здесь довольно безвредна. Местные старухи каждую осень ходят из дома в дом с ореховой скорлупой, полной оспенных корочек, и предлагают сделать «прививки». Через восемь дней решившиеся на эту процедуру как прежде здоровы» (и иммунизированы против оспы).
Леди Монтагью сразу поняла смысл этого обычая и рассказала о нем английским врачам. Доктор Чарльз Майтланд (Maitland) привил оспу ее сыну и дочери. Она добилась разрешения короля на прививку шести заключенных из Ньюгейтской тюрьмы. Эту прививку также провел доктор Майтланд. Испытания оказались успешными, после чего принцесса Уэльсская захотела привить своих дочерей. Заметим, что в Китае и Индии прививку оспы практиковали за несколько столетий до ее введения в Европе. Болячками больного оспой расцарапывали кожу здорового человека, который обычно после этого переносил инфекцию в слабой, не смертельной форме, выздоравливал и оставался устойчивым к последующим заражениям оспой.
Рис. 3.1. Антитела и киллерные Т-клетки. Сильно упрощенная схема защитной роли антител и киллерных Т-клеток (основные термины см. в табл. 3.1).
А. Вслед за стимуляцией антигеном В-клетки отбираются и активизируются для образования специфичных к данному антигену антител. Если антигеном являются бактериальные клетки (как показано на рисунке), антитела связываются с поверхностными антигенами бактерий, запуская реакции двух типов. С одной стороны, антитела могут привлекать другие белки плазмы (комплемент), которые действуют вместе с антителами, разрушая (лизируя) и, таким образом, убивая бактериальные клетки. С другой стороны, связанные антитела могут запускать поглощение и внутриклеточное переваривание бактериальных клеток особыми белыми кровяными клетками — фагоцитами (процесс переваривания называется фагоцитозом).
Б. Киллерные Т-клетки защищают от вирусных инфекций. Вирус заражает клетку и размножается. Синтезируются вирусные белки. В конце концов, происходит сборка новых вирусных частиц, которые заражают соседние клетки, вызывая, таким образом, острое заболевание. Зараженные клетки экспрессируют клеточные поверхностные антигены гистосовместимости, измененные в результате образования комплекса с фрагментами вирусного белка (пептидами). Именно этот измененный поверхностный антиген распознается Т-клетками с помощью поверхностных рецепторов (ТкР), что приводит к пролиферации и активации Т-клеток. Когда активированная Т-клетка связывается с клеткой-мишенью своими рецепторами, клетка-мишень разрушается и погибает. Так как измененный поверхностный антиген может экспресси-роваться до того, как завершится сборка зрелых вирусных частиц, Т-клетки способны разрушить эту «клеточную фабрику», т. е. предотвратить производство вирусного потомства и, таким образом, избежать дальнейшего заражения.
Большой вклад в разработку этой проблемы внес Эдуард Дженнер (Jenner). В 1798 г. он доказал, что оспу можно предупредить, если привить человеку коровью оспу, которую вызывает более слабый родственный вирус. Его исследования опирались на общее наблюдение, что доярки, переболевшие коровьей оспой, никогда не болеют во время эпидемий. Сам Дженнер помнил, что в детстве очень тяжело перенес прививку человеческой оспы, поэтому у него были личные причины улучшать метод. Прививка коровьей оспы оказалась более безопасной и легкой процедурой. С тех пор вакцинация против оспы и полиомиелита стали яркими примерами успеха профилактической медицины. В 1977 г. оспа была исключена из списка заболеваний, по которым Всемирная организация здравоохранения (ВОЗ) проводит обязательную вакцинацию.
Научные основы вакцинации были разработаны во второй половине девятнадцатого века отцом современной микробиологии и иммунологии Луи Пастером. В контролируемых испытаниях он установил эффективность использования «ослабленных», не представляющих угрозу, форм возбудителя для иммунизации против вирулентных штаммов. Ослабленные бактерии или вирусы несут те же антигены (или молекулярные признаки, распознаваемые иммунной системой), что и исходные болезнетворные штаммы, но они потеряли способность вызывать заболевание.
Рис. 3.2. Схема строения молекулы антитела. Антитела являются гетеродимерами, так как основная составляющая их единица состоит из разных белковых цепочек: тяжелой (Н) и легкой (L) цепей (см. табл. 3.1). Две Н + L-пары, образующие основную молекулу, удерживаются вместе химическими связями. Такое строение характерно для lgG-антител и связанных с клеточной поверхностью мономерных IgM (и IgD). Обратите внимание, что антигенсвязывающий центр образован взаимодействием вариабельных областей Н- и 1-цепей. Константная область Н-цепи определяет класс иммуноглобулина и защитную функцию антитела (см. табл.3.1). Внизу рисунка в рамке приведены сильно упрощенные изображения антител, которые используются в других рисунках (рис. 1.2, 3.1, 3.6, 3.7и 4.1).
И в настоящее время наиболее эффективные вакцины — ослабленные штаммы (например, против желтой лихорадки и полиомиелита). Сейчас для создания вакцин используются молекулярно-генетические методы. Этими методами в ослабленные вирусные или бактериальные штаммы вводят ДНК-последовательности, кодирующие нужные антигены, и получают чистые белковые антигены, используемые для вакцинации. Некоторые из таких вакцин нового поколения уже используются в клинике. Сейчас мы знаем, что вакцинация стимулирует образование активированных Т-лимфоцитов и защитных антител, которые помогают нашему организму ликвидировать вирусную или бактериальную инфекцию (рис. 3.1). В общих чертах структура антитела показана на рис. 3.2.
Переливание крови и начало современной иммунологии
К началу XX века стало ясно, что антитела против холеры (заболевания тонкого кишечника, сопровождающегося тяжелой диареей) высокоспецифичны, они связывают антигены холерного вибриона и неспособны связывать никакие другие антигены. За открытие специфической природы антител, роли антител и фа-гоцитирующих клеток в иммунном ответе Пауль Эрлих и Илья Мечников были удостоены Нобелевской премии. Специфичность антител всесторонне продемонстрирована в начале этого века Карлом Ландштейнером (Landsteiner). В 1930 году он был удостоен Нобелевской премии. Ему принадлежит и ряд других важных открытий. Но самые известные его работы касаются системы АВО эритроцитарных антигенов человека. Это открытие дало объяснение совместимости доноров и реципиентов при переливании крови:
Антигены эритроцитов Антитела, в плазме крови тех же людей A анти-В В анти-А АВ Нет 0 (нет ни А, ни В) анти-А и анти-ВЭритроциты (красные кровяные клетки) типа А, смешанные с плазмой крови, содержащей анти-А-антитела, слипаются (агглютинируют). Эритроциты типа А, подвергшиеся действию анти-В-плазмы, не агглютинируют. Таким образом, если человеку с группой крови А нечаянно перелита В-кровь, содержащая анти-А-антитела, в кровеносных сосудах может происходить агглютинация. Лучше всего человеку с группой крови А переливать кровь А, а человеку с группой крови В переливать кровь В. При отсутствии нужной донорской крови в случае острой необходимости людям с группами крови А или В можно переливать 0-эритроциты, отмытые от плазмы крови (в которой содержатся анти-А- и анти-В-антитела). У людей с группой крови 0 эритроциты не имеют на поверхности ни антигенов А, ни антигенов В, но в плазме таких людей присутствуют антитела двух типов (анти-А и анти-В). Вот почему переливать им кровь, несущую антигены А или В, нельзя. Это может вызвать гемолиз. Таким образом, 0 — универсальный донорский тип эритроцитов, а АВ, наоборот, — универсальный реципиент.
Открытие Ландштейнера помогло объяснить, почему переливания крови нередко заканчивались для пациентов трагически. В настоящее время вопрос о подборе донорской крови для переливания решить еще сложнее, требуется согласование по Rh-антигену, который имеет отношение к гемолитической болезни новорожденных. С тех первых иммунологических опытов многочисленные лабораторные исследования позволили выделить и полностью охарактеризовать многие белки, клетки и гены иммунной системы позвоночных. Мы уже не только знаем, как образуются антитела и рецепторы Т-клеток, но знаем и нук-леотидные последовательности генов, вовлеченных в этот процесс. Иммунология решает много важных проблем, и главная из них: сколько же существует специфических антител?
Насколько велик репертуар антител?
Этот ключевой вопрос был поставлен работами Ландштейнера. Его эксперименты в этой области менее известны неспециалистам, чем открытие системы АВО, хотя они и привели к далеко идущим выводам. Эксперименты Ландштейнера показали гигантский размах разнообразия антител, которые можно получить у лабораторных животных. Превосходный химик, он присоединял мелкие искусственно синтезированные молекулы сложных углеродных колец (например, производных бензола) к белковым антигенам разных типов и демонстрировал образование специфических антител к ним у лабораторных кроликов и мышей. Эти мелкие молекулы (гаптены) сами по себе обычно не вызывали образования антител. Однако будучи присоединенными к белковому носителю, они образовывали гаптен-бел-ковые комплексы, которые становились мощными антигенами, вызывающими образование антител, специфичных и к гаптеновой части, и — еще больше — к белковой.
Само по себе образование антител против таких антигенов не было сколько-нибудь удивительным, так как иммунологи давно получали антитела путем искусственной вакцинации крыс, мышей, кроликов, морских свинок, коз и лошадей. Поразительным было другое, Ландштейнер смог выявить антитела против всех новых химических соединений и лекарств, только что созданных зарождающейся в те годы фармацевтической промышленностью. Этих новых антигенов никогда раньше не было в природе! Этот результат поставил нас перед следующей научной — или даже философской — проблемой. Почему химические вещества, созданные в лабораториях современных фармацевтов, которых до этого никогда не было на Земле, могут вызывать иммунный ответ? Не могло быть никакого давления естественного отбора, направленного на образование антител против субстрата, которого никогда не существовало! Однако Ландштейнер смог показать, что лабораторные животные создают антитела, специфически связывающиеся с любой уникальной молекулярной структурой.
Истинную специфичность антител, полученных Ландштейнером, можно продемонстрировать простым лабораторным опытом. Например, было обнаружено, что антитела к гаптенуА не могут быть удалены из антисыворотки реакциями с гаптена-ми В, С, D, Е, G, Н... и т. д. Другими словами, антитела к гапте-ну А специфичны и не имеют сродства (или имеют очень слабое сродство) ко всему ряду рассматриваемых гаптенов. Однако в более чувствительных тестах — реакциях преципитации — можно наблюдать картину перекрестной реактивности (рис. 3.3). На рисунке знак минус (—) означает, что нет заметного осаждения; один или несколько знаков плюс (от + до +++) указывают на интенсивность осаждения и означают присутствие нерастворимого комплекса антиген—антитело; очень слабое осаждение обозначается (±). По-видимому, антигены D и G как-то связаны с А. И в самом деле, Ландштейнер смог показать, что D и G имеют с А общую молекулярную структуру.
Рис. 3.3. Основа специфичности антител. Иммунизация определенным антигеном (А) вызывает образование антител, которые связываются с А, но не с В, С и т. д. Простейший способ проверки антител состоит в смешивании сыворотки крови с антигенами. Антитела связывают антигены, и на дне пробирки образуется осадок (преципитат). Преципитат в пробирке свидетельствует о наличии антитела, которое может связываться с данным антигеном (- нет преципитата; + следы, +++ сильный преципитат). В данном примере антигены D и G имеют формы (эпитопы, или детерминанты), похожие на А; говорят, что они перекрестно реагируют с А. (также см. табл. 3.1 и рис. 3.6)
Эксперименты Ландштейнера послужили основой первой оценки размера потенциального репертуара антител. Тридцать лет назад был обычным такой комментарий генетических и эволюционных следствий, вытекающих из результатов Ландштейнера: «Тем не менее, трудно понять, какие преимущества дает существование генов для синтеза антител против многих недавно синтезированных органических соединений, таких как п-амино-бензоат, 2,4-динитробензол и т. д., которые совершенно не похожи на микробные патогены. Сохранение такого избытка генетического багажа в течение бесконечного времени до тех пор, пока не появится мишень для них, кажется неправдоподобным»
На самом деле это неправдоподобно в рамках дарвиновского естественного отбора генов, кодирующих определенные специфичные антитела.
Итак, к 1930-м годам стало ясно, что потенциальный репертуар антител должен быть гигантским и насчитывать миллионы или больше специфичностей. Ответ на другой фундаментальный вопрос все еще не был ясен: как могла в ходе эволюции появиться система, способная производить антитела, которые никогда не были частью эволюционной истории данного вида? Если инфекционные болезни были орудием эволюции современной иммунной системы, то, несомненно, частные и специфические молекулярные характеристики множества возможных антигенов никогда не были ее движущей силой. Правильнее, по-видимому, считать, что в ходе эволюции возникла биологическая стратегия, способная производить иммунный ответ на неожиданное.
Эволюция иммунной системы
Будем считать, что инфекционные болезни были главной, если не единственной, селективной силой в эволюции иммунной системы позвоночных. Тогда мы можем довольно легко рассматривать этот процесс в терминах дарвиновского «выживания наиболее приспособленной» иммунной системы. Если это так, то гены иммуноглобулинов (Ig), ответственные за кодирование антител, передаются потомкам через половые клетки, и их сохранение в ходе эволюции определяется теми же дарвиновскими правилами, которым подчинены и другие гены. Теперь мы критически рассмотрим сказанное.
Детальные сравнительные исследования разных видов беспозвоночных (насекомых) и позвоночных показывают, что система приобретенного иммунитета, которую мы сейчас обсуждаем, существует у хрящевых рыб (акул и скатов) и, следовательно, появилась по крайней мере 400—500 миллионов лет назад. У этих рыб есть гены, родственные генам вариабельной области Ig (IgV), или генам рецепторов Т-клеток (ТкР) [5]. В исследованиях Роберта Райсона (Raison) из Технологического университета Сиднея и других показано, что еще более примитивные позвоночные — круглоротые (миксины и миноги) — не имеют системы приобретенного иммунитета; у них нет ни IgV, ни ТкР-генов. До сих пор идет поиск недостающего звена. Однако пока не известны эволюционные переходы между кругло-ротыми и хрящевыми рыбами. И нет никаких гарантий, что недостающие звенья когда-нибудь будут найдены, так как все они, возможно, вымерли. На рис. 3.4 показаны основные представители позвоночных, у которых работа иммунной системы изучена подробно. Даже у холоднокровных позвоночных — рыб — можно обнаружить основные элементы системы приобретенного иммунитета теплокровных. Иммунные системы всех изученных позвоночных имеют следующие свойства:
• они способны создавать гигантское разнообразие антител и Т-клеток, обеспечивающее ответ на практически любой антиген;
• они способны к усиленному ответу при повторной встрече с антигеном (имеют память);
• они способны обеспечивать аутотолерантность.
Рис. 3.4. Позвоночные, у которых обнаружена сходная с млекопитающими система иммунитета.
Если мы иммунизированы коклюшной или столбнячной вакциной, наша иммунная система «помнит» первую встречу с этими антигенами, позволяя нам быстрее и сильнее реагировать на новую встречу с тем же самым антигеном образованием более высоких концентраций антител в крови. Эти свойства — направляемое антигеном изменение соматических клеток, специфичность, аутотолерантность и память — являются признаками иммунных систем всех позвоночных. У акул и других холоднокровных животных из-за низких температур окружающей среды иммунный ответ медленнее, чем у теплокровных наземных позвоночных.
Большая часть информации о клеточных и молекулярных процессах в иммунной системе получена экспериментальной иммунологией в опытах с иммунизацией мышей инбредных линий. Также много данных получено в клинических наблюдениях; сейчас мы знаем, что практически любая клетка, молекула и ген, обнаруженные у мышей, существуют и у человека. Хотя на других позвоночных проведено гораздо меньше исследований, очевидно, что при переходе от холоднокровных хрящевых рыб к теплокровным наземным животным сложность иммунной системы возрастала. Например, мы знаем, что генетическая стратегия, используемая для сохранения длинных последовательностей ДНК, кодирующих большое число различных антител у акул, менее экономична, чем у мышей и человека. У кроликов последовательности ДНК используются еще более эффективно. Однако самая эффективная система описана у кур и других птиц. Это станет понятным, когда мы обсудим уникальную природу генов, кодирующих антитела.
Структура антител
Теперь кратко рассмотрим структуру молекулы антитела. Все антитела имеют общий план строения — это белки, состоящие из нескольких субъединиц. На рис. 3.2 показано строение наиболее обычного антитела, называемого IgG. Эта структура была впервые описана в 1960-е годы в лаборатории Джералда Эдель-мана (Edelman) и Родни Портера ( Porter), которые были удостоены Нобелевской премии в 1972 г. Антигенсвязывающий центр состоит из вариабельных (V) областей тяжелой (Н) и легкой (L) белковых цепей, объединенных в HL-гетеродимер. Каждая молекула антитела состоит из двух идентичных HL ге-теродимеров, кроме пентамера IgM, у которого десять HL-гете-родимеров (рис. 3.2 и 3.5). Константная (постоянная) С-область молекулы запускает лизис (разрушение) или фагоцитоз (поглощение фагоцитом) чужих бактериальных клеток и частиц после связывания с ними антитела (рис. 3.1).
Рис. 3.5. Строение пентамерной молекулы IgМ антитела, состоящей из 10 HL-гетеродимеров (5 мономеров молекулы IgМ). Подробности в табл. 3.1. Каждый антигенсвязывающий центр имеет невысокую аффинность, но связывание во многих центрах увеличивает среднюю авидность антитела (см. рис. 3.7).
По правилам традиционной генетики для кодирования Н-цепи антитела нужен один ген, а для кодирования L-цепи — другой. Достаточно ли в нашем геноме ДНК для кодирования всех специфичных антител (скажем, миллиона)? Этот важный вопрос был поставлен в 1960-е годы Мелвином Коном (Cohn) и другими учеными сразу после расшифровки генетического кода. Этот вопрос и проблема механизма аутотолерантности заставили усилить внимание к стратегии, которой должна следовать иммунная система при создании того разнообразия связывающих антигены рецепторов, которое необходимо для борьбы с инфекционными заболеваниями. Стратегия ли это «зародышевой линии», при которой все специфичные антитела закодированы в яйцеклетках и сперматозоидах? Или же иммунная система использует особую «соматическую» стратегию, при которой гены в лимфоцитах мутируют или случайно рекомбинируют, образуя дополнительное разнообразие в репертуаре HL-центров?
В 1960-е и начале 1970-х годов среди ученых, придерживающихся этих двух принципиально различных мнений, происходили кратковременные, но частые теоретические сражения. Тем не менее к концу 1970-х годов благодаря молекулярно-ге-нетаческим работам Сусуми Тонегава (Tonegawa), получившего в 1987 г. Нобелевскую премию, эта проблема была в основном решена. Сейчас мы знаем, что часть разнообразия создается генами зародышевой линии, но случайные соматические процессы (рекомбинация и мутация) также необходимы для образования гигантского разнообразия антител и рецепторов Т-клеток. То есть, в течение жизни наш организм «учится» бороться с многочисленными захватчиками и создает в лимфоцитах много новых ДНК-последовательностей, кодирующих антитела. Далее мы обсудим данные, указывающие на то, что ДНК-последовательности из лимфоцитов могут быть включены в половые клетки и переданы следующим поколениям.
Теперь мы конкретизируем основные элементы проблемы создания репертуара антител и молекулярные детали иммунного ответа. Тяжелая цепь каждого антитела представляет собой белок, состоящий примерно из 400 аминокислот (100 в V-обла-сти и 300 в С-области), а каждая легкая цепь состоит примерно из 200 аминокислот (100 в V-области и 100 в С-области). Так как каждая аминокислота определяется кодоном из трех оснований (приложение), в последовательности ДНК, необходимой для кодирования каждого HL-гетеродимера, должно быть по крайней мере 1800 (600 • 3) оснований при условии, что и Н-, и L-це-пи кодируются традиционными генами. Если существует 1 млн. разнообразных антител (по современным представлениям эта оценка разумна), это означает, что в геноме человека почти 2 млрд. (1800 • 1 000 000 или 1,8 • 109) оснований кодируют только возможный репертуар антител. Даже если ограничиться только существенной информацией, то есть V-областями, а именно они составляют антигенсвязывающий центр, то это число уменьшится до 0,6 • 109 оснований. А весь геном человека содержит максимум 3—4 млрд. оснований! Таким образом, по самым минимальным оценкам, от 1/6 до 1/2 всей ДНК должны кодировать молекулы антител!
Когда 30 лет назад впервые оценили это число, исследователи поняли, что Ig-гены, кодирующие антитела, должны иметь особую стратегию хранения информации, отличную от других генов. Эти другие гены мы будем называть «однокопийными», или просто генами «домашнего хозяйства». Кроме того, в других работах, проведенных в 1970-е годы, было показано, что в промежутках между генами расположены некодирующие последовательности ДНК, (их часто называют «избыточной» ДНК). Было показано, что на «избыточную» ДНК приходится примерно 98 процентов или даже больше от всей ДНК генома позвоночных. («Избыточная» ДНК не кодирует белковые последовательности, но, по-видимому, играет какую-либо важную функциональную роль. Она может участвовать в упаковке хромосом или в регуляции активности генов и репликации ДНК.) Эти вычисления означали, что если антитела кодируются традиционными генами, то в зародышевой линии хватит кодирующей ДНК только для 10 000 антител, а не для 1 млн., как был оценен репертуар антител. А что же остается для всех генов «домашнего хозяйства?»
Итак, уже к концу 1960-х годов стало очевидно, что все разнообразие антител не может быть закодировано только в половых клетках. Жизнь нуждается в гораздо большем, чем только в производстве антител! Одним из возможных решений явилось предположение, что разнообразие Ig-генов, ответственных за кодирование антител, каким-то образом генерируется соматическими событиями. Работа Сусуми Тонегава, продемонстрировавшая уникальные перестройки ДНК, кодирующей V-области антител, и работы многих других исследователей, показавшие соматическое мутирование V-генов, наконец, разрешили эту проблему. Обсуждение этого вопроса мы продолжим в разделе, посвященном структуре Ig-генов.
Что происходит при заражении?
Иммунная система развивалась для борьбы с острыми инфекционными заболеваниями. Возбудитель, попадая в организм, начинает размножаться, но то же самое делают и его враги — Т- и В-лимфоциты. Исход болезни зависит от того, у кого скорость размножения выше. Теперь мы кратко рассмотрим, каковы роли некоторых действующих лиц в этом состязании.
Антитела относятся к классу растворимых белков, называемых иммуноглобулинами (сокращенно Ig). Их продуцируют и выделяют в кровь и тканевую жидкость белые кровяные клетки, которые называются В-лимфоцитами. В элиминации чужеродного агента участвуют и некоторые дополнительные факторы, которые вызывают лизис (разрушение) бактериальных клеток, покрытых антителами. Антитела могут нейтрализовать вирусные частицы, прочно связываясь с ними и тем самым препятствуя их проникновению в клетки-мишени. Кроме того, специальные клетки, называемые фагоцитами, могут заглатывать покрытые антителами частицы и разрушать их. Этот процесс изображен на рис. 3.1. Выгодно, если антитело связывается с антигеном при очень низких концентрациях того и другого, то есть на ранних стадиях инфекции, когда в организме присутствует только очень небольшое число болезнетворных агентов. Однако это возможно лишь в том случае, если защитные антитела прочно связываются с антигеном, или обладают высокой авидностью. Если авидность антитела низкая, связывания при низких концентрациях антигена или антитела может и не произойти.
Если заболевание вызвано вирусом, иммунная система реагирует также образованием «клеток-убийц» (цитотоксических Т-лимфоцитов). Каждый Т-лимфоцит несет на поверхности специфические рецепторы, сходные с антителами. Эти рецепторы называются рецепторами Т-клеток — ТкР. Они распознают и связывают измененные молекулы на поверхностной мембране инфицированных вирусом клеток, что приводит к лизису этих клеток. Цитотоксические Т-клетки не вредят нормальным незараженным клеткам, так как не могут связывать их своими ТкР.
К сожалению, не у всех из нас иммунная система работает надежно и эффективно. Кто-то страдает от астмы или аллергии из-за того, что в отношении какого-либо внешнего раздражителя иммунная система заходит слишком далеко. Другие живут с рассеяным склерозом, потому что иммунная система разрушает их собственные нервные волокна, или страдают от иммунного дефицита, который затрудняет борьбу с инфекциями.
К концу 1960-х годов исследования естественных иммуноде-фицитов человека показали, что существует две основные категории острых нарушений иммунитета. Дети, не способные производить антитела (агаммоглобулинемия), не могут бороться с обычными бактериальными инфекциями, но нормально переносят детские вирусные инфекции, например корь. И наоборот, дети, у которых не было нормального тимуса (атимиче-ские), производят антитела и удовлетворительно справляются с бактериальными инфекциями, но не способны излечиваться от вирусных инфекций. В конце 1960-х гг. Боб Бландэн, работавший в Центре медицинских исследований имени Джона Кертина в Канберре, экспериментально показал, что излечение от острых вирусных инфекций у мышей зависит от ответа Т-лимфоцитов на инфекцию. К началу 1970-х гг. Боб совместно с другими исследователями из его лаборатории обнаружил, что Т-лимфоциты убивают инфицированные вирусом клетки до завершения цикла репликации вируса, пресекая, таким образом, инфекцию в зародыше. Другие исследователи показали, что Т-лимфоциты выделяют растворимые факторы (интерфероны), которые предотвращают размножение вируса в окружающих клетках. Интерфероны и другие растворимые цитокины сейчас производят с помощью клонирования и экспрессии генов цитокинов в бактериальном хозяине. Чистые цитокины назначают пациентам, страдающим некоторыми формами иммунного дефицита, для увеличения активности костного мозга и Т-клеток и, следовательно, улучшения ответа на инфекцию.
В 1973 г. Питер Догерти и Ролф Цинкернагель, также работавшие в Центре медицинских исследований имени Джона Кертина, показали, что в процессе распознавания Т-лимфоцитами инфицированных вирусами клеток участвуют не только вирусные антигены (что ожидалось), но и основные антигены гистосовместимости, или тканевой совместимости, самой клетки (что было неожиданным). Антигены гистосовместимости — это молекулы, ответственные за отторжение чужих тканей. Они различны у разных людей и вызывают сильный ответ Т-лимфо-цитов. Однако пересадка чужих тканей — не естественное явление, так что истинная биологическая функция этих антигенов была неизвестна до открытия Догерти и Цинкернагеля. Это открытие произвело коренные перемены в клеточной иммунологии, а Догерти и Цинкернагель получили Нобелевскую премию по физиологии и медицине в 1996 г.
Антигенспецифичные рецепторы Т-клеток (ТкР) распознают вирусные антигены, ассоциированные с главными антигенами гистосовместимости. Антител, связывающихся с такой ассоциацией, не образуется. Таким образом, Т-клетки и антитела никогда в норме не конкурируют за одни и те же сайты на поверхности клетки. Это можно продемонстрировать простым экспериментом. Если искусственно создать антитела к сайтам, узнаваемым Т-клетками, и добавить их к смеси инфицированных клеток и Т-клеток, то лизиса клеток не происходит, и вирусная инфекция успешно развивается. Этот эксперимент иллюстрирует селективные преимущества иммунной системы позвоночных, в которой Т-клетки и антитела не конкурируют за связывание с одними и теми же сайтами на поверхности инфицированной клетки.
Изучение описанных выше естественных иммунодефицитов у человека показало, что в отсутствие тимуса (и Т-лимфоцитов, которые развиваются в тимусе) могут образовываться антитела против бактериальных инфекций. Эти антитела относятся к классу иммуноглобулинов IgM. Секретируемая форма IgM, появляющаяся в ответ на бактериальную инфекцию без участия Т-лимфоцитов, представляет собой пентамер, то есть состоит из пяти молекул, структура которьк показана на рис. 3.2. Каждая из этих молекул имеет два антигенсвязывающих центра. Таким образом, пентамерный IgM имеет десять антигенсвязывающих центров (рис. 3.5).
Важная аксиома биологии гласит, что эффективность биохимической реакции зависит от степени связывания или сли-пания разных молекул. Взаимодействие между отдельным центром связывания антитела с комплементарным ему антигеном можно оценить количественно. Для этого в пробирке смешивают антиген и антитело в разных концентрациях и определяют, какая часть смеси находится в связанной форме (комплекс антиген—антитело), а какая — в несвязанной (рис. 3.6). Этот метод дает возможность оценить аффинность (сродство) антигенсвязывающего центра. Когда связывается больше одного центра, как у IgG или мономера IgM, имеющих по два центра, или у пентамера IgM с десятью центрами, в действие вступает новый фактор. Если чужеродный агент имеет на поверхности множество идентичных структур (как у бактериальных или вирусных частиц), то, как только происходит одно взаимодействие антиген—антитело, вероятность второго возрастает, и так далее (рис. 3.7). Таким образом, пентамер IgM может прилипать к поверхности бактерии, даже если аффинность отдельного антигенсвязывающего центра низка (из-за относительно плохого соответствия антигену). Сила такого множественного связывания антигена с антителом называется авидностью. Итак, высокая авидность IgM обеспечивает организму селективные преимущества, так как он образуется в первые часы и дни инфекции и способен связывать бактерии в крови и вызывать их элиминацию.
Рис. 3.6. Схема образования комплексов антиген-антитело. Комплексы антигенов и антител часто нерастворимы и осаждаются из раствора (рис. 3.3). Такие комплексы связываются с поверхностной мембраной клеток, например, фагоцитов, константной областью Н-це-пи антитела, давая клетке возможность поглотить их и переварить (рис. 3.1). В центрах размножения особые клетки, которые называются фолликулярными дендритными клетками (ФДК), представляют такие комплексы для отбора мутантных вариабельных областей с высокой аффинностью (рис. 5.4). Детали описаны в табл. 3.1.
Пентамерный IgM — крупная молекула, которая не может проникать через стенки кровеносных сосудов. Необходимы антитела помельче; это — иммунноглобулины класса IgG. Обычно IgM-ответ длится несколько дней, а затем происходит переключение на образование более мелких антител класса IgG , которые имеют только два антигенсвязывающих центра вместо десяти (рис. 3.8). Это переключение достигается в результате ряда сложных молекулярных событий, которые затрагивают определенные ДНК-последовательности генов IgG (молекулярные детали этого процесса мы не рассматриваем).
Рис. 3.7. Связывание пентамерного IgM с рядом одинаковых антигенов. Пентамерный IgM имеет много одинаковых антигенсвязывающих центров, у каждого из которых может быть низкая аффинность (рис. 3.5). Однако в результате множественного связывания с поверхностью антигена, например, с бактериальной клеткой (которая представляет собой ряд одинаковых антигенных эпитопов) пентамерный IgM связывается очень прочно (имеет высокую авидность). На рисунке показано множественное связывание высокой авидности. Если один центр связывается с антигеном, вероятность связывания соседнего центра возрастает. Когда сцеплены множественные антигенсвязывающие центры, общая сила связывания (авидность) оказывается много выше, чем у одного связывающего центра.
Переключение с синтеза IgM на синтез IgG иллюстрирует одну аксиому иммунологии, которая признается еще не всеми иммунологами. Эта аксиома утверждает, что единственное эволюционное селективное преимущество, которое дает специфичность в системе приобретенного иммунитета (антитела и ТкР), это возможность различения своего от не-своего. Так, IgM полезны, потому что, несмотря на низкую специфичность и низкую аффинность (плохое соответствие) отдельного связывающего центра, десять связывающих центров пентамерного IgM дают возможность одному и тому же антителу связывать множество родственных антигенов различных инфекционных агентов. Однако нужда в мелких, проникающих через стенки сосудов, антителах привела к появлению механизма переключения с производства IgM на производство IgG. Два антигенс-вязывающих центра IgG должны иметь большую аффинность, чем десять центров пентамерного IgM. В процесс переключения вовлекаются В-клетки с самой высокой аффинностью. Отбор таких клеток основан на конкуренции за связывание антигена в особых участках лимфоидной ткани (гл. 5). Еще одно селективное преимущество, которое дает механизм переключения, связано с эволюцией других классов антител (IgA, IgE), выполняющих свои специфические функции в различных тканях организма.
Рис. 3.8. Первичный и вторичный гуморальный ответ. Типичная зависимость от времени гуморального ответа у лабораторных мышей. На практике у человека вторичное введение антигена отделено от первичного месяцами или даже годами. Аффинность антител первичного ответа обычно ниже, чем антител вторичного ответа, «ответа памяти». Антитела, образованные во вторичном ответе, обычно оказываются соматически мутировавшими молекулами IgG или IgM , которые имеют более высокую аффинность, чем IgG- или lgM-антитела, образованные ранее (см. табл. 3.1 и гл. 5).
Наша иммунная система распознает большое число различных антигенов и реагирует на них. Чаще всего антигены — это белки и углеводы. (Углеводы — это полимеры, состоящие из разного числа молекул глюкозы или других Сахаров.) Следовательно, мир потенциальных биологических антигенов огромен. Иммунная система характеризуется способностью синтезировать почти безграничное число специфичных антител против чужеродных белков и углеводов. Каждое антитело способно отличить чужеродный антиген от собственных антигенов и участвует в элиминации чужеродных антигенов из организма.
В отличие от этого практически безграничного репертуара антител Т-лимфоциты узнают только короткий фрагмент (пептид) чужого белка, связанный специальной полостью в молекуле МНС антигена на поверхности клетки. Репертуар рецепторов Т-лимфоцитов (ТкР) ограничен вариациями МНС антигенов, которые создаются при связывании их с коротким чужеродным пептидом. Сложный многоэтапный процесс отбора развивающихся в тимусе Т-лимфоцитов обеспечивает создание этого ограниченного репертуара рецепторов в популяции функционирующих Т-клеток. Другой ряд сложных процессов, вовлеченных в образование антител в В-лимфо-цитах, приводит к тому, что не образуется антител против измененных МНС антигенов. Таким образом, антитела и рецепторы узнают разные стороны мира чужих антигенов.
Как достигается эта удивительная способность распознавать целый мир различных чужеродных антигенов и в то же время избегать ответа против собственных антигенов? Ответ на этот вопрос удалось получить в результате 40 лет иммунологических исследований. Мы рассмотрим его в следующей главе при обсуждении «клональной селекции».
Необходимость аутотолерантности
Теперь оставим в стороне проблемы, связанные с разнообразием молекул иммунной системы, и рассмотрим другое фундаментальное свойство системы — невосприимчивость (толерантность) к собственным антигенам.
Реакция на чужеродные антигены («не-свое») — это только одна сторона медали, другая состоит в том, что у здоровых индивидов иммунная система почти никогда не производит антител и киллерных Т-клеток против тканей и клеток собственного организма. В норме может наблюдаться только очень кратковременная реакция против самого себя. И это несмотря на то, что химический состав белков и углеводов собственного организма очень похож на молекулярные структуры чужеродных антигенов. Эта неспособность организма реагировать на самого себя названа аутотолерантностью. Она была обнаружена в начале двадцатого века немецким микробиологом Паулем Эрлихом, который в общих чертах описал ее значение и проанализировал глубокие последствия, наступающие при нарушении аутотолерантности. Он назвал механизм, заставляющий иммунную систему организма отличать свое от не-своего, «страхом самоотравления» (horror autotoxicus). Сейчас мы знаем, что имел в виду Пауль Эрлих, когда говорил о выходе иммунной системы из-под контроля и нарушении аутотолерантности. Обнаружены подтачивающие здоровье аутоиммунные заболевания, когда организм стремится отторгнуть самого себя. К этим заболеваниям относятся, например, ревматоидный артрит (вызванный иммунной реакцией против соединительной ткани) и рассеяный склероз (вызванный иммунной атакой против нервной ткани). Если речь идет о реакции против «не-своего», мы знаем, что иммунная система важна для выживания. Если она работает неэффективно (при синдромах врожденных и приобретенных иммунных дефицитов), человек и другие позвоночные погибают от таких инфекционных агентов, которые в норме уничтожаются иммунной реакцией.
Так как же достигается аутотолерантность? Как она поддерживается, однажды появившись? Определяется ли она нашими генами и, таким образом, предопределена антигенами и антителами, унаследованными от родителей? Или она приобретается в течение жизни каждого индивида? С научной и философской точек зрения это не тривиальные вопросы. Только сейчас исследования на молекулярном и клеточном уровнях начинают давать ответы на них. Эти вопросы важны для поиска способов, которыми мы можем заставить иммунную систему нарушить нормальные правила поведения и начать бороться с раком (со «своим») или стать толерантной к пересадкам чужих органов и тканей (к «не-своему»).
Реакция на неожиданное
Способностью реагировать на неожиданное и памятью обладает еще только одна система — центральная нервная система. Основное отличительное свойство иммунной системы состоит в том, что ее клетки (лимфоциты, фагоциты и другие белые кровяные клетки) могут быть как подвижными, циркулирующими по всему организму (рис. 3.9), так и включаться в неподвижные (фиксированные) ткани печени, селезенки, лимфатических узлов, кожи и кишечного тракта. В центральной нервной системе, наоборот, все нейроны и нервные волокна образуются очень рано и занимают фиксированное положение на протяжении всей взрослой жизни. Подобно тому, как нервная система следит за состоянием тканей организма и подачей сигналов мышцам всего тела, так и иммунная система с помощью системы подвижных клеток, которые мигрируют через лимфатические и кровеносные сосуды, следит за антигенной целостностью организма (рис. 3.9). Во времени и пространстве осуществляется мощный поток клеток и молекул (антител и других белков).
У взрослых все белые кровяные клетки образуются в костном мозге. Ежедневно появляются миллионы таких клеток. Они необходимы, чтобы постоянно заменять клетки, погибшие в разных тканях. Лимфоциты, образовавшиеся в костном мозге, дифференцируются затем в В-клетки, производящие антитела, и в Т-клетки. Предшественники Т-клеток покидают костный мозг и попадают в тимус, где они проходят дальнейшее развитие (дифференцировку), и на их поверхностной мембране появляются рецепторы ТкР. После этого зрелые Т-клетки покидают тимус.
Рис. 3.9. Лимфоидная система человека. Лимфоидная система состоит из обширной сети лимфатических сосудов и лимфоидных органов (лимфатические узлы, селезенка, тимус). Лимфатические сосуды пронизывают большинство тканей и органов, соединяют лимфатические узлы и, наконец, впадают через грудной проток в кровь. Все В- и Т-лимфоциты (и другие белые кровяные клетки, и красные кровяные клетки) развиваются в костном мозге (стволовые клетки в костном мозге непрерывно делятся, образуя миллионы клеток в день). Те клетки, которые станут Т-лимфоцитами, мигрируют с кровью в тимус (вилочковую железу), где они созревают и экспортируются как зрелые Т-лимфоциты, способные к хелперным и киллерным функциям. В-лимфоциты, которые продуцируют антитела, сначала развиваются в костном мозге, затем мигрируют через кровь и лимфатический проток в лимфоидную систему и заселяют периферические лимфатические узлы, например, аденоиды, миндалины и селезенку. Лимфатические узлы в тонком кишечнике называются пейеровыми бляшками. Подвижные Т- и В-лимфоциты по кровеносным и лимфатическим сосудам могут мигрировать во все части тела, включая репродуктивные органы. Каждый лимфатический узел пронизан очень тонкими капиллярами, по которым идет движение молекул и клеток из крови в лимфу. ( По N.K. Jerne. Scientific American, vol.229: 52, 1973. Copyright ©Scientific American Inc. Мы признательны художнику Бунджи Тагава за разрешение перепечатать этот рисунок.)
Зрелые В- и Т-клетки (вместе с фагоцитами) заселяют периферические органы иммунной системы (селезенку и лимфатические узлы) и циркулируют по организму с кровью и лимфой. Лимфатические узлы расположены по всему телу, и те, которые находятся рядом с местом внедрения инфекционного агента, обычно реагируют первыми (рис. 3.9). Таким образом, иммунная система может быстро обнаружить попадание бактериальных или вирусных частиц в организм. Узлы увеличиваются (даже становятся болезненными), так как в них происходит быстрое деление и иммиграция из кровотока активированных антигеном лимфоцитов и других белых клеток. Каждый из нас знает по собственному опыту, что такое припухшие, болезненные лимфатические узлы (обычно в горле, паху, подмышке) после введения вакцины или во время болезни.
В 1930-х и 1940-х годах небольшая группа иммунологов и химиков (под руководством Фрэнка Макфарлейна Бернета, Лай-нуса Полинга (Pauling), Карла Ландштейнера, Фридриха Брени (Breini) и Феликса Горовица (Haurowitz) занялась выяснением механизма образования антител, обеспечивающего системе возможность реагировать на неожиданное. Это было задолго до того, как стали известны химический состав и структура генетического материала (ДНК) и законы, управляющие потоком генетической информации (т. е. ДНК<-^РНК->белок). В те годы общераспространенной была так называемая «инструктивная» модель Брени, Горовица и Полинга. Согласно этой модели, антиген как матрица просто воздействует на специфичное складывание гибкого Ig-белка в определенную форму и вызывает образование большого числа копий специфичного антитела, необходимого для борьбы с инфекцией (рис. 3.10).
Рис 3.10. Инструктивная модель образования антител Лайнуса Поллинга. Четыре стадии формирования молекулы нормального иммуноглобулина сыворотки крови и шесть стадий формирования антитела в результате взаимодействия белковой цепи иммуноглобулина с молекулой антигена. Внизу справа изображена молекула антигена, окруженная присоединенными к ней молекулами антител или их частями, что прекращает дальнейшее образование антител. (По рис. 1 из книги Linus Pauling. A Theory of the Structure and Process of Formation of Antibodies. Перепечатано с разрешения Химического общества Америки.)
Сейчас известно, что эта модель неверна. Белки антител не складываются под действием антигена в специфичную форму. Теперь мы знаем, что последовательность аминокислот диктует способ складывания белка, и осуществляется этот процесс с помощью недавно открытых белков — шаперонов. В свою очередь, последовательность аминокислот определяется линейной последовательностью оснований в ДНК и триплетным кодом при участии информационной РНК (см. гл. 2 и рис. 2.4). Инструктивной теорией нельзя объяснить и такие свойства иммунной системы, как экспоненциальный рост концентрации антител в ходе иммунного ответа и аутотолерантность. В конце концов, эти противоречия привели к кончине «инструкционизма» и появлению на свет альтернативных «селекционных» теорий, вершина которых — клонально-селекционная теория Бернета, впервые опубликованная в 1957 г.
Глава 4 КЛОНАЛЬНО-СЕЛЕКЦИОННАЯ ТЕОРИЯ
Первую «селекционную» теорию образования антител предложил в 1900 г. Пауль Эрлих (Ehrlich). Согласно его теории, существуют клетки (по-видимому, В-лимфоциты), на поверхностной мембране которых расположено много разных молекул антител. Эти клетки способны синтезировать любое из них. После того как происходит связывание чужеродного антигена с каким-то одним антителом, клетка начинает производить антитела только этой специфичности. Поскольку этот «селективный» процесс происходит одновременно в большом числе клеток, образуется много антител, специфичных к данному антигену. Сейчас известно, что идея Эрлиха не верна. Современные селекционные теории, основанные на представлениях о том, что одна клетка может продуцировать только антитела одного типа (а не многих), начали появляться только в 1950-х гг.
Первой среди них была теория, предложенная Нильсом Ерне (Jerne) в 1955 г. Несмотря на ошибочные представления об антителах как основных единицах отбора, его вклад в проблему был плодотворен. Его теория переместила интересы иммунологов с инструктивных теорий, по которым антитела принимают любую форму в зависимости от формы антигена, на селекционные. В 1957 г. Макфарлейн Бернет предположил, что основной единицей отбора антигеном является клетка, и что одна клетка отвечает за образование антител только одного типа. Именно Бернет придумал термин «клональная селекция» [I]. В основе этой теории лежит представление о том, что «одна клетка производит только одно антитело» (точнее, антитела одной специфичности). Существует много разных клеток (лимфоцитов), образующих и несущих на поверхности разные антитела. Клетка «отбирается» антигеном, форма которого соответствует антителам, производимым данной клеткой. Именно она начинает размножаться и дает клон идентичных клеток, причем все клетки клона продуцируют антитела одной специфичности. Согласно этой теории, должен существовать механизм, который обеспечивает проявление на поверхности клетки антител только одной специфичности и исключает все другие антитела. Теперь мы знаем, что «решение», какое антитело будет синтезироваться в В-клетке, принимается на ранних стадиях развития лимфоцита. Бернет не только нашел экспериментальные свидетельства в пользу этой теории, но и сформулировал ее следствия для проблемы различения «своего» и «не-своего».
В краткой форме мысль об отборе клеток была высказана Дэвидом Талмейджем (Talmage) в 1957 г., но Бернету мы обязаны всесторонней разработкой этой теории. Далее клонально-селекционная теория развивалась усилиями таких исследователей, как Мелвил Кон и Элистэр Каннингем (Cunningham). До сих пор основные представления этой теории объясняют, как иммунная система приспосабливается к разнообразным и постоянно меняющимся антигенам внешней среды. Основные положения клонально-селекционной теории подтверждены экспериментально (рис. 4.1).
Рис. 4.1. Клональная селекция. Эта идея иллюстрируется также на рис. 1.2 и в табл. 3.1.
Привлекательность этой теории состояла в том, что она давала разумные объяснения механизма аутотолерантности. Если рецептор на поверхности развивающегося незрелого лимфоцита связывается с собственным антигеном, клетка получает «отрицательный» сигнал и уничтожается. (В отличие от этого, зрелые лимфоциты должны размножаться, продуцировать и секре-тировать антитела, если их рецептор связан с антигеном.) Так как собственные антигены — это первые молекулы, которые встречаются незрелым лимфоцитам, этот процесс должен происходить в местах развития лимфоцитов. Бернет назвал его уничтожением «запрещенных» клонов. Это очень элегантное теоретическое объяснение проблемы аутотолерантности. Только лимфоциты, прошедшие этот селекционный фильтр (уничтожение запрещенных клонов), достигают зрелости и приобретают способность связываться с чужеродными антигенами. С тех пор, как в 1957 г. была сформулирована клонально-селекци-онная теория, проведено множество иммунологических исследований, выявлены разные классы лимфоцитов (В- и Т-клетки) и роль каждого из них в иммунном ответе, однако основные положения этой теории до сих пор справедливы.
Итак, мы видим, что в основе клональной селекции лежит простой дарвиновский отбор. Предполагается, что до встречи с антигеном уже существует множество разнообразных клеток, несущих рецепторы. Свои и чужие антигены играют только селективную роль (соответственно отрицательную или положительную) в формировании репертуара лимфоцитов в крови и лимфатической системе. Предполагается, что есть единственное событие, от которого зависит отбор, — это реакция связывания поверхностного антитела В-клеток (или рецепторов Т-клеток) с антигеном определенной формы. Популяции клеток, образовавшиеся в результате «клонального роста», продуцируют специфические антитела и Т-клетки, необходимые для борьбы с инфекцией. Клональный рост может увеличивать число клеток в тысячи раз. Это объясняет, почему концентрация антител в крови растет в экспоненциальной зависимости от времени после заражения или искусственного введения чужеродного антигена (рис. 3.8). Увеличение концентрации антител отражает экспоненциальный рост популяции продуцирующих их клеток, численность которых удваивается при каждом делении. После пятнадцати делений должно появиться около 30 тысяч клеток, возникших из одной исходной клетки, так как число клеток описывается 2"-степенньш рядом, где п равно числу делений. Такое увеличение численности клеток, секретирую-щих антитела, дает возможность быстро достичь эффективной концентрации антител, достаточной для борьбы с острой инфекцией. Как правило, это занимает от трех до пяти дней.
Легко представить себе, как клонально-селекционная теория объясняет иммунологическую память. Она является следствием (по крайней мере, частично) размножения стимулированных антигеном клеток (клональная экспансия). Если антигенспецифичные клетки размножились, некоторые из их потомков становятся долгоживущими. Эти клетки «памяти» могут оставаться в кровеносной системе и в лимфоидных тканях, дожидаясь следующей встречи с тем же самым антигеном спустя много лет.
Эта теория дает также объяснение феномена созревания аффинности (сродства антитела к антигену). Образующиеся на поздних стадиях иммунного ответа антитела имеют большую аффинность, чем те, что образовались ранее (рис. 3.8). По мере того, как концентрация антигена в лимфоидной ткани падает, конкуренция за связывание с редким антигеном приводит к тому, что для размножения «отбираются» более успешные В-клет-ки. В-лимфоциты с поверхностным рецептором самой высокой аффинности (антиген связывается более прочно) будут побеждать в соревновании, и синтезируемый ими тип антител станет, в конечном счете, преобладающим. В следующей главе (рис. 5.4) мы рассмотрим этот процесс отбора, основанного на сродстве, более подробно.
Если изучить каждое антитело в образце крови, то можно обнаружить тысячи разных молекул антител, причем каждое способно распознать специфичный антиген внешней среды. Если определить аминокислотную последовательность каждого из этих антител, окажется, что одно антитело отличается от другого последовательностью аминокислот в вариабельной V-области, которая образует антигенсвязывающий центр (рис. 3.2). Этот факт был установлен в 1960-х гг., и он дал решающие доказательства истинности клонально-селекционной теории Бернета.
Важная экспериментальная проверка клонально-селекционной теории была предпринята в конце 1960-х гг. нашим коллегой Гордоном Эйда (Ada), работавшим с Полин Берт (Byrt) в Институте медицинских исследований Уолтера и Элайзы Холл. В основе их эксперимента лежало предположение, что если популяцию лимфоцитов подвергнуть воздействию антигенов одного типа, с ними будет связываться только клон лимфоцитов с антителами, реагирующими на этот антиген, тогда как огромное большинство клеток не будет связываться, т. к. они продуцируют антитела, реагирующие на другие антигены. Создавая радиоактивные антигены, Эйда и Берт рассуждали так: лимфоциты, которые свяжут их, будут облучены и погибнут. Таким образом, популяция лимфоцитов окажется неспособной к иммунному ответу на проверяемый радиоактивный антиген, но будет нормально реагировать на другие антигены. Именно такой результат они и получили. Этот эксперимент стал известен как «эксперимент по самоубийству антигеном». Он был первым экспериментальным доказательством клонально-селекционной теории.
Отталкиваясь от клонально-селекционной теории, Тед Стил и Боб Бландэн стали изучать механизм эволюции генов антител. Эта новая область иммунологии исследует генетические особенности процессов, обеспечивающих разнообразие антител и созревание аффинности. С конца 1970-х гг. становится все больше известно об уникальной системе генов Ig и ТкР. Сейчас мы уже много знаем о структуре последовательностей ДНК этих генов. Мы можем объяснить, почему одна клетка производит антитела одной специфичности, и как мутация порождает новое антитело. Именно это делает иммунную систему способной продуцировать антитела высокой аффинности ко многим тысячам новых антигенов.
Клонально-селекционная теория поставила вопрос о том, подвергаются ли Ig-гены изменениям в отдельных В-лимфоци-тах после стимуляции антигеном. В общей форме этот вопрос обсуждал еще Бернет в 1957 г. Однако он полагал, что разные Ig-гены, кодирующие антитела различной специфичности, существуют уже до того, как чужеродные антигены внедряются в систему. (Дарвин в предьвдущем столетии также считал доказанным предсуществование генетической изменчивости животных и растений, на которую действует естественный отбор.) Таким образом, Бернет предполагал, что гены антител экспрес-сируются в популяции клеток, последние затем могут отбираться антигеном и клонально размножаться. (Современные методы молекулярной биологии, необходимые для ответа на вопрос о соматическом мутировании в то время были недоступны.)
Тем не менее в конце 1960-х-начале 1970-х гг. Мелвин Кон, а затем Элистэр Каннингем привели доводы в пользу того, что иммунная система имеет способность генерировать соматические мутации генов антител в ответ на внедрение чужеродных антигенов. По их мнению, по-видимому, выгодно, чтобы с ДНК зародышевой линии наследовалось только небольшое число необходимых Ig генов, а новые могли бы возникать в течение жизни животного в виде соматических мутаций, вызванных антигеном. В то время, когда эта теория соматического мутирования была высказана впервые, она была оценена по достоинству только небольшим числом иммунологов. Большинство продолжало придерживаться мнения, что все антитела закодированы в генах половых клеток, то есть они предсущест-вуют до рождения животного. Это предполагало, что изменчивость является результатом случайных (редких) мутаций в генах клеток зародышевой линии, которые передаются потомкам. Без преувеличения можно сказать, что споры между приверженцами идеи «соматических мутаций» и «мутаций в половых клетках» были в центре внимания большинства наиболее важных работ. Они сыграли ту же роль, что и дискуссия в физике о кор-пускулярно-волновой двойственности в квантовой механике в 1920-х годах. Поэтому мы вынуждены объяснять основные молекулярные механизмы в контексте их исторических корней.
Почему антитела специфичны и как приобретается аутотолерантность
Вернемся к проблеме различения своего и не-своего. Мы уже говорили, что для различения своего и не-своего антитела должны быть специфичными. Таким образом, для того чтобы отличать огромный внутренний мир молекул от внешнего мира (а некоторые химические характеристики этих миров одинаковы), эволюция обеспечила ошеломляющее разнообразие молекул, распознающих антигены. Антитела каждой специфичности клонально экспрессируются в популяции тысяч клеток, и простой механизм удаления клона выбраковывает те клетки, которые реагируют на самого себя. Это придает особое значение специфичности и разнообразию антител. В качестве простого, но не строго корректного сравнения [2] можно привести четкость изображения на экране телевизора, которая зависит от числа минимальных элементов изображения (пикселов) в строке экрана. Чем плотнее строка, тем четче изображение. Для того чтобы легко различать разные участки и, следовательно, идентифицировать изображение, необходимо иметь набор разных пикселов (светлые, темные, красные, зеленые и так далее). По аналогии, чем меньше специфичных антител и рецепторов Т-лимфоцитов, тем большему риску уничтожения они подвергаются в процессе установления аутотолерантности. Если бы все они были неспецифичны, было бы два возможных исхода. Первый — после того, как установилась аутотолерантность, у нас не осталось бы иммунной системы. И второй — если бы аутотолерантности не существовало, наша собственная иммунная система атаковала бы и разрушала организм, которому она принадлежит.
Поскольку мы приняли необходимость существования аутотолерантности, мы должны считать аксиомой утверждение, что аутотолерантность каждого индивида должна «обучаться» в дарвиновском смысле этого слова. Поясним это. Если самцы инб-редной линии А мышей скрещиваются с самками генетически другой инбредной линии В, то появляется потомство, которое унаследовало разные гены от разных родителей. Мыши линии А генетически запрограммированы производить в клетках и тканях молекулы А-антигена, тогда как мыши линии В запрограммированы производить В-антигены. В некотором смысле это напоминает правила переливания крови у человека для системы групп крови АВО. Взрослые особи линии А всегда будут развивать анти-В иммунную реактивность (естественно развивающиеся антитела и Т-клетки), а особи В будут развивать анти-А реактивность. Таким образом, ткань, пересаженная от А к В и, наоборот, от В к А, всегда будет отторгаться. Однако потомки генетически различающихся родителей будут по своему антигенному составу АВ, и это представляет для них серьезную проблему. Если бы аутотолерантность не приобреталась в ходе развития, АВ потомки этого скрещивания не могли бы выжить. Они должны были бы саморазрушиться, как только их иммунная система приобрела бы способность реагировать на свои собственные клетки. Однако мы знаем, что популяции человека и большинство популяций диких животных чрезвычайно разнообразны по генам, кодирующим антигены гистосовмести-мости. Следовательно, каждый из нас несет разные комбинации этих антигенов, унаследованных от родителей. То есть, все мы похожи на гибридов АхВ, изображенных на рис. 4.2.
Рис. 4.2. Толерантность к собственным антигенам не детерминирована генетически. Мелвин Кон и его коллеги Петер Бретчер и Род Лангман неоднократно подчеркивали этот ключевой момент. На рисунке показан результат эксперимента, поставленного природой (случайные скрещивания генетически различающихся индивидов). Поскольку взрослое потомство АВ не разрушает само себя аутоиммунной реакцией, это со всей очевидностью свидетельствует о том, что толерантность приобретается в ходе развития организма. Клонально-селекционная теория Макфарлейна Бернета объясняет, как это достигается путем дарвиновского отрицательного отбора в иммунной системе — уничтожением «запрещенных» клонов, направленных против собственных антигенов (рис. 4.1).
Очевидно, что индивид АВ на какой-то стадии своего развития должен «научиться» быть толерантным и к А-, и к В-антигенам. То есть, механизм аутотолерантности должен приобретаться «соматически». В начале 1950-х годов Питер Медавар и его коллеги экспериментально подтвердили эти теоретические предположения, впервые сформулированные Макфарлейном Бернетом и Фрэнком Феннером (Fenner) в 1949 г. Группа Медавара показала, что, если новорожденным мышам линии В ввести клетки линии А, они вырастают толерантными к трансплантатам кожи линии А. Таким образом, мышей линии В можно было соматически модифицировать так, что они приобретали способность не отторгать кожные трансплантаты линии А, которые в норме у взрослых отторгаются (рис. 4.3). Вернет и Медавар в 1960 г. получили Нобелевскую премию за открытие приобретенной иммунной толерантности.
Рис. 4.3. Эксперимент Питера Медавара по приобретенной неонатальной толерантности. Питер Медавар, Лесли Брент и Руперт Биллингем провели свои эксперименты в 1940-х-начале 1950-х годов. Результаты экспериментов согласуются с клонально-селекционной теорией Макфарлейна Бернета. Они показали, что введение в организм на ранних стадиях неонатально-го развития чужих клеток из костного мозга может индуцировать приобретенную иммунологическую толерантность. Введение на этих стадиях чужеродного антигена вызывает уничтожение клонов, направленных против чужих. В результате иммунная система начинает относиться к чужим тканям как к своим.
Итак, мы приходим к заключению, что необходимая для приобретения и иммунности, и толерантности соматически обучающаяся программа основана на ключевом взаимодействии (или связывании) антигенов с клонально экспрессирующи-мися поверхностными молекулами, распознающими антигены (антитела, ТкР). Это достигается в процессе дарвиновского отбора, действующего в популяции лимфоцитов. Это — основной принцип функционирования иммунной системы. Мы объясним в дальнейшем, что обратная связь между генами сомы и половых клеток дает логически последовательное объяснение всех уникальных молекулярно-генетических свойств иммунной системы. Но, прежде чем вести читателя дальше, мы должны потратить немного времени на описание деталей строения ДНК-последовательностей генов Ig и ТкР и некоторых необычных свойств этих генов.
Чем гены антител отличаются от других генов: перестройки ДНК вариабельной области
Принцип «ДНК делает РНК делает Белок», уже описанный в гл. 2, применим для всех организмов: от простых бактерий до сложньк позвоночных, включая человека. Однако существует одно важное отличие структуры генов высших клеток, включая клетки позвоночных, и соответствующих генов бактерий. Кодирующие последовательности эукариотических генов (экзо-ны) перемежаются с некодирующими участками ДНК (интронами).
В конце 1970-х годов Р. Роберте (Roberts) и П. Шарп (Sharp), получившие Нобелевскую премию в 1994 г., показали, что первичная копия информационной РНК (мРНК), образующаяся в клеточном ядре, содержит интронные последовательности, но к моменту выхода мРНК из ядра в цитоплазму, участки интронов в ней уже отсутствуют, а экзоны оказываются состыкованными, так что мРНК без запинки транслируется в белок.
Процесс удаления интронов называется сплайсингом РНК. Сплайсинг чрезвычайно точен, он редко разрезает РНК в неправильном месте. Сейчас известно, что для обозначения границ интронов существует сигнальная последовательность, узнаваемая особым ферментным комплексом (сплайсосомой). Некоторые интроны являются рибозимами (РНК-ферментами), способными к самосплайсингу. Возможно, это реликты «мира РНК», существовавшего много миллиардов лет назад. Часто сплайсосомы состоят из РНК и белка. Отметим один очень важный момент: места сшивок (разрезании), которые закодированы в ДНК-последовательности, разрезаются сплайсо-сомами, действующими на одноцепочечные последовательности РНК, только после транскрипции. Двухцепочечная ДНК генома никогда не разрезается в этих местах. Все гены, представленные одной копией (рис. 4.4), кодируют белки, необходимые для выполнения функций «домашнего хозяйства» клетки или многоклеточного организма. Именно эти гены являются предметом решения «жизнь или смерть» при дарвиновском отборе. Например, гены, кодирующие белковые субъединицы молекулы гемоглобина (которая переносит кислород от легких ко всем органам тела), представлены одной копией. Поврежденные молекулы, появившиеся в результате мутаций, обычно неэффективно переносят кислород и, следовательно, приводят к гибели организма или снижают его жизнеспособность.
Таким образом, в высших клетках имеется механизм редактирования РНК, который работает до того, как она появится в форме зрелой молекулы, кодирующей специфическую последовательность аминокислот — белок. Удаление интронов из РНК и соединение кодирующих последовательностей должны быть очень точными, чтобы гарантировать сохранение рамки считывания триплетов оснований (см. приложение). Если на этом этапе произойдет ошибка (и изредка они происходят), может образоваться мРНК с последовательностью «вне рамки». Обычно это приводит к синтезу ненормального белка и преждевременному прекращению синтеза из-за появления стоп-ко-дона. (Стоп-кодоны не определяют никакой аминокислоты. Таким образом, они прекращают добавление аминокислот к белковой цепи. Существует три стоп-кодона — это UAG, UAA и UGA.) Эти стоп-кодоны в норме определяют 3'-конец, или правую границу кодирующей последовательности гена. Преждевременная остановка (терминация) приводит к образованию более короткого белка, обычно со сниженной функцией. Следовательно, нормальные гены, кодирующие белки, можно представить как ряд соприкасающихся триплетных кодонов со стоп-кодоном на конце (подобно точке в конце предложения). Их называют открытой рамкой считывания (сокращенно ORF). Давление естественного отбора должно действовать против любой мутации, приводящей к появлению стоп-кодона внутри ORF.
Рис. 4.4. Строение бактериального гена и однокопийного эукариотического гена. На рисунке показаны различия в строении генов, кодирующих белок, у бактерий и у высших клеток. Обратите внимание, что левый конец цепи ДНК принято обозначать как 5'-конец, правый конец — как 3' (произносится как «пять штрих» и «три штрих», соответственно). Слово «однокопий-ный» означает, что в хромосоме находится только одна функциональная копия гена (в отличие от семейства V-генов, рис. 4.5, к которому относится много генов с очень высокой степенью сходства ДНК-последовательностей, расположенных в одной хромосоме). Участки ДНК, которые кодируют белок, изображены в виде прямоугольников. Двухцепочечная ДНК изображается прямой линией, одноцепочечная информационная мРНК — волнистой линией. Изогнутые стрелки указывают на точку начала транскрипции мРНК.
А. У бактерий участок, кодирующий белок, представлен непрерывной рядом триплетных кодонов, каждый из которых определяет одну аминокислоту (см. приложение). мРНК транскрибируется и немедленно транслируется в аминокислотную последовательность (белок) в рибосомах.
Б. У эукариот почти все гены, кодирующие белки, устроены сложнее. У них последовательности, кодирующие белок (экзоны), прерываются некодирующими последовательностями (интронами). На рисунке это обозначено промежутками между кодирующими участками. Редким исключением (гены без интронов) в высших клетках являются гены, кодирующие гистоны (табл. 5.1), а также псевдогены и функциональные ре-трогены, появившиеся в результате обратной транскрипции молекулы мРНК (см. гл. 7). Таким образом, по матрице ДНК создается длинная содержащая интроны молекула про-мРНК. Особая молекулярная внутриядерная органелла (сплайсосома) определяет границы между интронами и экзонами, вырезает интроны из про-мРНК и точно соединяет экзоны, образуя непрерывный кодирующий участок. Затем зрелая, или «процессированная», мРНК экспортируется из ядра в цитоплазму, где она транслируется в последовательность аминокислот в рибосоме.
Молекулярно-генетические исследования Ig-генов начались в середине 1960-х гг. К этому моменту было известно, что и тяжелые (Н), и легкие (L) цепи антитела выполняют двойственную функцию (рис. 3.2). Они состоят из вариабельной аминокислотной последовательности, или V-домена (служит для связывания антигена), и константной, или С -домена (служит, например, для запуска лизиса клетки-мишени или фагоцитоза). Гены антител отличаются от всех остальных генов, локализованных и картированных генетиками в определенных местах хромосом (называемых локусами). Гены, кодирующие V-и С-домены, отделены друг от друга огромным участком последовательности ДНК. Например, V- и С-домены тяжелых цепей мыши находятся в хромосоме 12, около концевого участка длинного плеча хромосомы. Генетическое картирование и последующее изучение последовательности нуклеотидов ясно показали, что V-участок отстоит от С-участка по крайней мере на 300 000 п. н. (300 тыс. п. н.) оснований! Почему?
Даже в середине 1970-х гг., когда стала известна экзоно-ин-тронная структура генов, такое большое расстояние казалось необычным. Однако десятью годами раньше Драйер (Dreyer) и Беннет (Bennet) предположили, что единый участок ДНК, кодирующий Н- или L-цепь, образуется в результате перемещения (транслокации) V-участка к С-участку. То есть, для объяснения удивительного свойства Ig-генов было предсказано существование особого типа редактирования, или сплайсинга ДНК-последовательностей. Далее, эти авторы допускали, что данный процесс происходит при созревании лимфоцита. Драй-ер и Беннет предположили, что часть Ig-локуса (или места локализации в хромосоме последовательности ДНК, кодирующей Ig-гены) содержит в зародышевой линии большое число (сотни) V-генов. В каждой отдельной В-клетке один из этих генов передвигается и становится рядом с одним из нескольких возможных С-генов. Случайное перемещение только одного V-ге-на из большого числа возможных приводит к тому, что клетка производит антитела только одной специфичности. После такой случайной перестройки генов Н- и L-цепей клетка из большого числа возможных комбинаций Н + L белковых цепей создает один полный белок. Затем клетка экспрессирует это антитело на поверхности, и ее судьба решается окончательно: если она окажется «против своих», она будет уничтожена. Если она выжила, она станет потенциальным участником иммунного ответа на чужие антигены.
Это теоретически привлекательное, хотя и достаточно смелое предсказание перестройки ДНК, было доказано лишь десять лет спустя Сусуми Тонегава, который описал организацию и перестройку генов Ig-локуса у мыши[3]. Оказалось, что перестройка ДНК много сложнее, чем предполагалось. Этот процесс изображен на рис. 4.5; он имеет место и у мыши, и у человека. У других позвоночных может быть несколько иная, но в принципе сходная организация кодирующих элементов Ig-локуса.
Несмотря на то, что до точного картирования и секвениро-вания (определения последовательности нуклеотидов) каждого V-элемента генома мыши и человека еще далеко, у нас есть четкая картина строения Ig-генов в клетках зародышевой линии и в соматических клетках. На рис 4.5 приведена схема строения гена тяжелой цепи Ig, но очень похожие схемы можно нарисовать и для генов легких цепей Ig, и для ТкР-генов. Обратите внимание, что около ста V-генов (или V-элементов) расположено левее соединительных J-элементов (от англ. joining — J) и D-элементов (от англ. diversity — разнообразие), а они, в свою очередь, отделены от небольшого числа (примерно 8) генов константной области (C-constant). D- и J-элементы кодируют от трех до пятнадцати аминокислот, тогда как V-элемент — около 100 аминокислот.
О генах антител в неперестроенном виде говорят, что они имеют «конфигурацию зародышевой линии». В таком виде находится ДНК в половых клетках (сперматозоидах и яйцеклетках) и во всех клетках организма, кроме зрелых лимфоцитов (в клетках печени, почек, поджелудочной железы, в других лимфоцитах, например, в фагоцитах). В каждом созревающем лимфоците мыши и человека ДНК подвергается случайной соматической перестройке. Один из V-элементов перемещается и соединяется с одним D- и одним J-элементом. Этот участок располагается перед первым С-геном. Кодирующий С-участок разделен рядом интронов. После этого все еще остается длинная промежуточная последовательность между перестроенным V-геном, который теперь называется V(D)J-ген, и С-участком. Эту структуру называют «соматической конфигурацией». Скобки вокруг D в общем символе гена появляются, потому что гены легких цепей Ig построены только из V- и J-элементов.
В конфигурации зародышевой линии ДНК не транскрибируется в мРНК, по которой могли бы синтезироваться Н- или L- белковые цепочки антитела. В соматической конфигурации перестроенные V(D)J- и С-участки активно транскрибируются, образуется мРНК, которая транслируется в Н- и L- цепи антитела. В неперестроенных V-элементах никогда не происходит соматического мутирования. Мутации появляются только в V(D)J-перестройке.
Перестройки ДНК выполняются набором особых рекомби-национных ферментов. Кодирующие их гены называются генами, активирующими рекомбинацию (recombination activating genes — RAG), и локализованы где-то в других местах генома. RAG-ферменты распознают ДНК-последовательности (реком-бинационные сигнальные последовательности) на соответствующих концах V-, D- и J-элементов, которые и соединяются. Первым шагом в экспрессии тяжелой цепи в созревающей В-клетке костного мозга человека или мыши является DJ-пере-стройка. Вся промежуточная ДНК между D-элементом (их может быть 20 или более) и J-элементом (их 4 или 5) удаляется. Следующий шаг — перемещение случайно выбранного V-эле-мента к перестроенному DJ-элементу, причем снова вся промежуточная ДНК удаляется.
Рис. 4.5. Строение генов, кодирующих V- и С-области тяжелых цепей антитела, в зародышевой линии и после соматической перестройки у человека и мыши.
А. В конфигурации зародышевой линии ряд очень похожих (но все-таки различных) вариабельных V-элементов лежит выше (левее) экзонов, кодирующих константную С-область. Эти V-элементы зародышевой линии (кодирующие примерно 95 аминокислот) называются неперестроенными. Между V- и С- элементами расположены D- и J-элементы (каждый кодирует короткую последовательность аминокислот). Каждый V-элемент имеет лидерную (L) последовательность, которая кодирует короткую последовательность аминокислот, сигнальный пептид. Все гены, кодирующие белки, например, антитела, предназначенные для выведения из клетки (для секреции) или для перехода в другие окруженные мембраной области клетки, имеют такие сигнальные пептиды, которые позволяют им перемещаться в нужные внутриклеточные или внеклеточные области. Интрон между L и V называется L-V-интроном (или лидерным интроном). Его значение для понимания следов интеграции сомы в зародышевую линию подробно описано в гл. 6.
Б. В ходе развития В-клеток в костном мозге в каждом В-лимфоците случайно перестраиваются V-, D- и J-элементы тяжелой цепи, и появляется перестроенная последовательность вариабельной области VDJ, которая теперь называется соматической конфигурацией. Для Н-цепей на первом этапе перестройки происходит объединение DJ, за ним следует объединение с V-элементом, и образование VDJ. После перестройки обнаруживается, что вся ДНК между случайно выбранным V-элементом и использованным J-элементом удаляется из клетки. Таким образом, каждая успешная перестройка ДНК вариабельной области уникальна для каждой зрелой В-клетки. Обратите внимание, что перестроенный участок (VDJ) лежит выше (левее) экзона, кодирующего С-белок. Заметьте также, что в участке между VDJ и С, названном J-C-интроном, лежит неиспользованный элемент (который в этом примере просто удаляется). Про-мРНК, содержащая вариабельный (VDJ) участок, присоединенный к С-участку, образуется в ядре. L-V и J-C интроны (и интроны внутри С -участка) затем вырезаются, что приводит к экспорту зрелой РНК молекулы в цитоплазму, где она транслируется на рибосоме в последовательность аминокислот. Лидерный (сигнальный) пептид отрезается от белка, когда он выделяется из клетки (объяснения терминов см. также в табл. 3.1 и 5.1, на рис. 4.4 и в тексте). Соматическая конфигурация и конфигурация зародышевой линии генов L-цепей такая же, кроме того, что легкие цепи не содержат D-участков.
Продемонстрированные Тонегавой V(D)J-nepecтройки (случайное использование примерно 100 V-генов, 20 D-генов и 4 J-генов и случайное объединение тяжелых и легких цепей для образования гетеродимерного связывающего центра) дают возможность продуцировать большое потенциальное разнообразие белков из сравнительно небольшого количества генетического материала. Кроме того, иногда слияние V, D, и J приводит к добавлению или потере оснований, увеличивая, таким образом, разнообразие.
Разобравшись в этих молекулярных процессах, мы можем теперь задать два очень важных вопроса. Почему В-лимфоцит производит антитела только одной специфичности? Почему соматические мутации (в В-лимфоцитах) возникают преимущественно в перестроенном V(D)J-участке?
Все соматические клетки (клетки тела) имеют двойной набор хромосом, один набор от матери, другой от отца. Такие клетки называются диплоидными. Сперматозоиды и яйцеклетки имеют только по одному набору хромосом (они гаплоидны). Оплодотворение, слияние сперматозоида и яйцеклетки, восстанавливает диплоидное состояние. Кроме половых хромосом (X и Y), все другие хромосомы диплоидного набора разбиваются на пары с очень похожими ДНК-последовательностями. По мере созревания В-лимфоцита начинается перестройка V-, D- и J-элементов. Успешная V(D)J-перестройка в одной хромосоме посылает сигнал, который выключает активность RAG-ферментов и препятствует перестройке в гомологичной хромосоме. Вот, в принципе, ответ на первый вопрос. Дальнейшие детали мы не рассматриваем.
Второй вопрос, почему мутации ограничиваются V(D)J-участком, чрезвычайно важен для обсуждения обратной связи между сомой и зародышевой линией, которая составляет главную тему этой книги. Мы подробно расскажем об этом в следующей главе. Здесь подчеркнем лишь некоторые общие принципы. Если мутации в вариабельной области антитела могут оказаться полезными, то мутации в константной области, скорее всего, вредны, так как они могут нарушить эффекторные функции антитела, запуск лизиса бактериальных клеток или стимулирование фагоцитоза (рис. 3.1). Разделение V- и С-участков позволило эволюции создать механизм, который обеспечивает мутации в V-участке, но сохраняет С-участок неизменным. Вот что происходит в В-лимфоците на определенных стадиях его жизни. Перестроенный V(D)J-ген может подвергаться очень высокому уровню соматических мутаций, и новое антитело оценивается по способности связывать антиген (см. следующую главу). Антитела с самой высокой аффинностью к чужеродному антигену выигрывают в отборочных соревнованиях за связывание антигена, сохраняются и становятся долго живущими клетками памяти. В-лимфоцит проиграет соревнование, если мутация уменьшает или уничтожает аффинность; такие клетки погибают. В-лимфоциты, кодирующие антитела, которые связывают собственные антигены, также уничтожаются, и, следовательно, сохраняется аутотолерантность.
Сейчас мы хорошо понимаем, как иммунная система может кодировать миллионы специфических антител, и что тем не менее все еще имеется достаточно ДНК для всех остальных генов, необходимых клетке и многоклеточному организму. Простыми вычислениями можно показать возможности зародышевой линии:
• у мыши или человека в конфигурации зародышевой линии Н-цепи закодировано примерно 100 V-элементов, примерно 20 D-элементов и 4 J-элемента. В соответствии с моделью случайных перестроек это может дать 100 х 20 х 4 = 8000 возможных Н-белковых цепей;
• конфигурация зародышевой линии главного генного кластера, определяющего L-цепь, кодирует примерно 100 V-элементов и 4 J-элемента, что может дать 100 х 4 = 400 возможных L-белковых цепей;
• таким образом, общее число возможных HL-белковых гете-родимеров, при условии, что все Н + L образуют жизнеспособные антитела, равно 8000 х 400 = 3,2 х 106, или примерно 3 миллиона специфичных антител.
В этих вычислениях не учитывается дополнительное разнообразие, возникающее в результате добавлений или потерь оснований в процессе слияния V(D)J.
Сколько же из этих 3 млн. потенциальных антител используется? Ответ прост — мы не знаем. Однако нам известно, что около половины V-элементов никогда не участвуют в образовании антитела (то есть обнаружено, что они не перестраивались в В-клетках). Род Лангман (Langman) и Мелвин Кон теоретически рассмотрели один фактор, который ограничивает репертуар антител. У мыши примерно 50 миллионов В-клеток. Если случайный репертуар из 3 млн. антител разных специфичностей равномерно распределен по 50 миллионам В-клеток, то среднее число клеток с данным антителом должно быть равно примерно семнадцати. При острой бактериальной инфекции для того чтобы победить в суровой борьбе с быстро размножающимися бактериями, иммунная система должна выработать большое количество антител с достаточной авидностью, чтобы уничтожать больше бактерий, чем их образуется при размножении. Так как бактерии могут делиться чаще, чем один раз в час, а В-клетки затрачивают по крайней мере 5—6 часов на деление, это соревнование может быть выиграно только при условии, что начальное число В-клеток, связывающих эти бактерии, велико. Другие критические факторы — это скорость образования белка антитела в В-клетках и их физическая локализация относительно места инфекции. Чем ближе они находятся, тем выше локальная концентрация антител и больше скорость уничтожения инфекции. Эти ограничения заставили Лангмана и Кона предположить, что начальный репертуар функциональных антител (до соматического мутирования) должен быть меньше потенциального репертуара. Они полагают, что разнообразие у мышей — около 10 тыс. специфичностей, что дает в среднем по 5 тыс. В-клеток на специфичность.
Однако эти оценки размера репертуара антител все еще велики. Основа стратегии иммунной системы как мыши, так и человека — это случайные перестройки V- , D- и J-генов. Полностью функциональные белки антител закодированы в зародышевой линии как отдельные участки ДНК, «ожидающие» соматической перестройки и сборки в функциональный V(D)J-ген (рис. 4.5). Затем случайная комбинация Н- и L-белковых цепочек образует HL-гетеродимер — антитело. Такая стратегия хранения генетической информации чрезвычайно экономна и позволяет зашифровать миллионы потенциально полезных вариантов.
Дополнительное соматическое варьирование перестроенных V(D)J-последовательностей в В-лимфоцитах также вносит вклад в разнообразие репертуара благодаря селективному размножению антител отдельных специфичностей. Действительно, сейчас мы знаем, что в зрелых В-клетках возникают вызванные антигеном соматические гипермутации перестроенных V(D)J-участков. Это важно, так как дает возможность отобрать и размножить мутантные В-клетки, производящие антитела высокой аффинности. Существует также явление, описанное группой ученых под руководством Мартина Уайгерта (Weigert) и другими, называемое «замещение V-гена» [5]. Оно происходит при образовании тяжелых цепей, и суть его состоит в том, что находящийся выше V-элемент может занять место уже существующего элемента в VDJ-последовательности. Во время клонального роста одна и та же линия В-клеток может подвергаться нескольким последовательным заменам V-гена.
Еще один момент, который следовало бы повторить, говоря о процессе перестройки и объединения V(D)J, заключается в том, что полный ген, кодирующий вариабельную область антитела, собирается из нескольких частей (битов) ДНК-последовательностей. Несколько членов каждого семейства этих частей (V, D и J) собираются случайно. V-D-J объединенный участок формирует связывающий центр антитела, который находится в непосредственном контакте с молекулой антигена.
Известно два исключения из этого общего правила, гласящего: что ни одного полного V-гена не существует в ДНК зародышевой линии. У скатов (хрящевые рыбы) одно семейство генов L-цепи в зародышевой линии состоит из «слитых» VJ-по-следовательностей [б]. Либо это семейство представляет собой первичный ген, который существовал до разделения V- и J-элементов, либо оно возникло в результате объединения V- и J-элементов. Группа Гэри Литмана (Litman), обнаружившая эти гены, отдает предпочтение последней интерпретации. Второе исключение — это группа V-псевдогенов тяжелых цепей у кур, которые содержат и «частички D», присоединенные к концу V-последовательности в предпочтительной рамке считывания, существующей в функциональных VDJ-перестройках [7]. Возможно, эти гены появились благодаря обратной транскрипции мРНК, кодирующей V(D)J-o6nacTb, в результате чего возникли ретротранскрипты кДНК с рамкой считывания объединенных VJ или VDJ, которые каким-то образом включились в половые клетки.
Мы подробно обсуждаем детали строения локусов Ig в конфигурации зародышевой линии и соматической конфигурации, поскольку это позволит интерпретировать их в рамках предположения о существовании ламарковского процесса обратной связи сомы и зародышевой линии. В следующих главах мы сравним эти конфигурации и увидим, что различия между ними высвечивают генетическую уникальность иммунной системы и позволяют назвать «умными» гены, кодирующие антитела и ТкР. Уникальные свойства Ig-генов и молекулярных продуктов этих генов, созданные в ходе эволюции позвоночных, дают возможность по-новому взглянуть на роль некоторых генетических процессов, протекающих в иммунной системе. К этим процессам относятся сплайсинг V(D)J-информационной РНК, обратная транскрипция и предполагаемый перенос ДНК от сомы в зародышевую линию.
Для многих читателей это утверждение может показаться непоследовательным. Действительно, если эволюция со всей своей мудростью смогла создать такую генетическую стратегию, которая способна кодировать более миллиона разных антител, достаточного для ответа на неожиданное, то нуждается
ли такая эффективная система в ламарковской обратной связи генов? Возможный ответ таков: дошедшая до наших дней система не могла появиться без соматического гипермутирования и без обратной связи генов сомы и зародышевой линии. Мы вернемся к этой проблеме позже.
Отступление: можно ли сравнивать иммунную систему с современными компьютерными антивирусными программами?
Нам кажется уместной следующая, связанная с компьютерами, аналогия. Одна из множества опасностей, перед лицом которых мы стоим в век Интернета, соединяющего миллионы персональных компьютеров, — это электронные «вирусы» — детище нашей кибернетической культуры. Многие компьютерные вирусы по своему поведению очень похожи на биологические. При заражении жесткого диска они могут уничтожать или портить и файлы, и программы. Если мы нечаянно посылаем зараженное сообщение коллегам и друзьям, то тем самым мы производим новые копии вируса, обеспечивающие его выживание. Сейчас доступны антивирусные пакеты программ, которые автоматически проверяют входящие файлы на наличие известных компьютерных вирусов. А что же абсолютно новые электронные вирусы? Как нам защитить от них свои-компьютеры? Насколько современные антивирусные компьютерные программы сравнимы с биологической стратегией иммунного ответа? Что, если кибернетики были бы в состоянии создать новые электронные вирусы со всеми врожденными эффективными стратегиями нашей собственной иммунной системы? Смогут ли интернетовские или телефонные линии и коммутирующие концентраторы начать страдать от болезней, подобньк СПИДу? Произойдет ли это до того, как программисты создадут антивирусные программы, которые способны эффективно отвечать на неожиданное? Это захватывающие вопросы. IBM в настоящий момент создает «иммунную систему» для борьбы с вирусами в киберпространстве [8]. Антивирусные программы живут в хозяине-компьютере и контролируют системные функции, изменения в программах или семействах сигнатур для того, чтобы распознавать и уничтожать вирусы. У компьютерной иммунной системы, создаваемой IBM, любой набор данных, подозреваемых на зараженность, автоматически посылается в аппарат вирусного анализа. Программа, действующая как подсадная утка, «соблазняет» вирус заразить ее, так что код вируса выявляется для дальнейшего анализа. Затем аппарат вирусного анализа обновляет свои файлы прежде, чем посылать эту новую информацию назад в инфицированную машину и в любой другой потенциально инфицированный узел в сети (иммунный ответ). Таким образом, новые антивирусные программные технологии основаны на элементарных моделях иммунной системы позвоночных. «Эволюция» уже действует на компьютерном поле боя. Дальнейшее развитие антивирусных технологий, возможно, будет изменяться параллельно знаниям о биологической эволюции.
В этой главе было описано много примеров эффективности и логики иммунной системы, которые, возможно, помогут тем, кто интересуется «биологическим» дизайном компьютерных программ, обнаружить некоторые фундаментальные принципы. Анализ того, почему самолеты не похожи на птиц, дает нам важные уроки. Птицы имеют более высоко развитые факторы стабильности и маневренности, чем самолеты, однако, самолеты летают быстрее. Создания природы, как правило, оказываются более гибкими и легкими, нежели сконструированные людьми аппараты. Веками природа служила источником вдохновения для разработчиков новых технологий. Однако нам еще далеко до уровня эффективности системы приобретенного иммунитета. Как заметил Ричард Фейнман (Feynman), говоря об эффективности природы в квантовом масштабе и размышляя о том, может ли эффективно обрабатываться информация на этом уровне: «Внизу еще много места...».
В физике твердого тела и ядерной физике ученые только сейчас открывают детали некоторых законов природы, описывающих поведение субатомных частиц. Со временем откроется возможность создать нанокомпьютерную технологию (порядка 10-9 метра, или 10-3 микрона). Вполне вероятно, создание компьютерной технологии, действующей с той же эффективностью, что и живая клетка, со всем набором врожденных разумных функций, размещенных и внутренне управляемых на площади примерно в 5—10 микрон (приблизительный диаметр клеточного ядра равен 10-5 метра). В ближайшем будущем, используя современные промышленные технологии, достижения ультрафиолетовых лазеров, роботов и линз, необходимых для гравировки микросхем на силиконовых чипах, люди могли бы породить новое поколение микропроцессоров с размерами не больше 0,13 микрон в поперечнике. Правда, есть ряд технических и физических преград, которые пока делают дальнейшую миниатюризацию невозможной. Возможно также, что программисты смогут имитировать некоторые природные стратегии обработки информации для повышения эффективности своих программ. Конечно, наше схематичное сравнение иммунной системы с современными сканирующими антивирусными программами далеко от реальности. Когда мы сравниваем стратегии антивирусных программ со стратегиями нашей иммунной системы, оказывается, что компьютерщикам надо еще многому научиться. Информационным технологиям придется сделать существенный скачок для того, чтобы достичь совершенства иммунной системы позвоночных, приобретенного ею за время эволюции.
Глава 5 СОМАТИЧЕСКИЕ МУТАЦИИ
В гл. 4 мы высказали предположение, что соматические мутации V-генов играли важную роль в эволюции иммунной системы позвоночных. Сформулируем теперь несколько вопросов и постараемся ответить на них. Вопрос первый: каким образом создается картина не-случайности мутаций в ДНК-последовательности, при том, что мутации возникают в результате случайных ошибок? Ответ: по-видимому, существует отбор мутантных ДНК-последовательностей, или их белковых (или РНК) продуктов, сохраняющий только те мутантные гены, которые удовлетворяют селекционному критерию, остальные отбрасываются.
Вопрос второй: каким может быть механизм, предотвращающий появление лишних мутаций, т. е. тех, которые превращают последовательность, уже отобранную как успешную, в плохую? Ответ: по-видимому, существует такой обратный сигнал, который гарантирует, что ген с успешной мутацией не будет мутировать дальше.
И последний вопрос: как обеспечивается мутирование только одного гена? (Большинство генов должно сохраняться неизменным для выполнения надлежащих функций.) Ответ: созданием уникального молекулярного стыковочного устройства, обеспечивающего связывание мутационной машины исключительно с ло-кусом гена-мишени, в котором должны возникать мутации.
С позиций современного неодарвинизма все эти вопросы кажутся вызывающими. Генетики утверждают, что почти все новые мутации вредны. Сейчас эта традиционная точка зрения нуждается в уточнении, так как стал известен особый класс мутаций, которые дают селективные преимущества. Эти мутации возникают в V(D)J-reHax, экспрессирующихся в зрелых В-лимфоцитах. Они обнаруживаются в антителах высокой аффинности, которые образуются примерно через неделю иммунного ответа (табл. 5.1). Такие антитела свойственны долгоживущим В-лимфоцитам памяти. Значит, в результате соматических мутаций появляются антитела, способные более эффективно защищать организм от инфекционного агента. На самом деле описанные выше механизмы «работали» в течение миллионов лет и были результатом биологического процесса «проб и ошибок» во взаимодействии молекул.
Основные понятия, относящиеся к процессам соматического гипермутирования и обратной связи генов сомы и зародышевой линии
• RT-мутаторсома (RT-mutatorsome)
Гипотетическая молекулярная органелла в ядре В-клетки, ответственная за соматическое гипермугирование (RT = обратная транскриптаза, reverse transcriptase). См. рис. 5.6
• Апоптоз
Биологически запрограммированная гибель клеток
• Гибридома
Продукт слияния нормальной В-клетки с непрерывно делящейся опухолевой В-клет-кой. Такая клетка ведет себя как раковая и может независимо расти в культуре ткани. Она секретирует антитела только одной специфичности (исходной В-клетки)
• Гистоны
В клетках эукариот очень длинные нити ДНК имеют вид упорядоченных петель, связа-ных с белками гистонами, что обеспечивает упаковку ДНК в небольшом пространстве ядра
• Конфигурация зародышевой линии
Структура ДНК-последовательности вариабельных, или V-элементов генов зародышевой линии. которые не подверглись перестройке с J или D/J элементами. Генетический символ V(D)J
• Локус-специфическое устройство
Термин используется для обозначения участка стыковки (связывания) RТ-мутаторсомы. Он позволяет ограничить соматические гипермутации только V(D)J и ближайшими ДНК-последовательностями
• Матричная молекула
Любая одноцепочечная ДНК- или РНК-последовательность, которая служит матрицей для создания копии с помощью репликазы
• мРНК
Информационная РНК, которая транскрибируется (копируется) с ДНК-последовательности гена
• Мутагены
Химические вещества или проникающая электромагнитная радиация, способные вызывать мутации
• Обратная связь сомы и зародышевой линии
Процесс, в ходе которого соматически мутированные V(D)J-reны обратно транскрибируются в кДНК, и эти копии рекомбинируют с гомологичной последовательностью V-гена половой клетки так, что замещают ее
• Обратная транскриптаза
Фермент, который копирует РНК-последовательность в ДНК-последовательность
• Перестроенный ген варибельной области
Сокращенное обозначение V(D)J, применимое к перестроенным генам вариабельных областей Н-цепи (VDJ) и L-цепи (VJ)
• Репликаза/полимераза
Общее название ферментов, которые создают дочерние копии ДНК- или РНК-последовательностей. К ним относятся ДНК-полимераза (осуществляет репликацию ДНК), РНК-полимераза (осуществляет транскрипцию) и обратная транскриптаза (создает ДНК-последовательность по матрице РНК)
• РНК-посредник
Этот термин отражает тот факт, что копия гена (ДНК-последовательность), превращенная (в процессе транскрипции) в РНК, может обратно транскрибироваться в кДНК, или ретротранскрипт
• Созревание аффинности
Мутантные антитела, продуцируемые В-клетками памяти, которые возникают в центрах размножения, имеют более высокую аффинность (сродство) к антигену, чем антитела на ранних стадиях иммунного ответа
• Соматическая конфигурация
Перестроенный V-ген вариабельной области, который обнаруживается только в зрелых В- и Т-лимфоцитах. Генетический символ V(D)J
• Соматическое гипермугирование
Мутационный процесс, вызванный стимуляцией В-клетки антигеном, затрагивающий перестроенный ген вариабельной области антитела V(D)J зрелой В-клетки в центре размножения
• Точковая мутация
Замена одного основания. Например, замена основания G на любое из трех других оснований Т, А и С (рис. 2.5)
• Центр размножения
Особая область в лимфатических узлах или селезенке, в которой обнаруживается интенсивная пролиферация (деление) и гибель (апоптоз) клеток. Большинство клеток в таком центре - это В-лимфоциты. Центры размножения являются местами соматического гипермутирования и созревания аффинности, вызываемых антигеном
25 лет назад словосочетание «соматическая мутация» вызывало горячий спор среди иммунологов. В последующие годы споры стали менее оживленными, а многочисленные молекулярные исследования, показали реальность высокого уровня вызываемых антигеном соматических мутаций. Теперь этот процесс называется «соматическим гипермутированием» генов вариабельной области антитела, V(D)J.
Интересно, что в недавних экспериментах, выполненных под руководством Нобелевского лауреата Ролфа Цинкернагеля, было показано, что при иммунном ответе на некоторые вирусные белки не обнаруживается созревания аффинности, основанного на соматическом гипермутировании. Кроме того, оказалось, что антитела высокой аффинности не лучше освобождают организм от вирусной инфекции, чем антитела низкой аффинности. Между тем сейчас считается, что соматическое гипермутирование необходимо для создания антител высокой аффинности, которые лучше защищают от инфекции. Если результаты группы Цинкернагеля подтвердятся для более широкого спектра инфекций и для других позвоночных, это будет означать, что оптимально функционирующие антитела могут быть отобраны из предсуществующего репертуара, и нет необходимости в мутациях. То есть, для ныне живущих позвоночных соматическое гипермутирование и созревание аффинности, возможно, излишни.
Однако в начале эволюционного развития системы приобретенного иммунитета, когда репертуар V-генов клеток зародышевой линии был много меньше, чем у срвременньис позвоночных (он должен был стартовать с одного гена), соматическое гипермутирование могло давать огромное селективное преимущество. Этот процесс мог обеспечивать формирование чрезвычайно широкого репертуара антител, экспрессирующихся в В-лимфоцитах в течение жизни одного животного. Далее, при существовании обратной связи сомы и зародышевой линии соматические мутации генов вариабельной области антител могли бы стать решающим инструментом эволюции, ускоряющим построение репертуара V-генов половых клеток. Все доступные данные согласуются с этим предположением. Соматическое гипермутирование обнаруживается у всех челюстных позвоночных, имеющих систему приобретенного иммунитета, включая наиболее примитивных — хрящевых рыб.
Явление соматического гипермутирования наиболее ярко продемонстрировано для В-лимфоцитов мыши, аналогичный процесс имеет место и у человека. У других позвоночных (кур, кроликов и овец) также наблюдается гипермутирование в В-лимфоцитах, хотя и несколько иное. Эксперименты по изучению механизма соматического гипермутирования проводились в основном на генетически модифицированных (трансгенных) мышах, в частности, в лаборатории Кембриджского университета под руководством Нобелевского лауреата Цезара Мильштейна (Milstein) и его сотрудника Майкла Нойбергера (Neuberger). Эти методы еще не применялись к другим видам.
В этой главе мы сначала рассмотрим, как возникают генные мутации вообще, а затем остановимся на процессе соматического гипермутирования генов V(D)J. Мы покажем, что это строго регулируемый процесс, в нем участвует «локус-специ-фичное устройство», которое ограничивает мутирование ДНК-последовательностью перестроенного V(D)J-yчастка, защищая гены константной области (С) и все другие гены в гено-ме от вредного влияния случайных мутаций.
Мутации возникают в склонных к ошибкам процессах копирования, включающих РНК-посредника
Мутацией называется изменение последовательности нуклеотидов в ДНК (рис. 2.6). Если мутация происходит в той области ДНК, которая кодирует белок, она изменяет триплетный кодон и может привести к замене аминокислоты, определяемой этим код оном. Таким образом, появление другой аминокислоты в белковой цепочке может быть вызвано изменением одного единственного основания в ДНК-последовательности (точковая мутация). Большая часть измененных белков функционирует ненормально (хотя иногда они и выполняют совершенно иную функцию, на ином физиологическом или метаболическом фоне). Поэтому с точки зрения дарвиновского «выживания наиболее приспособленного» большинство мутаций вредны и ставят клетку или многоклеточный организм в неблагоприятные условия при естественном отборе.
Рис. 5.1. Схема, показывающая как точковая мутация может привести к образованию нового мутантного белка с иной третичной структурой. Примечание: Дополнительную информацию см. в табл. 1.1, 5.1 и на рис. 2.5, 2.6 и 2.7.
Рис. 5.1 иллюстрирует эти рассуждения. На нем показаны нормальный и измененный белки. Обратите внимание, что одна единственная точковая мутация G -> С в кодоне, определяющем аспарагиновую кислоту (Asp), дает начало новому кодону, определяющему гистидин (His), в том же положении белковой цепочки (см. также приложение). Такая мутация может привести к радикальным последствиям для мутантного белка, который, складываясь, приобретает другую форму и, следовательно, — другую функцию (т. е. нормальная функция может быть утрачена). Этот принцип был продемонстрирован 40 лет назад, когда определили последовательность аминокислот бета-цепи гемоглобина здоровых людей и людей, страдающих серповидно-клеточной анемией. При этом наследственном заболевании нарушена способность гемоглобина переносить кислород. Молекула гемоглобина — гетеродимер, состоящий из двух альфа-цепей, или альфа-субъединиц, и двух бета-цепей, или бета-субъединиц. Заболевание проявляется у гомозиготных индивидов, у которых обе гомологичные хромосомы несут дефектный ген бета-цепи. Гетерозиготы, которые имеют одну нормальную и одну мутантную копию гена бета-цепи, болеют в легкой форме (так как половина их молекул гемоглобина способна нормально переносить кислород). Оказалось, что у больных серповидноклеточной анемией в 6-м положении бета-цепи вместо глутаминовой кислоты находится валин. И эта единственная замена в цепи из 146 аминокислот приводит к образованию больших агрегатов мутантных молекул гемоглобина в эритроцитах, деформирующих клетку так, что она принимает форму серпа. Интересно, что ген серповидноклеточной анемии сохраняется в Африке, потому что гетеро-зиготы имеют селективное преимущество при заражении малярией, так как плазмодий не может размножаться в серповидных эритроцитах столь же эффективно, как в нормальных.
Это опять возвращает нас к ключевому вопросу: как возникают генные мутации? Еще не так давно считалось, что они возникают «спонтанно» под влиянием космических лучей, рентгеновского излучения или ультрафиолетового света. Чарлз Дарвин называл такого рода изменения «спортами» и предполагал, что их случайно порождают условия Природы. Случай действительно играет роль, — разные мутации появляются с разной частотой. Однако сейчас, после 30—40-летнего периода накопления данных по вирусологии и молекулярной биологии, тайн вокруг причин появления мутаций гораздо меньше. В начале 1980-х гг. Дарил Ренни (Renney) из Университета Ла Троуб (Мельбурн) провел очень полезный анализ этой проблемы [7]. Благодаря его работе и выполненным ранее исследованиям Нобелевских лауреатов Артура Корнберга (Komberg), Манфреда Айгена и Говарда Темина (открывшего обратную транскрипцию у РНК-содержащих опухолевых вирусов) и вирусолога Джона Холленда (Holland), мы имеем логически последовательный способ анализа механизмов возникновения генных мутаций. Все дело в точности копирования ДНК- или РНК-последовательностей по матричным молекулам ДНК или РНК, которые осуществляются четырьмя ферментами, копирующими нуклеиновые кислоты: ДНК-полимеразой, РНК-полимера-зой, РНК-репликазой и обратной транскриптазой.
Исследования на молекулярном уровне показали, что ферменты, участвующие в репликации ДНК, способны к редактированию и исправлению ошибок. Возникновение мутаций в ходе репликации ДНК — редкое событие (рис. 5.2). Максимальная частота таких мутаций, вероятно, меньше, чем 10-8, а истинная частота ошибок, вероятно, еще меньше — около 10-10 (меньше, чем одна на 10 миллиардов реплицированных оснований). Чрезвычайно высокая точность копирования информации обеспечивается ДНК-полимеразой («машиной, копирующей ДНК»), которая по мере продвижения вдоль матричной ДНК-цепи проверяет, нет ли ошибок во вновь синтезированной копии. О наличии ошибок она «узнает» по искажению двойной спирали ДНК, которое имеет место, если Т соединится с G или С с А. Обнаружив такой участок, ДНК-полимеразный ферментный комплекс вырезает неправильное основание (или группу оснований) и вставляет то, которое должно быть на этом месте (законное основание). Скорость точной репликации у бактерий примерно 500 оснований в секунду, а у высших клеток (включая клетки человека) около 50 оснований в секунду. ДНК хромосом высших клеток много длиннее, а сами хромосомы устроены намного сложнее, чем маленькие и простые бактериальные геномы. У высших клеток, в отличие от бактерий, ДНК в хромосомах образует комплекс с белками (гистонами), которые участвуют в сворачивании длинных нитей ДНК в серию петель, для того чтобы их можно было упаковать внутри ядра. Репликация ДНК начинается одновременно в нескольких сайтах (точках) каждой хромосомы, поэтому большой набор ДНК-последовательностей реплицируется за 5—20 ч.
Рис. 5.2. Частота ошибок при синтезе ДНК и РНК. Примечание: о частоте ошибок судят по частоте включения неправильного основания на одно основание за одно событие копирования (см. также рис. 2.4); дц = двухцепочечная, оц = одноцепочечная.
Вспомним, что в гл. 2 мы уже обсуждали высокий уровень ошибок при образовании РНК по матрице ДНК (транскрипции) и при образовании ДНК по матрице РНК (обратной транскрипции). Оба этих типа копирования характеризуются частотой точковых мутаций Ю-3—Ю-4, что существенно выше, чем частота ошибок при репликации ДНК (от Ю-8 до Ю-9). Неточность, большое число ошибок имеют место и при репликации генома РНК-содержащих вирусов, например, вируса гриппа. Этим объясняется быстрое генетическое изменение вируса, приводящее к пандемиям гриппа. В жизненном цикле вируса СПИДа (ВИЧ) чередуются неточные процессы копирования РНК -> ДНК (на стадии интеграции) и ДНК -> РНК (на стадии экспрессии в течение инфекционного цикла). Для этого вируса также характерна высокая частота мутаций. Таким образом, все процессы копирования, включающие одноцепочечные РНК-посредники (превращение РНК в ДНК и наоборот), идут с большим числом ошибок, при этом репарация последовательности невозможна, поскольку ферменты, осуществляющие такое неточное копирование полинуклеотидов (РНК-полимераза, обратная транс -криптаза и РНК-репликаза), как оказалось, не имеют функций проверки и исправления ошибок.
Все сказанное выше означает, что какая-то доля мутаций в ДНК может возникать в результате ошибок копирования, включающего промежуточные РНК-посредники (рис. 5.2).
Мутации, которые передаются потомкам, появляются с низкой частотой. Они возникают в половых клетках и называются генеративными. Это редкие ошибки, которым удалось ускользнуть от «проверок» ДНК-полимеразы во время репликации ДНК и упаковки ее в гаметы самцов и самок (сперматозоиды и яйцеклетки). Они могут вызывать дефекты (т. е. влиять на фенотип и состояние здоровья индивида). Например, в случае серповидцоклеточной анемии такая мутация обуславливает тяжелую патологию у гомозигот (у которых обе копии гена дефектны) и более легкую форму болезни у гетерозигот, потому что белковый продукт нормальной копии гена частично компенсирует отрицательный эффект дефектной копии.
Однако существуют варианты некоторых генов (альтернативные формы генов называют аллелями), которые не влияют на здоровье индивида, у которого они проявляются. Эти варианты составляют нормальную изменчивость в популяциях организмов, существующую, по предположению Дарвина, до того, как начинает действовать естественный отбор. Важный вопрос: как появляются эти «добрые» аллели?. Согласно неодарвинистским представлениям, все эти аллели возникли в результате случайных мутаций в ДНК зародышевой линии и сохранились в популяции (так называемом «пуле генов») вследствие естественного отбора. В гл. 7 мы постараемся дать альтернативное объяснение этого феномена в рамках теории обратной связи соматических и половых клеток.
Предполагают, что рост числа врожденных аномалий и спонтанных абортов вызван факторами окружающей среды, такими как загрязнение токсическими химическими веществами. Например, резкое повышение частоты врожденных аномалий зарегистрировано в городах, расположенных вокруг сильно загрязненного, гибнущего Аральского моря. Такие же данные имеются относительно ветеранов вьетнамской войны и жителей северного Вьетнама, подвергшихся воздействию токсичных дефолиантов. Вещества, которые действуют на гены, изменяя кодирующую ДНК-последовательность, называются мутаге-нами. Возможно, их действие основано на том, что они нарушают нормальный процесс репарации. Установлено, что в клетках бактерий и эукариот, в которых индуцировано большое число повреждений ДНК, включается склонная к ошибкам репарация.
Теория соматических мутаций
Многоклеточный организм состоит из сотен миллионов клеток, некоторые из них непрерывно и быстро делятся. Например, у человека и других позвоночных все клетки крови обновляются со скоростью десять миллионов в день. Эпителиальные клетки кожи и слизистых (пищеварительного тракта и носоглотки) ежедневно образуют миллионы дочерних клеток, замещающих израсходованные, т. е. те клетки, которые слущиваются с эпителиальных поверхностей. Во внутренних органах (сердце, печени, почках и мозге) скорость замещения клеток низкая. Нейроны (нервные клетки) у взрослого человека не делятся вообще. При делении клетки ДНК в ядре удваивается, образуются копии всех хромосом, которые передаются дочерним клеткам. Если это происходит в большом числе клеток, надо ожидать появления какого-то числа соматических мутаций (несмотря даже на то, что частота мутаций при репликации ДНК низка). Следовательно, у крупных многоклеточных животных соматические мутации будут появляться все время, особенно в тех клеточных популяциях или тканях, где скорость замещения клеток очень высока.
Все виды злокачественных опухолей вызваны соматическими генными мутациями, которые делают клетки невосприимчивыми к сигналам, ограничивающим их рост или вызывающим гибель; такие клетки начинают «жить своей собственной жизнью». Они могут мутировать дальше, становясь локально агрессивными или давая начало метастазам. Наглядный пример последствия соматических мутаций — кожные формы рака. Они возникают из единичной мутантной клетки при ее делении. Клон клеток, подобно колонии плесневых грибов на черством хлебе, растет на ограниченном участке кожи. Наиболее злокачественная форма рака кожи — меланома (пигментированная опухоль). Сейчас известно, что ее образование провоцирует ультрафиолетовое излучение солнца.
Соматические мутации, приводящие к раку, как и мутации, неблагоприятно действующие на функции важных структурных белков и ферментов, несомненно вредны. Мы кратко рассказали о них, чтобы показать контраст с полезными мутациями, которые происходят в генах вариабельных областей антитела, и подчеркнуть исключительность процесса контроля/отбора в мутантных В-лимфоцитах. Теперь повторим наши ключевые вопросы и попытаемся установить возможные биологические механизмы, обеспечивающие эти процессы.
Сейчас известно, что в ходе иммунного ответа в перестроенных V(D)J-генax соматические мутации возникают с высокой частотой. В отобранных антигеном В-клетках частота мутаций V(D)J-генов составляет примерно 1/1000 — 1/10000 оснований на репликационное событие. Это в миллионы раз выше, чем частота мутирования генов, передающихся с половыми клетками. Мутантные V-области антитела появляются через 5—10 дней после воздействия антигена. Считается, что увеличение аффинности (сродства к антигену) антитела основано на соматическом мутировании и отборе в течение иммунного ответа (рис. 3.8). Несмотря на то, что молекулярные механизмы мутационного процесса в соматических клетках иммунной системы активно исследуются во многих лабораториях мира, включая и лабораторию Теда Стила и Боба Бландэна, еще остаются вопросы, требующие объяснения. Может ли биологическая система обеспечивать полезность соматических мутаций (например, удаляя вредные мутации, но сохраняя полезные)? По нашему мнению, ответ на этот вопрос — да, может. Иммунная система выработала два тесно связанных процесса — соматического мутирования и отбора наиболее приспособленных, которые обеспечивают животным потенциальные преимущества.
Тонкая структура вариабельной области -структуры Ву-Кэбота
Прежде, чем перейти к молекулярным и клеточным деталям процесса соматического мутирования, надо описать тонкую структуру вариабельной области, которая образует антигенсвязывающий центр антитела (ТкР имеют сходную структуру).
Почти 30 лет назад Элвин Кэбот (Kabat) с коллегами начали определять аминокислотные последовательности вариа-бельных областей антител человека. По мере того как накапливалась информация, Т. By (Wu) и Э. Кэбот смогли сравнить последовательности вариабельных областей тяжелых и легких цепей и построить график изменчивости аминокислот в каждом положении белковой цепи. Их результат, который называется графиком Ву—Кэбота, приведен на рис. 5.3. На этом графике выявляется три гипервариабельных участка, другие участки называются каркасными (FR, от англ. framework region). Гипервариабельные участки образуют поверхность, которая вступает в тесный контакт с поверхностью антигена. Каркасные участки составляют структурный скелет, или остов, V-областей антигенсвязывающего центра. В зависимости от природы антигена, поверхность антитела может быть разной: от относительно плоской с небольшими углублениями или выступами до глубоких «карманов», которые вмещают выступы поверхности антигена. Поверхность антитела высокой аффинности комплементарна поверхности антигена.
Рис. 5.3. График Ву-Кэбота.
График Ву—Кэбота показывает, что гипервариабельные участки вариабельной области Н- и L-цепей антител совпадают с антигенсвязываю-щими центрами, названными участками, определяющими комплементарность
В большом наборе антител человека разной специфичности относительную вариабельность рассчитывают для каждой из 100 позиций аминокислот вариабельной области тяжелых и легких цепей. Этот график показывает, что вариабельность не одинакова — выявляются три участка гипервариабельности (HV), между ними расположены участки с меньшей вариабельностью, названные каркасными сегментами (FR). Известно, что HV-участки совпадают с теми районами белковой цепи, которые вступают в непосредственный контакт с эпитопами антигена. Эти участки называются участками, определяющими комплементарность, или CDR. Нумерация начинается с левого конца молекулы (рис. 3.2), так что CDR3 расположен рядом с константной областью. Высоко неслучайная картина вариабельности, продемонстрированная By и Кэботом, свидетельствует о том, что вариабельные последовательности подвергаются положительному дарвиновскому отбору связыванием антигеном на уровне HL-гетеродимеров. Семейство V-генов всех позвоночных дает картину вариабельности Ву—Кэбота. См. табл. 3.1 и 5.1. (По J. Kuby. Immunology, 3rd edition. W. Н. Freeman & Co., 1997. Перепечатано с разрешения издателя. Основано на Е. A. Kabat et al. 1977. Sequence of Immunoglobulin Chains, US Department of Health Education and Welfare.)
Рис. 5.4. Соматическое мутирование и отбор мутантных клеток в центре размножения.
После отбора антигеном циркулирующей В-клетки активированная клетка будет или активнее секретировать антитело, или станет клеткой-основателем в центре размножения, где происходит мутирование V(D)J-reHOB вариабельной области. Антитела, образованные в начале ответа, формируют комплексы антиген — антитело, которые связываются с поверхностью фолликулярных дендритных клеток (ФДК). Эти анти-генпрезентирующие клетки образуют в центре размножения широкую мембранную сеть. После фазы быстрой пролиферации клеток (В-центробластов) меньшие по размеру неделящиеся В-центроциты проверяют свое мутантное антитело на связывание с антигеном, проявляющимся на ФДК. Если мутантное антитело не функционально или имеет низкую аффинность, клетка погибнет вследствие программированной гибели (апоптоза). Если у мутанта более высокая аффинность, чем у антитела, связанного с антигеном на поверхности ФДК, он вытесняет это антитело и связывает антиген. Это дает сигнал В-клетке, защищающий ее от гибели. Отобранная мутантная В-клетка покидает центр размножения и становится или плазматической клеткой (образующей и секретирующей антитела высокой аффинности), или долгоживущей клеткой памяти. Соматические мутанты данной У(0)и-последовательности аминокислот, проанализированные как на рис. 5.3, дают структуру By—Кэбота, свидетельствующую о том, что вариабельные области антител отбираются связыванием антигеном. (Перепечатано из Steele E. J. et al. Immuno-logical Reviews, vol. 135: 5-49,1993 с разрешения издателя Munksgaard International Publishers, Copenhagen.) Примечание: Ат — антитело, Аг — антиген, СЗb — активированный белок крови, который связывает Ат-Аг комплекс.
График Ву—Кэбота, следовательно, можно считать распределением аминокислот в вариабельных областях «успешных» антител, которые хорошо связываются с антигеном. В более поздних работах был построен график By—Кэбота для антител, которые возникли в результате соматических мутаций одной V-последовательности зародышевой линии в ответ на один антиген. Этот график ясно показывает, что изменчивость, появляющаяся в вариабельной области антитела, не случайна.
Если для какого-то набора данных о последовательностях аминокислот вариабельной V(D)J области антитела получен график, подобный приведенному на рис. 5.3 (мы будем называть его структурой By—Кэбота), можно считать, что есть серьезные указания на антигенсвязывающий отбор HL-гетеродиме-ров антитела. Другими словами, структура By—Кэбота (наличие на графике пиков изменчивости в районах контакта с антигеном) является показателем того, что изменчивость аминокислотных последовательностей в изучаемой популяции V(D)J-no-следовательностей создана антигенсвязывающим отбором. Мы вернемся к этому важному заключению в следующей главе, когда попытаемся объяснить, почему структура By—Кэбота наблюдается в популяциях неперестроенных V-элементов половых клеток.
Напомним (рис. 4.5), что полный ген вариабельной области является соматической конструкцией из V-, D- и J- элементов в тяжелой Н-цепи и V- и J-элементов в легкой L-цепи, соединенных в результате перестройки ДНК в В-клетках. Два участка гипервариабельности закодированы в V-элементе зародышевой линии, а третий, который затрагивает соединенные V-D-J или V-J перестройки, никогда не обнаруживается в зародышевой линии позвоночных, хотя есть исключения — у хрящевых рыб (скатов, рогатых акул) и V-псевдогенов курицы. Третий гипервариабельный участок очень важен для распознавания антигенов. Антитело, у которого нет этого участка (имеющее только два кодируемых в зародышевой линии гипервариабельных участка), не способно связывать антиген. Следовательно, V-гены зародышевой линии не могут подвергаться прямому дарвиновскому отбору. Отбор опосредован и должен затрагивать V-D-J-и V-J-перестройки, которые происходят только в соме.
Центр размножения: соматическое гипермутирование перестроенных V(D)J-генов
Все имеющиеся данные говорят о том, что в В-лимфоцитах мутируют только перестроенные V(D)J-гены, кодирующие белок антитела. Другими словами, вариабельные гены, остающиеся в конфигурации зародышевой линии, т. е. неперестроенными, не накапливают соматических мутаций. Следовательно, первым этапом контроля, позволяющим появляться только «благоприятным мутациям», является перестройка ДНК, в результате которой образуется V(D)J-мишень, на которую действует мутатор. Следующий этап контроля — это сама мутационная машина, которая должна связываться с уникальной структурой, ассоциированной с перестроенной V(D)J-последовательностью и ограничивающей мутирование только этим участком ДНК.
Надо отметить еще один важный момент. Процесс соматического гипермутирования у мышей и человека вызван стимуляцией антигеном. У других видов (например, овцы) соматический мутагенез в специализированных лимфоидных тканях, связанных с кишечником, включается другими сигналами (они пока неизвестны). Таким образом, изменчивость V(D)J-генов лимфоцитов вызвана влиянием окружающей среды или адаптивным сигналом. Это означает, что в ходе развития иммунной системы организма генетическая изменчивость может быть вызвана средой. Это противоречит неодарвинистской догме о том, что вся изменчивость генов зародышевой линии предсуществует до того, как начинает действовать отбор. Решающий эксперимент, доказывающий этот важный момент, был проведен Урсулой Сторб (Storb) с коллегами в середине 1980-х гг. Авторы ввели ограниченное число копий известного перестроенного гена легкой цепи (VJ) в ДНК зародышевой линии инбредных мышей (такие животные называются трансгенными). Им удалось показать, что у неиммунизированных трансгенных мышей VJ-трансген не мутировал: последовательность нуклеотидов этого участка ДНК, выделенного из В-лимфоцитов селезенки трансгенных мышей, не изменилась. Однако при иммунизации антигеном, который связывает антитела, кодируемые этой VJ-последовательностью, VJ-трансген накапливал многочисленные соматические мутации.
Где происходят соматические мутации? Могут ли они возникать в подвижных В-клетках в крови и лимфе, или они происходят в каких-то особых местах? В середине 1980-х гг. Дэвид Грей (Gray) и Йан Макленнан (MacLennan), работающие в Университете Бирмингема, предположили, что соматические мутации происходят в специализированных постантигенных образованиях, называемых центрами размножения. Такие участки интенсивного деления (пролиферации), появляющиеся после стимуляции антигеном в лимфатических узлах и селезенке, давно известны. Также было известно, что 80% В-клеток в центре размножения (или даже больше), по-видимому, там же и погибают. В 1960-х гг. Гас Носсал (Nossal) и Гордон Эйда, работающие в Медицинском центре Уолтера и Элайзы Холл, используя радиоактивно меченные белковые антигены установили, что недеградированные формы антигена, связанные с антителами, располагаются на поверхностной мембране клеток в центре размножения (и могут оставаться там в течение многих месяцев). Комплексы антиген—антитело располагаются на поверхности крупных специализированных клеток, выросты клеточной мембраны (дендритные выросты) которых распространяются по всему центру размножения. Эти клетки называются фолликулярными дендритными клетками (ФДК).
Фолликулярные дендритные клетки в центре размножения взаимодействуют с популяцией В-клеток (рис. 5.4). Грей и Макленнан предположили, что соматические мутации возникают в быстро делящихся В-клетках центра размножения. «Успешные» мутанты, способные связываться с антигеном и конкурировать за его молекулы, которые проявляются в комплексе антиген—антитело на ФДК, выживают, остальные гибнут. В то время это было очень смелое предположение, объясняющее созревание аффинности. В нем объединялись быстрое соматическое мутирование и связанный с антигеном процесс отбора, спасающий от гибели тех мутантов, которые успешно конкурируют за антиген на ФДК в силу высокой аффинности нового мутантного антитела.
За пять лет группа под руководством Гарнета Келсо, Клауса Раевского (Rajewsky) и Клаудии Берек (Berek) доказала правильность некоторых предсказаний Грея-Макленнана. Оказалось, что соматические мутации перестроенных V(D)J-генов действительно происходят в В-клетках центра размножения. Келсо и Раевский пошли еще дальше, продемонстрировав, что в делящихся В-клетках, которые не были в центре размножения, V(D)J-участок не мутирует. Это означает, что критический сигнал, активирующий «мутатор», находится в центре размножения. Примерно в то же время Йан Макленнан и его группа установили, что, если у потомков В-клетки особой обработкой вызвать сшивки мутантных Ig-молекул (этот процесс имитирует связывание антигена), то такие клетки не умирают.
Итак, к 1991 г. центры размножения представлялись как участки лимфоидной ткани, в которых активно идет соматическое гипермутирование — регулируемый процесс, связанный с анти-гензависимым отбором. Мы хотим подчеркнуть, что центр размножения и у человека, и у мыши развивается только в результате развития иммунного ответа на чужеродный антиген. Важнейшие события, происходящие в центрах размножения, приведены на рис 5.4.
Экспериментальные данные позволяют воссоздать картину возникновения центра размножения во времени и пространстве. В кровотоке в результате связывания с чужеродным антигеном происходит отбор В-клетки. После этого она мигрирует в лимфоидные зоны селезенки или лимфатических узлов. Затем, получив особый сигнал от хелперной Т-клетки, она начинает делиться. Эти активированные В-клетки продуцируют антитела, которые образуют комплексы антиген-антитело на поверхности фолликулярных дендритных клеток (ФДК). Несколько потомков исходной отобранной В-клетки заселяют особые участки лимфоидной ткани, содержащие ФДК, которые называются первичными фолликулами. Одна или несколько из этих клеток-основателей начинают быстро делиться (на рис. 5.4 они названы В-центробластами); на их поверхности нет антител.
Фаза пролиферации (деление клеток каждые пять-семь минут в течение примерно пяти дней) приводит к образованию популяции численностью порядка 20 тысяч дочерних клеток, которые называются центроцитами. Они прекращают деления, и на их поверхностной мембране снова появляются антитела. На каком-то этапе образования популяции центроцитов происходит гипермутирование перестроенных V(D)J-генов. Теперь центр размножения созрел, и сложная постантигенная структура содержит В-центроциты, хелперные Т-клетки и ФДК. Последние образуют развитую сеть комплексов антиген—антитело, включающих антитела, синтезированные в первые дни ответа (см. рис. 5.4).
Затем, по-видимому, происходят следующие события. Во-первых, тысячи центроцитов составляют гигантский репертуар клеток, поверхностные антитела которых кодируются соматическими мутациями. Большинство этих антител (примерно 80%) не способны связывать антиген. Как и для любых других белков, большинство мутаций приводит к изменению формы антитела, а это нарушает соответствие форме антигена. Однако некоторые редкие мутации могут приводить к антителам, лучше соответствующим форме антигена, чем исходные (т. е. с более высокой аффинностью). Новые антитела расположены на поверхности В-центроцитов и могут конкурировать за молекулы антигена, расположенные в комплексах антиген—антитело на поверхности фолликулярных дендритных клеток. Однако для того, чтобы успешно конкурировать с антителом из комплекса (образованным в первые дни ответа), новое мутантное антитело должно иметь ту же или большую аффинность. Вот суть механизма созревания аффинности — конкурентный антигенсвязы-вающий отбор. Центр размножения — это недолговечный «орган селекции и разведения» V(D)J-генов, где выживают только наиболее приспособленные В-клетки. Неудачные (с низкой аффинностью, нефункциональные) мутантные В-клетки (а их большинство) исчезают в результате запрограммированной клеточной гибели, которая называется апоптозом.
Итак, клональная селекция В-клеток происходит в два этапа. На первом чужеродный антиген отбирает В-лимфоцит из популяции разнообразных клеток. Затем эти В-центробласты быстро делятся, образуя популяцию в 20 тысяч новых В-клеток, имеющих мутантные вариабельные V(D)J-области. На втором этапе мутантные линии В-клеток с высокой аффинностью отбираются антигеном, выживают, делятся и секретируют антитела высокой аффинности или становятся долгоживущими клетками памяти. В этом нет ничего мистического. Это традиционный дарвиновский отбор, действующий в большой изменчивой клеточной популяции, из которой выживают немногие — только те, которые продуцируют мутантные антитела с наивысшей аффинностью к антигену. Центр размножения, следовательно, — котел, в котором «варится» генетическая гипервариа-бельность. Однако все процессы в нем строго регулируются и контролируются. V(D)J-гены (только эти гены, а не другие) В-лимфоцитов мутируют в высоко специализированной и регулируемой среде центра размножения.
До сих пор мы подчеркивали значение дарвиновского естественного отбора в иммунной системе. Однако мы ввели и определенно неоламаркистскую идею, а именно, роль сигнала внешней среды (антигена) в создании генетического разнообразия, на которое действует естественный отбор. Может ли этот ключевой эволюционный вывод вызвать такие же споры, которые были вызваны идеей «разнообразия, вызванного антигеном», впервые предложенной Элистэром Каннингемом в середине 1970-х гг.?
Подтверждение факта соматического мутирования, вызванного антигеном
Примерно 25 лет назад Элистэр Каннингем, работающий в Центре медицинских исследований Джона Куртина в Канберре, впервые высказал идею о соматическом мутировании вари-абельных генов антител, вызванном антигеном. Он также первым провел эксперименты, демонстрирующие это явление. Примерно в то же время исследовательские группы Мелвила Кона (Институт Салк, Сан-Диего, США) и Сусуми Тонегавы (Базельский институт иммунологии, Швейцария) получили молекулярные доказательства существования соматического мутирования (путем анализа последовательностей белка и ДНК). Оба эти открытия были сделаны в разгар споров между сторонниками идеи соматического разнообразия и идеи разнообразия, закодированного в зародышевой линии. Самая первая гипотеза о молекулярном механизме соматического мутирования Сиднея Бреннера и Цезара Мильштейна (Кэмбриджский университет, Англия) подразумевала существование некоего склонного к ошибкам типа репликации ДНК. Предполагалось, что высоко точное копирование матрицы ДНК нарушается при репликации генов вариабельной области антител. (Это нарушение объяснялось неспособностью ДНК-полимера-зы в данном случае исправлять ошибки.) Таким образом, первые модели соматического мутирования основывались на репликации ДНК и делении клетки: так как активированные антигеном В-клетки быстро делятся, появляются мутанты, у которых изменена ДНК, кодирующая вариабельную область.
Подобно всем новым научным гипотезам, экспериментам и интерпретациям пионерская работа Элистэра Каннингема вызвала споры. Однако к 1981 г. поток публикаций из лабораторий Патрисии Гирхарт (Gearhart), Урсулы Сторб, Эла Ботуэлла (Bothwell), Лероя Худа (Hood), Дэвида Балтимора и Клауса Раевского подтвердил правильность основного предположения Каннингема. Было показано, что у мышей мутации в ДНК-последовательности перестроенного V(D)J-reHa вариабельной области появляются после стимуляции антигеном. Дальнейшие доказательства были получены в новых экспериментах с трансгенными мышами.
Все эти работы стали возможными благодаря разработке в 1975 г. методов «гибридомы» и «моноклональных антител». За создание этих методов Георг Келер и Цезар Мильштейн получили в 1983 г. Нобелевскую премию (совместно с Нильсом Ерне). В этих методах используется слияние раковой клетки (способной расти и неограниченно делиться в культуре) с индивидуальной В-клеткой иммунизированного животного. Гибридная клетка продуцирует антитело В-клетки и приобретает бессмертие раковой клетки. Такие гибридомы позволили экспериментально показать существование клонов В-клеток, предсказанное клонально-селекционной теорией Бернета, причем все потомки одной клетки имеют одинаковые V(D)J-гeны и, таким образом, производят одинаковые антитела. Клон гибридомных клеток дает возможность сравнить ДНК-последовательности соматически перестроенного V(D)J-гена В-клеток и последовательности V-элемента зародышевой линии. Во многих случаях было показано, что В-клетки, изолированные после стимуляции антигеном, накапливают много соматических мутаций в том участке V-элемента, который кодирует последовательность аминокислот от 1-й до примерно 85-й позиции и включает первые два гипервариабельных участка (см. рис. 5.3). Эти данные соответствуют предположению об отборе антигеном в центрах размножения. Частота соматических мутаций очень высока: ДНК-последовательность, включающая перестроенный V(D)J-ген, накапливала изменения, которые отличались от немутантной последовательности зародышевой линии примерно по 5 процентам оснований.
Как мутации распределены по участку-мишени?
Нам известно, что соматические мутации локализованы в короткой ограниченной области ДНК В-клетки. Экспериментальные данные суммированы на рис. 5.5, где показаны перестроенный VDJ-ген тяжелой цепи в начале реакции в центре размножения и та же последовательность через семь и четырнадцать дней. Обратите внимание, что доля мутаций, по-видимому, увеличивается со временем, и что мутации ограничены ближайшим окружением перестроенного VDJ-гена и некодирующими фланкирующими (расположенными по краям) ДНК-последовательностями. Их не находят около промоторного сай-та, с которым связывается РНК-полимеразный ферментный комплекс и с которого начинается (инициируется) копирование мРНК по матрице ДНК (в кэп-сайте, обозначенном на рисунке маленькой витой стрелкой выше лидерного L-кодирующего участка). Не обнаруживаются они и за участком, который, по нашим предположениям, является «локус-специфичным устройством» (Ei/MAR, intronic Enhancer/Matrix Attachment Region).
В самом VDJ-кодирующем участке мутации, обнаруженные в коллекции последовательностей антител высокой аффинности, распределены не случайно, они демонстрируют «структуру Ву-Кэбота». Таким образом, точковые мутации, которые приводят к замене аминокислоты, накапливаются в гипервариабельных участках (или тех областях белка, которые формируют антигенсвязывающий центр). «Молчащие» точковые мутации (те изменения внутри кодона, которые не приводят к замене аминокислоты, см. приложение) накапливаются в консервативных каркасных участках. Наблюдаемые структуры Ву—Кэ-бота (рис. 5.3) означают, что мутантные антитела подвергаются антигенсвязывающему отбору.
Рис. 5.5. Схема, показывающая, что перестроенный V(D)J-reH и соседние фланкирующие участки ДНК служат мишенью для мутатора.
Изображена тяжелая цепь человека или мыши. Картина мутаций для главного семейства легких цепей (капла-цепей) у человека и мыши одинакова. На рисунке показано, что среди У(0)и-последовательностей, выделенных в позднем иммунном ответе (15 дней после воздействия антигена), выявляется большая доля соматических мутаций. Обратите внимание, что соматические точковые мутации расположены в участке, начинающемся недалеко от точки начала синтеза мРНК (транскрипции) и заканчивающемся в районе J-C-интрона около Ei/MAR. Также обратите внимание, что районы промотора (Р) выше VDJ и ниже константной (С) области не мутируют. Предполагается, что Ei/MAR является локус-спе-цифическим устройством, с которым стыкуется мутаторная машина; Х — точковая мутация, кэп — начало синтеза мРНК; т. п. н.— тысяч пар нуклеотидов. Участки, кодирующие белок, показаны прямоугольниками. Дополнительная информация в табл. 5.1 и на рис. 2.6, 4.5 и 5.1.
Такое распределение иллюстрирует две ключевые черты соматического гипермутирования. Разделение ДНК-последовательностей, кодирующих вариабельные (V) и константные (С) области, дает то эволюционное преимущество, что разрешаются мутации в V-генах, но сохраняются неизменными С-гены. То, что механизм соматического мутирования ограничен только перестроенным V(D)J-геном и не затрагивает гена С-области, особенно важно для тяжелых цепей. Они образуют ту часть молекулы антитела, которая определяет ее функциональные свойства, такие как лизис бактериальных клеток, поглощение и разрушение инфекционных агентов фагоцитами, сигналы В-клеткам к делению и продукции антител, процессы, приводящие к стимуляции Т-клеточной помощи В-клеткам. Для легких цепей этого не требуется, потому что константная область легкой цепи не выполняет этих функций.
Второй принцип, показанный на рис. 5.5, — мутации не распространяются вверх от гена. 5'-граница находится вблизи сайта начала транскрипции или лидерного интрона (некодирующая последовательность между L- и V-кодирующими участками, рис. 4.5). Тому есть очень важная причина, так как в этом участке находятся регуляторные последовательности (промоторный, или Р-район), которые определяют связывание РНК-полимеразного комплекса, инициацию транскрипции и образование мРНК.
Важно отметить, что мутации сосредоточены только там, где они не изменяют ни С-областей, ни Р-районов, которые контролируют экспрессию гена. Как достигается такое точное прицеливание?
Механизм соматического гипермутирования V(D)J-генов
Распределение мутаций, показанное на рис. 5.5, и известные уровни ошибок копирования молекул РНК (см. рис. 5.2) были двумя основными фактами, которые привели в 1987 г. Теда Стила и Джеффа Полларда (Pollard) к созданию «модели обратной транскриптазы» для объяснения механизма соматического гипермутирования (для краткости — КТ-модель). Эта идея родилась на год раньше в феврале в Волонгонге и была сформулирована летом 1986 г., когда Тед и Джефф встретились в Нью-Йорк Сити. (К этому моменту оба считали, что поняли почти все, и решили опубликовать свою идею.) Тед считал, что RT-модель следует из теории соматического отбора. Однако аргументы Боба Бландэна убедили Теда, что RT-модель соматического гипермутирования по смыслу должна предшествовать теории соматического отбора. (Также она должна предшествовать и в эволюционном смысле — соматические мутации небольшого начального набора V-генов зародышевой линии должны происходить до передачи информации V-генов от сомы к зародышевой линии. Этот гносеологический поворот на самом деле упрощает интерпретацию данных о ДНК-последовательностях, особенно касающихся генетической рекомбинации V-генов зародышевой линии (см. обсуждение следов интеграции сомы в зародышевую линию и рис. 6.3)
С 1986 г. работа над гипотезой обратной транскрипции продолжалась в нашей лаборатории с участием Джерри Бота (Both) и Гарри Ротенфлу (Rothenfluh). Сейчас мы можем привести детальную теоретическую молекулярную модель соматического гипермутирования в В-клетках: она включает неточную, склонную к ошибкам обратную транскрипцию и возврат генов в ДНК зародышевой линии (рис. 5.6). Эта модель согласуется с подавляющим большинством экспериментальных результатов, касающихся соматического гипермутирования. Ее можно распространить на молекулярные механизмы, которые приводят к соматическому разнообразию перестроенных V(D)J-генов вариабельных областей у кур, до сих пор называемые генной конверсией. Однако мы должны подчеркнуть, что до тех пор, пока все молекулярные детали не будут экспериментально обоснованы, наша модель останется гипотезой, хотя и совместимой со всеми доступными данными.
Мы предположили, что молекулярной машиной, которая с высокой частотой вызывает мутации перестроенной ДНК V(D)J-гена, должна быть «RT-мутаторсома» (RT — обратная транскриптаза). Существует много молекулярных органелл с суффиксом «сома», например «рибосома» (комплекс белков и РНК, необходимый для трансляции информационной РНК в последовательность аминокислот, см. приложение) и «сплай-сосома» (также РНК-белковый комплекс, который вырезает интроны из про-мРНК). Итак, гипотетическая RT-мутатор-сома использует несплайсированную про-мРНК как матрицу для синтеза кДНК. Термин кДНК, где «к» обозначает комплементарная — общий термин для всех ДНК-копий РНК-матрицы, созданных обратной транскриптазой (кДНК также называют «обратными транскриптами» или «ретротранскриптами».
Мы предположили, что обратная транскрипция, которая создает мутантную кДНК-копию перестроенного V(D)J-yчастка, начинается в особом районе, в «праймерном» сайте ниже V(D)J около Ei/MAR участка (рис. 5.6), и продолжается справа налево по направлению к кэп-сайту (5'-конец про-мРНК матрицы). Цезар Мильштейн с коллегами экспериментально показали на трансгенных мышах, что «локус-специфическое устройство», Ei/MAR, важно для соматического гипермутирования, тогда как V(D)J-кодирующий участок и промотор можно заменить копиями гемоглобинового гена без ущерба для мутации. Мы считаем Ei/MAR «локус-специфичным устройством», необходимым для стыковки RT-мутаторсомы с V(D)J-геном и ограничения мутаций этим геном. (В настоящее время мы экспериментально проверяем это предположение.) Мы также считаем, что мутантная кДНК-копия V(D)J-yчастка встраивается в хромосому и замещает исходный, немутированный V(D)J (на рисунке это показано петлеобразной стрелкой.). Возможность подобной генетической интеграции экспериментально продемонстрирована у многих организмов и называется гомологичной рекомбинацией, так как похожие ДНК-последовательности совмещаются, а за этим следует рекомбинация ДНК. Указанные предположения гарантируют, что участки выше промотора и ниже константного участка защищены от мутаций, а некодирующая ДНК в непосредственном соседстве с V(D)J мутирует с очень высокой частотой (тот же уровень ошибок, что и при транскрипции и обратной транскрипции — примерно 10-3—10-4 на цикл копирования пар оснований, рис. 5.2)
Таким образом, правила копирования ДНК- или РНК-матриц и склонные к ошибкам процессы синтеза РНК и кДНК полностью удовлетворяют «требованиям» соматического мути-рования. Существует единственное направление, в котором могут синтезироваться ДНК-копии по матрице про-мРНК — обратно к сайту начала транскрипции (кэп-сайту). Если синтез кДНК начинается в Ei/MAR-участке или рядом с ним, это автоматически обеспечит мутирование V(D)J без риска мутирова-ния промотора и константного участка. Для того чтобы «обессмертить» мутантную последовательность в организме, потребуется гомологичная рекомбинация для встраивания мутант-ной кДНК-копии в хромосомную ДНК, что обеспечит передачу ее последующим поколениям дочерних клеток.
У мышей 5', или верхняя, граница мутаций находится около кэп-сайта для Н цепей и в L-V интроне для легких цепей (рис. 5.5). Расположение этих сайтов согласуется с двумя главными точками, где заканчивается синтез кДНК, а) когда обратная транскриптаза подходит к 5'-концу матрицы про-мРНК, или б) около L-V-интрона, так как интрон может быть удален при сплайсинге, который превращает про-мРНК в мРНК.
Данные о соматическом мутировании не соответствуют традиционной модели, основанной на ДНК, но предсказываются RT-моделью
Какие еще данные свидетельствуют в пользу RT-модели и отличают ее от других мутационных моделей, которые мы определяем как «основанные на ДНК» (они зависят от локального склонного к ошибкам синтеза ДНК вблизи перестроенного V(D)J-участка)? Прежде всего, одно общее соображение: нет доказательств существования механизма, который избирательно прекращает синтез ДНК. Однажды начавшись, синтез продолжается до тех пор, пока не достигнет конца матрицы. Таким образом, для подтверждения таких моделей потребовалось бы придумать и экспериментально доказать особые правила синтеза ДНК.
Есть еще две группы данных, которые не соответствуют моделям, основанным на ДНК, но которые предсказываются RT-моделью. Они получены в лабораториях Патрисии Гир-харт и Эрика Сейсинга (Seising). В одних экспериментах сразу ниже перестроенного V(D)J-участка (между VDJ и J на рис. 5.6) была помещена так называемая «репортерная» последовательность. Оказалось, что эта последовательность подавляла появление мутаций в VDJ-участке. Такой результат несовместим с моделями, основанными на ДНК, но согласуется с RT-моделью. Действительно, репортерная последовательность — короткий участок ДНК, кодирующий транспортную РНК (тРНК), которая складывается в характерную трехмерную форму (транспортные РНК участвуют в синтезе белка, они переносят аминокислоты). Согласно RT-модели, синтез кДНК должен остановиться до V(D)J-участка, поскольку обратная транскриптаза не может продолжить движение через тРНК-структуру. Два других свойства тРНК также могут прекратить обратную транскрипцию. Первое, последовательность тРНК могла высвободиться из про-мРНК и, таким образом, РНК-матрица, по которой RT-мутаторсома копирует РНК в кДНК, обрывается. Второе, химическая модификация азотистых оснований в тРНК может подавлять синтез кДНК RT-мутаторсомой.
Рис. 5.6. RT-мутаторсома. Изображена тяжелая цепь человека или мыши. Предполагается, что RT-мутаторсома работает одинаково у человека и мыши в случае главного семейства легких цепей (таппа-цепей). События копирования и рекомбинации, изображенные на рисунке, происходят в ядре мутирующей В-клетки. Локус-специфическое устройство (Ei/MAR) стыкуется с RT-мутаторсомой. Поэтому обратная транскрипция матрицы про-мРНК начинается выше Ei/MAR, но ниже V(D)J. Это достигается благодаря тому, что все синтезы нуклеиновых кислот (или полинуклеотидов) всегда идут в направлении 5'— 3'. Значит, все копируемые матрицы должны иметь антипараллельную ориентацию 3'—5'. Матричная цепь ДНК для синтеза РНК — это 3'—5'-цепь. В кэп-сайте (cap site) начинается синтез про-мРНК, и, поскольку это склонный к ошибкам процесс, очень велика вероятность того, что транскрибированная копия V(D)J-участка будет нести замены оснований (обозначено X). Обратная транскрипция, которая также склонна к ошибкам, начинается на про-мРНК выше Ei/MAR и продолжается по направлению к 5'-концу про-мРНК. Мутантный ретротранскрипт (кДНК) гомологично встраивается в ДНК (показано дугообразной стрелкой) и замещает исходную немутантную У(0)и-последовательность. Затем мутантные РНК-транскрипты, подвергаются процессингу (вырезаются интроны) и экспортируются в цитоплазму, где они транслируются в Н- и L-цепи, из которых образуется белковое антитело (Ig), которое проверяется на поверхности В-клетки на связывание с антигеном, презентируемым ФДК. Высокая аффинность к антигену подает стоп-сигнал мутированию. Дополнительную информацию об обозначениях и идеях можно найти в табл. 5.1 и рис. 4.5, 5.4 и 5.5. (По Steele E. J., Rothenfluh H. S., Blanden R. V. Immunology and Cell Biology, vol. 75: 82-95, 1997.)
Другие эксперименты касаются гомологичной рекомбинации. В опытах на трансгенных мышах, имеющих два немного различающихся тесно сцепленных перестроенных V(D)J-reHa, было показано, что соматическая точковая мутация в V(D)J всегда приводит к гомологичной рекомбинации с другими тесно сцепленными У(0).?-последовательностями. Обязательная связь соматической точковой мутации с гомологичной рекомбинацией — поразительное открытие. Этот результат не имеет смысла в рамках мутационных моделей, основанных на ДНК, так как в них гомологичная рекомбинация не играет никакой роли. Однако в RT-модели гомологичная рекомбинация — неотъемлемая составная часть мутационного процесса (рис. 5.6). Таким образом, в хромосомной ДНК-последовательности точковая мутация не возникнет до тех пор, пока мутантная кДНК не рекомбинирует, заменив исходную немутантную V(D)J-пoследовательность.
Следовательно, в настоящее время теория мутаций, основанная на обратной транскрипции, дает лучшее объяснение всем существующим данным о соматическом гипермутиро-вании. Предложенный более 10 лет назад, этот механизм не опровергнут ни одним из многочисленных экспериментов, проведенных с тех пор. Он прошел, как сказал бы покойный философ науки сэр Карл Поппер (Popper), «суровые испытания».
Что является сигналом к прекращению соматического мутирования?
В начале этой главы, мы задались вопросом: «Каков механизм предотвращения лишних, портящих успешно отобранную последовательность, мутаций?» Ответ должен быть таким: селективное преимущество (в традиционном дарвиновском смысле) состоит в том, что когда антитело в центре размножения изменится настолько, что будет обладать высокой аффинностью к антигену, В-клетке должен быть дан сигнал остановить дальнейшее мутирование. Тогда мутаций не будет слишком много, и риск потери высокой аффинности к антигену будет минимизирован. Мы, следовательно, предполагаем, что сигнальная функция поверхностного Ig-рецептора была отобрана в ходе эволюции. Если мутантная В-клетка успешно связывает антиген, присутствующий на фолликулярной дендритной клетке (ФДК) в форме комплекса антиген—антитело, передается СТОП-сигнал для выключения процесса соматического мутирования (рис. 5.6). Этим сигналом может быть прекращение производства белковых субъединиц RT-мутаторсомы (белки постоянно разрушаются ферментами, называемыми протеаза-ми. Следовательно, они исчезают до тех пор, пока не начнется новый синтез).
Позволим себе коснуться другого важного момента, который молчаливо властвует в размышлениях о соматических мутациях. Все мутационные модели, основанные на ДНК, зависят от клеточных делений. Необходимым условием возникновения мутаций считается репликация ДНК и, следовательно, деление клеток. (Считается, что мутации возникают в результате ошибок репарации ДНК.) Сейчас предполагают, что мутации генерируются в фазе быстрого деления клеток (в центробластах), которая дает большую популяцию В-клеток (центроцитов) в центре размножения (рис. 5.4). Однако RT-модель не зависит ни от репликации ДНК, ни от клеточного деления — мутации могут возникать в отсутствие этих двух процессов. Репликация ДНК требуется только для размножения мутантной V(D)J-пoследовательности в делящихся В-клетках. Деление В-клеток, производящих антитела высокой аффинности, полезно, но деление мутантных В-клеток, которые потеряли аффинность к антигену, слишком расточительно.
Представление, что «клеточное деление необходимо для мутирования», настолько глубоко укоренилось в сознании многих, что скорость соматического мутирования записывают как «10-3 - 10-4 на основание на поколение». Другими словами, в традиционное описание скорости мутирования встроена идея клеточного деления, и она невольно оказывает влияние на представления о механизмах мутирования.
Так как RT-модель не зависит от клеточных делений, мы предлагаем циклический процесс «мутация — пауза (для экспрессии Ig) — проверка аффинности», протекающий в неделящейся транскрипционно активной клетке, которая продуцирует мРНК и белковые молекулы Н- и L-цепей антитела и компоненты RT-мутаторсомы. Этот путь организации процесса мутаций и отбора максимизирует образование антител высокой аффинности. Он более эффективен, чем модели, основанные на клеточных делениях.
«Направленные мутации» и наследование соматических мутаций
Мы описали протекающий в В-лимфоцитах процесс обратной связи V(D)J-генов, основанный на склонной к ошибкам обратной транскрипции. Он составляет основу определяемого антигеном мутирования генов антител. Все экспериментальные данные согласуются с этой теорией. Это приводит нас ко второй неоламаркистской концепции: «направленной» обратной связи генов.
Быстрое случайное мутирование, приводящее к различным измененным ДНК-последовательностям, и отбор среди них лучшей последовательности приводят к появлению «направленных соматических мутаций» — полной противоположности случайных мутаций. Играет ли эта соматическая генетическая изменчивость какую-нибудь роль в эволюции? Точнее, можно спросить: есть ли какие-нибудь свидетельства того, что приобретенные соматические мутации генов вариабельных областей могут вносить вклад в следующее поколение? Другими словами, могут ли приобретенные соматические мутации наследоваться с ДНК половых клеток? Может ли предполагаемая нами гомологичная рекомбинация приводить к переносу V-последовательности из В-лимфоцита в ДНК сперматозоидов или яйцеклеток?
Глава 6 ОБРАТНАЯ СВЯЗЬ СОМЫ И ЗАРОДЫШЕВОЙ ЛИНИИ
В этой главе мы рассматриваем, как могли изменяться последовательности ДНК вариабельных генов антител в клетках зародышевой линии за эволюционное время. Некоторые данные указывают на существование обратной связи генов, т. е. движения генетической информации от соматических клеток (лимфоцитов) к половым. Начнем с вопроса, впервые поставленного Тэдом Стилом лет двадцать назад в связи с состоянием знаний того времени по эволюционной генетике антител: «Как согласовать передачу с ДНК половых клеток тех признаков, которые по всем критериям возникают только в соме?»
Такого же типа вопрос не раз ставили философы и биологи, неудовлетворенные традиционным объяснением механизма эволюции. Со времени публикации дарвиновской теории подобный вопрос появлялся в трудах философа XIX века Герберта Спенсера, писателя Самюэля Батлера, писателя и философа Артура Кестлера, зоолога Фредерика Вуда Джоунза (Jones).
Неодарвинисты всегда отбрасывали этот вопрос как неуместный: раз доктрина Вейсмана закрывает дорогу наследованию приобретенных признаков — значит, вопросы такого рода неправомерны. Замкнутый круг рассуждений, подобных этому, очень часто встречается в современной научной литературе; даже крупные биологи, например, С. Дж. Гулд (Gould), делают категорические заявления:
«Природа... работает по дарвиновским, а не по ламарков-ским принципам. Приобретенные признаки не наследуются, и желанные улучшения происходят путем неумолимого отбора с исключением огромного большинства из репродуктивного потока».
Гулд даже не упоминает дарвиновскую теорию пангенезиса. Проблема, таким образом, вынесена за скобки, а все возражения рассматриваются как «бессвязная демагогия сумасшедшего» (читай «ламаркиста» с приставкой нео- или без нее). Однако будем справедливы к Гулду, он очень четко показывает, где ламарковские законы наследственности могут действовать:
«Но с другой стороны, основной механизм культурных изменений ламарковский. Любое знание, приобретенное в одном поколении, может прямо передаваться следующему с помощью того, что мы называем наиболее благородным словом — образование. ...Этот отчетливо ламаркистский характер культурной наследственности придает нашей технологической истории направленный и накопительный характер, чего не может дать дарвиновская эволюция».
В начале 1950-х гг. Вуд Джоунс в книге «Trends of Life» (Направление жизни) уже высказывал удивление, как долго может сохраняться это трагическое непонимание. Артур Кестлер в своей последней книге «Janus: a Summing up» (Двуликий Янус: Итоги), опубликованной в 1978 г., определил свойственные неодарвинистским взглядам противоречия и сделал вывод, что для ламаркистских представлений в биологии дверь должна быть слегка приоткрыта. Почему нельзя принять, что барьер Вейсмана мог быть селективно проницаем для соматической генетической информации за эволюционное время? Когда молекулярные биологи завершат секвенирование ДНК генома человека и других видов, противникам Ламарка вряд ли удастся игнорировать парадоксальное появление в зародышевой линии такой структуры генов, которая существует только в соме. Новые данные о последовательностях ДНК потребуют новых, непредвзятых интерпретаций. Мы уверены, что ламаркистские взгляды придется включить в научные интерпретации в биологии. В истории науки хорошо известны факты, когда ранее отброшенные идеи подтверждались.
Итак, мы вновь формулируем вопрос (впервые поставленный в 1992 г.) о вариабельных генах иммунной системы. Как объяснить высоко неслучайную структуру последовательностей ДНК V-генов зародышевой линии, которая возникает только в ходе прямого антигенсвязывающего отбора белкового продукта гена (антитела), а не прямо в ДНК?
Если структуры Ву—Кэбота могут сформироваться только в результате отбора на уровне связывания антигена функциональным гетеродимером (комплементарное складывание вариабельных областей Н- и L-цепей, составляющих антигенсвязы-вающий центр), то как получилось, что неэкспрессирующиеся элементы V-генов в зародышевой линии несут следы антиген-связывающего отбора? Наши исследования в настоящее время направлены на получение ответа на этот вопрос.
Наследование соматических мутаций
Итак, мы можем спросить, есть ли польза от антигензависимых соматических событий (мутаций и отбора) для ДНК-последовательностей V-генов зародышевой линии следующих поколений? В предьщущей главе мы уже рассказали, как много появляется новых мутантных ДНК-последовательностей в В-лимфоцитах и как они проходят отбор на успешность связывания антигена. Сейчас мы спросим, могут ли эти новые последовательности вливаться в ДНК зародышевой линии — в ДНК половых клеток, яйцеклеток и сперматозоидов?
Теория соматического отбора предполагает передачу приобретенных соматических мутаций V-генов антител половым клеткам. Эта передача может осуществляться при участии обратной транскриптазы (копирование соматической РНК в ДНК) и эндогенных РНК-ретровирусов (продуцируемых лимфоцитами), действующих как «генные челноки», перевозящие мутантные последовательности V-генов в половые клетки. После этого должна происходить интеграция возникшей в соматических клетках генетической информации в ДНК зародышевой линии и замещение ею ранее существовавшей ДНК-последовательности (рис. 1.2). Когда мы формулировали свою гипотезу, мы подчеркивали, что она — «полезный эвристический инструмент», подобный использованным в теоретической физике. Наша теория обращает внимание исследователя на возможность наследования приобретенных признаков. Она убедительно показывает, что теоретически барьер Вейсмана легко преодолим, а, следовательно, он может быть преодолимым и в реальности.
Книга Somatic Selection and Adaptive Evolution вызвала полярные реакции: от резкой критики до щедрой похвалы. Некоторые сочли ее просто фантастической, так как она требовала принятия ламаркистской «ереси», другие приняли ее. Философ Карл Поппер посчитал нашу книгу самой захватывающей из всех, что он читал в том году, а Питер Медавар выразил надежду, что Стил в конце концов окажется прав. Ричард Докинз в своей книге The Extended Phenotype назвал все происходящее тогда «ламаркистским психозом». Позже мы вернемся к критике гипотезы соматического отбора, которую дал Докинз.
Некоторые критики считают идею соматического отбора слишком сложной, так как она требует последовательного наступления слишком многих независимых, если не невероятных, событий. Это — появление мутации в соматических ДНК/РНК, клеточный отбор антигеном, доставка в половые клетки, копирование РНК в ДНК и, наконец, генетическая рекомбинация, приводящая к интеграции мутантной соматической копии кДНК в ДНК зародышевой линии (рис. 1.2). Однако ко времени создания этой теории было хорошо известно, что В-лимфоциты, стимулированные антигеном, продуцируют большое количество эндогенных ретровирусов (предположительно безвредных), несущих обратную транскриптазу. И мы утверждаем, что теория соматического отбора имеет один положительный момент — эволюционное преимущество возвращения мутантных V-последовательностей назад в зародышевую линию. Эндогенные ретровирусы могут рассматриваться в качестве векторов, обеспечивающих генетическую связь между генами соматических и половых клеток.
Тем не менее, главное оправдание теории соматического отбора — в том, что она позволяет критически оценить и интерпретировать весь набор молекулярных фактов, которые иначе бы остались невостребованными. Это то же самое, что аргументы в пользу эволюционной концепции «прерывистого равновесия», использованные недавно С. Дж. Гулдом. Идея обратной связи сомы и зародышевой линии в не меньшей степени полезна, потому что она отвергает непроницаемость барьера Вейсмана на основе научных данных.
В 1994 г. в престижном американском журнале Proceedings of the National Academy of Sciences Симона Бард (Bard), Дэвид Балтимор и Ирвин Вейсман (Weismann) высказали предположение о том, что гены могут перемещаться от вида к виду в результате вирусной инфекции и что этот процесс вносит вклад в эволюцию иммунной системы позвоночных. Эта идея подразумевает, что барьер Августа Вейсмана проницаем, и значит — еще более ответственна, чем идея Тэда Стила, которая не привлекает гипотезу вирусного переноса генов от одного животного к другому. Примечательно, что на эти рассуждения не было столь сильной реакции научной общественности и неодарвинистов, как на теорию соматического отбора. Возможно, потому что Ламарк не был упомянут. А, возможно, еще и потому что Дэвид Балтимор — Нобелевский лауреат, и он, и Ирвин Вейсман — члены Академии. Какими бы ни были причины, это интересный пример из жизни научного сообщества.
Опыты по передаче с отцовской стороны
Первые и очень спорные эксперименты по этому вопросу были проведены в конце 1970-х годов не на уровне генов, но на уровне функциональных характеристик иммунного ответа. Тэд Стил задал вопрос, приводят ли изменения иммунологических функций родителя (отца), вызванные активной обработкой антигеном, к каким-либо изменениям специфической или неспецифической иммунной реактивности у потомства, появившегося от скрещивания таких обработанных антигеном отцов с нормальными самками. Эти эксперименты были проведены на инбредных линиях мышей. Результаты оказались невоспроизводимыми — некоторые лаборатории смогли продемонстрировать отцовскую передачу специфических приобретенных иммунологических функций (или неспецифических нарушений), а другие не смогли. Первый положительный результат был получен Тэдом Стилом в соавторстве с Регом Гор-жински (Gorczynsky). Они использовали систему Медавара приобретенной неонатальной толерантности к чужим антигенам гистосовместимости (рис. 4.3). Эти эксперименты проводились в течение двух лет (1978—1979) в Онкологическом институте Онтарио (Торонто). Мы показали, что, если новорожденных самцов линии А повторно подвергать воздействию большого числа лимфоцитов линии В, то «толерантные» самцы могут передавать некоторые черты специфической толерантности к антигенам В-ткани своему потомству, полученному от , их скрещивания с нормальными самками линии А (рис. 6.1). , Иммунными эффекторными клетками в этом эксперименте почти несомненно были Т-лимфоциты, так как именно они вовлечены в реакцию отторжения. В более поздних экспериментах был проверен ответ В-лимфоцитов, причем была показана отцовская передача изменения силы ответа у потомков иммунизированных самцов.
Рис. 6.1. Передача приобретенной иммунолологической толерантности от отца. Эксперименты Горжински-Стила (Gorczynski-Steele). Мыши линии А приобрели толерантность к антигенам гистосовместимости линии В при инъекции новорожденным лимфоидных клеток линии В. (Это метод Медавара, см. рис. 4.3.) Эти мыши скрещиваются с нормальными самками линии А. У потомства проверяют образец киллерных Т-клеток на толерантность к антигенам гистосовместимости линии В. Согласно традиционной неодарвинистской теории потомство не должно быть толерантным, но в опыте было обнаружено много толерантных мышей. В контроле необработанных самцов линии А скрещивали с нормальными самками линии А. Родителей (контрольных и экспериментальных) и потомков содержали в одинаковых условиях в виварии. (По Steele E. J., Gorczynski R. M., Pollard J. W. In: Evolutionary Theory Path into the Future. Ed. J. W. Pollard. John Wiley, London, pp 217-237, 1984. Перепечатано с разрешения издателя).
В этих экспериментах мы столкнулись с материальными и техническими проблемами. В таких опытах необходимо долговременное разведение 10-20 обработанных и необработанных самцов и учет изменений ответа или на пересадку кожи, или на иммунизацию, или на стимулированный антигеном ответ лимфоцитов одновременно у 50—100 потомков. Правильная интерпретация результатов возможна только при большом числе контрольных животных и проверок реакций на каждом этапе. Положительная передача была непостоянной, появляясь с большой частотой у одного-двух из десяти самцов (среди самцов наблюдалась изменчивость по признаку «частоты передачи потомству»). Эти данные подтверждали прямую проницаемость барьера Вейсмана при активной иммунизации, так как предполагается, что следующему поколению самцы передают только спермий. С иммунизированными матерями экспериментов не проводили, так как на плод и новорожденного прямо воздействуют антитела и лимфоциты, проникающие от матери или в матке, или после рождения с молозивом.
Неудивительно, что эти эксперименты вызвали серьезные возражения и стали отчасти причиной эмоционального приема идей, упомянутых ранее, а невоспроизводимость результатов вызвала скептицизм у некоторых исследователей. Биологические тесты, использованные в некоторых из этих работ, очень изменчивы [10]. Сейчас технически возможны более точные эксперименты, так как новые молекулярные методы позволяют создать линии мышей, на которых можно обнаружить передачу информации от сомы к зародышевой линии. Однако частота такого события все еще неизвестна.
«Печать» соматических мутаций и отбора стоит на всех V-генах зародышевой линии
Наш интерес к анализу ДНК-последовательностей V-генов зародышевой линии начался с наблюдений нашего коллеги Гарри Ротенфлу. В 1992 г, выполняя свою диссертационную работу, он изолировал и секвенировал V-элементы зародышевой линии из Ig-локуса тяжелой цепи мыши (различие между «конфигурацией зародышевой линии» и «соматической конфигурацией» V-генов описано в гл. 4). Напомним, что перестроенные V(D)J-гены вариабельной области появляются только в зрелых В-клетках, и эти гены являются непосредственными мишенями антигензависимых процессов — соматического мутирова-ния и отбора в центре размножения. Данные Гарри Ротенфлу показали, что особенности ДНК-последовательностей соматической конфигурации свойственны и конфигурации зародышевой линии!
Такое строение ДНК-последовательностей V-генов в зародышевой линии трудно объяснить в рамках любой теории, опирающейся на полное запрещение переноса генетической информации от сомы к зародышевой линии. Во-первьгх, V-элементы половых клеток никогда не могли быть прямой мишенью для естественного отбора (т. е. связывания антигена). Отбору подвергается только полностью собранный белок антитела (H+L гетеродимер) на поверхности В-лимфоцита, и только он проходит проверку на антигенсвязывающую функцию. Сами по себе V-элементы клеток зародышевой линии никогда не превращаются в РНК (не транскрибируются) или в белок (не транслируются). Они экспрессируются в зрелом В-лимфоците только после перемещения ДНК в хромосоме соматической клетки, приводящего к созданию типичного перестроенного V(D)J-участка (рис. 4.5). Функциональные исследования обнаружили, что только половина репертуара V-генов зародышевой линии появляется в V(D)J-последовательностях. Многие, возможно, никогда не использовались в зрелых V(D)J-перестройках и, по-видимому, никогда не подвергались отбору.
Во-вторых, геном мыши и человека содержит много V-генов зародышевой линии (примерно по 100 для Н- и L-цепей). И хотя их последовательности в каждой из групп (Н или L) высоко гомологичны, но есть и довольно заметные различия. Изменчивость V-элементов зародышевой линии и для Н-, и для L-цепей характеризуется кривой Ву—Кэбота, т. е. высоко неслучайна (рис. 5.3). В предыдущей главе мы уже рассказали, что такая картина неслучайной изменчивости создается только прямым антигенсвязывающим отбором, действующим на молекулу антитела, расположенную на поверхности В-лимфоцита. Этот вопрос обсуждался в предыдущей главе.
В-третьих, V-гены зародышевой линии мыши и человека «не затронуты» стоп-кодонами. Другими словами, многие V-гены зародышевой линии являются «открытыми рамками считывания». Обнаруживается статистически значимое снижение наблюдаемой частоты стоп-кодонов внутри кодирующих участков V-генов по сравнению с ожидаемой на основании процесса случайных мутаций. Это относится и к так называемым V-псевдогенам — нефункциональным V-генам, которые не могут экспрессироваться как мРНК и белок вследствие мутационных повреждений, нарушивших рамку считывания кодирующего участка или изменивших регуляторную последовательность. Считается, что такие поврежденные гены накапливают мутации, так как они не могут подвергаться действию отбора. Итак, низкая встречаемость точковых мутаций (или мутаций «сдвига рамки» из-за вставок или потерь оснований), приводящих к появлению стоп-кодона и в функциональных генах, и в псевдогенах предполагает существование механизма, который направлен на поддержание «открытой рамки считывания» V-генов зародышевой линии. Однако открытая рамка считывания может подвергаться отбору только на уровне связывания антигеном, связывания интактного гетеродимера, расположенного на поверхности клетки, и антигена.
Таким образом, структура ДНК-последовательности V-генов зародышевой линии млекопитающих предлагает нам сложную загадку. Согласно модели случайного дрейфа, эти гены должны накапливать довольно большое число фоновьк мутаций. Поскольку этого не происходит, то следовательно, эти последовательности несут следы отбора на уровне белка. Указанные особенности последовательностей V-генов наблюдаются у всех изученных до сих пор позвоночных, от хрящевых рыб, амфибий (лягушки) до кроликов, овец, мышей и человека.
Противоречия станут еще глубже, если рассмотреть ДНК-последовательности V-генов зародышевой линии у кур, изученные французскими и американскими исследователями под руководством Жан-Клода Вейля (Weill) и Крейга Томпсона (Thompson) в течение последних 10 лет. У кур процесс образования антител несколько отличается от такового у мышей и человека. Первое отличие заключается в том, что локусы тяжелой и легкой цепей содержат только по одному функциональному V-элементу, включающему сигнальную последовательность для активирующего рекомбинацию генов фермента (RAG), который обеспечивает перестройку ДНК. Вверх (к 5' концу) от этого функционального V-гена находится 20—100 псевдогенов. Они в основном нефункциональны из-за того, что у них укорочен участок, контролирующий транскрипцию (промотор), который может тянуться до последовательности, кодирующей лидерньш пептид (L). У них также отсутствует и сигнальная последовательность для RAG-фермента. Эти псевдогены тесно упакованы в ДНК зародышевой линии, по краям каждого кодирующего участка расположено всего несколько сот (самое большое) оснований. В отличие от них V-элементы генов зародышевой линии у человека и мыши отделены друг от друга 10—20 килобазами ДНК. Таким образом, размер IgV локусов курицы составляет примерно 1/20 размера этих локусов мыши и человека.
В развивающихся куриных В-лимфоцитах происходит перестройка единственного интактного V-гена и образование функционального вариабельного V(D)J-гена. Затем к нему добавляются фрагменты разной длины (5—100 оснований) расположенных выше V-псевдогенов. Этот процесс называют генной конверсией. Разные результаты генной конверсии в разных В-клетках приводят к образованию большого репертуара V(D)J-последовательностей. Такой источник разнообразия функциональных антител так же эффективен, как у мышей и человека, но требует гораздо меньшего (1/20) количества ДНК зародышевой линии.
Но самое поразительное в строении V-псевдогенов это то, что если сравнить их ДНК-последовательности с помощью компьютерных программ, то обнаруживается структура By— Кэбота»! (рис. 6.2). Более того, если различия между псевдогенами обусловлены вставкой и потерей нуклеотидов в кодирующих участках, они всегда кратны трем (т. е. триплету); таким образом, сохраняется правильная трансляционная рамка считывания! Это показано на рис. 6.2. Напомним, что триплетный ко-дон определяет аминокислоту в цепочке белка (см. приложение). Вдобавок у кур псевдогены тяжелой цепи на 3'-(правом) конце несут короткую D-последовательность (и все они находятся в предпочтительной рамке считывания, наблюдаемой только в соматически экспрессирующихся V(D)J-последовательностях). Псевдогены как тяжелых, так и легких цепей отличают вставки или потери нуклеотидов, которые, как известно, происходят в В-лимфоцитах при образовании V(D)J-пepeстройки. Эти вставки и потери создают третий гипервариабельный участок! Такие действительно поразительные и необычные свойства обнаружены в ДНК зародышевой линии, кодирующей псевдогены. Она несет «печать» соматических событий.
Рис. 6.2. Вариабельность ДНК и аминокислот (Ву-Кэбот) V-псевдогенов зародышевой линии у кур. Графики Ву—Кэбота для вариабельных областей псевдогенов 18 тяжелых {А) и 25 легких (Б) цепей генома кур. И для тяжелых, и для легких цепей наблюдаются неслучайные структуры Ву—Кэбота, свидетельствующие об антигенсвязывающем отборе В-клеток на уровне белка Ig. Этот результат противоречит структуре их последовательностей, которая гарантирует, что сами по себе эти гены никогда не экспрессируются как белковая последовательность. Верхние графики показывают вариабельность нуклеотидов в ДНК-последовательностях по длине участка, а нижние — вариабельность аминокислот (после трансляции успешной ДНК-последовательности триплетных кодонов в аминокислотную последовательность, см. приложение). Первое основание или аминокислота предполагаемого кодирующего участка обозначено как положение 0. Обратите внимание, что гипервариабельные последовательности совпадают с антигенсвязывающим центром (CDR), такая картина графика Ву—Кэбота ожидается для функционального белка вариабельной области (рис. 5.3). Положения, в которых произошли вставки (+) или потери (-) триплетов оснований обозначены светлыми стрелками. Относительные положения CDR1, CDR2 и CDR3 показаны на диаграммах под графиками. Появление вставок или потерь оснований наборами триплетных кодонов в правильной рамке считывания (см. приложение) снова свидетельствует об антигензависимом отборе, действующем на уровне белка — что невозможно, так как эти гены — псевдогены! Разумное объяснение таково, что эти последовательности оснований в V-псевдогенах зародышевой линии поддерживаются как открытые рамки считывания обратной связью сомы и зародышевой линии функциональных V(D)J-последовательностей после направляемого антигеном соматического отбора. (По Rothenfluh H. S., Blanden R. V., Steele E. J. Immuno-genetics, vol. 42: 159-171, 1995 с разрешения издателя, Springer-Verlag Gmbh &Co. Kg.)
Следовательно, куриные псевдогены — это чудовищный вызов традиционной молекулярной генетике, основанной на строгой неодарвинистской парадигме. Парадоксально, у них проявляются все черты прямого антигенсвязывающего отбора на уровне антитела, хотя ДНК-последовательности, характерные для зародышевой линии, транскрибируются (в мРНК) и транслируются (мРНК в белок) только по частям, после процесса соматической генной конверсии. Такая структура ДНК-последовательностей разумно объясняется только генетической моделью отбора антигеном соматического V(D)J-гена и последующей обратной связи генов вариабельной области сомы и зародышевой линии (наиболее вероятно, через РНК-> ДНК-копирование, или обратную транскрипцию). См. рис. 6.3 и рис. 1.2.
Структура Ву—Кэбота и другие соматические черты V-генов и псевдогенов зародышевой линии позвоночных (особенно поразительные свойства псевдогенов кур, описанные выше) указывают на действие процесса обратной связи генов сомы и зародышевой линии, активного в течение 400—500 миллионов лет эволюции V-генов. Следовательно, сейчас у нас есть причины для введения в современную эволюционную теорию третьей неоламарковской концепции: прямое проникновение через барьер Вейсмана некоторых семейств генов, например, V-генов иммуноглобулинов.
Рис. 6.3. Обратная связь сомы и зародышевой линии (тяжелая цепь). В гл. 5 говорилось, что соматические мутации накапливаются в вариа-6enbHbixV(D)J-reHax В-лимфоцитов (рис. 5.5 и 5.6). Мутантные обратные транскрипты (кДНК), доставленные в половые клетки подвижными В-клетками и/или ретровирусами, встраиваются в ДНК зародышевой линии в результате гомологичной рекомбинации. Картина рекомбинации V-генов зародышевой линии установлена с помощью алгоритма генетической рекомбинации, разработанного Джорджем Уайлером (см. текст и Weiller et al., 1998). Главные точки рекомбинации в зародышевой линии обнаружены в точке начала транскрипции, на границе между L-V интроном и концом кодирующего V-участка. Этот результат согласуется с предположением о следах интеграции, которые обсуждаются в этой главе. Этот процесс показан и на рис 1.2, но не так подробно. См. также подписи к рис. 4.5, 5.5 и 5.6.
Простейшие модели этого процесса включают создание кДНК по матрице про-мРНК с помощью обратной транскрипции и последующую доставку этой копии в репродуктивные ткани мобильными клетками (например, лимфоцитами) или эндогенными ретровирусами, действующими как «генные челноки». (Напомним, что предполагаемый механизм соматического гипермутирования, обсуждаемый в предыдущей главе, также включает создание кДНК.) Последнее — это гомологич-ная рекомбинация, причем созданная кДНК замещает исходную последовательность зародышевой линии. У нас нет способа оценки частоты возникновения таких событий в ходе эволюции, хотя сила «соматической печати», которую мы видим на ДНК зародышевой линии, заставляет считать их довольно частым эволюционным событием.
«Следы интеграции» сомы в зародышевую линию
Модель соматического отбора, объясняющая эволюционный цикл V-генов антител, приведена на рис. 1.2 и 6.3. Мы предполагаем, что новый варианту-последовательности зародышевой линии «рождается» в соме в результате гипермутирования «выбранного» антигеном перестроенного V(D)J-гена вариабельной области, экспрессирующегося в В-лимфоците. Интенсивные циклы соматического гипермутирования и отбора антигеном в центре размножения приводят к появлению новых, успешных V(D)J-последовательностей с мутациями в определяющих ком-плементарность участках (CDR, от англ complementarity-determining regions), или гипервариабельных участках, которые вступают в контакт с антигеном. Затем эти новые последовательности ДНК доставляются в репродуктивные ткани, где они совмещаются с существующим V-геном, имеющим очень похожую последовательность. После этого происходит процесс, который называется гомологичной рекомбинацией. Он включает разрыв хромосомной ДНК и ее воссоединение с концами нового гена, который, таким образом, интегрируется (встраивается) в хромосому (этот процесс обозначен перекрещивающимися линиями на рис. 6.3).
Все свойства V-генов зародышевой линии, описанные в этой книге, согласуются с этим «жизненным циклом» от сомы к зародышевой линии. Но мы нашли еще одно свидетельство, согласующееся с гипотезой движения информации от сомы к половым клеткам. А именно, если соматическая генная последовательность встраивается в зародышевую линию в результате рекомбинации, то мы должны увидеть свидетельства процесса рекомбинации самого по себе (рис. 6.3). Одним из таких свидетельств может быть распределение событий «вставка/потеря» нуклеотидов. Когда две гомологичные двухцепочечные спирали ДНК рекомбинируют, они должны разрушаться (разрезаться ферментом нуклеазой) и затем воссоединяться (с помощью фермента лигазы). Этот процесс может быть неточным и приводить к потере или вставке нуклеотидов на концах цепочек ДНК. Соответственно, появляются или потери, или вставки нуклеотидов в месте соединения. Поэтому среди последовательностей V-генов зародышевой линии должны быть вставки и потери разной длины по границам генов. В том же смысле, в каком структура Ву—Кэбота служит показателем антигенсвязывающего отбора, неслучайное распределение событий вставка/делеция должно свидетельствовать о существовании обратной связи генов сомы и зародышевой линии. И мы нашли это свидетельство не только в своих данных, полученных на мышах, но и во всех других семействах V-генов зародышевой линии позвоночных. Такое неслучайное распределение рекомбинационных ошибок точно соответствует предсказаниям модели «от сомы к зародышевой линии». На этом уровне наших знаний, по крайней мере для эволюционной генетики V-элементов зародышевой линии, мы не знаем иного объяснения наблюдаемой картине (кроме обращения к разумному манипулятору генами, или божественному вмешательству, а для этого нет оснований!).
Недавно мы начали разрабатывать другой подход к более точной идентификации рекомбинационных сайтов в V-генах зародышевой линии и, таким образом, к «более аккуратному» изучению следов интеграции сомы в зародышевую линию. Мы объединились с Джоржем Уайлером (Weiller) из Школы биологических исследований при Австралийском национальном университете. Джордж разработал новый способ определения сайтов рекомбинации в генных последовательностях, эффективность которого доказана на известных бактериальных ДНК-последовательностях. Поэтому мы могли точно локализовать сайты рекомбинации в коллекции последовательностей V-генов зародышевой линии. Результаты этой работы четко показывают, что рекомбинация в V-генах зародышевой линии происходит в местах, предсказанных теорией встраивания кДНК (обратных транскриптов), возникающей из несплайсированных или сплайсированных про-мРНК соматических L-V(D)J-генов. Таким образом, в зародышевой ДНК мы находим следы интеграции, которые согласуются с «печатью процессинга» соматической РНК. Этот потрясающий результат невозможно логично интерпретировать с позиций традиционных неодарвини-стских взглядов, но они полностью согласуются с предсказаниями теории соматического отбора.
Отступление: Комета Шумейкер Леви 9
Полезной аналогией, которая поможет нам пояснить идею следов интеграции, могут служить размер и форма кратеров на поверхности Луны и других тел Солнечной системы (включая и поверхность Земли), которые считаются результатом падения метеоритов и астероидов. У нас нет сомнений в том, что они были вызваны падениями метеоритов, астероидов или комет в прошлом. Мы даже можем по размерам кратера оценить массу и размеры этих болидов. Для земных и лунных кратеров геологи и астрономы могут также оценить время, когда произошло столкновение. Мы не сомневаемся в причинах, хотя сами редко бываем свидетелями подобных столкновений. Однако в июле 1994 г. мы получили драматические доказательства силы таких вторжений. Мы видели по телевидению (благодаря космическому кораблю «Галилей») падение 21 фрагмента кометы Шумейкер Леви 9 на поверхность Юпитера. Следовательно, с помощью видеозаписи человечество стало свидетелем события, которое может приводить к образованию кратеров на поверхности планет солнечной системы и их спутников. Шестьдесят пять миллионов лет назад болид диаметром примерно 10 километров образовал огромный кратер диаметром примерно 330 километров недалеко от полуострова Юкатан в Мексике.
Однако эта аналогия с кратерами, вызванными падением метеоритов или комет, неполная. Мы не можем точно оценить, как часто и когда происходили «генетические столкновения сомы и зародышевой линии». Данные о современных ДНК-последовательностях V-генов иммуноглобулинов свидетельствуют о том, что они происходили со значительной частотой в эволюционном прошлом, так как оставили отчетливый след в виде неслучайного распределения последовательностей, которое отличается от случайного фонового мутационного «шума». Более того, у разных видов позвоночных наблюдаются разные картины неслучайных последовательностей, а это означает, что столкновения сомы и зародышевой линии происходили много раз после дивергенции этих видов от общего предка.
Эволюционная значимость обратной связи сомы и зародышевой линии
Сейчас мы попытаемся ответить на вопрос, поставленный в конце главы 4. Поскольку иммунная система ныне живущих позвоночных, по-видимому, хорошо приспособлена к ответу на неожиданные антигены, есть ли сейчас нужда в обратной связи сомы и зародышевой линии? Для ответа на этот вопрос рассмотрим вероятные события в эволюции позвоночных, которые привели к появлению генов антител. Мы считаем, что, рассмотрев все известные генетические данные, можно дать следующее простейшее объяснение эволюции V-генов антител.
• Первым шагом было появление в зародышевой линии позвоночных небольшого числа вариабельных генов. Это произошло во время Кембрийского «взрыва» примерно 550-500 миллионов лет назад. Набор тесно сцепленных, хотя и различных генов мог возникнуть только в результате удвоения одного исходного гена и последующих мутационных изменений в образовавшихся дупликациях. Считается, что дуп-ликации генов появляются вследствие неравного кроссин-говера. Он происходит у организмов, размножающихся половым путем, в ходе мейоза, приводящего к образованию гамет (яйцеклеток и сперматозоидов) с гаплоидньш набором хромосом. Повторные дупликации и последующие мутации приводят к образованию рядов тесно сцепленных генов (тандемов) [15].-
• Затем, должен был существовать интенсивный отбор в пользу тех организмов, которые способны к соматическому ги-пермутированию V-генов. Это позволяло создавать большой репертуар антител для борьбы с инфекционными заболеваниями быстрее, чем медленно мутирующий небольшой набор генов зародышевой линии.
• Кроме того, должно было существовать давление отбора на увеличение репертуара V-генов зародышевой линии. Случайные мутации в половых клетках и последующий естественный отбор были бы чрезвычайно медленным способом построения такого репертуара. Кроме того, как мы уже обсуждали, эволюция гетеродимерных антигенсвязывающих центров антител и сегментация генов зародышевой линии, требующая соматической перестройки последовательностей ДНК, заметно ослабляют скорость отбора V-генов зародышевой линии. Каждое изменение структуры V-гена зародышевой линии требовало бы также образования нового репертуара генов. В этих условиях обратная связь успешных функциональных му-тантных последовательностей V-генов сомы и зародышевой линии давала бы большие селективные преимущества.
Нужно ли соматическое мутирование современным позвоночным? Конечно, соматическое гипермутирование можно продемонстрировать экспериментально. Однако в некоторых экспериментах с инбредными мышами и патогенными вирусами (гл. 3) показано, что в ходе антивирусного ответа соматические мутации или не происходят, или, если происходят, ничего не добавляют к иммунному ответу. В самом деле, в настоящее время соматическое гипермутирование само по себе кажется почти неуместным. Существующее в зародышевой линии разнообразие генетических элементов, кодирующих тяжелые и легкие цепи антител, и комбинаторные возможности соматических клеток, которые обеспечивают быстрое образование большого репертуара антител, достаточны для ответа на неожиданности. Поэтому у ныне живущих позвоночных соматическое гипермутирование, должно быть, излишне. Тем не менее, возможно, оно до сих пор дает селективное преимущество как источник новых успешных открытых рамок считывания, возвращающихся в зародышевую линию. Его действие может уменьшать вредный эффект случайного генетического дрейфа, который потенциально направлен на уменьшение репертуара V-генов зародышевой линии в результате появления стоп-кодонов в кодирующих участках из-за точковых мутаций или вставок/потерь нуклеотидов. Короче, роль обратной связи сомы и зародышевой линии у современных позвоночных, возможно, состоит в «генетическом домашнем хозяйстве»: она поддерживает открытые рамки считывания в тандемном наборе V-генов зародышевой линии.
Проницаемость барьера Вейсмана
Можно предположить несколько путей, какими соматическая генетическая информация могла бы попасть в зародышевую линию. Один — с помощью прототипных эндогенных ретровирус-ных векторов. Другой путь, предложенный Гарри Ротенфлу, состоит в том, что долгоживущие В-лимфоциты памяти проникают в репродуктивные ткани и иногда передают новые последовательности V-генов прямо в сперматозоиды и яйцеклетки. Но оба способа должны включать этап обратной транскрипции. Эта проблема является предметом исследований в наших лабораториях. Они включают комплекс экспериментов, в которых надо собрать и проанализировать огромную информацию о последовательностях ДНК. При современных возможностях результатов может не быть много лет. Однако прогресс все-таки есть, особенно за последние десять лет, и нет никаких причин считать, что дальнейшие исследования не будут плодотворными. Мы собираемся действовать на два фронта одновременно. Первый — это выяснение механизма соматического гипермути-рования, так как этот процесс может быть логически связан с обратной связью сомы и зародышевой линии. Вторая наша задача — сконструировать генетически модифицированных мышей, с помощью которых можно будет продемонстрировать генетическое столкновение сомы и зародышевой линии в настоящее время. Уже существуют линии трансгенных мышей, у которых экспрессируется небольшой набор V-, D-, J-, и С-элементов тяжелых и легких цепей человека; генетическая «операция» у таких мышей (удаление существенных ДНК-последовательностей) приведет к тому, что «свои» гены Ig-локуса не смогут экспрессироваться. У этих мышей при иммунизации антигеном будут синтезироваться и подвергаться соматическому гипермутированию только человеческие антитела. Проверка тандемного набора мышиных V-генов зародышевой линии у потомков иммунизированных родителей могла бы обнаружить свидетельства интеграции человеческих последовательностей V-генов.
Глава 7 ЗА ПРЕДЕЛАМИ ИММУННОЙ СИСТЕМЫ
Эволюция по Ламарку, не отвергая дарвиновского естественного отбора, требует следующей причинно-следственной связи для «запоминания» приобретенного признака клетками в зародышевой линии животных. Измененные условия внешней среды (например, доступность пищи, новые хищники) могут приводить к изменениям поведения, строения тела, физиологических функций. Новые иммунологические воздействия могут приводить к появлению новых генов антител в В-лимфоцитах. Со временем такие соматические мутации могли бы встроиться в ДНК половых клеток. А это расширило бы репертуар наследственной изменчивости, на которую затем действует естественный отбор, сохраняющий «наиболее приспособленных» и приводящий к распространению адаптивных вариаций. Такая последовательность событий есть ни что иное, как проницаемость барьера Вейсмана.
Чарлз Дарвин придерживался именно этой точки зрения. Согласно его теории пангенезиса об использовании и неиспользовании органов, измененные условия среды и/или привычки дают значительный вклад в наследственную изменчивость, на которую действует естественный отбор (рис. 1.1). Почему нам не удается легко получить какие-либо свидетельства истинности или ложности такого важного предположения? В работах Фредерика Вуда Джоунза, мы находим следующий ответ: «Природа чрезвычайно медленно осуществляет постепенные изменения живых существ. Есть все основания полагать, что если приобретенные признаки все-таки наследуются, их включение в наследственные структуры животного, по-видимому, очень медленный процесс. Вряд ли человек способен зафиксировать его завершение за время, доступное для лабораторного эксперимента».
Таким образом, необходимо длительное время для становления генетических адаптации. Успешная интеграция приобретенного признака в зародышевую линию, возможно, требует повторных воздействий в течение многих поколений, особенно, если это сложный признак, включающий изменения ДНК-последовательностей многих генов. Тед Стил начал такой эксперимент двадцать лет назад с целью доказать возможность передачи соматически приобретенных иммунологических изменений с отцовской стороны. Он сумел показать передачу уже во втором поколении. Эти попытки в какой-то мере опровергают утверждение Вуда Джоунза. Фактор времени в таких экспериментах заменялся одновременно проводимыми контрольными скрещиваниями в идентичных условиях внешней среды «необработанных» отцов. Эти контрольные скрещивания как бы выполняли функцию «часового», следящего за нежелательными изменениями среды, например, за вирусом мышиного гепатита, который оказывает заметное воздействие на иммунорегуляцию. (Это и происходило несколько раз, что влекло за собой прекращение эксперимента.)
Сейчас мы рассмотрим некоторые «эксперименты, поставленные природой», которые, возможно, объясняются передачей приобретенных признаков. Рассмотрение этих примеров полезно, поскольку они дают возможность рассуждать и обобщать и, таким образом, стимулируют развитие идей о генетических механизмах, ответственных за наследование приобретенных признаков.
Наследование индуцированных химическими веществами метаболических нарушений
В 1960-х — начале 1970-х гг. в опытах на лабораторных крысах была получена отчетливая картина «приобретенного наследования», или трансгенерации, вызванного нарушением эндокринных органов. Известно, что препарат аллоксан вызывает у крыс и мышей диабет (очень высокую концентрацию сахара в крови) вследствие необратимого нарушения клеток поджелудочной железы, синтезирующих инсулин (р-клеток). В Японии (Okamoto), а затем в США (Goldner, Spergel) было показано, что диабет развивается и у потомков заболевших крыс. Инбридинг приводил к тому, что болезнь становилась все тяжелее от поколения к поколению. Несколько лет назад Тед Стил попытался повторить этот опыт на инбредных мышах, однако успех его эксперимента был ограниченным. Диабет индуцировали у самцов препаратом стрептозацин, влияющим на р-клетки. На ранних стадиях развития потомков первого поколения был обнаружен значительный диабетогенный эффект (увеличение или уменьшение среднего веса тела у новорожденных), однако, только у одного мышонка развился спонтанный диабет.
В других экспериментах (Bakke et al.) изучали функцию щитовидной железы у крыс. Оказалось, что в потомстве самцов и самок с нарушенной химическими веществами функцией щитовидной железы регистрируются спонтанные нарушения метаболизма гормонов щитовидной железы, причем проявляются они у большинства потомков в помете.
Как объяснить эти явления? Конечно, можно предположить, что описанные наследственные эффекты вызваны прямым мутагенным действием химических веществ на половые клетки; однако не исключено и то, что соматические мутации генов, вовлеченных в функционирование эндокринной системы, могли быть переданы генам половых клеток. Этот процесс должен был приводить к спонтанным и геноспецифичным изменениям в функции генов в следующем поколении. Еще один способ объяснить полученные данные — предположить, что измененный в результате специфической обработки гормональный статус меняет «условия регуляции» генов зародышевой линии. Молекулы гормонов из крови проникают в репродуктивные ткани, связываются с рецепторами гормонов в половых клетках, которые в свою очередь, возможно, прямо изменяют уровень активности соответствующих генов, когда они экс-прессируются в эмбрионе (этот механизм предложен профессором медицинского факультета UCLA Джоном Кэмпбелом (Campbell)).
Наследование мозолистых утолщений
Сейчас мы рассмотрим некоторые явления наследования анатомических признаков в экспериментах, проведенных природой. Некоторые из них детально описаны Джоунзом в его книге 1943 г. Поскольку животные «сами приноравливают себя к условиям окружающей среды» вследствие повторяющихся привычных действий, можно попытаться найти свидетельства «приобретенной наследственности», согласующейся с этими привычками.
У некоторых животных, например у страусов и африканских бородавочников, на разных частях тела (грудине, передних и задних конечностях) обнаруживаются большие выпуклые мозолистые утолщения, по-видимому, являющиеся результатом их привычек. Разыскивая пищу, бородавочник становится передними ногами на колени, а страусы, отдыхая, ложатся на ноги, при этом их грудина упирается в землю. Мозолистые утолщения у этих животных можно обнаружить на всех тех частях тела, где кожа соприкасается с землей. Появление мозолей можно считать «приобретенной» соматической адаптацией. Но что особенно интересно, так это то, что все заметные естественные мозоли, обнаруживаемые у взрослых страусов и бородавочников, уже хорошо сформированы у эмбрионов в отсутствие трения. Это означает, что мозоли, локализованные в стратегически важных местах, закодированы в зародышевой линии. Для таких зоологов, как Вуд Джоунз, подобное наблюдение является убедительным доказательством наследования приобретенных признаков. Реакция неодарвинистов (последователей Дарвина, но не самого Дарвина) на эти факты иная: эти мозолистые утолщения — результат естественного отбора. Обладатели таких мозолей имеют явное селективное преимущество, поскольку риск проникновения болезнетворных бактерий через поврежденную кожу для них существенно меньше.
Единственный способ решить, кто прав в этом споре — эксперимент, включающий скрещивания и индуцирование мозолей в нетипичном месте в каждом поколении, однако вероятнее всего этот эксперимент не принесет пользы по причине, сформулированной Вудом Джоунзом. Проблема для ламаркистской интерпретации состоит в том, что трудно представить, основываясь на современном знании, как информация о такой анатомической структуре может попасть в ДНК половых клеток. Для этого необходимо знать путь передачи от сомы в зародышевую линию, а также идентифицировать гены, контролирующие этот процесс. На таком фоне экспериментирование с V-генами выглядит очень легкой задачей!
Итак, образование мозолей — процесс хорошо заметный, но не поддающийся анализу. В противоположность этому V-гены антител нельзя увидеть, но с ними можно экспериментировать, анализировать полученные результаты и делать выводы.
Наследование анатомических особенностей, связанных с привычкой сидеть на корточках
В книге Habit and Heritage Вуд Джоунз обсуждал также манеру сидеть на корточках в разных популяциях человека. У многих азиатских народов принято сидеть на корточках так, что ступни стоят плоско на земле. Аборигены Австралии делают это иначе, их ступни подобраны под ягодицы (рис. 7.1). У тех, кто сидит в азиатской позе (рис. 7.2), в месте соединения голени и таранной кости (ступни) есть хорошо выраженная поверхность, которая, по-видимому, позволяет очень долго удобно сидеть на корточках на рисовых полях и базарах (для большинства европеоидов это очень трудное дело). Этой особенной суставной поверхности нет у аборигенов Австралии, у них она совершенно другая. Далее, ни той, ни другой поверхности нет у тех людей, которые привыкли сидеть на стульях. И что самое интересное, все эти структуры уже присутствуют в костях эмбрионов и маленьких детей у тех народов, которые имеют привычку сидеть на корточках, но их нет у эмбрионов и маленьких детей в тех популяциях, где люди для сидения используют стулья. Для объяснений с неодарвинистских позиций надо признать наличие селективного преимущества (т. е. повышенный репродуктивный успех) спонтанных генеративных мутаций, которые затрагивают форму костей ноги и ступни. Ключевой вопрос: сколь пригодны такие объяснения, поскольку указанные анатомические черты эволюционно должны были возникнуть совсем недавно.
Рис. 7.1. Манера сидеть на корточках у жителей востока и аборигенов Австралии. А. Жители Востока. Б. Аборигены Австралии. (Перепечатано из F. Wood Jones 1943 Habit and Heritage, с разрешения издателя, Kegan Paul International Ltd.).
Рис. 7.2. Структура костей и поза. Суставные поверхности (показаны стрелкой), на большой берцовой и таранной кости у жителей Востока, имеющих особую манеру сидеть на корточках. (F. Wood Jones 1943 Habit and Heritage, с разрешения издателя, Kegan Paul International Ltd.).
Это очень интересный пример. Цель будущего — организация и проведение новых экспериментов, направленных непосредственно на выяснение механизма наследования таких анатомических особенностей.
Приобретенная наследственность у бактерий
Здесь мы хотим коротко упомянуть спорное явление, впервые описанное в журнале Nature в 1988 году профессором Гарвардского университета Джоном Кэрнзом (Cairns) и его коллегами. Не входя в детали, скажем, что они смогли генерировать в культуре бактерий генные мутации, которые интерпретировались как направленные. Они показали, что определенные классы мутаций в гене, кодирующем определенный фермент, появлялись только в том случае, если в питательной среде присутствовали химические субстраты, связанные с этим ферментом. Эти эксперименты были оспорены, потому что другие ученые получили экспериментальные результаты, которые позволяют дать традиционное неодарвинистское объяснение, т. е. субстратный отбор функциональных мутантов. Однако первоначальное объяснение появления этих мутантов интригующее: Кэрнз привлек обратную связь генов, основанную на обратной транскрипции, предложенную Тедом Стилом для вариабельных генов иммунной системы.
Приобретенная наследственность у растений
А что же у растений? У них нет барьера Вейсмана, отделяющего сому от зародышевой линии. Приобретенные соматические модификации у растений, связанные с изменением генов, могут, в принципе, передаваться потомству, если семена образуются из тех частей растения, в которых возникла соматическая мутация. Итак, это уже не секрет: эволюция по Ламарку была и есть, это факт из жизни растений! Можно легко продемонстрировать, например, наследование индуцированной устойчивости к тяжелым металлам. Особенно полезным для демонстрации роли стресса, вызванного внешней средой и запускающего наследственные изменения в геноме растений, оказался лен. Ценность изучения таких проблем на растениях подчеркнула пионерская работа Нобелевского лауреата Барбары МакКлин-ток (McClintock) о мобильных генетических элементах у кукурузы.
Можно ли распространить нашу гипотезу за пределы иммунной системы ?
Картина ламарковской обратной связи для появления и поддержания У-генов иммунной системы, которую мы нарисовали в этой работе, основана на ясной и на наш взгляд неоспоримой логике. Но можем ли мы распространить идею об обратной связи сомы и зародышевой линии (основанной на обратной транскрипции) для генов, вовлеченных в выполнение других функций?
Прежде всего, мы должны сказать, что многие коллеги, которые считают наши аргументы в пользу ламарковского наследования V-генов убедительными, ограничивают этот процесс только V-генами. Так, доктор Арно Маллбачер (Mull-bacher) из Центра медицинских исследований Джона Керти-на, замечательный полемист и критик, внесший существенный вклад в успех нашей исследовательской программы, не принимает мысли о том, что эта концепция справедлива за пределами имунной системы. Позицию Арно разделяют сейчас многие другие ученые. Они готовы принять, хотя и неохотно, что передача в зародышевую линию соматической генетической информации имеет место для V-генов, но отвергают ее для генов, ответственных за другие функции, ткани и органы.
В качестве возражения этому взгляду можно привести такой аргумент. В живом мире уникальные процессы и функции редки. Если какой-нибудь феномен обнаружен в одной живой системе, рано или поздно его выявят и в других клетках, тканях или организмах. Например, не так давно (в начале 1970-х годов) считалось, что обратная транскрипция, впервые описанная Говардом Теминым, ограничивается только С-типом РНК-содер-жащих опухолевых вирусов (Темину поначалу тоже пришлось вьвдержать ожесточенную критику). Однако сейчас мы знаем, что РНК->ДНК копирование широко распространено в вирусных и невирусных биологических системах, от бактерий до человека и царства растений. Похожая история произошла и с открытием широко распространенного ферментоподобного РНК-катализа (так называемых рибозимов). О нем ничего не было известно до 1982 г., когда это явление бьмо впервые описано для бактерий и одноклеточных простейших Томасом Ке-чем (Cech) и Сиднеем Альтманом (Altman). Как мы увидим, невирусная, обобщенная обратная транскрипция оказала значительное и всеобщее влияние на создание структуры ДНК-последовательностей геномов высших позвоночных и млекопитающих. Она играет не только ту роль, которую мы приписываем ей в эволюции V-генов.
Модель миграции В-лимфоцитов памяти: приложения для генов «домашнего хозяйства»
Могут ли соматические клетки проникать в репродуктивные органы и, таким образом, вступать в тесный физический контакт с половыми клетками? По мнению Гарри Ротенфлу роль такого «связника» могут играть В-лимфоциты. Они способны мигрировать в репродуктивные ткани самцов и самок, доставляя возникшие в соме мутантные информационные ДНК-последовательности вариабельных областей к мужским и женским гаметам (сперматозоидам и яйцеклеткам). Для этого, возможно, требуются в качестве генного вектора или источника обратной транскриптазы эндогенные ретровирусы. А может быть, они и не нужны.
Из модели Ротенфлу вытекает одно возможное следствие: мигрирующий В-лимфоцит потенциально способен служить транспортным средством для доставки ДНК-последовательностей любых генов в зародышевую линию. Данные, рассмотренные в гл. 2, предполагают возможность того, что эндогенная ретровирусная обратная транскриптаза могла бы продуцировать кДНК копии клеточных генов, которые еще содержат инт-роны (некодирующие последовательности). Это может быть кДНК других, не имеющих отношение к антителам генов, экс-прессирующихся в В-клетке. Их могут быть сотни. Это могут быть гены, принадлежащие и к семействам тканеспецифичных генов, которые определяют функции лимфоцитов, и гены «домашнего хозяйства», обеспечивающие жизнедеятельность клетки. Белковые продукты большинства генов «домашнего хозяйства» высоко консервативны. Многие из этих генов эволюционно очень древние, они необходимы для функционирования клетки. (К ним относятся, например, гены, контролирующие энергетические пути, синтез новых мембран, репликацию хромосомной ДНК, а также упаковку молекул ДНК в хромосомах.)
По определению, пока не появится редкая полезная для генов «домашнего хозяйства» мутация, такие гены должны иметь ДНК-последовательность, которая сохраняет функцию генного продукта (обычно белка). Ожидается, что в ретротран-скриптах (кДНК) должны часто встречаться замены оснований вследствие ошибок процесса копирования от ДНК к РНК и обратно. Часть таких замен оснований в кДНК должна быть молчащей (например, замена основания в третьем положении), и не влиять на аминокислотную последовательность кодируемого белка из-за вырожденности генетического кода (см. приложение). Остальные замены оснований должны изменять аминокислотную последовательность белка и обычно они оказывают вредное влияние на функцию белка [14]. Вероятнее всего, такие замены уменьшают приспособленность любого организма, несущего мутантный ген, и естественный отбор будет элиминировать такие мутации. Однако гены с молчащими заменами должны сохраняться. Итак, тот факт, что функция генов «домашнего хозяйства» должна сохраняться, приводит к очевидному предсказанию: предполагается, что в таких генах доля молчащих замен будет больше, чем ожидается из предположения об отсутствии отбора среди мутаций. Такая картина согласуется с кДНК, построенной по матрице про-мРНК, включенной в ходе эволюции в зародышевую линию (однако повышенный уровень молчащих замен можно объяснить также с неодарвинистских позиций, предполагающих отбор против мутаций в зародышевой линии, приводящих к замене аминокислоты).
Сейчас необходим детальный анализ генов «домашнего хозяйства» в свете идеи обратной связи соматических и половых клеток. Можно сделать несколько интересных предсказаний, и предварительный анализ показывает, что они подтверждаются!. Например, модель передачи генов от сомы к зародышевой линии, основанная на мобильных клетках, предсказывает, что уровень замен оснований в генах «домашнего хозяйства» и в тканеспецифичных генах, экспрессирующихся в В-лимфоцитах (а их много), должен быть выше, чем в генах, экспрессирующихся в немобильных клетках. Богатым источником данных могли бы быть тканеспецифичные гены, которые кодируют цитокины и поверхностные белки только лимфоцитов. В этих генах участки ДНК, которые транскрибируются в РНК и транслируются в белок, должны иметь более высокую эволюционную скорость замен оснований, чем нетранскрибируемые/нетранслируемые участки. Эта модель также предсказывает интенсивность рекомбинационного сигнала Уайлера (след вторжения сомы в зародышевую линию) в разных группах гомологичных генных последовательностей (гл. 6). Сигнал Уайлера будет слабее в семействах не-иммуноглобулиновых генов, так как они не должны подвергаться соматическим гипермутациям. Следовательно, они не должны часто проходить через склонную к ошибкам информационную петлю ДНК-РНК-ДНК.
Есть свидетельства того, что переход генов от сомы в зародышевую линию, основанный на обратной транскрипции, происходил за эволюционное время для многих генов «домашнего хозяйства». Поскольку все эти данные косвенные, им можно дать альтернативное неодарвинистское объяснение. Но есть молекулярные свидетельства, предсказанные теорией передачи генов от сомы к зародышевой линии, существенным элементом которой является интеграция кДНК-ретротранскриптов. Имеющий к этому отношение результат, полученный за последние двадцать лет при выделении и секвенировании ДНК многих генов «домашнего хозяйства», состоит в том, что большинство этих генов существует в виде одной (в крайнем случае, двух) функциональной копии на хромосому (копии, которые транскрибируются в мРНК, а затем транслируются в белок). К удивлению, во многих случаях обнаружены близкородственные ДНК-последовательности в форме нефункциональных генов, названных псевдогенами (они укорочены в результате одной или нескольких мутаций). Но самым интригующим оказалось то, что эти псевдогены были копированы с мРНК (после вырезания некодирующих интрон-ных последовательностей из про-мРНК) в кДНК обратной транскриптазой и, таким образом, являются «интегрированными ретротранскриптами», или «ретропсевдогенами».
Исключительная картина, которую мы сейчас имеем для многих генов «домашнего хозяйства» млекопитающих, такова: единственную функциональную высоко консервативную копию гена может сопровождать множество родственных ре-тропсевдогенов, число которых в 10—100 раз больше. Часто они локализованы в других частях генома (например, в другой хромосоме). Процитируем авторитетный текст по молекулярной эволюции:
«Благодаря наличию обратной транскриптазы, геномы млекопитающих буквально бомбардируются копиями обратно транскрибированных последовательностей. Огромное большинство этих копий с момента интеграции в геном нефункциональны ...[и] большей частью они локализованы далеко от родительского функционального гена ...это явление подобно вулканическому извержению, и такой эволюционный процесс назван моделью Везувия».
Это общая черта многих видов высших животных. В некоторых случаях можно обнаружить от тысяч до сотен тысяч копий ретропоследовательностей, разбросанных по всему геному. Стандартная неодарвин истекая или неовейсманистская модель этого явления такова. Некоторые формы синтеза про-мРНК, продуцирующие множество РНК-копий гена и использующие в качестве матрицы ДНК генов, происходят в половых клетках. Затем гипотетический процесс обратной транскрипции должен создавать много нефункциональных кДНК-ре-тротранскриптов, которые встраиваются в разные места хромосомной ДНК тех половых клеток, в которых они образовались. Поскольку образуются ретропсевдогены, требуется сплайсинг про-мРНК для удаления интронов; это событие связано с нормальной экспрессией гена (транскрипцией и трансляцией). Согласно этой модели, фактически все гены «домашнего хозяйства» и тканеспецифичные гены подвергаются транскрипции, сплайсингу и обратной транскрипции в клетках репродуктивных тканей, из которых образуются сперматозоиды и яйцеклетки. Однако не известно каких-либо доказательств такого механизма. Кроме того, содержащие ошибки кодирующие последовательности могут заменить путем гомологичной рекомбинации стандартный ген, и значит, многие из этих новых генов должны быть летальными или эволюционно невыгодными.
Мы обнаруживаем ретропсевдогены, потому что они являются своего рода реликтами, «молекулярными ископаемыми». Их широкое распространение также может свидетельствовать в пользу интеграции сомы в зародышевую плазму с участием ретротранскрипта, образованного в соматических клетках путем обратной транскрипции несплайсированной про-мРНК. Такие кДНК-последовательности могут быть мутантными, с молчащими и кодирующими заменами оснований. Гомологичная рекомбинация в соматических клетках, заменяющая исходный ген, дала бы возможность проверить функцию нового гена. Выживут и размножатся только соматические клетки с молчащими заменами (функционально консервативные). Некоторые из этих мутантных соматических клеток могли бы иногда передавать новый ген в половые клетки или в результате миграции (например, лимфоцитов), или с помощью ретровирусного вектора, подобно тому, как обсуждалось для генов антител. Однако частота таких событий должна быть много ниже, чем для V-генов антител, потому что только V-гены подвергаются соматическому гипермутированию. Замещение исходного гена новым в результате гомологичной рекомбинации нельзя было бы идентифицировать именно как событие ретротранспозиции от сомы к зародышевой линии, потому что нет способов отличить его от генеративной мутации и естественного отбора: ген будет классифицирован как «аллель» (альтернативный функциональный вариант) исходного гена.
Следовательно, общая теория обратной связи сомы и зародышевой линии утверждает, что за эволюционное время в соматических клетках возникают кДНК-последовательности (и функциональные гены с интронами, и нефункциональные ретропсевдогены) и что они способны встраиваться в ДНК зародышевой линии. Она предполагает также, что случайная интеграция сомы в зародышевую линию (гомологичная рекомбинация) — это событие, которое в ходе эволюции поддерживает функционально консервативное состояние генов «домашнего хозяйства» (так как последовательность сразу проверяется на приспособленность в жизнеспособной соматической клетке) и, следовательно, создает новые функциональные аллели. Однако, нефункциональные кДНК-посдедовательности, возможно, встраиваются в разные места генома, увеличивая число ретропсевдогенов.
Как сделать выбор между этой неоламаркистской моделью и моделью Везувия, которая придерживается строгой неодар-винистской или неовейсманистской парадигмы? Почему мы должны считать, что предполагаемый механизм передачи генов от сомы к зародышевой линии ограничен только V-генами иммунной системы, когда общность природы обратной транскрипции — факт, установленный для многих генов? Масштаб распространения геномных ретропоследовательно-стей говорит о том, что нет видимых причин, по которым этот процесс должен быть ограничен только генами иммунной системы.
По нашему мнению, данные, рассмотренные в этой книге, поддерживают, скорее, обратную связь сомы и зародышевой линии, чем альтернативную модель Везувия. Кажется вероятным, что перенос кДНК от сомы к зародышевой линии поддерживает и разнообразие открытых рамок считывания в V-генах зародышевой линии, и функционально консервативное состояние генов «домашнего хозяйства» и тканеспецифичных генов.
Ретротранскрипты характерны не только для геномов животных и растений. В вирусных геномах обнаружены функциональные гены с высокой степенью сходства с последовательностями клеточных генов. При этом вирусные гены не имеют интронов, это четкий показатель того, что в какой-то момент эволюции они возникли в клетке хозяина из зрелой мРНК в результате обратной транскрипции. Эти гены используются вирусом в клетке животного-хозяина. Возможно, они кодируют аналоги исходного животного белка, которые действуют в пользу вируса, снижая эффективность иммунного ответа. Существование таких генов приводит нас к предположению о межвидовом (горизонтальном) переносе генов вирусами, что мы детально обсуждали раньше. Насколько нам известно, это предположение не вызывает отторжения у неодарвинистов, что удивительно, ибо для такого переноса требуется проницаемость барьера Вейсмана. Для того, чтобы обеспечить возможность интеграции гена в хромосомную ДНК .зародышевой линии другого вида, вирус, содержащий ген одного вида, должен внедриться в половые клетки другого вида. Если это может происходить между видами, то почему бы этому не случиться в одном организме?
Эпигенетическое наследование
Нашу экспериментальную и теоретическую работу по «ретрогенетике» V-генов иммунной системы можно рассматривать как пример жесткого наследования, затрагивающего генетическую информацию, воплощенную в последовательности оснований ДНК. Однако существуют и другие формы структурного и функционального наследования у животных, растений и свободно-живущих одноклеточных организмов, разные этапы которых не включают прямого изменения последовательности оснований в ДНК. Существует обширная литература о таких явлениях, кстати широко распространенных у растений. Мы их не касались в этой книге не потому, что мы не считаем их важными для понимания происхождения эволюционно значимых признаков. Просто нашей целью было обсуждение проницаемости барьера Вейсмана, так как это дает самые яркие примеры ламарковско-го феномена, который вовсе не отвергает установленных принципов генетики и естественного отбора. Эта тема была прекрасно освещена в книге Евы Яблонки ( Jablonka) и Марион Лам (Lamb) Epigenetic Inheritance and Evolution: The Lamarckian Dimension (1994) («Эпигенетическое наследование и эволюция: ламаркистское измерение»).
Будущие эксперименты
Очевидно, что для исследования механизмов «приобретенного наследования» необходимы тщательные эксперименты. Новые молекулярные методы обеспечивают нам не имеющую себе равной возможность работать практически с любым интересующим геном, и мы использовали информацию о ДНК-последовательностях для поиска «следов» возможной обратной связи сомы и зародышевой линии. Однако такие свидетельства будут всегда оставаться косвенными. Программа скрещиваний, необходимая для получения прямых свидетельств, требует жесткого контроля и, возможно, очень большого числа животных и очень длительного времени. В настоящее время мы пытаемся решить эту проблему, анализируя изменения V-генов линий мышей, происходящих от одной инбредной генетической линии, но разводимых в разных лабораториях мира в течение 40 и более лет.
Сейчас наука должна оставить в стороне догматические, идеологические и эмоциональные споры прошлого и сосредоточиться на объективном анализе. Ламарковские идеи могут не только объяснять, но и стимулировать изучение наследственных явлений, связанных с адаптивным соматическим ответом, например иммунным. Мы надеемся, что представленные нами гипотезы и умозаключения послужат стимулом к дальнейшим теоретическим и экспериментальным исследованиям. В основе нашего подхода лежит тот факт, что РНК может служить матрицей для синтеза ДНК. Этот факт, установленный Говардом Теминым, поколебал центральную догму молекулярной биологии, какой она формулировалась в шестидесятые годы. Работа Темина касалась преимущественно ретровирусов, но он увидел ее широкие приложения в биологии и эволюции. Мы верим, что значение его открытия еще грандиознее, чем он мог себе представить.
Эпилог
Если наследование приобретенных признаков в иммунной системе считать реальностью, а дальнейшие исследования покажут, что обсуждавшиеся нами механизмы передачи наследственной информации от соматических клеток к половым применимы и к другим семействам генов, это приведет к существенным последствиям для науки и человечества. Некоторые из них мы бы хотели обсудить в конце нашей книги. Читателю предоставляется возможность поразмышлять вместе с нами.
Ответ неодарвинистам
В 1858 г. в Лондоне Чарлз Дарвин и Альфред Расселл Уоллес впервые представили Линнеевскому обществу свою теорию эволюции путем естественного отбора. Противники тут же яростно заклеймили ее как разрушающую теологические представления о происхождении человека. Как верно отмечает Дэниэл К. Деннет в книге Darwin's Dangerous Idea (Опасная идея Дарвина), «буря, сопровождавшая этот разрыв с прошлым, до сих пор бушует в социологии, искусстве, да и просто в умах людей. До 1858 г. никому не могло придти в голову, что человек представляет собой всего лишь животное высшего порядка, произошедшее от нематод и приматов».
Дарвиновская революция принесла пользу науке. Однако проблема интеллектуальных революций заключается в том, что «победившее» представление со временем превращается в догму. Какое-то время догма полезна, но затем неминуемо образуется «сообщество», члены которого почти не способны выйти за ее рамки, так как это подвергло бы риску их карьеру и финансовое положение. Это противоречит духу научного исследования (но, как это ни печально, точно отражает состояние человеческого общества). Сегодня, к сожалению, очевидно, что неодарвинистские представления в некоторой части научного сообщества превратились почти что в религию. Неоламаркистская идея обратной связи сомы и зародышевой линии до сих пор встречает сильное сопротивление. А в ряде теоретических исследований все еще используют неприменимую в данном случае теорию нейтральной молекулярной эволюции Кимура (Kimura). Однако мы показали в этой книге, что в эволюции и структуре семейства V-генов иммунной системы позвоночных многое объясняется и предсказывается теорией обратной связи генов. Сейчас задача заключается в том, чтобы выяснить, можно ли распространить ее за пределы иммунной системы. В гл. 7 мы попытались убедить читателя в том, что такой подход может оказаться весьма плодотворным.
Возвращение к идеям Ламарка можно проследить в трудах Вуда Джоунза, затем Г. Кэннона (Cannon) и Артура Кестлера в 1960-х и 1970-х гг. За последние двадцать лет концепция передачи генетической информации от сомы к зародышевой линии, касающаяся V-генов лимфоцитов, претерпела бурную историю. Критика этой идеи как среди иммунологов, так и в более широком кругу биологов, была настолько сильной, что Теду Стилу в пору было бросить заниматься наукой! Это дает и нам полное право покритиковать наиболее рьяных противников нашей гипотезы: Дэниела Деннета (философа из Университета Тафте) и Ричарда Докинза (Оксфордский университет). Именно они в конце XX века стали апологетами того, что Стивен Гулд назвал «дарвинистским фундаментализмом».
В своей книге «Darwin's Dangerous Idea», вышедшей в свет в 1995 г., Деннет называет палеонтолога Тейяра де Шардена, придерживающегося ламаркистских воззрений, самого Ламарка и направленные мутации «тремя проигравшими». Здесь мы остановимся исключительно на его низкой оценке научного вклада Ламарка. Она поверхностна и наивна, хотя автор и признает, что сам Дарвин, «как это печально известно», в теории пангенезиса придерживался ламарковского принципа упражнения и неупражнения органов. Деннет абсолютно уверен в том, что барьер Вейсмана генетически непроницаем. Он полностью отвергает возможность наследования приобретенных признаков, заявляя: «... для того, чтобы ламаркизм мог действовать, информация о приобретенных признаках, о которых здесь идет речь, должна была бы передаваться от измененного органа, сомы, в яйцеклетки и сперму. В общем, такую передачу информации можно считать невозможной — каналы связи, которые могли бы нести сообщение, не обнаружены...».
Это догматическое утверждение противоречит тому, что мы знаем теперь об иммунной системе. Обратная транскрипция и соматическое гипермутирование совсем не упоминаются в его книге. Мы полагаем, что это может быть следствием его неосведомленности, так как он не занимается ни молекулярной биологией, ни иммунологией. Несмотря на это, в глазах общественности он равноправный «участник эволюционной игры».
Ричард Докинз в своей книге «The Extendend Phenotype» (1982 г.) пространно рассуждает о гипотезе соматического отбора. Цель его аргументации — преуменьшить значение гипотезы Стила. В конце раздела, посвященного соматическому отбору, мы с изумлением прочли следующее: «Теория Стила несомненно верна, он ошибается только в определении того, что считать зародышевой линией. Любой ген в соматической клетке, который является кандидатом для про-вирусной [читай, ретровирусной] передачи в зародышевую клетку, по определению является репликатором зародышевой линии. Книгу Стила можно было бы заново озаглавить «The Extendend Germ-line»! Вовсе не задевая неовейсманистов, она оказывается глубоко близкой нам».
Попытка Докинза превратить лимфоцит и его гены в «продолжение зародышевой линии», с научной точки зрения, абсурдна. Сначала он принимает идею о том, что соматическая клетка может передавать новые гены половым клеткам, т. е. концепцию, противоречащую догме Вейсмана, и тут же он говорит, что такая концепция «оказывается глубоко близкой» неовейсманистам. Это акробатический номер, на который способен только догматичный неодарвинист, пообещавший съесть свою шляпу, если неоламаркизм окажется истинным. Если бы Вейсман мог прочесть этот абзац из книги Докинза, он бы перевернулся в гробу!
Однако в истории науки известно довольно много случаев, когда сторонники ортодоксальных точек зрения отказываются принимать ставшие уже всем очевидными новые факты и идеи. Наиболее известный из них нежелание врагов Галилея взглянуть на спутники Юпитера через телескоп, который Галилей установил специально для них. А в конце XVIII века сторонники теории неизменяемости видов, пытаясь совместить ее с противоречащими геологическими данными, дошли до абсурда, утверждая, что «каждый день имеет неопределенную (или варьирующую) длину» [З]. В современной иммунологии таких эпизодов тоже было немало, например длительная приверженность ряда ученых инструктивным теориям образования антител, несмотря на то, что клонально-селекционная теория Бернета была уже давно опубликована и признана.
Видообразование и конвергенция
Теперь нам бы хотелось обсудить значение ламарковской гипотезы об обратной связи сомы и зародышевой линии для теории видообразования и конвергенции. Помимо катастрофического исчезновения видов, например, из-за падения метеоритов или усиленной вулканической активности, наименее понятное явление эволюции живых организмов — это происхождение новых видов и планов строения, то есть возникновение новых и отличных от всех прочих жизненных форм. В своих ярких и увлекательных книгах (особенно в «Wonderful Life»), Стивен Гулд убедительно показал, насколько противоречива история жизни на Земле. «Кембрийский взрыв» многоклеточных (приблизительно 570 млн. лет назад) явился моментом возникновения многих сохранившихся до наших дней многоклеточных форм. Но в этот же геологический период происходила массовая гибель многих видов. Действительно, очевидное подлаживание выживших планов строения и видов во время такой адаптивной радиации соответствует теории прерывистого равновесия, предложенной Гулдом и его коллегой Найлзом Элдреджем (Eldredge) в 1972 г. (длинные периоды «застоя», или эволюционного постоянства, прерываются мощными эволюционными взрывами). Одна из ярких черт адаптивной радиации — отсутствие многих промежуточных форм. Майкл Дентон (Denton) подробно рассмотрел надежность подобных отрицательных данных в книге «Evolution: A Theory in Crisis», вышедшей в середине 1980-х годов. Могут ли общая теория передачи наследственной информации от сомы к зародышевой линии и концепция упражнения и неупражнения органов добавить что-либо к дискуссии о происхождении новых форм жизни? Можно ли понять, как сложные соматические приспособления переводятся в новые сложные морфологические/физиологические формы (или виды)? Другими словами, могут ли соматические мутации пройти по «каналу» от сомы к зародышевой линии за короткий период времени (одно или несколько поколений)? Теоретически подобные события могут иметь место, когда происходят резкие сдвиги в окружающей среде. В этом случае необходимо достаточно быстро (за одно поколение, чтобы новая сложная форма выжила) создать потенциально приспособленную форму, т. е. того самого «счастливого монстра», о котором писал в своей книге «The Material Basis of Evolution» в 1940-х годах эволюционный генетик Ричард Голдшмидт (Goldschmidt).
Однако связь соматических и половых клеток может быть только одним из возможных механизмов приспособления и создания разнообразия на этапе адаптивной радиации. Из других механизмов укажем горизонтальный перенос генов между видами. В книге «Our Place in the Cosmos» Хойл и Викрамасинг приводят доводы в пользу того, что эволюционный скачок был вызван попаданием на Землю генетического материала из другой области Солнечной системы (см. рис. 1.4). Интересные идеи относительно того, как могут в результате самоорганизации спонтанно появляться сложные упорядоченные системы высказывает Стюатр Кауфман (Kauffman) из Института Санта-Фе. Весьма плодотворной нам представляется гипотеза Линн Мар-гулис (Margulis), согласно которой решающую роль в создании разнообразия эукариотических клеток сыграл эндосимбиоз (поглощение без переваривания), заключающийся в слиянии клеток. Каждая внутриклеточная органелла, вероятно, сначала вела независимую жизнь, но потом стала полностью зависимым симбионтом для блага клетки. Вполне возможно, что явление независимой конвергенции форм или физиологических характеристик у не-родственных видов (и даже у разных родов) может быть объяснено передачей информации от сомы к зародышевой линии. Но опять-таки такая реконструкция должна была бы рассматриваться вместе с взаимодействием (горизонтальные «перекрестные инфекции») генов и клеток, как это только что были описано. Для установившегося вида, чувствительная к окружав ющей среде обратная связь сомы и зародышевой линии может! иметь большую эволюционную значимость, потому что она позволяет геному быстро и эффективно «отслеживать среду».
Другими словами, в долгие периоды покоя ламарковская обратная связь сомы и зародышевой линии может приводить к адаптивной настройке, позволяя видам занять свою нишу.
Генная инженерия
Еще одна область, в которой следует ожидать важных результатов, если обратная связь сомы и зародышевой линии будет доказана, — это генная инженерия эукариот. Сейчас развивается новая область лечения «врожденных» генетических ошибок — соматическая генная терапия. Мы стоим на пороге широкого применения этой технологии в медицине. Если существует «генетический канал» от сомы к зародышевой линии (хотя бы только для V-генов), можно надеяться, что «соматическая коррекция» приведет и к фиксации исправленного гена в половых клетках? Если бы этот механизм работал, можно было бы, используя ретровирусные векторы, встроить исправленные гены в ядерный геном лимфоцитов пациента, а затем ввести эти клетки в его организм при переливании крови. Это должны быть кроветворные стволовые клетки, которые, дифференцируясь, постоянно пополняют популяции кровяных клеток всех типов. Это означает, что подвижные лимфоциты, включая В-лимфоциты, которые несут и экспрессируют РНК нового функционального гена, могли бы проникать в репродуктивные ткани и передавать новую последовательность ДНК зародышевой линии. Однако вероятность такой передачи неизвестна.
Основная идея нашей книги состоит в том, что соматические мутации в клетках иммунной системы могут быть унаследованы зародышевой линией. Главный аргумент в пользу обобщения этих представлений для других систем организма состоит в следующем. Известно, что как только какой-либо процесс или механизм обнаруживается в одной биологической системе, он начинает использоваться и в других системах. Вряд ли возможно чтобы высокая частота соматического мутирования была не замечена в других «адаптивных» генетических локусах, таких например, как система цитохрома Р-450, обеспечивающего детоксикацию печени, или в такой «сенсорной» генетической системе, как гены, ответственные за обоняние? Вызывает большой интерес, стабильны ли в действительности «сенсорные» гены (продукты которых взаимодействуют непосредственно с молекулами, обеспечивающими внешние стимулы) в ткани-мишени в условиях перенесенного соматического стресса? Не исключено, что возникновение опухолей может оказаться обратной стороной соматических генетических адаптации (ценой прогресса) у многоклеточных эукариотиче-ских организмов, способных на адаптивную соматическую реакцию.
Известно, что онкологические и аутоиммунные заболевания в общем являются заболеваниями пострепродуктивного возраста. В самом деле, лишь в этом столетии большое число людей живет достаточно долго для того, чтобы заболеть ими. Любые соматические адаптивные реакции организма, которые могли бы исправить их и перейти к генам зародышевой линии после завершения периода размножении, таким образом, будут потеряны для последующих поколений. Отбора против этих заболеваний также почти не было, так как большинство наших предков начинали производить на свет детей в раннем возрасте и умирали в том возрасте, который мы теперь называем средним.
В благополучном западном обществе возникло новое явление, а именно, люди заводят детей во все более позднем возрасте. В свою очередь, это означает, что временной промежуток, в котором соматические генетические нарушения могут быть переданы генам половых клеток, становится длиннее. В результате, потомство более старых родителей может оказаться с генетической точки зрения в невыгодном положении. И наоборот, некоторые соматические адаптации, возникшие в результате, скажем «выбора образа жизни», могут дать и генетическое преимущество детям старых родителей. Поскольку этот вывод основан на допущении о связи сомы и зародышевой линии, вероятность такого рода событий неизвестна.
Эволюция сознания
Возникновение сознания — самый значительный результат эволюции жизни на Земле. Даже если разум возник по воле «слепого случая», сейчас — это реальный факт, и он должен быть включен в любой сценарий дальнейшего эволюционного пути человечества. Значение этого факта выразилось в создании нового журнала Journal of Consciousness Studies, посвященного исключительно этой теме, и в интересных идеях об «антропоцентричном ментальном реализме» и общей роли сознания в эволюции Вселенной, высказанных Гэри Ричард -соном (Richardson), философом из Блю Маунтинз в Австралии. То, что человек овладевает генетическим инструментарием, безусловно будет иметь социальные и экологические последствия.
Какое отношение к этому имеет соматический отбор и обратная связь сомы и зародышевой линии? Если эти процессы носят универсальный характер, нам следует исключить те действия и условия жизни, которые могут вести к генетическим нарушениям. В этом отношении уже осуществляются соответствующие общественные программы (что имеет смысл как при неоламаркистской, так и при неодарвинистской парадигме).
Этические последствия также очень существенны. В соответствии с неодарвинистской парадигмой внешняя среда производит проверку возникающих случайных мутаций в зародышевой линии, из которых формируется наше будущее генетическое наследство. Если общие идеи, вытекающие из теории соматического отбора, подтвердятся для большего числа семейств генов, придется также считаться с организменными, или внутренними, «агентами изменения» — факторами, воздействующими на нашу наследственность. Если мы сочтем, что барьер Вейсмана пошатнулся (хотя бы теоретически), надо будет с серьезностью отнестись к гипотезе о том, что наши идеи и жизненная философия (через выбор образа жизни) могут воздействовать на наш будущий генетический багаж. Возможно, что мы не только лучше поймем наше генетическое «настоящее», но и сможем планировать наше генетическое будущее. Несомненно, мы уже способны создавать новый генетический материал. Но данная идея идет гораздо дальше современной «генной терапии» и заставляет нас направить свои мысли вперед, в то время, когда сознательный выбор образа жизни станет частью «семейной евгеники».
Наша цель состоит не в том, чтобы подробно останавливаться на этих вопросах, а в том, чтобы указать на возможную связь межцу нашими представлениями о том, как следует жить, и нашим генофондом. Эта возможность ставит перед нами множество этических и философских проблем. Этические убеждения, в конце концов, — это общественная структура, обусловленная многими факторами. Но что, если наш генофонд, в конечном итоге, тоже «общественная структура», обусловленная нашим сознанием? Возможно, обе эти структуры тесно связаны и на протяжении эволюции действуют, усиливая друг друга.
Поговорим теперь о «конечной причине» — понятии, которое неодарвинист мог бы приписать любой форме ламар-ковского наследования. Конечно, «божественное назначение» или «конечная причина» лежат за пределами научной работы. Однако по иронии судьбы, пытаясь исключить все следы «божественного вмешательства» или «намеренного планирования» из своего крайнего неодарвинизма, Ричард Докинз в своей книге выбирает роль верховного «изобретателя плана»! Это четко показано в эссе Дэвида Берлински. Так, его компьютерные модели, демонстрирующие «могущество естественного отбора», зависят непосредственно от того, как Докинз определяет все критерии отбора и алгоритм получения желаемого результата селекционной программы. Таким образом, «божественное вмешательство» со стороны программиста — неотъемлемая черта всех компьютерных программ эволюционного отбора. Это во многом похоже на то, как молекулярные биологи регулярно используют «обратную генетику», чтобы вычислить последовательность ДНК из последовательностей аминокислот белка. С нашей точки зрения, единственной полезной концепцией была бы концепция «упреждающей цели» или «генетической ответственности» — научное знание, этические и моральные взгляды и выбор образа жизни могут воздействовать на наше будущее генетическое наследие.
Сейчас мы стоим у порога новой захватывающей эры в генетических исследованиях. В наших силах попытаться ответить на вопрос, проницаем ли барьер Вейсмана, наследуются ли приобретенные признаки, и если да, каковы молекулярные механизмы такого наследования. Однако сделать это мы можем только в том случае, если все вместе решим это сделать. Между тем, многие биологи, придерживающиеся неодарвини-стских взглядов, яростно сопротивляются подобного рода исследованиям. Их позицию можно сравнить с позицией Церкви в 1850-е гг., которая в штыки приняла идею эволюции путем естественного отбора. Остается надеяться, что демократия и терпимость, восторжествовашие в политике большинства развитых стран, восторжествуют и в науке. Ответы на вопросы, возникающие в связи с идеей соматического отбора, только-только начинают появляться. Мы рады, что одними из первых призвали к обсуждению этих проблем.
Так сможем ли мы сознательно влиять на наше генетическое будущее?
Список литературы
Ada G. L, Nossal G. (1987). The Clonal Selection Theory. Scientific American, vol. 255: 50—57.
Alexander R. D. (1979). Darwinism and Human Affairs. University of Washington Press, Seattle.
Anderson M. K., Shamblott M. J., Litman R. Т., Litman G. W. (1995). Generation of Immunoglobulin Light Chain Gene Diversity in Raja erinacea Is Not Associated with Somatic Rearrangement, an Exception to a Central Paradigm of В Cell Immunity. Journal of Experimental Medicine, vol. 182:109-119.
Bachmann M. F., Kalinke U., Althage A., Preer G., Burkhart C., Roost H-P., Aguet M., Hengartner H., Zinkemagel R.M. (1997). The Role of Antibody Concentration and Avidity in Antiviral Protection. Science, vol. 276: 2024-2027.
Bakke J. L., Lawrence N. L., Bennett J., Robinson S. (1975). Endocrine Syndromes Produced by Neonatal Hyper-thyroidism, Hypothyroidism, or Altered Nutrition and Effects Seen in Untreated Progeny. In: Perinatal Thyroid Physiology and Disease. D. A. Fisher and G. N. Burrow (Eds). Raven Press, New York, pp 79-116.
Barti S., Baltimore D., Weissman I. L. (1994). Molecular Evol.ution of the Vertebrate Immune System. Proceedings National Academy of Science, USA, vol. 91: 10769-10770.
Beardsley Т. (1997). Evolution Evolving. Scientific American, vol. 277: 9-12.
Berlinski D. (1996). The Deniable Darwin. Commentary June, pp 19-29.
Blanden R. V., Steele E. J. (1998). A Unifying Hypothesis for the Molecular Mechanism of Somatic Mutation and Gene Conversion in Rearranged Immunoglobulin Variable Genes. Immunology, and Cell Biology, vol. 76: 288-293.
Cairns J., Overbaugh J., Miller S. (1988). The Origin of Mutants. Nature, vol. 335: 142-145.
Campbell J. H. (1982). Autoevolution. In: Perspectives on Evolution. R. Milkman (Ed.). Sinauer Associates, New York, pp 190-201.
Cannon H. G. (1959). Lamarck and Modem Genetics. Manchester University Press, Manchester.
Cech T. R. (1986). RNA as an Enzyme. Scientific American, vol. 255: 76-84.
Chen С., Nagy Z., Prak E. L., Weigert M. (1995). Immuno-globulin Heavy Chain Gene Replacement: A Mechanism of Receptor Editing. Immunity, vol. 3: 747-755.
Cohn M. (1968). The Molecular Biology of Expectation. In: Nucleic Acids in Immunology. 0. J. Plescia, W. Braun (Eds). Springer-Verlag, New York, pp 671—715.
Cohn M. (1974) A Rationale for Ordering the Data on Antibody Diversity. In: Progress in Immunology II: Biological Aspects I. L. Brent, J. Holborow (Eds). North-Holland Pub. Co., Amsterdam, pp 261-284.
Collins Dictionary of Biology 2nd Edition (1995). Hale, W. G., Margham, J. P., Saunders, V. A. (Eds). Harper Collins Publishers, Glasgow, UK.
Crick F. H., Orgel L. E. (1973). Directed Panspermia. Icarus, vol. 19: 341-346.
Culhs С. А. (1984). Environmentally Induced DNA Changes. In: Evolutionary Theory-: Paths into the Future. J. W. Pollard (Ed.). John Wiley, London, pp 203-216.
Cunningham A. J. (1977). Evol.ution in Microcosm: The Rapid Somatic Diversification of Lymphocytes. Cold Spring Harbor Symposium on Quantitative Biology, vol. 41: 761—770.
Darwin С. (1859) The Origin of Species. New American Library, Mentor Edition, 1958. Дарвин Ч. Происхождение видов путем естественного отбора или сохранения благоприятных рас в борьбе за жизнь. Ред. А. Л. Тахтаджян. СПб.: Наука, 1991.-539 с.
Darwin С. (1868). The Variation of Animals and Plants Under Domestication. 2 vols, John Murray, London. Дарвин Ч. Изменения животных и растений в домашнем состоянии. Ред. К. А. Тимирязев. M.: Сельхозгиз, 1941. — 619 с. (Классики естествознания)
Davis B.D., Dulbecco R., Eisen H.N., Ginsberg H.S., Wood W.B. Jr (1969). Microbiology. Harper and Row, New York. Dawkins R. (1982). The Extended Phenotype. Oxford University Press, Oxford.
Dawkins R. (1986). The Blind Watchmaker. Longman, London. Dennett D.C. (1995). Darwin's Dangerous Idea. Penguin Books, Ringwood, Vic. Denton M. (1985). Evol.ution: A Theory in Crisis. Bumett Books, London.
Detlefsen J. A. (1925). The Inheritance of Acquired Characters. Physiological Reviews, vol. 5: 244—278.
Eigen M., Gardiner W., Schuster P., Winkler-Oswatitsch R. (1981). The Origin of Genetic Information. Scientific American, vol. 244: 78-94.
Eldredge N., Gould S.J. (1972). Punctuated equilibria: an alternative to phyletic gradualism. In: Models in Paleobiology. T. J. M. Schopf (Ed.). Freeman, Cooper and Co., San Francisco, pp 82—115.
Fenner F., Henderson D. A., Arita I., Jezek Z., Ladnyi I. D. (1988). Smallpox and its Eradication. World Health Organisation.
Foote J., Eisen H. N. (1995). Kinetic and Affinity Limits on Antibodies Produced During Immune Responses. Proceedings National Academy of Science, USA, vol. 92: 1254-1256.
Gesteland R. F., AtkinsJ. F. (Eds) (1993). The RNAWorld. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York.
Gillman M.A. (1996). Envy as a Retarding Force in Science, Avebury, Aldershot, UK.
Goldner M.G., Spergel G. (1972). On the Transmission of Alloxan Diabetes and Other Diabetogenic Influences. Advances in Metabolic Disorders, vol. 6: 57—72.
Goldschmidt R. (1940). The Material Basis of Evolution. Yale University Press, New Haven.
Gould S.J. (1991). Wonderful Life: the Burgess Shale and the Nature of history. Penguin Books, Ringwood, Vic.
Gould S.J. (1997). Dinosaur in a Haystack. Penguin Books, Ringwood, Vic.
Gould S.J. (1997). Life's Grandeur: the spread of excellence from Plato to Darwin. Vintage Books, London.
Greenberg A. S., Avila D., Hughes M., Hughes A., McKinney E. G., Flajnik M. F. (1995). A New Antigen Receptor Gene Family that Undergoes Rearrangement and Extensive Somatic Diversification in Sharks. Nature, vol. 374:168-173.
Henderson's Dictionary of Biological Terms Uth Edition (1995). Lawrence E. (Ed.). Addison Wesley Longman Ltd, Hariow,Essex, UK.
Hinds-Frey K. R., Nishikata H., Litman R. Т., Litman G. W. (1993). Somatic Variation Precedes Extensive Diversificationof Germline Sequences and Combinatorial Joining in the Evolution oflmmunoglobulin Heavy Chain Diversity. Journal of Experimental Medicine, vol. 178: 825-834.
Но M. W. (1997). Genetic Engineering: Dream or Nightmare? Gateway Books, Bath, UK.
Holland H. D. (1997). Evidence for Life on Earth More Than 3850 Million Years Ago. Science, vol. 275: 38-39.
Hopkins D. R. (1983). Princes and Peasants: Smallpox in History. University of Chicago Press, Chicago.
Hoyle F. and Wickramasinghe N. C. (1978). Life Cloud: The Origin of Life in the Universe. Sphere Books, London.
Hoyle F. and Wickramasinghe N. C. (1996). Our Place in the Cosmos. Phoenix Paperback, Orion Books Ltd, UK.
Jablonka E., Lamb M.J. (1994). Epigenetic Inheritance and Evolution: The Lamarckian Dimension. Oxford University Press, Oxford.
Jeme N. K. (1973). The Immune System. Scientific American, vol. 229: 52-60.
Johnson G. (1997). Fire in the Mind: Science, Faith and the Search for Order. Penguin Books, Ringwood, Vic.
Judson H. F. (1979). The Eighth Day of Creation. Simon and Schuster, New York.
Kauffman S. (1996). At Home in the Universe: The Search for Laws of Complexity. Penguin Books, Ringwood, Vic.
Kephart J. 0., Sorkin G. В., Chess D. M., White S. R. (1997). Fighting computer viruses. Scientific American, vol. 277: 56-61.
Kimura M. (1983). The Neutral Theory of Molecular Evolution. Cambridge University Press, Cambridge. Кимура M. Молекулярная эволюция: теория нейтральности. M.: Мир, 1985. — 398 с.
Kitcher P. (1996). The Lives to Come: The Genetic Revolution and Human Possibilities. Penguin Books, Ringwood, Vic.
KlenermanP., HengartnerH., ZinkemagelR. M. (1997).ANon-retroviral RNA Virus Persists in DNA Form. Nature, vol. 390: 298-301.
KoestlerA. (1971). The Case of the Midwife Toad. Hutchinson, London.
KoestlerA. (1978). Janus. A Summing Up. Hutchinson, London.
KoestlerA. (1981). Bricks to Babel. Hutchinson, London.
Kuby J. (1997). Immunology 3rd edition. W.H. Freeman & Co., New York.
Kuhn, T. S. (1977). The Essential Tension. Selected Studies in Scientific Tradition and Change. University of Chicago Press, Chicago.
Lamarck J. B. (1809) Zoological Philosophy. Translated by Hugh Elliot. University of Chicago Press, Chicago, 1984. Ламарк Ж-Б. Философия зоологии. /Пер. С. В. Сапожникова/ Т.1-2. М.-Л.: Биомедгиз, 1935-37. - 331 с. 484с.
Lambert D. M., Stevens P.M., White C. S., Gentle M. Т., Phillips N. R., Millar C. D., Barker J. R., Newcomb R. D. (1989). Phenocopies, Heredity and Evolution. Evolutionary Theory, vol. 8: 285-304.
Langman R. E., Cohn M. (1987). The E-T (Elephant-Tadpole) Paradox Necessitates the Concept of a Unit of B-Cell Function: The Protecton. Molecular Immunology, vol. 24: 675-697.
Lewin R. (1981). Lamarck Will Not Lie Down. Science, vol. 213: 316-321.
Li W-H., Graur D. (1991). Fundamentals of Molecular Evolution. Sinauer Associates, Sunderland, MA.
Litman G.W. (1996). Sharks and the Origin of Vertebrate Immunity. Scientific American, vol. 275: 47—51.
Lonberg N., Taylor L. D. et al. (another 16 co-authors) (1994). Antigen-Specific Human Antibodies from Mice Comprising Four Distinct Genetic Modifications. Nature, vol. 368: 856-859.
Madigan M. Т., Marrs B. L. (1997). Extremophiles. Scientific American, vol. 276: 66—71.
Margulis L. (1981). Symbiosis in Cell Evolution. W. H. Freeman and Co., San Francisco.
McClintock В. (1978). «Mechanisms that Rapidly Reorganize the Genome». Stadler Symposium, vol. 10: 25—48.
McGraw-Hill Dictionary of BioScience (1997). S. P. Parker (Ed.). McGraw-Hill, New York.
Medvedev Z. A. (1969). The Rise and Fall of T. D. Lysenko. Translated by I. M. Lemer. Columbia University Press, New York. Медведев Ж. А. Взлет и падение Лысенко: История биологической дискуссии в СССР (1929-1968). M.: Книга, 1993.-347 с.
Mehra J. (1994). The Beat of a Different Drum: The Life and Science of Richard Feynman. Clarendon Press, Oxford.
Milbum G. (1998). The Feynman Processor: An Introduction to Quantum Computation. Alien & Unwin, Sydney.
Mullis К. В., Ferre F., Gibbs R. A. (Eds). (1994). The Polymerase Chain Reaction. Birkhauser, Boston.
Neuberger M. S., Milstein C. (1995). Somatic Hypermutation. Current Opinion in Immunology, vol. 7: 248-254.
Ohno S. (1970). Evolution by Gene Duplication. Springer, Berlin. Оно С. Генетические механизмы прогрессивной эволюции. M.: Мир, 1973.-227с.
Okamoto К. (1965). Apparent Transmittance of Factors to Offspring by Animals with Experimental Diabetes. In: On the Nature, and Treatment of Diabetes. B. S. Leibel, G. A. Wrenshall (Eds). Excerpta Med., Amsterdam, pp 627-631.
Oxford Dictionary of Biology 3rd Edition (1996). E. Martin, M. Ruse, E. Holmes (Eds). Oxford University Press, Oxford and New York.
Parham P. (1995). A Boost to Immunity from Nurse Sharks. Current Biology, vol. 5: 696-699.
Pasteur L. (1881). Vaccination in Relation to Chicken-cholera and Splenic Fever. Transactions of the International Medical Congress, 7th session, London, Aug 2—9 vol. 1: 85—90.
Pauling L. (1940). A Theory of the Structure and Process of Formation of Antibodies. Journal American Chemical Society, vol. 62: 2643-2657.
Penguin Dictionary of Biology, 9th Edition (1994). M. Thain, M. Hickman (Eds). Penguin Books, Ringwood, Vic.
Pollard J.W. (1984). Is Weismann's Barrier Absolute? In: Beyond neo-Darwinism: Introduction to the New Evolutionary Paradigm. M. W. Ho and P. T. Saunders (Eds). Academic Press, London, pp 291-315.
Pollard J. W. (Ed.) (1984). Evolutionary Theory: Paths into the Future. John Wiley & Sons, Chichester, UK.
Prem Das 0., Levi-Minzi S., Koury M., Benner M., Messin J. (1990). A Somatic Gene Rearrangement Contributing to Genetic Diversity in Maize. Proceedings National Academy of Science USA. vol. 87: 7809-7813.
Prowse S.J., Lafferty K.J., Simeonovic C.J., Agostino M., Bowen K.M., Steele E.J. (1982). The Reversal of Diabetes by Pancreatic Islet Transplantation. Diabetes, vol. 31 (Suppl. 4): 30-37.
Prowse S. J., Steele E. J., Lafferty K. J. (1982). Islet Allografting Without Immuno-suppression. Reversal of Insulitis-associat-ed and Spontaneous Diabetes in Non-immuno-suppressed Mice by Islet Allografts. Aust. J. Exp. Biol. Med. Sci. (now Immunology and Cell Biology), vol. 60: 619—627.
Radman M., Wagner R. (1988). The High Fidelity of DNA Replication. Scientific American, vol. 259: 24—30.
Reanney D. С. (1986). Genetic Error and Genome Design. Trends in Genetics, vol. 2: 41—46.
Richardson G. (1997). Love as Conscious Action: Towards the New Society. Gavemer Publishing, Sydney.
Roost H-P., Bachmann M. F., Haag A., Kalinke U., Pliska V., Hengartner H., Zinkernagel R. M. (1995). Early High-Affinity Neutralizing Anti-viral IgG Responses Without Further Improvements of Affinity. Proceedings National Academy of Science, USA vol. 92: 1257-1261.
Rothenfluh H. S. (1995). Hypothesis: A Memory Lymphocyte-Specific Soma-to-Germline Genetic Feedback Loop. Immunology and Cell Biology, vol. 73: 174—180.
Rothenfluh H. S., Blanden R. V., Steele E. J. (1995). Evolution of V Genes: DNA Sequence Structure of Functional Germ-line Genes and Pseudogenes. Immunogenetics, vol. 42: 159—171.
Rothenfluh H. S., Steele E. J. (1993). Origin and Maintenance of Germ-line V-genes. Immunology and Cell Biology, vol. 71: 227-232.
Rothenfluh H., Steele T. (1993). Lamarck, Darwin and the Immune System. Today's Life Science, vol. 5(7): 8—15 и vol. 5(8): 16-22.
Sekevich T. G., Bugert J. J., Sisler J. R., Koonin E. V., Dara G., Moss B. (1996). Genome Sequence of a Human Tumorigenic Poxvirus: Prediction of Specific Host Response-Evasion Genes. Science, vol. 273: 813-816.
Spergel G., Khan P., Goldner M. G. (1975). Emergence of Overt Diabetes in Offspring of Rats with Induced Latent Diabetes. Metabolism, vol. 24: 1311-1319.
Steele E. J. (1979). Somatic Selection and Adaptive Evolution: On the Inheritance of Acquired Characters. Williams and Wallace, Toronto, 2nd edition University of Chicago Press, Chicago, 1981.
Steele E. J. (1986). Idiotypes, allotypes and a paradox of inheritance In: Paradoxes in Immunology. G. W. Hoffman, J. G. Levy, G. T. Nepom (Eds). CRC Press Inc., pp 243-252.
Steele E. J. (1988). Observations on Offspring of Mice Made Diabetic with Streptozocin. Diabetes, vol. 37: 1035-1043.
Steele E. J. (Ed.) (1991). Somatic Hypermutation in V-Regions. CRC Press, Boca Raton, FL.
Steele E. J. (1992). Alistair Cunningham and the generation of antibody diversity after antigen. Immunology and Cell Biology, vol. 70: 111-117.
Steele E. J. (1996). Lamarckism: Still Alive and Thriving (Interview) AEON, vol. 1V(3): 39-49.
Steele E., Blanden R., Rothenfluh H. (1996). How Have Antibody Genes Evolved? Australasian Science, vol. 17(4): 46—49.
Steele E.J., Caims J. (1989). Dispute resolved. Nature, vol. 340: 336.
Steele E. J., Gorczynski R. M., Pollard J. W. (1984). The Somatic Selection of Acquired Characters. In: Evol.utionary Theory: Paths into the Future. J. W. Pollard (Ed.). John Wiley, London, pp 217—237.
Steele E. J., Pollard J. W. (1987). Hypothesis: Somatic Hypermutation by Gene Conversion via the Error Prone DNA->RNA->DNA Information Loop. Molecular Immunology, vol. 24: 667-673.
Steele E. J., Rothenffu, H. S., Ada G. L., Blanden R. V. (1993). Affinity Maturation of Lymphocyte Receptors and Positive Selection ofT Cells in the Thymus. Immunological Reviews, vol. 135: 5-49.
Steele E. J., Rothenfluh H. S., Blanden R. V. (1997). Mechanism of Antigen-Driven Somatic Hypermutation of Rearranged Immunoglobulin V(D)J Genes in the Mouse. Immunology and Cell Biology, vol. 75: 82-95.
Steele T. (1981). Lamarck and Immunity; a Conflict Resolved. New Scientist, vol. 90: 360-361.
Storb U., Ritchie K. A., O'Brien R. L., Агр В., Brinster R. (1986). Expression, Allelic Exclusion and Somatic Mutation of Mouse Immunoglobulin Kappa genes. Immunological Reviews, vol. 89: 85-101.
Temm H. M. (1989). Retrons in Bacteria. Nature, vol. 339: 254-255.
Tomlinson I. M., Walter G., Jones P. Т., Dear P.H., Sonn-hammer E. L. L., Winter G. (1996). The Imprint of Somatic Hypermutation on the Repertoire of Human Germline V Genes. Journal of Molecular Biology, vol. 256: 813-817.
Tonegawa S. (1983). Somatic Generation of Antibody Diversity. Nature, vol. 302: 575-581.
Waugh J. (1987). An investigation into the induction of heavy metal tolerance in three plant species. MSc thesis. Department of Zoology, University of Auckland, New Zealand.
Wedemayer G. J., Pattern P. A., Wang L. H., Schultze P. G., Stevens R. C. (1997). Structural Insights into the Evolution of an Antibody Combining Site. Science, vol. 276: 1665-1669.
Weiller G. F., Rothenfluh H. S., Zylstra P., Gay L. M., Aver-dunk H., Steele E. J., Blanden R. V. (1998). Recombination Signature of Germline Immunoglobulin Variable Genes. Immunology and Cell Biology, vol. 76: 179-185.
Wood Jones F. (1943). Habit and Heritage. Kegan Paul, Trench, Trubner & Co., London.
Wood Jones F. (1953). Trends of Life. Edward Arnold & Co., London.
Woese C. R. (1994). Universal Phylogenetic Tree in Rooted Form. Microbiological Reviews, vol. 58: 1—9.
Zoraqi G., Spadafora C. (1997). Integration of Foreign DNA Sequences into Mouse Sperm Genome. DNA and Cell Biology, vol. 16: 291-300.

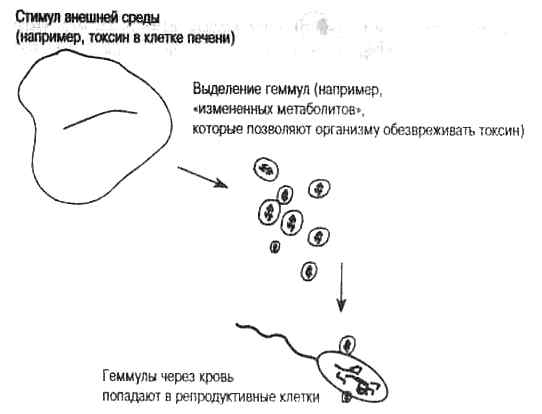









Комментарии к книге «Что, если Ламарк прав? Иммуногенетика и эволюция», Эдвард Стил
Всего 0 комментариев